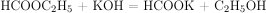Задание с ответами: химия. ЕГЭ — 2018
При полном сгорании органического вещества массой 25,9 г образовалось 23,52 л (при н. у.) углекислого газа и 18,9 г воды. Относительная плотность паров этого вещества по водороду равна 37. Установлено, что оно не реагирует с гидрокарбонатом натрия, но взаимодействует со щелочами и даёт реакцию «серебряного зеркала». Установите молекулярную формулу вещества, изобразите его структурную формулу и напишите уравнение реакции с гидроксидом калия.
1) Определены количества элементов в сжигаемом веществе.
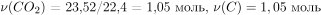
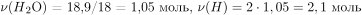
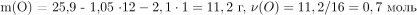
2) Определена молекулярная формула вещества.
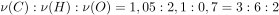
Простейшая формула: 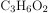 (M = 74 г/моль).
(M = 74 г/моль).
Молярная масса вещества: M = 37 · 2 = 74 г/моль. Молекулярная формула совпадает с простейшей формулой, 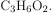
(Принимается также любой другой правильный способ определения молекулярной формулы по продуктам сгорания)
3) Изображена структурная формула.
Вещество относится к гомологическому ряду 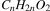 и реагирует со щелочью, следовательно, это карбоновая кислота или сложный эфир.
и реагирует со щелочью, следовательно, это карбоновая кислота или сложный эфир.
С гидрокарбонатом не реагирует, значит — не кислота, а сложный эфир, метилацетат или этилформиат. Реакция «серебряного зеркала» свидетельствует о том, что искомое вещество – сложный эфир муравьиной кислоты, этилформиат:
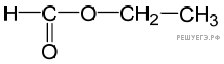
4) Написано уравнение реакции этилформиата с гидроксидом калия.