Задание с ответами: химия. ЕГЭ — 2018
При сгорании 17,5 г органического вещества получили 28 л (н. у.) углекислого газа и 22,5 мл воды. Плотность паров этого вещества (н. у.) составляет 3,125 г/л. Известно также, что это вещество было получено в результате дегидратации третичного спирта. На основании данных условия задачи:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу органического вещества;
3) составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции получения данного вещества дегидратацией соответствующего третичного спирта.
1) Найдено количество вещества продуктов сгорания:



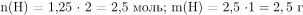
Значит никаких других элементов в состав вещества не входит, так как его масса равна сумме масс водорода и углерода.
2) Установлена молекулярная формула вещества: 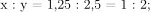 простейшая формула
простейшая формула  — это алкен или циклоалкан.
— это алкен или циклоалкан.
Так как вещество может быть получено при дегидратации спирта, то это алкен.
Для определения его молекулярной формулы напишем реакцию горения в общем виде

Вспомним, что плотность паров этого вещества (н.у.) составляет 3,125 г/л.
Значит  .
.
По уравнению реакции
получаем, что 
Молекулярная формула соединения 
3) Учитывая, что вещество может быть получено из третичного спирта, получаем структурную формулу вещества:

4) Составлено уравнение реакции дегидратации:
