Задание с ответами: химия. ЕГЭ — 2018
При разложении нитрата серебра выделилась смесь газов объемом 6,72 л (в пересчете на н. у.). Масса остатка составила 25 г. После этого остаток поместили в 50 мл воды и добавили 18,25 г 20%-ного раствора соляной кислоты. Определите массовую долю соляной кислоты в полученном растворе. В ответе напишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления.
При разложении нитрата серебра выделяется серебро и выделяются диоксид азота и кислород:
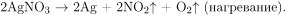
С соляной кислотой реагирует только нитрат серебра:
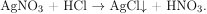
Серебро не взаимодействует с соляной кислотой.
Вычислим количество газов, образующихся при разложении нитрата серебра:
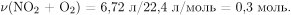
По уравнению реакции разложения нитрата серебра: 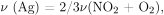 следовательно,
следовательно, 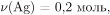
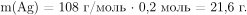 Масса остатка складывается из образовавшегося при разложении нитрата серебра металлического серебра и не прореагировавшей полностью соли, следовательно,
Масса остатка складывается из образовавшегося при разложении нитрата серебра металлического серебра и не прореагировавшей полностью соли, следовательно,
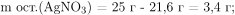
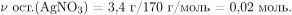
Вычислим массу и количество вещества соляной кислоты в ее исходном растворе:
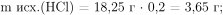
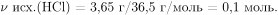
По уравнению взаимодействия нитрата серебра с соляной кислотой 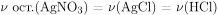 пошедшую на реакцию с ним. Следовательно, количество вещества и масса непрореагировавшей соляной кислоты:
пошедшую на реакцию с ним. Следовательно, количество вещества и масса непрореагировавшей соляной кислоты:
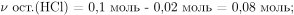
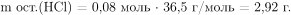
Вычислим массу выпавшего осадка 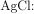
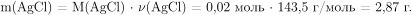
Масса получившегося раствора равна:
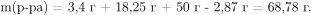
Массовая доля в получившемся растворе соляной кислоты равна:
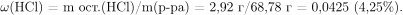
Правильный ответ: 4,25%.