Задание с ответами: химия. ЕГЭ — 2018
Фосфид кальция массой 36,4 г подвергли гидролизу. Образовавшийся газ сожгли в избытке кислорода. Полученную кислоту смешали с 50 мл 25%-ного раствора натриевой щелочи (плотность ρ = 1,28 г/см3). Определите состав образовавшейся соли и ее массовую долю в растворе. В ответе напишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления.
Фосфид кальция гидролизуется с образованием щелочи и выделением фосфина:
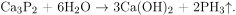
В присутствии кислорода фосфин самопроизвольно воспламеняется:
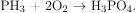
С гидроксидом натрия ортофосфорная кислота реагирует с образованием средней либо кислых солей ортофосфорной кислоты в зависимости от соотношений реагентов. Вычислим количество вещества фосфида кальция:
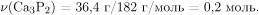
По уравнению гидролиза фосфида кальция 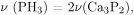 следовательно,
следовательно,
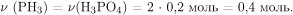
Вычислим массу раствора натриевой щелочи, массу и количество вещества гидроксида натрия:
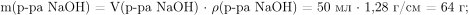
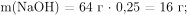
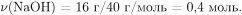
По условию задачи 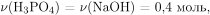 следовательно, продуктом реакции эквимолярных количеств щелочи и ортофосфорной кислоты является дигидроортофосфат натрия —
следовательно, продуктом реакции эквимолярных количеств щелочи и ортофосфорной кислоты является дигидроортофосфат натрия — 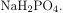
Уравнение реакции между эквимолярными количествами гидроксида натрия и ортофосфорной кислоты записывается в виде:
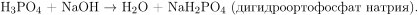
Для нахождения массы раствора необходимо вычислить массы ортофосфорной кислоты и дигидроортофосфата натрия:
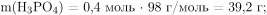
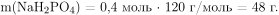
Вычислим массу образовавшегося раствора:
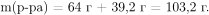
Определим массовую долю дигидроортофосфата натрия в образовавшемся растворе:
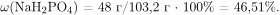
Правильный ответ: 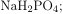 46,51%.
46,51%.