Задание с ответами: химия. ЕГЭ — 2018
При разложении образца карбоната бария выделился газ объемом 1,12 л (в пересчете на н. у.). Масса твердого остатка составила 27,35 г. После этого к остатку добавили 73 г 30%-ного раствора соляной кислоты. Определите массовую долю соляной кислоты в образовавшемся растворе. В ответе напишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления.
При разложении карбоната бария – соли слабой угольной кислоты образуется оксид бария и выделяется углекислый газ:
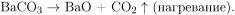
Вычислим количество углекислого газа, выделившегося при прокаливании карбоната бария: 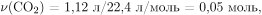 следовательно, в результате реакции разложения карбоната бария образовалось 0,05 моль оксида бария и прореагировало также 0,05 моль карбоната бария. Вычислим массу образовавшегося оксида бария:
следовательно, в результате реакции разложения карбоната бария образовалось 0,05 моль оксида бария и прореагировало также 0,05 моль карбоната бария. Вычислим массу образовавшегося оксида бария:
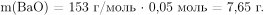
Вычислим массу и количество вещества оставшегося карбоната бария:
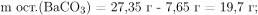
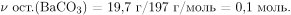
С соляной кислотой взаимодействуют и оксид бария, и карбонат бария:
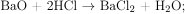
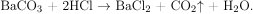
Вычислим количество вещества и массу хлороводорода, взаимодействующего с оксидом и карбонатом бария:
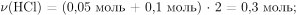
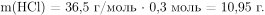
Вычислим массу оставшегося хлороводорода:
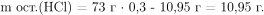
Масса раствора состоит из оставшейся хлороводородной кислоты, воды из ее раствора, воды образовавшейся в ходе реакций и хлорида бария:
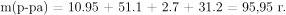
Массовая доля оставшейся соляной кислоты в растворе равна:
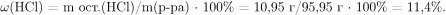
Правильный ответ: 11,4%.