Задание с ответами: химия. ЕГЭ — 2018
При разложении образца нитрата магния выделилась смесь газов объемом 10,08 л (в пересчете на н. у.). Масса остатка составила 69,36 г. После этого остаток поместили в 100 мл воды и добавили к нему 240 г 20%-ного раствора гидроксида натрия. Определите массовую долю гидроксида натрия в образовавшемся растворе. В ответе напишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления.
При разложении нитрата магния образуются оксид магния, диоксид азота и кислород:
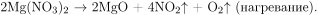
Вычислим количество смеси газов, выделившихся при прокаливании нитрата магния: 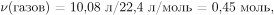 следовательно, в результате реакции разложения нитрата магния образовалось 0,18 моль оксида магния и прореагировало также 0,18 моль нитрата магния.
следовательно, в результате реакции разложения нитрата магния образовалось 0,18 моль оксида магния и прореагировало также 0,18 моль нитрата магния.
Вычислим массу образовавшегося оксида магния:
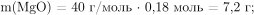
тогда масса и количество вещества оставшегося нитрата магния равна:
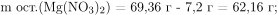
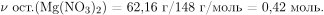
Плотность воды при н. у. 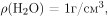 следовательно, ее масса в 100 мл равна 100 г. После того как остаток поместили в 100 мл воды, оставшийся нитрат магния растворился, оксид магния реагирует с водой только при кипячении, поэтому в раствор не переходит. С гидроксидом натрия реагирует нитрат магния с образованием осадка – не растворимого в воде гидроксида магния:
следовательно, ее масса в 100 мл равна 100 г. После того как остаток поместили в 100 мл воды, оставшийся нитрат магния растворился, оксид магния реагирует с водой только при кипячении, поэтому в раствор не переходит. С гидроксидом натрия реагирует нитрат магния с образованием осадка – не растворимого в воде гидроксида магния:
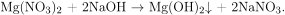
По уравнению реакции 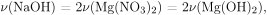 следовательно,
следовательно,
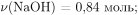
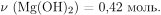
Вычислим массу и количество вещества гидроксида натрия, оставшегося при взаимодействии с нитратом магния, и массу гидроксида магния:
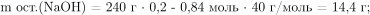
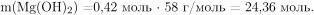
Вычислим массу образовавшегося раствора с учетом нерастворимости оксида и гидроксида магния:
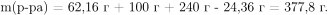
Определим массовую долю гидроксида натрия в образовавшемся растворе:
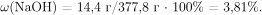
Правильный ответ: 3,81%.