Задание с ответами: химия. ЕГЭ — 2018
Хлорат калия разложили в присутствии катализатора — оксида марганца (IV), в результате чего выделился кислород объемом 6,72 л (в пересчете на н. у.). Масса сухого остатка составила 16 г. Этот остаток прореагировал с 170 г 30 %-ного раствора нитрата серебра. Определите массовую долю нитрата серебра в образовавшемся растворе. В ответе напишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления.
При разложении хлората калия в присутствии катализатора образуются хлорид калия и кислород:
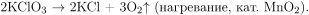
Вычислим количество вещества выделяющегося кислорода: 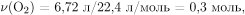 следовательно, по уравнению реакции образуется
следовательно, по уравнению реакции образуется 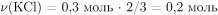 и расходуется 0,2 моль
и расходуется 0,2 моль 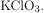
Вычислим массы образующегося хлорида калия:
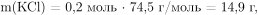
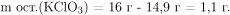
Таким образом, в результате прокаливания хлората калия образовалось 14,9 г хлорида калия и 1,1 г хлората калия не подверглась разложению. В воде растворяются и хлорат, и хлорид, однако с раствором нитрата серебра взаимодействует только хлорид калия, в результате чего выпадает белый творожистый осадок — хлорид серебра:
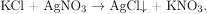
По уравнению реакции 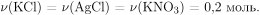 Поскольку нитрата серебра дан в избытке, по завершении реакции он остается в растворе. Вычислим его оставшуюся после реакции массу:
Поскольку нитрата серебра дан в избытке, по завершении реакции он остается в растворе. Вычислим его оставшуюся после реакции массу:
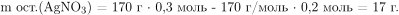
При расчете массы образующегося раствора необходимо учесть массу выпадающего в осадок хлорида серебра:
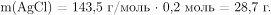
Вычислим массу образовавшегося раствора:
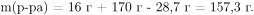
Массовая доля оставшегося нитрата серебра в растворе равна:
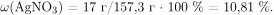
Правильный ответ: 10,81 %.