Гострий інфаркт міокарда, ускладнений гострою лівошлуночковою недостатністю: клініко-патогенетичні та хронобіологічні детермінанти, результати тривалого спостереження та медикаментозної корекції
МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ'Я УКРАЇНИ
ІВАНО-ФРАНКІВСЬКИЙ ДЕРЖАВНИЙ МЕДИЧНИЙ УНІВЕРСИТЕТ
Ілащук Тетяна Олександрівна
УДК 616.12-008.64-092+612.017.2]-07-08
Гострий інфаркт міокарда, ускладнений гострою ЛІВОШЛУНОЧКОВОЮ недостатністю: клініко-патогенетичні та хронобіологічні детермінанти, результати тривалого спостереження та медикаментозної корекції
14.01.11 – кардіологія
Автореферат
дисертації на здобуття наукового ступеня
доктора медичних наук
Івано-Франківськ – 2008
Дисертацією є рукопис.
Робота виконана в Буковинському державному медичному університеті МОЗ України, м. Чернівці.
|
Науковий консультант: Офіційні опоненти: |
доктор медичних наук, професор Тащук Віктор Корнійович, Буковинський державний медичний університет МОЗ України, кафедра кардіології, функціональної діагностики, лікувальної фізкультури та спортивної медицини, завідувач кафедри доктор медичних наук, професор Вакалюк Ігор Петрович, Івано-Франківський державний медичний університет МОЗ України, кафедра внутрішньої медицини з курсом сестринської справи, завідувач кафедри доктор медичних наук, профессор, академік АМН України, член-кореспондент НАН України, член-кореспондент РАМН Коркушко Олег Васильович, Інститут геронтології АМН України, відділ клінічної фізіології та патології внутрішніх органів, завідувач відділу доктор медичних наук, професор Шумаков Валентин Олександрович, Національний науковий центр “Інститут кардіології імені академіка М.Д.Стражеска” АМН України, відділ інфаркту міокарда та відновлювального лікування, завідувач відділу. |
Захист дисертації відбудеться “_8_” лютого 2008 р. об 11 годині на засіданні спеціалізованої вченої ради Д 20.601.01 при Івано-Франківському державному медичному університеті МОЗ України (76018, Івано-Франківськ, вул.Галицька, 2).
З дисертацією можна ознайомитись у бібліотеці Івано-Франківського державного медичного університету МОЗ України за адресою: 76018, Івано-Франківськ, вул.Галицька, 7.
Автореферат розісланий “_25___” __грудня__ 2007 р.
Вчений секретар
спеціалізованої вченої ради О.І.Дєльцова
доктор медичних наук, професор
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ
Актуальність теми. Розвиток наукового-технічного прогресу, впровадження у виробництво високоефективних технологій, процентне зростання кількості міського населення, економічні катаклізми в окремих державах, висока міграція населення спричиняють вплив стресових ситуацій на людський організм, що не може не вплинути на тривалість життя, структуру захворюваності, причини інвалідизації та смерті (К.М.Амосова, 2002; G. Davey Smith et al, 2006).
Із середини 20-го століття хвороби системи кровообігу (ХСК) у розвинених країнах світу за показниками медико-соціального навантаження вийшли на перше місце. В Україні за останні 10 років питома вага смертності від ХСК зросла з 56,5% до 62,5% (В.І.Коломієць та ін., 2003, В.М.Коваленко, 2006).
Одним із найпоширеніших ускладнень ІХС, зокрема інфаркту міокарда (ІМ), є серцева недостатність (СН). Згідно з експертними оцінками поширеність симптоматичної СН в європейській популяції коливається від 0,4 до 2% (M.E.Bertrand et al, 2002, Г.В.Яновський та ін., 2003). Спостерігається невпинне зростання смертності від СН у всіх вікових категоріях. Загалом у країнах, що входять до Європейської спільноти кардіологів, проживає 900 млн чоловік, серед яких щонайменш 10 млн страждають на СН. Приблизно стільки ж мають дисфункцію міокарда без ознак недостатності (Ю.В.Бєлов та ін., 2003). У разі неможливості адекватної корекції захворювання, що лежить в основі СН, її перебіг, незалежно від стадії, характеризується несприятливим прогнозом. Приблизно половина пацієнтів із СН помирає впродовж перших 4 років із моменту постановки діагнозу, а у випадку тяжкої СН стільки ж пацієнтів помирає впродовж першого року (D.Anthony, 2005, Л.Г.Воронков та ін., 2007). Як показано в недавніх дослідженнях (GRACE, 2001), пацієнти з асимптоматичною дисфункцією міокарда також мають несприятливий віддалений прогноз.
Упродовж останніх років у багатьох публікаціях у кардіологічних і загальномедичних виданнях було викладено нові принципи діагностики та лікування хронічної СН (ХСН), яка часто трапляється в практиці лікаря (К.М.Амосова, 1998; Ю.А.Карпов, 2005). Прогрес пізнання механізмів формування гострої СН (ГСН) був не таким відчутним, а традиції лікування цього клінічного синдрому виявилися значно сильнішими.
Основними факторами, що впливають на віддалений прогноз хворих, які перенесли ІМ та виписані зі стаціонару, вважають: важкість атеросклеротичного ураження коронарних артерій (КА) (із наявністю спонтанно рецидивуючої або індукованої ішемії міокарда); стійке порушення скоротливої функції лівого шлуночка (ЛШ) та виявлення рецидивуючої аритмії (Д.М.Аронов, 2000; О.М.Пархоменко та ін., 2005). Розвиток стійкої дисфункції ЛШ призводить до того, що ці пацієнти потрапляють у групу високого ризику серцевої смерті. Доведено, що смертність та ризик ішемічних ускладнень обернено пропорційні величині фракції викиду (ФВ) (J.J.Bax et al, 2006). Більш того, прогностична цінність цього показника однакова при лікуванні ІМ з використанням тромболітиків або без них. Таким чином, клінічна оцінка функції ЛШ у хворих, що перенесли ІМ, показана як для оцінки прогнозу, так і для вибору лікування.
В останні роки з’явилось багато публікацій, що свідчать про значне поліпшення виживаності серед пацієнтів із СН на фоні сучасної терапії (С.Г.Канорський та ін., 2005). У ході рандомізованих клінічних досліджень було показано, що правильно підібране лікування (наприклад, застосування інгібіторів ангіотензинперетворювального ферменту (ІАПФ)) дозволяє покращити віддалений прогноз у хворих з дисфункцією ЛШ після ІМ (К.М.Амосова, 2005).
До сьогоднішнього є невирішені питання відносно генезису симптомів СН. Факт патогенетичного взаємозв’язку СН та підвищеної експресії цитокінів у теперішній час уже ні в кого не викликає сумнівів (Є.Л.Насонов та ін., 1999), але не причинно-наслідковий характер цього зв’язку до кінця встановлено. Обговорюється питання, чи вказує звільнення прозапальних цитокінів, біомаркерів некрозу після вогнищевої ішемії на певний патогенетичний етап тканинного пошкодження, чи просто відображує величину ішемічного вогнища, а також яка їх роль у прогресуванні післяінфарктного ремоделювання серця в пацієнтів із СН (M.Azzavi et al, 1999).
У клініці серцево-судинних захворювань користуються загальноприйнятою класифікацією ГСН за Killip (Л.Т.Малая, 1999). Однак, ця класифікація є досить умовною й грунтується виключно на даних клінічного перебігу захворювання. Немає чіткого розділення між стадіями ГСН згідно з даними функціональних досліджень, зокрема ехокардіографії (ЕхоКГ) і даних біохімічного дослідження крові. Немає чітких даних відносно того, яким чином ГСН впливає на подальший прогноз, розвиток та стадію ХСН і чи є між цими процесами будь-який корелятивний зв’язок.
Таким чином, важливим моментом є оцінка впливу СН на віддалений прогноз ІМ при використанні сучасних методів лікування. Подальше вивчення цієї проблеми сприятиме зниженню смертності від ускладнень ГІМ і поліпшенню показників здоров’я населення України.
Зв’язок роботи з науковими програмами, планами, темами. Дисертаційна робота виконувалась у рамках науково-дослідної роботи кафедри кардіології, функціональної діагностики, лікувальної фізкультури та спортивної медицини Буковинського державного медичного університету на тему: “Статеві та вікові детермінанти ІХС: реєстр Північної Буковини, клініко-функціональні аспекти” (державний реєстраційний № 01.02U004226), відповідальним виконавцем якої є дисертант.
Мета і задачі дослідження. Метою даної роботи є створення прогностичної моделі перебігу ГІМ, ускладненого гострою лівошлуночковою недостатністю (ГЛШН) із оптимізацією схем лікування шляхом вивчення ранніх маркерів розвитку, прогресування СН та її запобігання з використанням реваскуляризації міокарда й ад′ювантної кардіопротекторної терапії.
Завдання дослідження:
Дослідити зміни рівнів прозапальних цитокінів (інтерлейкіну-1-б (Іл-1-б), інтерлейкіну-6 (Іл-6), інтерлейкіну-10 (Іл-10), туморнекротичного фактору- (ТНФ-), С-реактивного протеїну (СРП), неоптерину (Нп)), тропоніну-І (Тр-І), тестостерону (Тст), показників функціонального стану та реґіонарної скоротливості міокарда ЛШ серця при ГСН в залежності від стадії за Killip.
Визначити особливості функціонального стану міокарда в пацієнтів із ГСН в зіставленні з динамікою рівня прозапальних цитокінів, Тр-І та особливості їх взаємообумовленості при поєднанні з різними стадіями за Killip, із вивченням їх впливу на несприятливий прогноз захворювання.
Довести наявність взаємозв’язку між стадією та клінікою ГСН та наявністю і важкістю перебігу ХСН при тривалому спостереженні.
Вивчити стан ліпідного спектру крові та коронарного русла в пацієнтів із різними стадіями ГСН за Killip.
Прослідкувати основні хронобіологічні особливості перебігу різних стадій ГСН за річний інтервал часу та встановити вплив зовнішніх факторів на клінічний перебіг захворювання.
Оцінити взаємозв’язок добового профілю артеріального тиску (АТ) у пацієнтів із ГІМ, ускладненим ГСН, з активацією запального й некротичного процесу та прогресуванням ознак СН.
Порівняти ефективність застосування ранньої реваскуляризації міокарда шляхом стентування інфарктзв’язаної КА з тромболізисом, із вивченням їх впливу на прогноз захворювання.
Ідентифікувати плазмові показники прозапальних цитокінів, тропонінів, вивчити функціональний стан міокарда й показники регіональної скоротливості у хворих із різними стадіями ГСН до та після базової медикаментозної терапії та проаналізувати вплив на них раннього призначення внутрішньовенної форми кверцетину.
Об’єкт дослідження. Хворі на ГІМ, ускладнений ГЛШН, які поступили до відділення реанімації впродовж перших 24 год із моменту появи перших симптомів захворювання..
Предмет дослідження. ГЛШН у хворих га ГІМ, зв’язок із клінічним перебігом захворювання, формуванням зони некрозу міокарда, станом коронарного кровообігу, вираженість запальної відповіді та можливості профілактики шляхом ранньої реваскуляризації інфарктзв’язаної КА та кардіопротекторної терапії.
Методи дослідження. Поставлені завдання вирішувалися за допомогою клініко-інструментальних і лабораторних методів дослідження. Загальноклінічні дані були отримані шляхом аналізу скарг, анамнестичного й фізикального дослідження, проводились ЕхоКГ в М- та В-режимах, добове моніторування артеріального тиску (ДМАТ), коронароангіографія (КАГ). Лабораторні дослідження включали визначення рівня маркерів запалення (Іл-1-б, Іл-6, Іл-10, СРП, ТНФ-, Нп), Тр-І, Тст та основних біохімічних показників крові.
Наукова новизна одержаних результатів. На основі дослідження, що включало клінічну, лабораторну й інструментальну частини, уперше в Україні:
Визначено клініко-функціональні характеристики перебігу різних стадій ГСН з урахуванням рівнів прозапальних цитокінів, біомаркерів некрозу міокарда, показників функціонального стану та регіонарної скоротливості міокарда ЛШ.
Виявлено, що зростання рівня прозапальних цитокінів (Іл-1-б, Іл-6, Іл-10, СРП, ТНФ-, Нп) та Тр-І поряд із погіршенням вихідних даних ЕхоКГ сприяють зростанню ймовірності виникнення летальної події в пацієнтів із ГІМ та ГСН.
Установлено, що найбільш прогностично несприятливою для розвитку СН в післяінфарктному періоді (через 1 рік після виникнення ІМ) є сукупність наступних анамнестичних та клінічних ознак: стенокардія, що передувала інфаркту, артеріальна гіпертензія, передня локалізація ІМ, повторний інфаркт, наявність будь-яких ознак ГЛШН, а також збільшення вихідного рівня прозапальних цитокінів, СРП, Тр-І, а також початкове та поетапне зменшення загальної фракції викиду (ЗФВ) в досліджуваної категорії пацієнтів.
Виявлено, що розвиток летальних подій серед пацієнтів із ГІМ, ускладненим ГЛШН, має хроноритмологічне підґрунтя та підпорядковується циркадним та циркадіанним ритмам.
Досліджено, що реєстрація добового профілю АТ “non-dipper” у пацієнтів із ГІМ, ускладненим ГЛШН, є прогностично несприятливим фактором і асоціюється з активацією запального та некротичного процесу та прогресуванням ознак СН.
Включення ін’єкційної форми блокатора 5-ліпоксигенази кверцетину – препарату Корвітин – у комплексну терапію в пацієнтів із ГІМ та ГЛШН пригнічує активність цитокінової ланки патогенезу інфаркту, обмежує зону некрозу міокарда та сприяє зростанню насосної функції серця.
Практичне значення одержаних результатів. У процесі дослідження встановлені основні причини розвитку та прогресування ГЛШН та визначено її вплив на прогноз життя впродовж одного року спостереження. Проведена оцінка прогностичної значимості різних маркерів запалення та некрозу у хворих на ГІМ та ГЛШН. Проведена оцінка впливу різних видів реваскуляризаційних втручань, а також препаратів, які мають мембранопротекторні властивості, на частоту розвитку летальних подій та прогресування ознак СН в даної категорії хворих. За матеріалами дисертації отримано два патенти України на корисну модель “Спосіб лікування гострого інфаркту міокарда, ускладненого гострою серцевою недостатністю” (№ 25242) та “Спосіб прогнозування летального випадку у пацієнтів з гострою серцевою недостатністю” (№ 25243).
Впровадження результатів дослідження. Основні результати дисертаційної роботи використовуються в навчальному процесі на кафедрах терапевтичного профілю Буковинського державного медичного університету, Вінницького національного медичного університету ім.М.І.Пирогова, Тернопільського державного медичного університету імені Горбачевського, Івано-Франківського державного медичного університету; впроваджені в практику профільних відділень Закарпатського, Івано-Франківського, Чернівецького обласних кардіологічних диспансерів, Луцької міської клінічної лікарні, міської клінічної лікарні №1 м. Вінниці, що підтверджено відповідними актами впроваджень.
Особистий внесок здобувача. Дисертація являє собою наукову працю здобувача. Внесок автора в її виконання полягає в виборі напрямку, обсягу та методів дослідження, формуванні мети та завдань роботи, визначенні груп обстежуваних хворих, проведенні клінічних та інструментальних досліджень, створенні бази даних, обробці й узагальненні результатів дослідження, формулюванні висновків та оформленні дисертації. Автор самостійно обстежила значну частину хворих, контролювала їх лікування та обстеження, здійснювала моніторинг клінічного стану, проводила ЕхоКГ частині хворих, здійснювала патентно-інформаційний пошук, брала участь у формуванні матеріалів до статей і тезів, самостійно підготувала дисертаційну роботу до друку. Матеріали, положення та висновки кандидатської дисертації автором не використовувались.
Апробація результатів дисертації. Матеріали дисертаційного дослідження оприлюднені на 88-й підсумковій науковій конференції професорсько-викладацького персоналу Буковинського державного медичного університету (Чернівці, 2007), кафедр внутрішніх хвороб, Чернівецького обласного товариства терапевтів ім. акад. В.Х.Василенка, асоціації кардіологів Північної Буковини, IV Національному Конгресі патофізіологів України (Чернівці, 2004), VII Національному конгресі кардіологів України (Дніпропетровськ, 2004), І Національному конгресі лікарів внутрішньої медицини (Київ, 2005), Міжнародному форумі “Кардіологія вчора, сьогодні, завтра” (Київ, 2006), Науково-практичній конференції “Первинна та вторинна профілактика цереброваскулярних ускладнень артеріальної гіпертензії” (Київ, 2006), Об’єднаному пленумі правлінь асоціацій кардіологів, серцево-судинних хірургів, нейрохірургів та невропатологів України (Київ, 2006), Регіональній науково-практичній конференції “Артеріальна гіпертензія: виявлення, поширеність, диспансеризація, профілактика та лікування” (Івано-Франківськ, 2004), Українській науково-практичній конференції “Профілактика і лікування артеріальної гіпертензії в Україні” (Київ, 2004), Науково-практичній конференції з міжнародною участю “Сучасні методи діагностики і лікування в клініці внутрішніх хвороб” (Вінниця, 2004), Регіональній науково-практичній конференції “Артеріальна гіпертензія: виявлення, поширеність, диспансеризація, профілактика та лікування” (Івано-Франківськ, 2005), VIII з’їзді Всеукраїнського лікарського товариства (Івано-Франківськ, 2005), ІІ науково-практичній конференції з міжнародною участю “Оздоровчі ресурси Карпат і прилеглих регіонів” (Чернівці, 2005), Науково-практичній конференції з міжнародною участю “Сучасна медична наука обличчям до терапевтичної практики” (Харків, 2005), Регіональній науково-практичній конференції “Артеріальна гіпертензія: виявлення, поширеність, диспансеризація, профілактика та лікування” (Івано-Франківськ, 2006), Регіональній науково-практичній конференції “Новітні погляди в лікуванні гострих коронарних інцидентів” (Чернівці, 2006), Науково-практичній конференції з міжнародною участю “Хронобіологія і хрономедицина: теоретичні та клінічні перспективи” (Чернівці, 2006).
Публікації. За матеріалами дисертації опубліковано 37 наукових праць, із яких 18 статей (із них 8 одноосібних) – у фахових виданнях, рекомендованих ВАК України, 2 патенти України на корисну модель та 17 тез – у матеріалах наукових конгресів, пленумів, конференцій.
Структура та обсяг дисертації. Дисертація викладена на 326 сторінках машинописного тексту (з них 276 – основного), містить 30 таблиць та 67 рисунків. Робота складається зі вступу, огляду літератури, клінічної характеристики обстежених хворих та опису методик дослідження, трьох розділів результатів власних досліджень, аналізу та узагальнення отриманих результатів, висновків та практичних рекомендацій. Список використаних джерел містить 334 літературні найменування, із яких 64 роботи кирилицею та 270 - латиницею.
ОСНОВНИЙ ЗМІСТ РОБОТИ
Матеріал і методи. Робота базується на обстеженні 368 хворих на ГІМ, ускладнений ГЛШН. Із них 312 пацієнтів надійшли в блок кардіореанімації Чернівецького обласного кардіологічного диспансеру в період 2003-2005 рр. та спостерігалися на кафедрі кардіології, функціональної діагностики, лікувальної фізкультури та спортивної медицини Буковинського державного медичного університету впродовж одного року після поступлення. Окрім того, ретроспективно проаналізовано результати спостереження за 56 пацієнтами з ГІМ, ускладненим ГЛШН, що проходили обстеження та лікування в центральних кардіологічних клініках м.Москви (Росія). У результаті комплексного клініко-інструментального обстеження, яке включало в себе детальний збір скарг, анамнезу, ретельне об’єктивне обстеження, електрокардіограму в динаміці, лабораторні дослідження, ЕхоКГ, селективну КАГ, встановлено, що трансмуральний ГІМ трапився в 141 (38,32%) випадку, великовогнищевий ГІМ – у 166 (45,11%) і дрібновогнищевий ГІМ – у 61 (16,57%), тобто частота розподілу Q- та неQ-форм ГІМ відповідала співвідношенню 83,43% / 16,57%.
Включення пацієнтів до груп, що аналізувалися, було проведено згідно зі скринінговим розподілом хворих, які доставлені в стаціонар службою “швидкої допомоги” й були відібрані випадковим методом відповідно до надходження. Усі пацієнти спостерігалися впродовж 28 діб перебування в стаціонарі та впродовж 1-го року після виписки додому. Проводилась реєстрація всіх первинних і вторинних кінцевих точок (смерть пацієнта, рецидив та повторний ГІМ) упродовж 1-го року з моменту виникнення ГІМ, ускладненого ГЛШН.
Обстеження, що було проведено пацієнтам, які увійшли до групи спостереження та лікування, включало в себе ретельний аналіз клінічних проявів патології, що вивчалася в рамках створення реєстру ГІМ, зокрема, аналіз скарг, анамнезу життя та захворювання, оцінка динаміки ЕКГ у першу – другу, 14-у, 28-у доби та через рік після перенесеного ГІМ, проведення ЕхоКГ у М- та В- режимах із оцінкою регіонарної скоротливості ЛШ в 12 сегментах у першу – другу, 14-у та 28-у доби, лабораторні дослідження з оцінкою загального аналізу крові, ферментів, коагулограми, Іл-1-б, Іл-6, Іл-10, ТНФ-, Нп, Тр-І, СРП, Тст, що визначали імуноферментним методом у першу – другу добу ГІМ та після проведеного лікування. Також проаналізовано результати КАГ, що проводилась у 56 пацієнтів у перші доби ІМ з наступною реваскуляризацією шляхом стентування в 33 (8,55%) або тромболізису в 23 (6,25%) випадках.
Як свідчить аналіз локалізації ІМ, передня стінка була некротизована в 25,16% випадків, задня – у 22,52%, перетинка – у 21,74%, верхівка – у 18,71%, бічна стінка – у 11,87% пацієнтів.
Серед 368 обстежених пацієнтів було 259 (70,38%) чоловіків та 109 (29,62%) жінок. Середній вік обстежених хворих становив 59,6+1,76 року (від 22 до 93 років). АГ було зафіксовано в 128 (34,78%) пацієнтів. Тривалість ІХС, за даними анамнезу, коливалась від 3 до 25 років (у середньому 9,78+1,12 року). ГІМ в анамнезі і, відповідно, постінфарктний кардіосклероз зареєстрований у 73 (19,84%) пацієнтів.
У найгострішому періоді ІМ оцінювався стан гемодинаміки та клас ГСН з використанням класифікації T. Killip (1967). Так, ознаки ГСН Killip І реєструвались у 117 (31,79%) пацієнтів, Killip ІІ – у 115 (31,25%), Killip ІІІ – у 89 (24,19%) та Killip ІV – у 47 (12,77%) хворих на ГІМ.
Упродовж 1-го року спостереження визначено наступний розподіл діагнозів відносно ХСН: СН І класу за NYHA зафіксовано в 34,67% пацієнтів, СН ІІ – у 25,18%, СН ІІІ – у 22,63% та СН VI – у 17,52% пацієнтів. Розподіл супутньої соматичної патології відбувався наступним чином: цукровий діабет ІІ типу трапився в 64 (17,39%) пацієнтів, захворювання шлунково-кишкового тракту (гастрити, виразкова хвороба, некалькульозний холецистит) – у 68 (18,49%), ішемічні інсульти в анамнезі – у 22 (5,98%) випадках. Аналіз факторів ризику в розвитку серцево-судинних подій показав, що активно курили 114 (30,98%) пацієнтів, зловживали алкоголем 26 (7,07%), мали обтяжену спадковість (наявність ІХС або АГ в одного з батьків) 174 (47,28%) особи, страждали надмірною вагою тіла 92 (25%) хворих.
Серед 368 пацієнтів, що підлягали аналізу, за весь період спостереження померло 123 (33,42%) особи, зокрема 94 (25,54%) хворих – упродовж 28 діб перебування в стаціонарі, а 29 (7,88%) – за рік спостереження.
Комплекс обстежень, що були використані з метою об’єктивізації стану 368 пацієнтів, які надійшли в Чернівецький обласний кардіологічний диспансер та кардіологічні відділення центральних клінік м.Москви (Росія), складався з клініко-лабораторної частини (ретельний аналіз скарг, даних анамнезу життя та захворювання, обстеження крові з імуноферментною частиною, що виконана на базі медичного центру “Авіценна”, м. Чернівці) та функціональної (ЕКГ, ЕхоКГ в М- та В-режимах, які було виконано на кафедрі кардіології, функціональної діагностики, лікувальної фізкультури і спортивної медицини Буковинського державного медичного університету) у пацієнтів із ГІМ, ускладненим ГЛШН, у середньому в першу-другу, 14-ту та 28-му доби та через один рік після перенесеного ГІМ. У 56 пацієнтів ретроспективно оцінено результати проведення селективної багатопроекційної КАГ і екстреної реканалізації інфарктзалежної КА.
ЕхоКГ-дослідження виконувалося з урахуванням рекомендацій Європейської та Американської асоціацій кардіологів, у положенні хворого на спині та на лівому боці, із парастернального доступу, по довгій та короткій вісях, у першу-третю, 14-ту та 28-му доби перебігу ГІМ, ускладненого ГЛШН, і через один рік спостереження. ЕхоКГ проводили з використанням наступного апаратного забезпечення – ультразвуковий діагностичний апарат “INTERSPEС XL” (“BBC Medical Electronic AB”, США). Дослідження проводили в ранішні години, в парастернальній позиції по довгій вісі ЛШ на 1-й, 14-й, 28-й добі та через рік після перенесеного ГІМ, спочатку в М-режимі, далі в В-режимі за варіантом секторального сканування в 4-камерній проекції.
Окремий підрахунок реґіонарної скоротливості ЛШ проводився з використанням комп’ютерного графічного напівавтоматичного аналізу методом суміщення центрів ваги для діастоли і систоли, проведення апроксимації за довгою віссю, використанням автоматичного розподілу суміщеної фігури на 12 сегментів і формули для конусоподібної моделі з розрахунками реґіональної фракції викиду (РФВ, %) відповідно до методу H. T. Dodge для “площі/довгої вісі”.
Визначення вмісту Іл-1-б, Іл-6, Іл-10, ТНФ-, Нп, Тр-І, СРП, Тст проводили з урахуванням інструкцій до імуноферментного аналізу двічі (при надходженні й на фоні проведеного лікування) на базі медико-діагностичного центру “Авіценна” (м.Чернівці). Апарат “Уніплан” (“Пікон”, Росія) сертифікований та метрологічно повірений.
Динамічне дослідження вмісту Іл-1-б, Іл-6, Іл-10, ТНФ-, Нп, Тр-І, СРП, Тст проведено на фоні курсу антиішемічного лікування з використанням базової терапії (низькомолекулярні гепарини, антиагреганти, в-адреноблокатори, ІАПФ, статини, пролонговані нітрати), до якої додано внутрішньовенний інгібітор 5-ліпоксигенази кверцетин – препарат українського виробництва – Корвітин.
Проводився аналіз результатів селективної багатопроекційної КАГ, яка була виконана в 56 пацієнтів з ГІМ та ГСН на базі відділень інтервенційної кардіології центральних клінік м. Москви (Росія). Аналізувалися історії хвороб, що зберігаються в архіві Державного закладу “Міська поліклініка №220 Департаменту охорони здоров’я м. Москви”. Під час аналізу коронарограми оцінювались: переважний тип кровопостачання серця, кількість ушкодженних КА, локалізація стенозу, кількість ділянок стенозу, його ступінь та поширеність.
Із метою виявлення типу добової кривої АТ у 84 пацієнтів із ГІМ, ускладненим ГЛШН, використано метод ДМАТ. ДМАТ проводилось за допомогою моніторного комплексу ABPM-02/M (“Meditech”, Угорщина), який забеспечував автоматичне вимірювання систолічного АТ (САТ), діастолічного АТ (ДАТ) та частоти серцевих скорочень (ЧСС) впродовж доби, а також збереження даних в пам’яті прибору. Інтервали між вимірюваннями становили: у денний час – кожні 15 хв, у нічний – кожні 30 хв. Отримані дані аналізували з урахуванням щоденників пацієнтів за комп’ютерною програмою (Арабидзе Г.Г., Атьков О.Ю., 1997; Горбунов В.М., 1997; Сіренко Ю.М., Гранич В.М., 1999; Свищенко Е.П., Коваленко В.Н., 2001).
Математичний аналіз отриманих результатів проводився з оцінкою середнього значення, стандартної помилки середнього, вірогідність кількісних параметрів визначена в межах перевірки “нульової гіпотези” з використанням t-критерію Стьюдента з оцінкою за рівня значущості для р<0,05 (при використанні парного t-критерію Стьюдента для аналізу в двох залежних вибірках при нормальному розподілі масивів та t-критерію Вілкоксона – при ненормальному розподілі масивів; у двох незалежних вибірках при нормальному розподілі двовибіркового t-критерію Стьюдента, двох незалежних вибірках при ненормальному розподілі – U-критерію Вілкоксона). Із метою математичного прогнозування використали зіставлення корелятивних взаємовідношень із оцінкою можливостей кореляційних зіставлень із використанням тестів Спірмена і Пірсона й одночасної побудови математичної залежності між гемостазіологічними та гемодинамічними показниками, що вивчаються. Вплив перемінної на ймовірність клінічної події визначався відношенням шансів та відповідним 95% інтервалом довіри (ІД), що були розраховані методом бінарної логістичної регресії, як в однофакторному, так і в багатофакторному регресійному аналізі. Для даного математичного аналізу використані можливості персонального комп’ютера РС “Пентіум” з математично-інформаційними пакетами електронних баз даних і їх обробки “Microsoft Excel 97” (Microsoft), “Statistica for Windows 5.0” (StatGraphics Plus 5.1, США).
Результати дослідження. На першому етапі дослідження нами було проведено аналіз обстеження 368 пацієнтів із ГІМ, який ускладнився ГЛШН І – ІV класів за Т.Кіllip. Гендерний аналіз показав, що кількість чоловіків переважала в усіх чотирьох групах, причому у співвідношенні чоловіки / жінки число чоловіків збільшувалося зі зростанням класу ГСН. Щодо вікового розподілу пацієнтів, було виявлено, що в групі Killip І середній вік пацієнтів складав 59,3+0,96 року, Killip ІІ – 61,7+0,67 року, Killip ІІІ – 63,7+0,78 та Killip ІV – 65,5+0,93 року. Таким чином, можна зробити висновок, що ГЛШН має більш тяжкий перебіг в осіб старшого віку.
Аналіз розподілу Q- неQ-форм ІМ показав, що зі зростанням класу ГЛШН збільшувалась кількість пацієнтів із зареєстрованим Q-ІМ. Щодо розподілу локалізації ураження в обстежених пацієнтів, виявлено збільшення частоти реєстрації ГІМ передньої стінки ЛШ в пацієнтів із більш важким перебігом ГСН. Нами виявлено, що наявність попереднього ГІМ в анамнезі ускладнює перебіг ГЛШН.
Аналіз летальності впродовж 1-го року спостереження свідчив, що загальний показник летальності був найвищим у групі Killip IV та складав 91,11%. Розподіл факторів ризику в пацієнтів з ГЛШН різних класів показав, що зі збільшенням класу ГСН зростає відсоток пацієнтів, які активно курили, мали обтяжену спадковість із ІХС або надмірну масу тіла.
Погрупове порівняння загальноклінічного аналізу крові не показало вірогідних відмінностей за переважною кількістю показників між групами пацієнтів без видимих клінічних ознак ГСН та з клінічно виявленою ГСН. Вірогідні відмінності виявлені між рівнем глюкози крові (p>1->>IV><0,05), загального холестерину (p>1- >>IV> <0,05) та сегментоядерних нейтрофілів (p>1- >>IV> <0,05).
На наступному етапі проаналізовано значення середнього рівня біомаркерів запалення та некрозу серцевого м’яза в обстежених пацієнтів у залежності від класу ГЛШН. Нами визначався середній рівень Іл-1-б, Іл-6, Іл -10, ТНФ-, Нп, ТрІ, СРП та чоловічого статевого гормону Тст на 1 добу перебування пацієнтів у стаціонарі та після адекватного комплексного патогенетичного лікування. Для зручності порівняння обстежені пацієнти були розділені наступним чином: група 1 (117 пацієнтів) – пацієнти без видимих клінічних ознак ГЛШН, група 2 (251 пацієнт) – пацієнти з вираженими проявами ГЛШН (Killip II – IV). Порівнювалися міжгрупові рівні досліджуваних біомаркерів та внутрішньогрупова динаміка цих показників у процесі лікування. Аналіз вмісту прозапальних цитокінів Іл-1-б, Іл-6 та ТНФ- та протизапального цитокіну Іл-10 у пацієнтів із ГІМ, перебіг якого ускладнився ГЛШН, показав, що в пацієнтів обох груп спостерігається значне збільшення порівняно з нормою рівнів Іл-1-б (45,06+6,35 проти 19,68+2,96 пг/мл, р<0,01), Іл-6 (45,69+7,1 проти 13,14+3,05 пг/мл, р<0,01) та ТНФ- (59,12+3,08 проти 42,85+2,22 пг/мл, р<0,01), причому в пацієнтів з клінічно вираженими проявами ГЛШН усі три показники були вірогідно більшими, ніж у пацієнтів без клінічних ознак ГЛШН. Також нами було виявлено несуттєво вищий рівень Іл-10 у пацієнтів без клінічних ознак ГЛШН (5,47+1,63 (група 1) проти 3,89+0,72 пг/мл (група 2), р>0,5), однак упродовж лікування середні значення Іл-10 в обох групах вірогідно не змінилися.
Аналіз вмісту Нп в сироватці крові пацієнтів із різними класами ГЛШН показав, що його рівень перевищував нормативний в обох групах (23,82+4,15 проти 12,02+2,80 нмоль/л, р<0,05), причому в групі 2 він був вірогідно вищим у порівнянні з групою 1. Після лікування відбулося вірогідне зниження рівня Нп в обох групах, але в групі 2 цей показник залишався вірогідно більшим, у порівнянні з групою 1 (11,49+2,12 проти 5,6+1,12 нмоль/л, р<0,02). Нами вивчався рівень Тр-І, СРП і Тст у пацієнтів з різними класами ГЛШН. Виявлено, що у пацієнтів групи 2 середній рівень Тр-І (37,41+6,49 проти 25,52+4,22 нг/мл, р<0,01) та СРП (0,11+0,02 (група 1) проти 0,17+0,02 (група 2) мг/л, р<0,05) був вірогідно вищим, ніж у пацієнтів групи 1.
На наступному етапі нами оцінювались основні ЕхоКГ показники в пацієнтів із ГІМ, ускладненим ГЛШН, у залежності від ступеня її вираженості на 1-у – 2-у, 14-у, 28-у добу перебування в стаціонарі та через 1 рік після перенесеного ГІМ. Виявлено вірогідно меншу ЗФВ у пацієнтів групи 2 в порівнянні з групою 1 на всіх етапах спостереження. Також звертає на себе увагу вірогідний приріст ЗФВ в пацієнтів групи 1 через 28 діб перебування в стаціонарі (Д% +10,82%, р<0,05) та невірогідне (Д% -4,26%, р>0,05) його зменшення через 1 рік після перенесеного ГІМ. ЗФВ у пацієнтів групи 2 вірогідно не змінювалась (р>0,05) на всіх етапах спостереження, але спостерігався її незначний приріст (Д% +6,72%, р>0,05) упродовж перших 28 діб ГІМ та поступове зменшення цього показника (Д% – 7,67%, р>0,05) через 1 рік спостереження. Можна припустити, що чоловіча стать, старший вік, передня локалізація ІМ, наявність післяінфарктного кардіосклерозу в анамнезі є незалежними предикторами більш важкого перебігу ГЛШН. Водночас клінічно виражена ГЛШН характеризується більш високим рівнем прозапальних цитокінів (Іл-1-б, Іл-6, ТНФ-, Нп), Тр-І, СРП, Тст та зниженням ЗФВ порівняно з неускладненим перебігом ГІМ.
Однією з найважливіших проблем сучасної кардіології є стратифікація ризику з метою своєчасного проведення профілактичних заходів у пацієнтів, які перенесли ГІМ. Віддалений прогноз пацієнтів ііз ГІМ багато в чому визначається характером перебігу захворювання в перші години та дні, тому дуже важливим моментом є прогнозування подальшого перебігу захворювання та ймовірності розвитку тих чи інших ускладнень у гострому періоді ІМ.
Нами була зроблена спроба систематизувати обстежених пацієнтів у залежності від ймовірності виникнення летальної події впродовж 1-го року спостереження та визначення найбільш вагомих факторів з указанням їх частки в розвитку летального виходу. Встановлено, що серед 368 обстежених пацієнтів за весь період спостереження померло 123 (33,42%) особи. Ретроспективний аналіз ЕКГ-динаміки показав, що в переважної частини померлих пацієнтів (76,59%) було зареєстровано ГІМ передньої локалізації й лише в 23,41% пацієнтів – ГІМ задньої локалізації. Гендерний та віковий аналіз групи госпітальної летальності показав, що серед померлих пацієнтів переважали чоловіки (72,34% проти 27,66% жінок), середній вік померлих хворих становив 67,24+ 1,92 року.
Із метою створення прогностичних моделей ГІМ, перебіг якого ускладнився ГЛШН, всіх пацієнтів розділено на дві групи: група 1 (245 пацієнтів) – пацієнти зі сприятливим виходом ГІМ та група 2 (123 особи) – пацієнти з летальним виходом.
На наступному етапі дослідження нами було проаналізовано загальнохарактерологічні дані обстежених пацієнтів, у залежності від виходу захворювання. Встановлено, що померлі пацієнти були в середньому на 9 років старшими від пацієнтів зі сприятливим виходом захворювання. Серед них переважали чоловіки (р<0,001). Окрім того серед пацієнтів групи 2 значно частіше реєструвався повторний ГІМ (79,6% проти 39,19% в групі 1, р<0,001). Ознаки ГЛШН ІІ – ІV класу за T. Killip з вірогідно більшою частотою реєструвалися серед пацієнтів групи 2 (р<0,001). Наявність АГ та ЦД в анамнезі також із вірогідно більшою частотою реєструвалася серед пацієнтів групи 2 (р<0,01). Аналіз поширеності факторів ризику серед пацієнтів обох груп показав вірогідне переважання активного куріння (р<0,01) та ожиріння (р<0,001) також серед пацієнтів групи 2.
Результати однофакторного регресійного аналізу вказують на те, що ризик виникнення летальної події в обстежених пацієнтів збільшувався з віком: на кожні 5 років після 50 припадало збільшення ризику в 1,5 рази. Також ризик виникнення летальної події збільшувався в 2 рази з кожним збільшенням класу ГЛШН за Killip, в 1,02 рази при збільшенні ЧСС надходження на 10 уд/хв. після 60 уд/хв., у 1,3 рази в пацієнтів із цукровим діабетом, у 1,15 рази при наявності ожиріння, у 3 рази в пацієнтів зі хронічною СН, у 1,2 рази при реєстрації в 1-у – 2-у добу поступлення ЗФВ менше 40% та в 4,5 рази при передній локалізації ІМ (табл. 1).
Таблиця 1
Предиктори летальної події в пацієнтів із ГІМ, ускладненим ГЛШН
(результати однофакторного регресійного аналізу)
|
Ознака |
Відношення шансів (95% ІД) |
|
Вік, + 5 років (після 50) |
1,5 (1,4; 1,8) |
|
Killip, + 1 клас |
2,0 (1,2; 2,9) |
|
ЧСС, + 10 уд/хв (>60 уд/хв.) |
1,02 (1,01; 1,03) |
|
Цукровий діабет в анамнезі |
1,3 (1,2; 1,4) |
|
Ожиріння |
1,15 (0,48; 2,76) |
|
ХСН в анамнезі |
3,0 (1,4; 6,6) |
|
ЗФВ ≤ 40% |
1,2 (1,1; 1,3) |
|
Передня локалізація ГІМ |
4,5 (2,2; 9,4) |
Нами проаналізовано, яким чином співвідносився вміст про- та протизапальних цитокінів у пацієнтів із ГІМ, ускладненим ГЛШН, у залежності від виходу захворювання. Встановлено, що рівень Іл-1-б, Іл-6, ТНФ-, Нп, Тр-І та СРП був вірогідно вищим у пацієнтів групи 2, рівень Іл-10 був дещо вищим у пацієнтів групи 1, а Тст переважав також у групі 2, хоча дані вірогідно не розрізнялися. Погруповий аналіз даних ЕхоКГ показав вірогідне зменшення ЗФВ у пацієнтів групи 2 на 1-у – 2-у добу перебування в стаціонарі та більш оптимальний вихідний характер регіональної скоротливості в групі 1.
Результати однофакторного регресійного аналізу вказують на те, що ризик виникнення летальної події в пацієнтів із ГІМ та ГЛШН збільшувався зі зростанням рівню СРП в 1,3 рази, ТНФ- – у 2,4 рази, Нп – у 2,6 рази, Іл-1-б + Іл-6 – у 3,6 рази, Тр-І – у 3,2 рази (рис. 1).
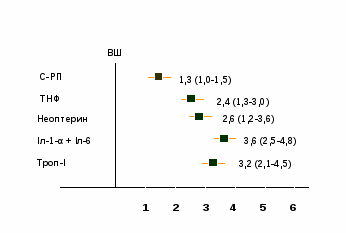
Рис. 1. Предиктори летальної події в пацієнтів із ГІМ, ускладненим ГЛШН.
Таким чином, старший вік пацієнтів, більш високий клас ГЛШН, наявність ЦД та СН в анамнезі, передня локалізація ІМ, куріння та ожиріння, ЗФВ менше 40% є незалежними предикторами виникнення летальної події в пацієнтів із ГІМ та ГЛШН. Окрім того, підвищення рівня прозапальних цитокінів (Іл-1-б, Іл-6, ТНФ-, Нп, СРП) та Тр-І поряд із погіршенням вихідних даних ЕхоКГ також сприяють зростанню ймовірності виникнення летальної події в даної категорії пацієнтів.
Дані зарубіжних епідеміологічних досліджень свідчать про те, що СН залишається одним із найбільш поширених, прогресуючих та прогностично несприятливих захворювань серцево-судинної системи. Спільним для всіх епідеміологічних досліджень є висновок щодо різкого зростання частоти виявлення СН в зв’язку зі збільшенням віку пацієнтів. Поряді з цим, прогноз пацієнтів із СН надалі залишається одним із найбільш несприятливих. Отже, у зв’язку з тим, що СН істотно впливає на вихід захворювання, її прогнозування в пацієнтів, що перенесли ГІМ, стає самостійною клінічною задачею.
У ході дослідження нами виявлено, що ознаки СН І класу за NYHA через 1 рік після виникнення ГІМ зафіксовано в 34,67% пацієнтів, СН ІІ – у 25,18%, СН ІІІ – у 22,63% та СН VI – у 17,52% пацієнтів. Для зручності аналізу в подальшому пацієнти з ХСН І класу були об’єднані в групу А, а пацієнти з клінічними та Ехо-КГ ознаками ХСН (СН ІІ, СН ІІІ та ІV класів), що виявлені через 1 рік спостереження, були об’єднані в групу В.
Віковий аналіз груп показав, що група А характеризувалась молодшим віком пацієнтів (58,24+0,96 року) порівняно з групою В – 64,46+0,87 року. Гендерний розподіл пацієнтів свідчить про те, що в обох групах кількісно переважали чоловіки, але співвідношення чоловіків та жінок було наступним: у групі А – 68,42% чоловіків та 31,58% жінок, а в групі В – 69,27% чоловіків та 30,73% жінок. Окрім того виявлено, що пацієнти групи В характеризувалися більш частим анамнезом стенокардії, що виникла більше року до розвитку ІМ та АГ, а також більш частою передньою локалізацією ІМ та розвитком ознак ГЛШН. Усі ці ознаки носили несприятливий прогностичний характер у плані розвитку СН у віддаленому післяінфарктному періоді, про що свідчать дані одно- та двофакторного дисперсійного аналізу.
Нами проведене ретроспективне погрупове порівняння загальноклінічного аналізу крові в обстежених пацієнтів. Виявлено відсутність вірогідних відмінностей за переважною кількістю показників, окрім вірогідного зменшення кількості еритроцитів, збільшення - лейкоцитів і швидкості осідання еритроцитів у пацієнтів групи В у зіставленні з групою А. Аналіз вихідного вмісту прозапальних цитокінів (Іл-1-б, Іл-6, ТНФ-, Нп), СРП, Тр-І і Тст показав вірогідне їх збільшення в групі пацієнтів із виявленою через 1 рік СН, порівняно з пацієнтами без клінічно виявленої СН. Аналіз даних ЕхоКГ, проведеної на 1-у – 2-у, 14-у, 28-у добу та через 1 рік після перенесеного ІМ, а також даних реґіонарної скоротливості ЛШ на 1-у – 2-у добу ГІМ, свідчив про більш оптимальні гемодинамічні умови та більш сприятливий вихідний характер регіональної скоротливості у пацієнтів групи А порівняно з групою В. Поряд із цим аналіз наявності та сили кореляційного зв’язку між показниками, що характеризують систолічну дисфункцію ЛШ, і наявністю та вираженістю СН в післяінфарктному періоді через 1 рік спостереження показав, що найбільш тісна кореляція існувала між величинами кінцево-систолічного об’єму (КСО) та кінцево-діастолічного об’єму (КДО), а, починаючи з 14-ї доби ІМ і ЗФВ та важкістю СН в післяінфарктному періоді. На 28-у добу ГІМ кореляція всіх указаних показників ставала вірогідною. Таким чином, найбільш прогностично несприятливою для розвитку СН у післяінфарктному періоді (через 1 рік після виникнення ІМ) є сукупність наступних анамнестичних та клінічних ознак: стенокардія, що передувала ІМ, артеріальна гіпертензія, передня локалізація ІМ, повторний ІМ, наявність будь-яких ознак ГЛШН, а також збільшення вихідного рівня прозапальних цитокінів, СРП, Тр-І та початкове й поетапне зменшення ЗФВ у пацієнтів із ГІМ, перебіг якого ускладнився ГЛШН.
На наступному етапі дослідження нами проаналізовано результати КАГ 56 пацієнтів із ГІМ, ускладненим ГЛШН, що проходили обстеження та лікування в центральних кардіологічних клініках м.Москви (Росія). В усіх пацієнтів проведено селективну багатопроекційну КАГ за методикою M.Judkins. Обстежених пацієнтів було розділено на дві групи залежно від вираженості ГЛШН: група І (34 особи) – пацієнти без видимих клінічних ознак ГЛШН або з помірно вираженою ГЛШН (Killip I – ІІ) та група ІІ (22 хворих) – пацієнти з вираженими проявами ГЛШН (Killip IIІ – IV).
Встановлено, що групи пацієнтів із ГІМ, ускладненим ГЛШН, які були виділені в залежності від класу останньої, характеризувалися підвищеним рівнем ліпідів крові, причому в пацієнтів ІІ групи вміст ЗХС, ТГ та ЛПНЩ був вірогідно вищим порівняно з хворими І групи.
Нами було проаналізовано яким чином змінюється коронарний кровоток у пацієнтів із ГІМ та ГЛШН у залежності від класу останньої. Виявлено, що в пацієнтів обох груп спостерігалось переважання дво- та трисудинного ураження КА над односудинним, а в пацієнтів ІІ групи трисудинне ураження зустрічалось вірогідно частіше, ніж в осіб І групи. Аналіз стану КА у пацієнтів із різними класами ГЛШН показав, що гемодинамічно значимі стенози вінцевих судин вірогідно частіше виявлялися в пацієнтів ІІ групи в порівнянні з хворими І групи. Повна оклюзія КА дещо частіше виявлялась також у пацієнтів ІІ групи. Аналіз локалізації уражень КА та ступеня їх вираженості показав, що у хворих ІІ групи дещо частіше пошкоджується стовбур лівої КА, дистальна порція лівої передньої низхідної артерії (ЛПНА), проксимальна частина огинаючої артерії (ОА) та дистальна ділянка правої КА, вірогідно частіше – серединна порція ЛПНА, ОА та серединна ділянка правої КА, порівняно з хворими І групи. Величини сумарного ураження стовбура лівої КА, серединної та дистальної порцій ЛПНА, медіальної частини ОА, проксимальної та медіальної ділянок правої КА були вірогідно більшими в пацієнтів ІІ групи, що вказує на більш важкий перебіг коронарного атеросклерозу в цієї категорії хворих. Інші дослідники вказують на те, що при проведенні коронароангіографії в таких пацієнтів у 40 – 60% хворих виявляється багатосудинне ураження коронарного русла, у 10 – 15% – стеноз стовбура лівої КА, у 20 – 30% – ураження однієї судини, частіше ЛПНА, у 10% пацієнтів суттєві звуження просвіту відсутні.
Згідно результатів однофакторного регресійного аналізу, ризик прогресування ГЛШН у пацієнтів із ГІМ збільшується з виявленням при проведенні КАГ двосудинного ураження – у 0,8 рази, трисудинного ураження – у 2 рази, повної оклюзії КА – у 2,8 рази, стенозу >50% - у 1,8 рази (рис. 2).
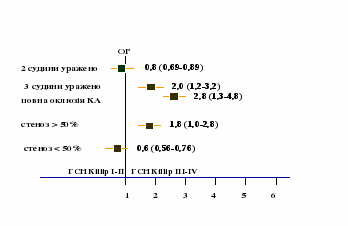
Рис. 2. Предиктори прогресування ГЛШН в пацієнтів із ГІМ за даними КАГ
Таким чином, у пацієнтів із ГІМ, перебіг якого ускладнився ГЛШН, спостерігається підвищення вмісту ліпідів крові, збільшується частота виявлення багатосудинного ураження вінцевих артерій та гемодинамічно значимих стенозів, причому наведені процеси прогресують зі зростанням класу ГЛШН.
Відомо, що в органiзмi людини, як i в інших бiологiчних істот узагалi, усi процеси перебiгають завдяки певній хроноритмологічній детермінації якiсних і кiлькiсних змiн, які означають перебіг часу в живому середовищi відповідно до концепцiї “бiологiчного часу”. Нами було зроблено спробу визначити хронобіологічні детермінанти розвитку летальності від ГІМ, ускладненого ГЛШН, у розподілі класів ГЛШН та ймовірності розвитку ускладнень із урахуванням циркадної мотивації. Встановлено, що хронобіологічна детермінованість розвитку летальної події в пацієнтів зі ГІМ, ускладненим ГЛШН, свідчить про перевагу нічних епізодів (0 – 6 год) над ранковими (6 – 12 год), денними (12 – 18 год) і вечірніми (18 – 24 год). На основі отриманих даних можна дійти висновку, що часом “підвищеного ризику” у розвитку летальної події слід вважати нічні години, а денні – годинами “відносного благополуччя”. На збільшення летальності в нічний час можуть впливати такі фактори, як частий розвиток тяжких форм ГЛШН, що є характерним для цього часу, порушення ритму, у тому числі фатальні аритмії, суттєве підвищення коагуляційного потенціалу крові та підвищення артеріального тиску. Окрім того, відомо, що нічні години, із точки зору управління регулюючими системами організму, є найменш сприятливими.
Аналіз розвитку летальної події в пацієнтів із ГІМ та ГЛШН у тижневому розподілі показав, що ймовірність її виникнення коливалась у діапазоні 8 – 21% випадків на день і була пов’язана з перевагою для п’ятниці, суботи та понеділка при меншій кількості летальних епізодів у вівторок, середу, четвер та неділю (рис. 3).
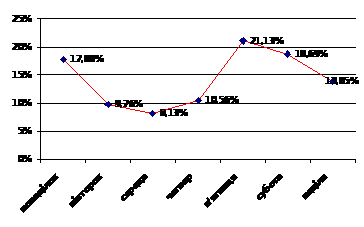
Рис. 3. Тижневий розподіл розвитку летальних подій
у пацієнтів із ГІМ, ускладненим ГЛШН
Проведено хронобіологічний розподіл виникнення летальних ускладнень ГІМ та ГЛШН упродовж одного року спостереження. Виявлено, що найвищим показник летальності серед хворих на ГІМ, ускладнений ГЛШН, був у зимовий період року – грудень, січень, лютий, у весняний період року (березень, квітень, травень) кількість летальних подій дещо зменшувалася, улітку (червень, липень, серпень) кількість летальних подій незначно зростала й найменшим показник летальності виявився в осінні місяці – вересень, жовтень і листопад (рис. 4).
Для зручності порівняння пацієнтів із ГЛШН І – ІІ класу було об’єднано в групу 1 (232 особи), а пацієнтів із ГЛШН ІІІ – ІV класу – у групу 2 (136 осіб). Аналіз основних клініко-лабораторних показників показав, що в пацієнтів групи 1, на відміну від групи 2, суттєвих коливань АТ залежно від хронобіологічно мотивованого летального наслідку не відмічено. Коливання глюкози також суттєво не розрізнялися в погодинному розподілі при ГІМ, ускладненому ГЛШН І – ІІ класів, і смерті внаслідок його ускладнень.
Аналіз ймовірності змін основних клініко-лабораторних показників у погодинному розподілі летальності для пацієнтів групи 2 свідчив про підвищення в ранішні години рівнів таких показників, як систолічний АТ, глюкоза, протромбіновий індекс, гематокрит, швидкість осідання еритроцитів, лімфоцити та зменшення ЗФВ і, навпаки, збільшення у вечірні години фібриногену, трансаміназ і лейкоцитів.
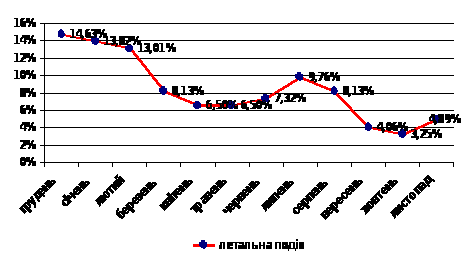
Рис. 4. Помісячний розподіл розвитку летальних подій
у пацієнтів з ГІМ, ускладненим ГЛШН
Таким чином, отримані нами дані вказують на наявність циркадних та циркадіанних ритмів у розвитку летальних подій серед пацієнтів із ГІМ, ускладненим ГЛШН. Отже, слід враховувати значення періодів “підвищеного ризику” та “відносного благополуччя” у розвитку летальних подій у побудові відповідної схеми терапії та розробці темпів фізичної активності на госпітальному етапі в такої категорії пацієнтів.
Метою наступного етапу дослідження стало встановлення характеру добових кривих АТ у пацієнтів із ГІМ, ускладненим ГЛШН, та вивчення особливостей перебігу цього захворювання в залежності від варіанту добового профілю АТ. Нами відмічено абсолютну перевагу монофазної (79,76%) добової кривої з добовим індексом (ДІ) менше 10% – “non-dipper”. Решта 20,24% пацієнтів відносились до групи “dipper” (11,9%) та “night-peaker” (8,34%). Проведене погрупове порівняння загальноклінічного аналізу крові в обстежених пацієнтів. Виявлено відсутність вірогідних відмінностей за переважною кількістю показників. Вірогідні погрупові відмінності виявлено лише між рівнем глюкози крові, фібриногену та швидкістю зсідання еритроцитів.
Нами було проаналізовано яким чином поводять себе маркери запалення та некрозу в пацієнтів із ГІМ, ускладненим ГЛШН, залежно від типу добового профілю артеріального тиску. Встановлено, що в пацієнтів із добовим профілем АТ “non-dipper” спостерігається підвищення рівня прозапальних цитокінів, маркерів некрозу та Тст, що дає підстави стверджувати про більш прогностично несприятливий перебіг ГІМ у даної категорії пацієнтів.
Аналіз змін ЗФВ показав вірогідно нижчі її рівні в пацієнтів групи А на 1-у – 2-у, 14-у, 28-у добу ГІМ та через 1 рік, що дає підставу стверджувати про більш виражені прояви СН в даної категорії пацієнтів. Отже, реєстрація добового профілю АТ “non-dipper” у пацієнтів із ГІМ, ускладненим ГЛШН, є прогностично несприятливим фактором і асоціюється з активацією запального та некротичного процесу й прогресуванням ознак СН.
Нашою метою було вивчення впливу негайної механічної реканалізації інфарктзв’язаної КА в пацієнтів із ГІМ, ускладненим ГЛШН, на основні клініко-лабораторні та інструментальні показники, госпітальну та позагоспітальну летальність у даної категорії пацієнтів. Було проаналізовано результати КАГ 56 пацієнтів із ГІМ, ускладненим ГЛШН, що проходили обстеження та лікування в центральних кардіологічних клініках м. Москви (Росія). Обстежених пацієнтів було розділено на дві групи залежно від ефективності проведеної ангіопластики. У групу І увійшли пацієнти з ефективною реваскуляризацією (58,93% осіб), у групу ІІ – пацієнти, в яких ефективної реваскуляризації шляхом черезшкірної ангіопластики досягнути не вдалося, тому реперфузія досягалася виключно шляхом тромболізису (41,07%). Виділені групи були цілком зіставимі за віком, статтю, основними параметрами загального аналізу крові, основними показниками Ехо-КГ обстеження на момент поступлення й ангіографічною характеристикою КА.
Погруповий аналіз змін ліпідного профілю крові продемонстрував підвищення рівня ЗХС, ТГ та ЛПНЩ у плазмі крові пацієнтів обох груп, але, поряд із цим, був вірогідно більшим у пацієнтів групи ІІ, у порівнянні з пацієнтами групи І, що свідчить про більш інтенсивну вираженість атеросклеротичного процесу в даної категорії пацієнтів.
Із 56 відібраних для аналізу пацієнтів за 1 рік після перенесеного ГІМ померло 21,42% пацієнтів, із них 14,28% - під час перебування в стаціонарі, а 7,14% – упродовж одного року спостереження. Погруповий аналіз летальності показав, що в групі І показник госпітальної летальності складав 5,35%, а за 1 рік спостереження померло 1,78% пацієнтів, таким чином загальний показник летальності складав – 7,13%. Серед пацієнтів групи ІІ загальний показник летальності за рік після перенесеного ГІМ складав 14,29%, із них 8,93% припадало на госпітальну летальність, а 5,36% – на позагоспітальну. Отже, в групі пацієнтів із проведеною механічною реканалізацією та стентуванням інфарктзв’язаної КА показники летальності значно менші на всіх етапах у порівнянні з групою тромболізису, що дає підстави стверджувати про високу ефективність інтервенційних втручань в обраної категорії пацієнтів. Частота виникнення повторного ГІМ упродовж одного року спостереження була теж значно нижчою в пацієнтів групи І і складала 3,57% проти 7,14% осіб групи ІІ.
Нами проаналізовано яким чином змінювався вміст основного маркера некрозу міокарда – Тр-І у пацієнтів обох груп у момент поступлення та на фоні лікування ГІМ. Виявлено, що вихідний рівень Тр-І перевищував нормативні значення в обох групах (42,64+6,01 нг/мл в групі І та 39,41+5,79 нг/мл (р>0,5), що свідчить про вираженість некротичного процесу в цієї категорії пацієнтів. На 10-й день ГІМ відмічався вірогідно вищий рівень Тр-І (р<0,001) у пацієнтів групи ІІ (0,53+0,01 нг/мл (група І) проти 2,14+0,12 нг/мл (група ІІ)), що свідчить про більшу ефективність механічної реканалізації в порівнянні з тромболітичною терапією стосовно зменшення рівня маркерів некрозу міокарда.
Важливим аспектом оцінки ефективності проведеного лікування є зіставлення змін показників ЕхоКГ всередині груп І і ІІ. Визначено, що в групі успішної механічної реканалізації інфарктзв’язаної КА відбувся вірогідний приріст КДО (+14,61%, p<0,01), невірогідні коливання КСО (-5,12%, p>0,2), вірогідна позитивна динаміка ЗФВ (+29,14%, p<0,001), в групі тромболітичної терапії гемодинамічний ефект був менш вираженим згідно зі змінами КДО (+5,84%, p>0,1) та КСО (-2,6%, p>0,5), відмічався вірогідний приріст ЗФВ (+15,69%, p<0,01), але зміни були менш виражені у порівнянні з групою І.
Отже, у пацієнтів із ГІМ, ускладненим ГЛШН, рання механічна реканалізація з наступним стентуванням інфарктзв’язаної КА є безпечним підходом, якому можна надати перевагу перед консервативною стратегією ведення пацієнтів, оскільки це покращує показники скоротливої функції міокарда та зменшує кількість летальних подій упродовж одного року спостереження.
Незважаючи на відновлення кровотоку в інфарктзалежній КА, систолічна та діастолічна функції міокарда ЛШ досить часто відновлюються лише через кілька діб і навіть тижнів після його реперфузії. Поряд із цим, попри позитивний вплив (відновлення кровотоку в зоні інфаркту), реперфузія може супроводжуватися збільшенням пошкодження міокарда (так зване реперфузійне пошкодження) або реперфузійною аритмією. Із урахуванням теоретичних та експериментальних уявлень про патогенез реперфузійного ушкодження потенційно корисними можуть бути скевенджери вільних радикалів, антиоксиданти, засоби, що знижують активність нейтрофілів. До таких препаратів належить блокатор 5-ліпоксигенази кверцетин в ін’єкційній формі. Найбільш важливими якостями препарату є потужна антиоксидантна дія, гальмування активності ряду мембранозв’язаних ферментів, модуляція рівня оксиду азоту в ушкоджених тканинах та крові, а також протекція мембранозв’язаних ферментів, які корегують іонний гомеостаз.
Отже, із метою вивчення додаткових можливостей оптимізації лікування пацієнтів із ГІМ, ускладненим ГЛШН, в умовах лікування базовою терапією (пролонговані нітропрепарати, антикоагулянти і антиагреганти, в-адреноблокатори за умов стабілізації стану, ІАПФ, статини, діуретики та інотропні засоби за потребою) обстежено 30 хворих (група 1), яким до загальноприйнятої схеми лікування було додано внутрішньовенний інгібітор 5-ліпоксигенази кверцетин – препарат українського виробництва – корвітин упродовж 5 діб за загальноприйнятою схемою, у зіставленні з іншими хворими (30 осіб), які отримували стандартну антиішемічну терапію (група 2). Усім обстеженим хворим на початку та після закінчення терапії корвітином у динаміці 28 діб спостереження проведено оцінку основних параметрів гемодинаміки та змін геометрії ЛШ з використанням Ехо-КГ в М-В-режимах, а також визначався вміст прозапальних цитокінів (Іл-1-б, Іл-6, Іл-10, ТНФ-, Нп), біомаркерів пошкодження міокарда (Тр-І) та імуноферментні показники вмісту гормонів (СРП, Тст).
Виділені в рамках проведеного дослідження групи, вірогідно розрізнялися лише за віком, який був меншим у групі корвітину (p<0,001) та рівнем гематокриту, який переважав у групі 1, за всіма останніми клініко-анамнестичними даними обидві групи були цілком зіставимі між собою.
Аналіз змін вмісту прозапальних цитокінів Іл-1-б, Іл-6, ФНП, Нп та протизапального цитокіну Іл-10 у пацієнтів з ГІМ, перебіг якого ускладнився ГЛШН, у залежності від обраної схеми лікування, показав, що в пацієнтів обох груп спостерігається значне підвищення порівняно з нормою рівнів Іл-1-б (29,01+4,15 пг/мл (група 1) та 32,16+4,76 пг/мл (група 2)), Іл-6 (36,45+5,12 (група 2) проти 30,27+4,32 (група 1) пг/мл), ТНФ- (48,31+3,12 (група 2) проти 44,26+2,67 (група 1) пг/мл, р>0,2) та Нп (18,27+2,78 (група 2) проти 15,36+2,34 (група 1) нмоль/л, р<0,05), причому в пацієнтів групи 2 всі три показники були дещо більшими, ніж у пацієнтів групи 1, хоча дані вірогідно не розрізнялись. У процесі лікування відбулося вірогідне зниження рівнів Іл-1-б (18,64+3,28 проти 9,73+1,36 пг/мл, р<0,02), Іл-6 (13,27+2,06 пг/мл проти 4,83+1,45 пг/мл), ТНФ- (22,16+1,41 проти 16,57+1,02 пг/мл, р<0,02), Нп (10,29+2,07 проти 4,24+1,21 нмоль/л, р<0,02), причому в групі пацієнтів, в яких до стандартної антиішемічної терапії було додано корвітин, зменшення показників, що вивчалися, було більш суттєвим, аніж у пацієнтів із ізольованою антиішемічною терапією, що вказує на здатність корвітину пригнічувати запальну ланку патогенезу ГІМ.
Проведено аналіз вмісту біомаркерів ГІМ з метою виявлення ефективності розроблених схем лікування. Встановлено, що, незважаючи на нижчий вихідний рівень Тр-І у групі 1 (39,40+1,71 (група 2) проти 29,52+2,31 (група 1) нг/мл відповідно, p<0,001), зменшення цього біомаркера некротичного процесу в міокарді було більш суттєвим на фоні призначення корвітину (15,45+1,25 проти 3,73+0,50 (група 1) нг/мл, p<0,001), що дає підстави говорити про його здатність сприяти швидшій нормалізації вмісту кардіоспецифічних ферментів та зменшенню кінцевої маси некрозу міокарда. Зіставлення змін вмісту СРП відповідно до запропонованого терапевтичного підходу показало, що вихідний рівень СРП в обох групах вірогідно не розрізнявся (0,14+0,01 (група 1) проти 0,15+0,03 мг/л (група 2), p>0,5), на фоні проведеного лікування залишився невірогідно більшим у групі 1 (0,09+0,01 проти 0,07+0,03 мг/л (група 2), p>0,2), однак відсоткове зниження рівня СРП було вірогідним як в групі 1, так і в групі 2.
Вивчення основних параметрів гемодинаміки на момент поступлення пацієнтів із ГІМ, ускладненим ГЛШН, у стаціонар і на фоні запропонованого лікування проведене в умовах виконання ЕхоКГ обстеження в М- та В-режимах із оцінкою сегментарної скоротливості ЛШ у групах додавання до базової терапії корвітину та ізольованої антиішемічної терапії. Порівняння основних гемодинамічних показників у групах 1 і 2 на початку та після проведеного лікування дало змогу виявити, що в групі корвітину відбувся вірогідний приріст КДО, невірогідні коливання КСО, вірогідне збільшення ЗФВ, у той час як в групі без включення в комплекс лікування корвітину гемодинамічний ефект був меншим відповідно до змін КДО, КСО, ЗФВ. Подальший аналіз стосувався результатів Ехо-КГ дослідження в В-режимі з секторальним сканування в 4-камерній проекції на фоні лікування корвітином (група 1) і базисної антиішемічної терапії (група 2). Виявлено, що на фоні включення до базисної антиішемічної терапії корвітину (група 1) проти ізольованої антиішемічної терапії (група 2) профіль регіональної скоротливості був подібним в обох групах, однак спостерігалось вірогідне збільшення показника скоротливості в сегменті РФВ>12 >(р<0,05) для групи з додаванням корвітину.
Отже, включення ін’єкційної форми блокатора 5-ліпоксигенази кверцетину – препарату Корвітин – у комплексну терапію в пацієнтів з ГІМ та ГЛШН пригнічує активність цитокінової ланки патогенезу ГІМ, обмежує зону некрозу міокарда та сприяє поліпшенню насосної функції серця.
Таким чином, у результаті комплексного клініко-діагностичного дослідження створено прогностичну модель перебігу ГІМ, ускладненого ГЛШН, що дозволяє спрогнозувати ймовірність виникнення летального випадку в обраної категорії пацієнтів та оптимізувати лікувальну тактику шляхом проведення негайної реканалізації інфарктзв’язаної КА та додаванням до базисного лікування внутрішньовенної форми кверцетину.
ВИСНОВКИ
У дисертаційній роботі наведено узагальнення результатів визначення основних клініко-анамнестичних, біохімічних, імуноферментних, інструментальних предикторів розвитку та прогресування синдрому гострої лівошлуночкової недостатності в пацієнтів із гострим інфарктом міокарда. На підставі розробки даної концепції пропонується нове вирішення науково-практичної проблеми, що виявляється в створенні прогностичної моделі перебігу гострого інфаркту міокарда, ускладненого гострою лівошлуночковою недостатністю з оптимізацією схем лікування, шляхом вивчення ранніх маркерів розвитку, прогресування серцевої недостатності та її запобігання з використанням реваскуляризації шляхом коронарного втручання та тромболітичної терапії міокарда й ад′ювантної кардіопротекторної терапії.
1. Чоловіча стать (р<0,001), старший вік (р<0,01), передня локалізація інфаркту міокарда (р<0,001), наявність післяінфарктного кардіосклерозу в анамнезі (р<0,01) є незалежними предикторами більш важкого перебігу гострої лівошлуночкової недостатності. У той же час клінічно виражена гостра лівошлуночкова недостатність характеризується більш високим рівнем прозапальних цитокінів (інтерлейкіну-1-б, інтерлейкіну-6, туморнекротичного фактора, неоптеріну), тропоніну-І, С-реактивного протеїну, тестостерону та зниженням загальної фракції викиду порівняно з неускладненим перебігом гострого інфаркту міокарда.
2. Старший вік пацієнтів (ВШ – 1,5), більш високий клас гострої лівошлуночкової недостатності (ВШ – 2), наявність цукрового діабету (ВШ – 1,3) та серцевої недостатності в анамнезі (ВШ – 3), передня локалізація інфаркту міокарда (ВШ – 4,5), ожиріння (ВШ – 1,15), загальна фракція викиду менше 40% (ВШ – 1,2) є незалежними предикторами виникнення летальної події в пацієнтів із гострим інфарктом міокарда й гострою лівошлуночковою недостатністю. Окрім того, зростання рівня прозапальних цитокінів (інтерлейкіну-1-б, інтерлейкіну-6, туморнекротичного фактора, неоптеріну, С-реактивного протеїну) та тропоніну-І поряд із погіршенням вихідних даних Ехо-КГ також сприяють зростанню ймовірності виникнення летальної події в даної категорії пацієнтів.
3. Найбільш прогностично несприятливою для розвитку серцевої недостатності в післяінфарктному періоді (через 1 рік після виникнення інфаркту міокарда) є сукупність наступних анамнестичних і клінічних ознак: стенокардія, що передувала інфаркту (р<0,001), артеріальна гіпертензія (р<0,001), передня локалізація інфаркту міокарда (р<0,001), повторний інфаркт (р<0,001), наявність будь-яких ознак гострої лівошлуночкової недостатності, а також збільшення вихідного рівня прозапальних цитокінів, С-реактивного протеїну, тропоніну-І, а також початкове та поетапне зменшення загальної фракції викиду в пацієнтів із гострим інфарктом міокарда, перебіг якого ускладнився синдромом гострої лівошлуночкової недостатності.
4. У пацієнтів із гострим інфарктом міокарда, перебіг якого ускладнився синдромом гострої лівошлуночкової недостатності, спостерігається підвищення вмісту ліпідів крові (р<0,01), збільшується частота виявлення багатосудинного ураження вінцевих артерій та гемодинамічно значимих стенозів (р<0,01) за даними селекційної коронароангіографії, причому наведені процеси прогресують зі зростанням класу серцевої недостатності.
5. Розвиток летальних подій серед пацієнтів з гострим інфарктом міокарда, ускладненим гострою лівошлуночковою недостатністю, має хроноритмологічне підґрунтя та підпорядковується циркадним та циркадіанним ритмам. Аналіз ймовірності змін основних клініко-лабораторних показників у погодинному розподілі летальності для пацієнтів із ознаками вираженої лівошлуночкової недостатності свідчив про підвищення в ранішні години рівнів систолічного артеріального тиску, глюкози, протромбінового індексу, гематокриту, швидкості зсідання еритроцитів, лімфоцитів і зменшення загальної фракції викиду й, навпаки, збільшення у вечірні години фібриногену, трансаміназ та лейкоцитів.
6. Реєстрація добового профілю артеріального тиску “non-dipper” у пацієнтів із гострим інфарктом міокарда, ускладненим гострою лівошлуночковою недостатністю, є прогностично несприятливим фактором і асоціюється з активацією запального та некротичного процесу й прогресуванням ознак серцевої недостатності.
7. У пацієнтів із гострим інфарктом міокарда, ускладненим гострою лівошлуночковою недостатністю, рання механічна реканалізація з наступним стентуванням інфарктзв’язаної коронарної артерії є безпечним підходом, якому можна надати перевагу перед консервативною стратегією ведення пацієнтів, оскільки це покращує показники скоротливої функції міокарда й зменшує кількість летальних подій упродовж одного року спостереження.
8. Включення ін’єкційної форми блокатора 5-ліпоксигенази кверцетину – препарату Корвітин – у комплексну терапію в пацієнтів із гострим інфарктом міокарда та гострою лівошлуночковою недостатністю пригнічує активність цитокінової ланки патогенезу інфаркту, обмежує зону некрозу міокарда та сприяє зростанню насосної функції серця.
ПРАКТИЧНІ РЕКОМЕНДАЦІЇ
1. Для оцінки ризику розвитку летальної події в пацієнтів із гострим інфарктом міокарда, ускладненим синдромом гострої лівошлуночкової недостатності, слід враховувати показники, які найбільше впливають на ймовірність її виникнення, із використанням наступного рівняння множинної регресії:
Летальна подія=19,34 + 0,564925*клас ГСН + 0,080519*ТрІ + 0,04435*Іл-1-б + 0,063774* ТНФ- + 0,06615*Нп – 0,117*ЗФВ>1-2доба>
(Середня відносна похибка наближення = 3%)
2. При побудові відповідної схеми терапії та розробці темпів фізичної активності на госпітальному етапі в пацієнтів, які перенесли гострий інфаркт міокарда, ускладнений гострою лівошлуночковою недостатністю, слід враховувати значення хроноритмологічних періодів “підвищеного ризику” та “відносного благополуччя” в плані розвитку летальних подій.
3. Для пригнічення активності цитокінової ланки патогенезу інфаркту міокарда, обмеження зони некрозу, профілактики прогресування серцевої недостатності в пацієнтів з гострим інфарктом міокарда, ускладненим синдромом гострої лівошлуночкової недостатності, рекомендовано використання з першої доби препаратів, які володіють мембранопротекторними властивостями (внутрішньовенної форми кверцетину).
СПИСОК ОПУБЛІКОВАНИХ ПРАЦЬ ЗА ТЕМОЮ ДИСЕРТАЦІЇ
1. Ілащук Т.О. Особливості коронарного кровотоку залежно від добового профілю артеріального тиску у пацієнтів з артеріальною гіпертензією та ішемічною хворобою серця // Буковинський медичний вісник. – 2002. – Т. 6, № 3-4. – С. 32-34.
2. Тащук В.К., Ілащук Т.О., Демешко М.І., Ілащук І.І., Полянська О.С., Поліщук О.Ю. Особливості порушень добового ритму артеріального тиску у хворих на артеріальну гіпертензію в залежності від реакції на стрес-тести // Галицький лікарський вісник.- 2003.- №1.- С.27-28. (Здобувач брала участь у лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь у підготовці матеріалів до друку).
3. Тащук В.К., Ілащук Т.О., Турубарова-Леунова Н.А., Дячук О.В., Шевчук В.А. Особливості впливу антикоагулянтів на коронарний резерв і гемодинамічні особливості перебігу гострого інфаркту міокарда // Клінічна та експериментальна патологія. – 2004. - Том 3, №2. - С.36-38. (Дисертант брала участь у лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь у підготовці матеріалів до друку).
4. Тащук В.К., Владковський І.К., Поліщук О.Ю., Ілащук Т.О., Гречко С.І., Іванчук П.Р., Турубарова-Леунова Н.А., Тащук І.А., Ель-Халіфа С.М., Міссауі Хашмі. Статеві аспекти розвитку кардіальної патології // Буковинський медичний вісник. – 2004. – Т. 8, № 3-4. – С. 92-95. (Здобувач брала участь у лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь у підготовці матеріалів до друку).
5. Тащук В.К., Ілащук Т.О., Турубарова-Леунова Н.А., Гречко С.І. Особливості добових коливань артеріального тиску у хворих з гострими формами ішемічної хвороби серця та артеріальною гіпертензією // Вісник Української медичної стоматологічної академії. – 2005. – Т. 5, № 3(11). – С.43-45. (Здобувач брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь у підготовці матеріалів до друку).
6. В.К.Тащук, Т.О.Ілащук, І.О.Маковійчук. Вікові та статеві аспекти гомеостазіологічної ланки гострих форм ішемічної хвороби серця // Кровообіг та гемостаз. – 2005. - №3-4. – С. 84-87. (Здобувач брала участь у лікуванні та обстеженні хворих, самостійно проводила аналіз клінічного перебігу захворювання і готувала матеріали до друку).
7. В.К. Тащук, Т.О. Ілащук, І.О. Маковійчук. Реєстр гострого інфаркту міокарда Північної Буковини: статеві аспекти гомеостазіологічних детермінант // Мат. Міжнародного форуму Кардіологія вчора, сьогодні, завтра”. – Український кардіологічний журнал. - 2006.– Спеціальний випуск. – С. 204-206. (Дисертантом самостійно здійснено клініко-інструментальне обстеження переважної кількості хворих, статистичну обробку та підготовку матеріалів до друку).
8. Ілащук Т.О. Гостра серцева недостатність на фоні інфаркту міокарда: клінічні та функціональні аспекти // Клінічна та експериментальна патологія. – 2006. – Т.V, №2. – С. 27-29.
9. В.К.Тащук, Т.О.Ілащук, І.І.Ілащук. Реєстр гострого інфаркту міокарда у мешканців Північної Буковини // Буковинський медичний вісник. – 2006. – Т. 10, №3. – С. 86-88. (Дисертант брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь в підготовці матеріалів до друку).
10. В.К.Тащук, Т.О.Ілащук. Хронобіологічні аспекти розвитку гострої серцевої недостатності на фоні гострого інфаркту міокарда: мотивація летальності // Буковинський медичний вісник. – 2006. – Т. 10, №4. – С. 175-177. (Дисертантом самостійно здійснено клініко-інструментальне обстеження переважної кількості хворих, статистичну обробку та підготовку матеріалів до друку).
11. Тащук В.К., Ілащук Т.О., Турубарова-Леунова Н.А., Поліщук О.Ю., Окіпняк І.В. Клініко-функціональні особливості перебігу інфаркту міокарда, ускладненого гострою серцевою недостатністю // Вісник наукових досліджень. – 2006. - №4. – С. 62 -63. (Здобувач брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь в підготовці матеріалів до друку).
12. Тащук В.К., Ілащук І.І., Ілащук Т.О. Сучасні аспекти лікування гострої серцевої недостатності: клінічний досвід // Клінічна та експериментальна патологія. – 2007. – Т.VІ, №1. – С. 106-108. (Дисертант брала участь в клінічних дослідженнях, аналізі та узагальненні результатів).
13. Ілащук Т.О. Корвітин у лікуванні пацієнтів із гострим інфарктом міокарда, ускладненим гострою лівошлуночковою недостатністю // Буковинський медичний вісник. – 2007. – Т. 11, №2. – С. 48-50.
14. Патент на корисну модель 25242 А61Р 9/00 Спосіб лікування гострого інфаркту міокарда, ускладненого гострою серцевою недостатністю / Ілащук Т.О. №25242 // Бюл. №11.- 2007.
15. Ілащук Т.О. Порівняльна характеристика ефективності екстреної черезшкірної реваскуляризації та тромболітичної терапії у пацієнтів із гострим інфарктом міокарда, ускладненим гострою лівошлуночковою недостатністю // Буковинський медичний вісник. - 2007. – Т. 11, № 3. – С. 37-39.
16. Ілащук Т.О. Особливості перебігу гострого інфаркту міокарда, ускладненого гострою лівошлуночковою недостатністю в залежності від типу добового профілю артеріального тиску // Клінічна та експериментальна патологія. – 2007. – Том 6, №3. – С. 50-52.
17. Ілащук Т.О. Стан коронарного кровотоку в пацієнтів з гострим інфарктом міокарда, ускладненим гострою лівошлуночковою недостатністю // Клінічна та експериментальна патологія. – 2007. – Т.VI, № 2. – С. 39-41.
18. Ілащук Т.О. Клініко-інструментальні маркери оцінки перебігу гострого інфаркту міокарда, ускладненого гострою лівошлуночковою недостатністю// Biomedical and Biosocial anthropology. – 2007. - №8. – С. 95-98.
19. Патент на корисну модель 25243 А61В 5/0205 А61Р 9/00 Спосіб прогнозування летального випадку у пацієнтів з гострою серцевою недостатністю / Ілащук Т.О. №25243 // Бюл. №11.- 2007.
20. Ілащук Т.О. Клінічні особливості перебігу гострого інфаркту міокарда, ускладненого гострою лівошлуночковою недостатністю залежно від важкості перебігу серцевої недостатності // Клінічна анатомія та оперативна хірургія. – 2007. – Том 6, № 3. – С. 80-83.
21. Ілащук Т.О., Тащук В.К., Владковський І.К., Горобець К.В. Особливості добового профілю артеріального тиску у хворих на інфаркт міокарда // Всеукраїнська науково-практична конференція "Сучасні методи діагностики і лікування в клініці внутрішніх хвороб".-2004.-Вінниця. - №8 (1). С.12. (Дисертант брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь в підготовці матеріалів до друку).
22. Ілащук Т.О., Поліщук О.Ю., Полянська О.С., Тащук В.К. Добовий ритм артеріального тиску при артеріальній гіпертензії залежно від реакції на стрес-тести, структурно-функціональні зміни лівого шлуночка та стан вінцевих судин // Українська науково-практична конференція "Профілактика і лікування артеріальної гіпертензії в Україні".- 2004.- Київ. – С.66. (Дисертантом самостійно здійснено клініко-інструментальне обстеження переважної кількості хворих, статистичну обробку та підготовку матеріалів до друку).
23. Тащук В.К., Ілащук Т.О., Полянська О.С., Маковійчук І.О. Стать-детерміновані гомеостазіологічні аспекти атерогенезу // VII національний конгрес кардіологів України.-2004.-Дніпропетровськ. - С.190. (Дисертант брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання та статистичну обробку матеріалів, брала участь в підготовці матеріалів до друку).
24. Ілащук Т.О., Поліщук О.Ю., Ілащук І.І., Гречко С.І. Циркадність коливань артеріального тиску у пацієнтів з артеріальною гіпертензією та ішемічною хворобою серця // VII національний конгрес кардіологів України.-2004.-Дніпропетровськ. - С.190. (Дисертант брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь в підготовці матеріалів до друку).
25. Тащук В.К., Ілащук Т.О., Турубарова-Леунова Н.А., Владковський І.К., Полянська О.С., Іванчук П.Р. Гемодинамічні особливості дії антикоагулянтів при гострому інфаркті міокарду // Всеукраїнська науково-практична конференція “Терапевтичні читання пам’яті академіка Л.Т.Малої", Харків, 20-21 травня 2004 року, С. 233. (Дисертантом самостійно здійснено клініко-інструментальне обстеження переважної кількості хворих, статистичну обробку та підготовку матеріалів до друку).
26. В.К.Тащук, Т.О.Ілащук, C.І.Гречко, О.П.Дінова. Особливості добових коливань артеріального тиску у хворих на артеріальну гіпертензію та ішемічну хворобу серця // Всеукраїнська науково-практична конференція "Артеріальна гіпертензія: виявлення, поширеність, диспансеризація, профілактика та лікування". - Івано-Франківськ, 2005. - С. 43. (Дисертант брала участь в клінічних дослідженнях, аналізі та узагальненні результатів).
27. Т.О.Ілащук, В.К.Тащук. Стан коронарного кровотоку у пацієнтів з артеріальною гіпертензією та ІХС залежно від добового профіля артеріального тиску // Ліки України, додаток, спеціалізоване інформаійне видання, 2005 р. Збірка наукових праць I Національного конгресу лікарів внутрішньої медицини. - Київ, 2005. - С. 45-46. (Дисертант брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь в підготовці матеріалів до друку).
28. Т.О.Ілащук, В.К.Тащук, І.О.Маковійчук, І.К.Владковський, Міссауі Хашмі. Статеві особливості розвитку та перебігу гострого Q-інфаркту міокарда за даними дослідження "Регіон" // ІІ науково-практична конференція з міжнародною участю "Оздоровчі ресурси Карпат і прилеглих регіонів". - Чернівці, 2005. - С. 173-174. (Дисертантом самостійно здійснено клініко-інструментальне обстеження переважної кількості хворих, статистичну обробку та підготовку матеріалів до друку).
29. В.К.Тащук, Н.А.Турубарова-Леунова, Т.О.Ілащук, П.Р.Іванчук, С.В.Світун. Особливості раннього ремоделювання лівого шлуночка хворих на гострий інфаркт міокарда за даними дослідження "Регіон" // ІІ науково-практична конференція з міжнародною участю "Оздоровчі ресурси Карпат і прилеглих регіонів". - Чернівці, 2005. - С. 179-180. (Дисертант брала участь в клінічних дослідженнях, аналізі та узагальненні результатів).
30. Ілащук Т.О., Тащук В.К., Поліщук О.Ю. І.І.Ілащук. Статеві особливості розвитку та перебігу гострого Q-інфаркту міокарда // Мат. VIII З’їзду Всеукраїнського лікарського товариства (ВУЛТ).- Київ, 2005.- С.67-68. (Дисертантом самостійно здійснено клініко-інструментальне обстеження переважної кількості хворих, статистичну обробку та підготовку матеріалів до друку).
31. Ілащук Т.О., Тащук В.К., Ілащук І.І. Стан коронарного кровотоку у пацієнтів з артеріальною гіпертензією та ІХС // Мат. науково-практичної конференції “Первинна та вторинна профілактика церебро-васкулярних ускладнень артеріальної гіпертензії” - Київ, 2006. – С. 77. (Дисертант брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь в підготовці матеріалів до друку).
32. Тащук В.К., Ілащук Т.О., Турубарова Н.А. Скоротливість міокарда та гепарин при гострому інфаркті міокарда і артеріальній гіпертензії // Мат. науково-практичної конференції “Первинна та вторинна профілактика церебро-васкулярних ускладнень артеріальної гіпертензії” - Київ, 2006. – С. 162. (Дисертант брала участь в клінічних дослідженнях, аналізі та узагальненні результатів).
33. Тащук В.К., Ілащук Т.О., Іванчук П.Р. Добовий профіль артеріального тиску у пацієнтів з інфарктом міокарда та серцевою недостатністю // Мат. науково-практичної конференції “Первинна та вторинна профілактика церебро-васкулярних ускладнень артеріальної гіпертензії” - Київ, 2006. – С. 163. (Дисертант брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь в підготовці матеріалів до друку).
34. Тащук В.К., Ілащук Т.О. Особливості добового профілю артеріального тиску у пацієнтів з інфарктом міокарда та серцевою недостатністю // Мат. науково-практичної конференції “Первинна та вторинна профілактика церебро-васкулярних ускладнень артеріальної гіпертензії” - Київ, 2006. – С. 164. (Дисертантом самостійно здійснено клініко-інструментальне обстеження переважної кількості хворих, статистичну обробку та підготовку матеріалів до друку).
35. В.К.Тащук, Т.О.Ілащук. Варіанти добового профілю артеріального тиску у пацієнтів з інфарктом міокарда та серцевою недостатністю у поєднанні з артеріальною гіпертензією // Матеріали науково-практичної конференції “Артеріальна гіпертензія: виявлення, поширеність, диспансеризація, профілактика та лікування”, 23 березня 2006 року, м. Івано-Франківськ; 2006. – С.83-84. (Дисертант брала участь в клінічних дослідженнях, аналізі та узагальненні результатів).
36. Т.О.Ілащук, В.К.Тащук. Інфаркт міокарда та гостра серцева недостатність: клінічні особливості перебігу // Матеріали Об’єднаного пленуму правлінь асоціацій кардіологів, серцево-судинних хірургів, нейрохірургів та невропатологів України в рамках виконання Державної програми запобігання та лікування серцево-судинних та судинно-мозкових захворювань на 2006 – 2010 роки. – Київ, 2006. – С. 72. (Дисертантом самостійно здійснено клініко-інструментальне обстеження переважної кількості хворих, статистичну обробку та підготовку матеріалів до друку).
37. В.К.Тащук, Т.О.Ілащук. Розвиток та перебіг гострого інфаркту міокарда із зубцем Q у статевому аспекті // Матеріали Об’єднаного пленуму правлінь асоціацій кардіологів, серцево-судинних хірургів, нейрохірургів та невропатологів України в рамках виконання Державної програми запобігання та лікування серцево-судинних та судинно-мозкових захворювань на 2006 – 2010 роки. – Київ, 2006. – С. 73. (Дисертант брала участь в лікуванні та обстеженні переважної більшості хворих, самостійно проводила аналіз клінічного перебігу захворювання, брала участь в підготовці матеріалів до друку).
АНОТАЦІЯ
Ілащук Т.О. Гострий інфаркт міокарда, ускладнений гострою лівошлуночковою недостатністю: клініко-патогенетичні та хронобіологічні детермінанти, результати тривалого спостереження та медикаментозної корекції. - Рукопис.
Дисертація на здобуття наукового ступеня доктора медичних наук за спеціальністю 14.01.11 - кардіологія. – Івано-Франківський державний медичний університет МОЗ України, Івано-Франківськ, 2008.
Використано клініко-діагностичний комплекс (електрокардіографія, ехокардіографія, добове моніторування артеріального тиску, селективна коронароангіографія, імуноферментний аналіз) у 368 пацієнтів із гострим інфарктом міокарда, ускладненим гострою лівошлуночковою недостатністю з метою створення прогностичної моделі перебігу ускладненого інфаркту міокарда з оптимізацією схем лікування, шляхом вивчення ранніх маркерів розвитку, прогресування серцевої недостатності та її запобігання з використанням реваскуляризації міокарда й ад′ювантної кардіопротекторної терапії. Проведено порівняльний аналіз використання медикаментозної та механічної реваскуляризації міокарда та вивчено ефективність додаванням до базисного лікування внутрішньовенної форми кверцетину.
Ключові слова: інфаркт міокарда, гостра лівошлуночкова недостатність, прогноз, прозапальні цитокіни, реваскуляризація, кардіопротекторна терапія.
АННОТАЦИЯ
Илащук Т.А. Острый инфаркт миокарда, осложненный острой левожелудочковой недостаточностью: клинико-патогенетические и хронобиологические детерминанты, результаты длительного наблюдения и медикаментозной корекции. - Рукопись.
Диссертация на соискание ученой степени доктора медицинских наук по специальности 14.01.11 - кардиология. – Ивано-Франковский государственный медицинский университет МЗ Украины, Ивано-Франковск, 2008.
Обследовано 368 пациентов с остром инфарктом миокарда, осложненным острой левожелудочковой недостаточностью с использованием клинико-диагностического комплекса (электрокардиография, эхокардиография, суточное мониторирование артериального давления, селективная коронароангиография, иммуноферментный анализ) с целью создания прогностической модели течения осложненного инфаркта миокарда с оптимизацией схем лечения, путем изучения ранних маркеров развития, прогресирования сердечной недостаточности и ее предупреждения с использованием реваскуляризации миокарда и адьювантной кардиопротекторной терапии.
Обследования, проведенные пациентам, которые вошли в группу наблюдения и лечения, состояли из тщательного анализа клинических проявлений патологии, которая изучалась в рамках создания регистра острого инфаркта миокарда, в частности анализ жалоб, анамнез жизни и заболевания, оценка динамики электрокардиографии в первые – вторые, 14-е и 28-е сутки и через год после перенесенного острого инфаркта миокарда, проведение эхокардиографии в М- и В-режимах с оценкой регионарной сократимости левого желудочка в 12 сегментах в первые – вторые, 14-е и 28-е сутки, лабораторные исследования с оценкой общего анализа крови, ферментов, коагулограммы, содержания интерлейкина-1-б, интерлейкина-6, интерлейкина-10, туморнекротического фактора, неоптерина, тропонинов, С-реактивного протеина, тестостерона, которые определяли иммуноферментным методом. Также проанализированы результаты коронароангиографии, которая проводилась у 56 пациентов в первые сутки инфаркта миокарда с последующей реваскуляризацией путем стентирования в 33 (8,55%) или тромболизиса в 23 (6,25%) случаев.
Нами определены клинико-функциональные характеристики течения разных стадий острой левожелудочковой недостаточности с учетом уровней провоспалительных цитокинов, биомаркеров некроза миокарда, показателей функцинального состояния и регионарной сократимости миокарда левого желудочка. Показано, что увеличение уровня провоспалительных цитокинов (интерлейкина-1-б, интерлейкина-6, туморнекротического фактора-б, неоптерина, С-реактивного протеина) и тропонина-І паралельно с ухудшением исходных даннях эхокардиографии способствуют росту вероятности возникновения летального события у пациентов с инфарктом миокарда, осложненным острой левожелудочковой недостаточностью. Установлено, что наиболее прогностически неблагоприятным в плане развития сердечной недостаточности в послеинфарктном периоде (через 1 год после возникновения инфаркта миокарда) является сочетание следующих анамнестических и клинических признаков: стенокардия, которая предшествовала инфаркту, артериальная гипертензия, передняя локализация инфаркта миокарда, повторний инфаркт, наличие любых признаков острой левожелудочковой недостачности, а также увеличение исходного уровня провоспалительных цитокинов, С-реактивного протеина, тропонина-І, также начальное и поэтапное уменьшение общей фракции выброса у исследуемой категории пациентов. Доказано, что развитие летальних исходов среди пациентов с острым инфарктом миокарда, осложненным острой левожелудочковой недостаточностью, имеет хроноритмологическую основу и подчиняется циркадным и циркадианным ритмам. Показано, что регистрация суточного профиля артериального давления “non-dipper” у пациентов с острым инфарктом миокарда, осложненным острой левожелудочковой недостаточностью, является прогностически неблагоприятным фактором и ассоциируется с активацией воспалительного и некротического процесса и прогрессированием признаков сердечной недостаточности.
Включение инъекционной формы блокатора 5-липоксигеназы кверцетина – препарата Корвитин – в комплексную терапию у пациентов с острым инфарктом миокарда и острой левожелудочковой недостаточностью угнетает активность цитокинового звена патогенеза инфаркта, ограничивает зону некроза миокарда и способствует улучшению насосной функции сердца.
Ключевые слова: инфаркт миокарда, острая левожелудочковая недостаточность, прогноз, провоспалительные цитокины, реваскуляризация, кардиопротекторная терапия.
ANNOTATION
Ilashchuk T.O. Acute myocardial infarction complicating with аcute left ventricle heart failure: clinical, pathogenical and chronobiological determinants, results of the long observation and medical correction. - Manuscript.
Dissertation on competition of the Doctor of Medical Sciences degree in the speciality 14.01.11 - cardiology. – Ivano-Frankivsk state medical university, Ministry of Public Health of Ukraine, Ivano-Frankivsk, 2008.
The clinical and diagnostical complex (elektrocardiography, echocardiography, 24-hour blood pressure monitoring, angiography, imunoenzyme analysis) was used in 368 patients with acute myocardial infarction, complicated with acute left ventricle heart failure with the purpose of creation of complicated myocardial infarction prognostic model with treatment algorithms optimization by means of learning early markers of development, progressing of heart failure and its prevention by means of myocardial revascularization and adjuvant сardioproteсtive therapy. The comparison analysis of medical and mechanical revascularization of myocardium were done and the efficacy of adding intravenous form of kvercetin to the basic therapy were learned.
Key words: myocardial infarction, acute left ventricle heart failure, prognosis, proinflamation cytokines, revascularization, сardioproteсtive therapy.
Перелік умовних позначень
|
АГ АТ ГІМ (ІМ) ГЛШН ГСН ДІ ДАТ ДМАТ ЕКГ ЕхоКГ ЗФВ ЗХС ІАПФ Іл-1-б Іл-6 Іл-10 ІХС КА КАГ КДО КСО ЛПВЩ ЛПНЩ ЛШ Нп РФВ САТ СН СРП ТГ Тр-І Тст ТНФ- ФК ХСК ЧСС |
– артеріальна гіпертензія – артеріальний тиск – гострий інфаркт міокарда (інфаркт міокарда) – гостра лівошлуночкова недостатність – гостра серцева недостатність – добовий індекс – діастолічний артеріальний тиск – добове моніторування артеріального тиску – електрокардіографія – ехокардіографія – загальна фракція викиду – загальний холестерин – інгібітори ангіотензинперетворюючого ферменту – інтерлейкін-1-альфа – інтерлейкін-6 – інтерлейкін-10 – ішемічна хвороба серця – коронарні артерії – коронароангіографія – кінцевий діастолічний об’єм – кінцевий систолічний об’єм – ліпопротеїни високої щільності – ліпопротеїни низької щільності – лівий шлуночок – неоптерин – реґіонарна фракція викиду – систолічний артеріальний тиск – серцева недостатність – С-реактивний протеїн – тригліцериди – тропонін-І – тестостерон – туморнекротичний фактор- – функціональний клас – хвороби системи кровообігу – частота серцевих скорочень |
Підписано до друку 18.12.2007. Формат 60х84 1/16
Гарнітура Times.
Умов.-друк.арк. 1,8. Обл.-вид.арк. 2,0.
Замовлення № 148. Тираж 100.
Видавництво “Книги – ХХІ”
Україна, 5900, м.Сторожинець, Чернівецької обл.
Вул.О.Кобилянської,7
Тел./факс: (о372) 58060-21 58-64-64, моб.8-050-9183202
Свідоцтво про державну реєестрацію
ДК № 1839 від 10-06.2004 р.
Друк ПП Валь Л.О.