Иммунологические и иммуногенетические особенности увеитов при синдроме Фогта-Коянаги-Харада
Иммунологические и иммуногенетические особенности увеитов при синдроме Фогта-Коянаги-Харада
Г.К. Мамбеткулова, Л.Ш. Ишбердина, В.Б. Мальханов, Уфимский НИИ глазных болезней, г. Уфа
В развитии увеитов ведущая роль принадлежит аутоиммунным реакциям, обусловленным генетическим статусом больного. Обнаружение антител к меланоцитам и выявление в высоком титре антител к наружным сегментам фоторецепторов и мюллеровским клеткам у больных с активным увеитом при синдроме Фогта–Коянаги–Харада, по мнению многих авторов, является пусковым механизмом в развитии аутоиммунной реакции [4, 5, 8].
Известно, что система HLA обеспечивает взаимодействие всех иммунокомпетентных клеток организма, распознавание своих и чужеродных, в том числе измененных собственных клеток, запуск и реализацию иммунного ответа и в целом обеспечивает выживание человека как вида в условиях экзогенной и эндогенной агрессии [1, 3, 5, 6, 9].
Однако параллельное изучение иммунологических и иммуногенетических особенностей увеитов у больных с синдромом Фогта–Коянаги–Харада в Южно–Уральской популяции не проводилось, что явилось предметом наших исследований.
Материалы и методы исследования
Под нашим наблюдением находилось 17 больных (34 глаза) рецидивирующим увеаменингитом с синдромом Фогта–Коянаги–Харада в возрасте 10–42 лет. Офтальмологическое обследование включало биомикро– и офтальмоскопию, визо– и периметрию, А– и В–сканирование, электроретино– и электроокулографию.
Иммунологическое исследование периферической крови заключалось в определении общего количества Т– и В–лимфоцитов в реакциях розеткообразования с эритроцитами барана и мышей, содержания субпопуляций Т–лимфоцитов моноклональными антителами (анти– CD3, CD4, CD8, CD4/CD8, CD16, CD19) методом непрямого иммунофлуоресцентного окрашивания [7], уровня циркулирующих иммунных комплексов – с помощью ПЭГ–преципитации [2], сывороточных иммуноглобулинов – методом радиальной иммунодиффузии [14]. Ткан–специфическую сенсибилизацию к антигенам хрусталика (a–кристаллин) и сетчатки (S–антиген) выявляли методом твердофазного иммуноферментного анализа по разнице оптической плотности [10]. Анализ антигенов гистосовместимости проводили в стандартном микролимфоцитотоксическом тесте по известной методике [15]. Статистическая обработка полученных данных определялась по установленным формулам (Л.А. Певницкий, 1988).
Контрольную группу составили 52 здоровых донора Республиканской станции переливания крови.
Результаты и обсуждение
В известных исследованиях установлена определенная взаимосвязь между наличием антигена HLA–Bw22, HLA–DRMT3, HLA–DR4 и развитием увеита при синдроме Фогта–Коянаги–Харада [11–13].
Проведенные нами иммуногенетические исследования выявили характерные для Южно–Уральской популяции ассоциации некоторых антигенов гистосовместимости с синдромом Фогта–Коянаги–Харада.
Частота встречаемости (Ах) антигенов В35 и В56 оказалась одинаково высокой по сравнению с другими антигенами исследуемой группы и составила 29,4% при достоверности различий (c2) в частоте встречаемости данных антигенов среди контрольной группы – 4,87 и 6,60 соответственно. Частота гена (Px) наибольшей оказалась у больных увеитом при синдроме Фогта–Коянаги–Харада с антигенами HLA В35 и В56. Больные с увеитом при синдроме Фогта–Коянаги–Харада отличались от здоровых доноров также более частой встречаемостью антигенов HLA В12, В14, В22, В51, полным отсутствием антигенов В18, В21, В27, В41; а антигены В7, В8, В16, В40 встречались в единичных случаях. Достоверных различий по локусу А (HLA A1–A11) в своих исследованиях мы не наблюдали (табл. 1).

Установлено, что носительство антигенов В12, В14 при синдроме Фогта–Коянаги–Харада характерно для передних увеитов, В22, В35, В51, В56 – для задних. Одновременное наличие антигенов В35 и В56 является прогностически неблагоприятным фактором в отношении развития экссудативной отслойки сетчатки на фоне заднего увеита. Результаты изучения зависимости офтальмологических проявлений при синдроме Фогта–Коянаги–Харада от носительства антигенов HLA–комплекса представлены в таблице 2.

Взаимосвязь иммунологических и иммуногенетических показателей представлена в таблице 3. Первую группу (n=4) составили больные – носители антигенов В12 и В14 с передним увеитом. Во вторую группу (n=13) вошли больные с задним увеитом, в том числе с экссудативной отслойкой сетчатки (n=5) на его фоне.
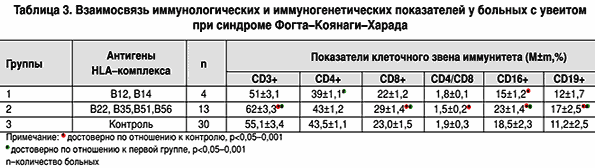
В первой группе больных у носителей HLA–антигенов В12 и В14 достоверно (р<0,001) снижено число CD4+ по сравнению с контролем и CD16+ относительно второй группы (p<0,05). Во второй группе больных у носителей антигенов В22, В35, В51, В56 достоверно (p<0,05) повышено число CD3+, CD8+, CD16+ и CD19+ лимфоцитов как по сравнению с контролем, так и относительно первой группы. В этой группе больных нашли сниженным иммунорегуляторный индекс.
Иммунологические исследования обнаружили в сыворотке крови накопление избыточных концентраций циркулирующих иммунных комплексов у 15 больных (87%), гипериммуноглобулинемию IgG (20,7±0,95 г/л) и IgМ (2,26±0,03 г/л), в контроле соответственно – 11,63±0,25 и 1,64±0,061 г/л.
Результаты тканеспецифического исследования позволили установить более высокие, чем в контрольной группе, значения средней концентрации антител к S–антигену, a–кристаллину, роговице (табл. 4). Их уровни были высокими соответственно у 11 (64,7%), у 12 (70,6%) и у 6 (35,3%) больных.

Высокие уровни аутоантител к тканеспецифическим белкам сетчатки, хрусталика и роговицы свидетельствуют о поражении всех оболочек глазного яблока и существенной роли аутоагрессии в развитии данного заболевания.
Итак, увеит при синдроме Фогта–Коянаги–Харада характеризуется носительством антигенов В12, В14, В22, В35, В51, В56 и изменениями клеточного иммунитета, более выраженными при углублении и осложнении воспалительного процесса. Значительную роль в патогенезе увеита при синдроме Фогта–Коянаги–Харада играет аутоиммунный процесс, что доказывает наличие высоких уровней тканевых антител, накопление в сыворотке крови избыточных концентраций циркулирующих иммунных комплексов и иммуноглобулинов классов G и М. Изучение иммунных и иммуногенетических механизмов увеита при синдроме Фогта–Коянаги–Харада открывает новые возможности для своевременной диагностики и патогенетически ориентированной терапии этого заболевания.
Список литературы
1. Бондаренко А.Л. HLA и болезни. – Киров, 1999. – 194 с.
2. Зайцева Н.С., Слепова О.С., Теплинская Л.Е. с соавт. //Иммунологические методы в диагностике увеитов. – Метод. Рекомендации. – М., 1989. – 40 с.
3. Зарецкая Ю.М. Клиническая иммуногенетика. – М., Медицина, 1983. – 208 с.
4. Кацнельсон Л.А., Танковский В.Э. Увеиты (клиника, лечение).– М., 1998. – 203с.
5. Мамбеткулова Г.К. Клиника, иммунологические особенности и лечение ревматоидных увеитов: Автореф. дисс. ... к.м.н. – Уфа, 2000. – 22 с.
6. Панченко Н.В. Особенности нарушений клеточного иммунитета у больных увеитами, осложненными отеком макулярной области. //Офтальмол. журн.–1998. – № 4. – С. 229–301.
7. Петров Р.В. Современные проблемы клинической иммунологии. // Сов. медицина. – 1978. – № 7. – С. 8 – 15.
8. Пименов И.В., Зайцева Н.С., Слепова О.С., Векслер Х.М. Комплексная иммунологическая оценка состояния больных с некоторыми формами увеаретинальной патологии. //Вестн. офтальмол. – 1991. – № 4. – С. 49–53
9. Хаитов Р.М., Алексеев Л.П.//Int. J.Immunorehabil. – 1998. – № 10. – С. 30–38.
10. Яковлева В.Г., Сибиряк С.В., Головин В.П., Киреев В.Л. Выделение и очистка родопсинкиназы //Актуальные вопросы прикладной биохимии и биотехнологии. – Уфа, 1998. – С. 273–277.
11. Bodmer W. //HLA 1997 Eds P.Terasaki, D.Gjertson. – 1998. – P. 1–7.
12. Boutimzine N., Laghmari A., Ouazzani I., Ibrahimy W., Mohcine Z. // J. Fr. Ophtalmol. – 1998. – Dec; 21 (10). – P. 746–754
13. Desarnaulds–A.B., Borruat–F.X., Herbort–C.P., Spertini–F. //Klin.–Monatsbl.–Augenheilkd. – 1996. – May. – 208 (5). – P. 301–302
14. Mancini G. et al. //Int. Immunochem. – 1965. – Vol .2 – Р.235–254.
15. Terasaki P.I., Bernoco D., Park M.S. et al. //Amer.J.Clin.Pathol. – 1978. – Vol. 69. – P. 103–120