Наркотические анальгетики

.
Наркотические анальгетики. Реферат.
ОГЛАВЛЕНИЕ
Введение. 3
Механизмы действия наркотических анальгетиков. 5
Алкалоиды–производные фенантренизохинолина и их синтетические аналоги. 9
Морфин 11
Фармакологические эффекты 11
Фармакокинетика 12
Показания к назначению, дозировка 13
Побочные эффекты и противопоказания 14
Хранение и формы выпуска 14
Морфилонг 14
Фармакокинетика 15
Показания к назначению, дозировка 15
Хранение и формы выпуска 15
Омнопон 15
Показания к назначению, дозировка 15
Хранение и формы выпуска 16
Кодеин 16
Фармакологические эффекты 17
Показания к назначению, дозировка 17
Хранение и формы выпуска 17
Этилморфин (дионин) 18
Фармакологические эффекты 18
Показания к назначению, дозировка 18
Хранение и формы выпуска 19
Другие производные морфинана. 19
Производные пиперидина. 21
Промедол 21
Фармакологические эффекты 22
Фармакокинетика 22
Показания к назначению, дозировка 22
Противопоказания и побочные эффекты 23
Хранение и формы выпуска 23
Фентанил. 23
Фармакокинетика 24
Показания к назначению, дозировка 24
Хранение и формы выпуска 24
Производные циклогексана. 24
Трамадол. 25
Производные дифенилэтоксиуксусной кислоты. 25
Эстоцин. 25
Введение.
Анальгезирующими средствами, или анальгетиками ( от греч. algos – боль и an – без), называют лекарственные средства, обладающие специфической способностью ослаблять или устранять чувство боли, т.е. средства, доминирующим эффектом которых является анальгезия, наступающая в результате резорбтивного действия и не сопровождающаяся в терапевтических дозах выключением сознания и выраженным нарушением двигательных функций. По химической природе, характеру и механизмам фармакологической активности современные анальгетики делят на две основные группы: Наркотические и ненаркотические анальгетики. Настоящий реферат посвящен обзору наркотических анальгетиков, их классификации, особенностям фармакологического действия.
Для наркотических анальгетиков, в отличие от ненаркотических, характерны следующие основные свойства:
Сильная анальгезирующая активность, обеспечивающая возможность их использования в качестве высокоэффективных болеутоляющих средств в различных областях медицины, особенно при травмах и заболеваниях, сопровождающихся выраженным болевым синдромом;
Особое влияние на ЦНС человека, выражающееся в развитии эйфории и появлении при повторном применении синдромов физической и психической зависимости;
Развитие болезненного синдрома – абстиненции у лиц с развившимся синдромом физической и психической зависимости при лишении их анальгетического препарата;
Снятие вызываемых токсических явлений на ЦНС, нарушений сердечной деятельности, а также анальгезии специфическими антагонистами.
Фармакологические эффекты при приеме наркотических анальгетиков обуславливаются их механизмами действия (см.) и заключаются в следующем: кроме анальгетического эффекта, все наркотические анальгетики в той или иной степени оказывают снотворное действие, угнетают дыхание и кашлевой рефлекс, повышают тонус кишечника и мочевого пузыря, вызывать диспепсические расстройства (тошноту, рвоту), нарушения со стороны ЦНС (галлюцинации) и другие побочные явления.
По выраженности анальгетического действия и побочным эффектам разные препараты группы наркотических анальгетиков различаются между собой, что связано с особенностями их химической структуры и физико-химическими свойствами и соответственно со взаимодействием с рецепторами, вовлеченными в осуществление их фармакологических эффектов.
По источникам получения и химическому строению современные наркотические анальгетики делятся на 3 основные группы:
Природные алкалоиды — морфин и кодеин, содержащиеся в маке снотворном (Papaver somniferum) в нативном состоянии;
Полусинтетические соединения, полученные путем химического видоизменения молекулы морфина — этилморфин и др.;
Синтетические соединения, полученные методом полного химического синтеза и не имеющие аналогов в природе — промедол, трамадол, фентанил и др.
По химическому строению основной части молекулы наркотические анальгетики делятся на 4 основные группы:
Производные фенантренизохинолина (морфинана) и близкие по структуре соединения;
Производные фенилпиперидина и N-пропилфенилпиперидина;
Производные циклогексана;
Ациклические (производные дифенилэтоксиуксусной кислоты и схожие по структуре)
Большинство синтетических и полусинтетических препаратов получены путем химического видоизменения молекулы родоначальника группы наркотических анальгетиков – морфина с сохранением элементов его структуры или ее упрощением. Этим путем был создан ряд препаратов, различающихся по силе и степени развития анальгетического эффекта, по быстроте и степени развития привыкания, пристрастия и других побочных эффектов, по силе воздействия на различные отделы ЦНС, по способности тормозить двигательную функцию кишечника и др. Путем химического видоизменения молекулы морфина были также получены его антагонисты (налоксон и др.).
В настоящее время, когда механизм действия наркотических анальгетиков почти полностью установлен и выделены медиаторы опиатных рецепторов, препараты–медиаторы проходят клинические испытания и, возможно, в скором времени в каких-то случаях частично заменят наркотические анальгетики.
Механизмы действия наркотических анальгетиков.
Нейрофизиологические исследования свидетельствуют об угнетении наркотическими анальгетиками таламических центров болевой чувствительности и блокировании передачи болевых импульсов к коре. Этот эффект является, по всей вероятности, ведущим в физиологическом механизме анальгетического действия наркотических анальгетиков. Угнетение передачи болевых импульсов наркотическими анальгетиками происходит, по-видимому, на уровне таламуса. Болеутоляющее действие также связано с нарушением функции ассоциативных и неспецифических ядер таламуса и их связи с корой головного мозга. Одновременно блокируется передача нервных импульсов с коллатералей специфических путей на ретикулярную формацию ствола головного мозга.
Роль психического состояния в развитии анальгетического эффекта наркотических анальгетиков очень велика. Достаточно отметить, что положительный эффект «плацебо» (лекарственной формы, не содержащей активного препарата) достигает 30–40%. Изменение восприятия боли связано с эйфорией, диссоциативном эффекте наркотических анальгетиков, их успокаивающем действии. Последнее сказывается на оценке боли и ее вегетативных проявлениях.
В нейрохимическом аспекте большое значение имеет изучение влияния этих веществ на нейромедиаторные процессы мозга и периферических органов. В нервной системе человека имеется сложная антиноцицептивная (противоболевая) система, включающая энкефалиновые пресинаптические тормозящие рецепторы (см. рис. 1). В качестве нейротрансмиттеров (медиаторов) передачи импульса в этих рецепторах выступают олигопептиды: эндорфины и энкефалины, а также другие пептиды (динорфины и др.). По химической природе эти соединения состоят из нескольких остатков аминокислот, например, мет-энкефалин состоит из 5 аминокислот, а -эндорфин из 31 аминокислоты. Они не являются типичными нейромедиаторами, поскольку по способу выделения из нейронов и трансмиссии через нейронную жидкость к другим нейронам они аналогичны нейрогормонам, а по типу действия являются модуляторами, участвующими в снижении чувствительности к боли, в передаче импульса на другой нейрон. Эндорфины и энкефалины, связываясь с опиатными рецепторами, оказывают анальгетическое действие.
В настоящее время установлено, что опиатные рецепторы существуют в виде нескольких субпопуляций: имеющих различную функциональную значимость. Полагают, что –рецепторы определяют супраспинальную анальгезию, эйфорию, угнетение дыхания и физическую зависимость; –рецепторы определяют спинальную анальгезию, миоз, седативный эффект; –рецепторы влияют на восприятие действительности (считают, что эти рецепторы играют важную роль в патогенезе шизофрении).
Рисунок 1. Тормозное модуляторное и тормозное нейротрансмиттерное пресинаптическое действие эндорфинов и энкефалинов

Опиатные рецепторы представляют собой быстрые ион–канальные рецепторы, которые в физиологических условиях активируются олигопептидами (эндорфинами и энкефалинами) возможно, при участии аминокислоты глицина. Наркотические анальгетики связываются с опиатными рецепторами, т.е. являются блокаторами открытых каналов. Во время открытия ионного канала, анальгетик поступает в него, связывается и препятствует переходу ионов в канал. При этом потенциал действия на пресинаптической части нейрона, проводящего болевой импульс, не возникает и происходит развитие торможения в этом нейроне. Есть мнение, что действие экзогенных наркотических анальгетиков связано также со стабилизацией эндогенных нейропептидов путем инактивации энкефалиназ – ферментов, разрушающих эндорфины и энкефалины.
Связывание наркотических анальгетиков с опиатными рецепторами обусловлено тем, что определенная часть молекулы всех наркотических анальгетиков имеет структурное и конформационное сходство с частью молекул (тирозиновым остатком) энкефалинов и эндорфинов. У природных опиатных нейропептидов конформационная структура молекулы строго определена четвертичной структурой белка, поэтому различные нейропептиды воздействуют только на те опиатные рецепторы, с которыми они имеют конформационное сходство. У наркотических анальгетиков молекула имеет значительные расхождения в расстояниях между активными центрами и конформационной структуры в сравнении с опиатными рецепторами. Это объясняет факт, что наркотические анальгетики действуют в гораздо более высоких дозах (по сравнению с эндогенными опиатными пептидами), а также их неспецифичность действия (один и тот же наркотический анальгетик воздействует на различные субпопуляции опиатных рецепторов). В последнее время синтезированы наркотические анальгетики, избирательно воздействующие на определенные субпопуляции опиатных рецепторов. Примерами могут служить декстрометорфан (не используется в СНГ), который является средством, избирательно подавляющим кашлевой центр, без побочных эффектов, свойственных кодеину (является избирательным агонистом – и –рецепторов; побочный эффект заключается в развитии галлюцинаций и др. нарушений психики при использовании очень высоких доз (700–900 мг) вследствие возбуждения -рецепторов); лоперамид, избирательно связывающийся с -рецепторами кишечника и вызывающий в терапевтических дозах антидиарейный эффект без основных эффектов, свойственных наркотическим анальгетикам (скорее всего, за счет использования малой дозы или за счет того, что препарат плохо проникает через гематоэнцефалический барьер).
Различные наркотические анальгетики различаются также по характеру связывания с опиатными рецепторами. Одни из них (морфин, промедол, фентанил и др.) являются «чистыми» (полными) агонистами опиатных рецепторов; связываясь с ними, они оказывают характерное для эндогенных опиатных нейропептидов физиологическое действие. Другие (налоксон и др.), являясь «чистыми» антагонистами, связываются с опиатными рецепторами, блокируют действие эндогенных опиатных нейропептидов и чистых агонистов опиатных рецепторов. Третья, наиболее перспективная в фармакологическом отношении группа, представляет собой препараты смешанного типа действия (агонисты–антагонисты), по-разному связывающиеся с разными подтипами опиатных рецепторов и оказывающие в связи с этим двоякий эффект.
Действие наркотических анальгетиков на периферические органы (кишечник) обусловлено также связыванием с опиатными рецепторами, локализующимися в этих органах.
С опиатными рецепторами сопряжены нейроны, содержащие холинэргические синапсы. При использовании м-холиноблокаторов (например, атропина) анальгезирующая активность наркотических анальгетиков усиливается, а при совместном использовании со средствами, снижающими уровень катехоламинов в ЦНС (симпатолитики, напр., резерпин), обезболивающее действие анальгетиков значительно снижается.
Алкалоиды–производные фенантренизохинолина и их синтетические аналоги.
Родоначальником этой группы, а также родоначальником всех наркотических анальгетиков является морфин, алкалоид, содержащийся в млечном соке мака снотворного (Papaver somniferum). Высушенный млечный сок из незрелых плодов мака снотворного называется опиумом (опием). Опий содержит около 25 алкалоидов (20–25% общей массы) в солях с молочной, меконовой (-окси--пирон-,’-дикарбоновой), серной и другими кислотами. Основные алкалоиды опия — морфин, кодеин, папаверин, наркотин, тебаин либо сами применяются в качестве лекарственных средств, либо служат источниками получения их полусинтетических аналогов. Кроме алкалоидов в состав опия входят углеводы, белки, смолы, воски, жиры, пигменты и другие вещества. Разделение смеси алкалоидов опия представляет собой сложный и трудоемкий процесс. В России широко применяют метод Каневской–Клячкиной, отличающийся простотой и позволяющий произвести разделение с неплохим выходом и более-менее высокой степенью чистоты.
Опий содержит алкалоиды двух основных групп: производные 1-бензилизохинолина и морфинана. Свойствами наркотических анальгетиков, однако, обладают только производные морфинана, что связано, по-видимому, наличием пиперидинового кольца, замещенного в 2, 3, 4 положении объемными радикалами.
В настоящее время, хотя и полный химический синтез морфина и др. алкалоидов этой группы осуществлен, природные источники обеспечивают покрытие потребности в морфине, т.к. синтез весьма трудоемкий и выход морфина незначителен.
В зависимости от заместителей при 3, 6, 17 положении в молекуле морфинана его производные оказывают различные фармакологические эффекты. Безусловно, все основные эффекты наркотических анальгетиков присущи всем препаратам этой группы, но некоторые из них становятся преобладающими.
В таблице 1 приведена взаимосвязь химических свойств и фармакологического эффекта в зависимости от структуры производных морфинана. Морфин и этилморфин применяют в медицине в виде гидрохлоридов, а кодеин — в виде основания и фосфата. Все препараты представляют собой кристаллогидраты, которые на воздухе постепенно выветриваются, теряя кристаллизационную воду.
Рисунок 2. Общая структура алкалоидов—производных морфинана.
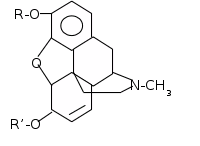
Таблица 1. Алкалоиды группы морфинана и их производные.
|
Препарат |
Радикалы-заместители (см. рисунок 2) |
Основной фармакологический эффект |
Физические свойства |
|
Морфина гидрохлорид |
R=OH R’=OH *HCl*3H>2>0 |
Анальгетический |
Белые игольчатые кристаллы или белый кристаллический порошок, слегка сереющий при хранении. Удельное вращение -97..-990 (2% водный раствор) |
|
Кодеин |
R=OCH>3> R’=OH *H>2>O |
Противокашлевой |
Бесцв. кристаллы или белый кристаллический порошок без запаха, горького вкуса; T>пл.>=154-157С0. |
|
Кодеина фосфат |
R=OCH>3> R’=OH *H>3>PO>4>*1.5H>2>O |
Противокашлевой |
Белый кристаллический порошок без запаха, горького вкуса. |
|
Этилморфина гидрохлорид (дионин) |
R=OC>2>H>5> R’=OH *HCl*2H>2>O |
Противовоспалительный; противокашлевой |
Белый кристаллический порошок без запаха, горького вкуса. |
Морфин
Впервые морфин был выделен в 1806 г. Сертюнером из снотворного мака. Это был первый алкалоид, полученный в очищенном виде. В начале 20 века морфин был получен синтетически. Синтез морфина включал в себя 17 стадий и протекал с очень низким выходом. В настоящее время потребность в морфине полностью покрывается за счет его получения из природных источников.
Алкалоиды морфин и кодеин сходны по химической структуре (см. рис 2). Они представляют собой N-метилпроизводные морфинана, конденсированного с фурановым циклом. Путем изменения радикалов при гидроксильных группах были получены многочисленные полусинтетические производные морфина.
Морфина гидрохлорид представляет собой белые игольчатые кристаллы или белый кристаллический порошок, слегка желтеющий при хранении. Медленно растворим в воде, трудно растворим в спирте (1:50). Растворы морфина гидрохлорида несовместимы с щелочными растворами (выпадает осадок).
Фармакологические эффекты
Морфина гидрохлорид отличается сильным болеутоляющим действием. Понижая возбудимость болевых центров, он способен оказать противошоковое действие при травмах. В больших дозах морфин оказывает снотворный эффект, который больше выражен при нарушениях сна, связанных с болевыми ощущениями.
Морфин вызывает выраженную эйфорию, и при его повторном применении быстро развивается болезненное пристрастие (морфинизм).
Морфин оказывает тормозящее влияние на условные рефлексы, понижает суммационную способность ЦНС, усиливает действие наркотических, снотворных и местноанестезирующих средств. Также морфин понижает возбудимость кашлевого центра.
Морфин также вызывает возбуждение центра блуждающих нервов (N. vagus), что ведет к появлению брадикардии. В результате активации нейронов глазодвигательных нервов под влиянием морфина появляется миоз. Эти эффекты могут быть сняты атропином или другими м–холиноблокаторами.
Рвота, которая может наблюдаться при применении морфина, связана с возбуждением хеморецепторных пусковых (триггерных) зон продолговатого мозга. Однако, морфин угнетает рвотный центр, поэтому повторные дозы морфина и рвотные средства, вводимые после морфина, рвоты не вызывают.
Под влиянием морфина повышается тонус гладкомышечных органов, наблюдается повышение тонуса сфинктеров желудочно-кишечного тракта, повышается тонус мускулатуры антральной части желудка, тонкого и толстого отделов кишечника, ослабляется перистальтика, замедляется продвижение пищевых масс, что приводит к развитию обстипации. Морфин тормозит секреторную активность желудочно-кишечного тракта. Отмечается также спазм мускулатуры желчевыводящих путей и сфинктера Одди. Повышается тонус сфинктеров мочевого пузыря. Может увеличиться тонус бронхов с развитием бронхоспазма.
Морфин оказывает морфин действие также и на обмен веществ, вызывая снижение основного обмена, температуры тела, изменения скорости выделения гипофизарных гормонов: выделение АДГ и пролактина увеличивается, что может вызвать уменьшение мочеотделения и гипергалакторею соответственно, а выделение ЛГ уменьшается (особенно при длительном применении).
Характерным для действия морфина является угнетение дыхательного центра. Малые дозы вызывают урежение и увеличение глубины дыхательных движений; большие дозы обеспечивают дальнейшее урежение и уменьшение глубины дыхания со снижением легочной вентиляции. Токсические дозы вызывают появление периодического дыхания по типу Чейна–Стокса и последующую остановку дыхания.
Фармакокинетика
Морфин быстро всасывается как при приеме внутрь, так и при парентеральном введении. Биодоступность при применении морфина per os составляет 20-30%. Плазмо-белковый коэффициент составляет 20%, что обуславливает продолжительность действия морфина и скорость наступления фармакологического эффекта. Высокая липофильность морфина и наличие третичного азота в его молекуле обеспечивают легкую проходимость морфина через биологические барьеры.
Действие морфина развивается через 10-15 мин после подкожного введения и через 20-30 мин после перорального введения. Период полувыведения морфина составляет около 12-24 часов. Действие однократной дозы продолжается 3-6 часов.
Показания к назначению, дозировка
Применяют морфин в качестве мощного болеутоляющего средства при травмах и различных заболеваниях с выраженным болевым синдромом (злокачественные новообразования, инфаркт миокарда и др.), при подготовке к операции и в послеоперационном периоде, при бессоннице, связанной с сильными болями.
Для обезболивания родов морфин не применяют, так как он легко проникает через фетоплацентарный барьер и может вызвать угнетение дыхания у новорожденного.
Иногда морфином пользуются в рентгенологической практике при исследовании желудка, двенадцатиперстной кишки, желчного пузыря. Введение морфина усиливает растяжение двенадцатиперстной кишки контрастным веществом, что способствует выявлению язвы и опухолей желудка. Вызываемое морфином сокращение мышц сфинктера Одди создает благоприятные условия для рентгенологического исследования желчного пузыря.
Использование морфина в настоящее время сильно ограничено в связи с его высоким наркогенным потенциалом (высокой вероятности возникновения физической зависимости) и токсичности. Для снижения риска возникновения зависимости и снижения побочных эффектов используются пролонгированные лекарственные формы морфина гидрохлорида, например, морфилонг (см. ниже), а также нетрадиционные пути введения морфина1.
Высшие дозы для взрослых: разовая 0.02 г, суточная 0.05 г. Обычно морфин назначают подкожно по 1 мл 1% раствора, внутрь по 0,01-0,02 г в порошках или каплях. Детям старше 2 лет морфин назначают в зависимости от возраста по 0,001-0,005 г на прием. В последние годы при наличии у больных острых и хронических болей стали назначать морфин и другие опиаты перидурально2 и эпидурально3. При этом выраженный и вдвое длительный эффект наступает при втрое меньших дозах.
Побочные эффекты и противопоказания
При применении морфина возможны тошнота, рвота, угнетение дыхания и другие побочные эффекты, связанные с особенностями его влияния на разные органы и системы организма (см. Морфин, Фармакологическое действие). Для уменьшения побочных эффектов морфин часто назначают вместе с м–холиноблокаторами (атропин, метацин).
Морфин не назначают детям до 2 лет; также морфин противопоказан при общем сильном истощении, недостаточности дыхательного центра. Осторожность применения морфина необходима у больных старческого возраста (замедлены обмен и выделение морфина; наблюдается более высокое содержание морфина в плазме крови).
Хранение и формы выпуска
Морфина гидрохлорид хранится по списку А, с соблюдением правил хранения наркотических веществ. Во избежание окисления препарат хранят в хорошо укупоренной таре, предохраняющей от действия света. Следует заметить, что при ненадлежащих условиях хранения морфина гидрохлорид может терять кристаллизационную воду, что может привести к завышению терапевтических доз.
Формы выпуска: таблетки по 0.01 г; 1% раствор в ампулах и шприц–тюбиках по 1 мл.
Морфилонг
Морфилонг4 является пролонгированной формой морфина гидрохлорида. Представляет собой 0,5% раствор морфина гидрохлорида в 30% водном растворе поливинилпирролидона с молекулярной массой 3500±5000.
Внешний вид морфилонга: прозрачная вязкая жидкость желтого цвета со слабым специфическим запахом поливинилпирролидона, растворимая в воде и спирте; рН 3,5-4,5. В 1 мл содержит 5,5 мг морфина гидрохлорида.
Фармакологическое действие полностью идентично морфину гидрохлориду. Возможные побочные эффекты, меры предосторожности и противопоказания идентичны морфину гидрохлориду.
Фармакокинетика
Биодоступность препарата, плазмо-белковый коэффициент аналогичны морфину гидрохлориду.
При внутримышечном введении происходит медленное всасывание морфина, болеутоляющий эффект развивается обычно через 30-40 мин и продолжается 22-24 часа.
Показания к назначению, дозировка
Применяют морфилонг у взрослых и детей старше 7 лет в послеоперационном периоде и при выраженном болевом синдроме у онкологических больных.
Вводят морфилонг только внутримышечно один раз в сутки из расчета 0,1 мл на 1 кг массы тела.
Хранение и формы выпуска
Морфилонг хранится по списку А, с соблюдением правил хранения наркотических веществ, в прохладном, защищенном от света месте. Выпускается в ампулах темного стекла по 2 мл в упаковке по 5 шт.
Омнопон
Омнопон представляет собой смесь гидрохлоридов алкалоидов опия; содержит 48-50% морфина и 32-35% других алкалоидов опия.
По внешнему виду омнопон — порошок от кремового до коричневато-желтого цвета. Растворим в воде (1:15), трудно растворим в спирте (1:50). Водный раствор при взбалтывании сильно пенится. рН 1% раствора 2,5-3,5.
1% раствор омнопона в 1 мл содержит: морфина гидрохлорида 6,7 мг; кодеина гидрохлорида 0,72 мг; папаверина гидрохлорида 0,36 мг; наркотина гидрохлорида 2,7 мг; тебаина гидрохлорида 0,05 мг.
Показания к назначению, дозировка
Показания к применению те же, что и для морфина. Однако омнопон лучше переносится, чем морфин, реже вызывает развитие спазмов гладкой мускулатуры (очевидно, за счет наличия в составе омнопона спазмолитика папаверина). Перорально назначают омнопон взрослым в дозе 0,01-0,02 г на прием; подкожно вводят по 1 мл 1% или 2% раствора. Детям старше 2 лет назначают по 0,001-0,0075 омнопона на прием в зависимости от возраста.
Высшие дозы для взрослых: разовая 0,03 г, суточная 0,1 г.
Противопоказания и побочные эффекты те же, что и у морфина.
Хранение и формы выпуска
Омнопон хранится по списку А, с соблюдением правил хранения наркотических веществ. Порошок хранится в хорошо укупоренной таре, предохраняющей от действия света; ампулы — в защищенном от света месте.
Формы выпуска: порошок; 1% и 2% растворы в ампулах по 1 мл.
Кодеин
По химической природе кодеин представляет собой метилморфин, т.е. морфин, в котором вместо гидроксильной группы в 3 положении имеется метокси–группа:

В
природе кодеин в небольшом количестве
содержится в опии. Содержание кодеина
в опии невелико (0.2–2%), поэтому кодеин
получают полусинтетическим путем из
морфина.
Кодеин применяется в медицине в виде основания и виде фосфата. Кодеин (основание) представляет собой бесцветные кристаллы или белый кристаллический порошок без запаха, горького вкуса. На воздухе выветривается, т.к. содержит одну молекулу кристаллизационной воды. Медленно и мало растворим в холодной воде (1:150), растворим в горячей воде (1:17), легко растворим в спирте. Водный и спиртовой растворы имеют щелочную реакцию. Кодеина фосфат представляет собой белый кристаллический порошок без запаха, горьковатого вкуса. На воздухе выветривается (содержит 1,5 молекулы кристаллизационной воды). Легко растворим в воде (1:3,5), мало — в спирте.
Фармакологические эффекты
По характеру действия кодеин близок к морфину, но болеутоляющие свойства выражены слабее. Считают, что болеутоляющие свойства кодеина обусловлены тем, что в процессе кодеина в организме образуется морфин. У кодеина сильно выражена способность уменьшать возбудимость кашлевого центра.
Кодеин в меньшей степени, чем морфин, угнетает дыхание; также меньше тормозит деятельность желудочно-кишечного тракта, однако может вызвать запор.
Кодеина фосфат представляет собой еще менее токсичный препарат, чем кодеин–основание (за счет меньшего содержания кодеина — около 80%).
Показания к назначению, дозировка
Применяют кодеин главным образом для успокоения кашля. В сочетании с ненаркотическими анальгетиками (анальгин, парацетамол), кофеином, фенобарбиталом применяется при головных болях, невралгиях в составе комбинированных препаратов. Входит в состав микстуры Бехтерева, применяемой в качестве успокаивающего средства.
Назначают кодеин внутрь в порошках, таблетках и растворах взрослым по 0,01-0,02 г на прием; детям старше 2 лет — по 0,001-0,0075 г на прием в зависимости от возраста. Высшие дозы для взрослых внутрь: разовая 0,05 г, суточная 0,2 г. Детям до 2 лет кодеин не назначают.
Кодеина фосфат допускается к применению у детей более раннего возраста и в несколько больших дозах. Назначают детям старше 6 мес. по 0,002-0,01 г на прием. Взрослым назначают практически в тех же дозах, что и кодеин–основание. в зависимости от возраста. Высшие дозы для взрослых внутрь: разовая 0,1 г, суточная 0,3 г.
Кодеин и кодеина фосфат входят в состав комбинированных таблетированных препаратов: «Кодтерпин» (0,015 г кодеина в 1 таблетке); «Таблетки от кашля» (0,02 г кодеина); «Пенталгин», «Седалгин», «Солпадеин» (0,012 г кодеина) и др.
Хранение и формы выпуска
Хранение кодеина, кодеина фосфата и содержащих кодеин лекарственных форм осуществляется по списку Б. Порошок хранят в герметичной таре, т.к. кодеин при хранении в ненадлежащих условиях может выветриваться (терять кристаллизационную воду), что может привести к завышению доз. Порошок и таблетки необходимо хранить в защищенном от света месте.
В связи с тем, что при повторном применении кодеина могут наблюдаться явления пристрастия (наркомании), кодеин в чистом виде и легко разделяемые комбинированные лекарственные формы (кодтерпин, таблетки от кашля) отпускаются с такими же ограничениями, как и другие наркотические анальгетики.
Этилморфин (дионин)
Этилморфин, как и кодеин, является полусинтетическим препаратом. Этилморфин не содержится в природных объектах, в промышленности получается путем этилирования морфина. В медицине этилморфин применяется в виде гидрохлорида.
Гидрохлорид этилморфина представляет собой белый кристаллический порошок без запаха, горького вкуса. Растворим в воде (1:12) и в спирте (1:25).
Фармакологические эффекты
По общему действию на организм этилморфин близок к кодеину. Особенностью фармакологического эффекта этилморфина является его способность вызывать гиперемию конъюнктивы с последующим ее отеком и местной анестезией. Этот факт позволяет использовать этилморфин в офтальмологической практике.
Показания к назначению, дозировка
Применяют этилморфина гидрохлорид внутрь для успокоения кашля при хронических бронхитах, туберкулезе легких и т.д., а также как болеутоляющее средство.
Иногда этилморфина гидрохлорид применяется в офтальмологической практике — препарат действует успокаивающе на глаза при кератите, инфильтрате роговой оболочки и др. заболеваниях глаз.
Внутрь взрослым этилморфина гидрохлорид назначают по 0,01-0,03 г на прием; детям старше 2 лет по 0,001-0,0075 г на прием в зависимости от возраста. В глазной практике используют растворы или мази, начиная с 1% до 10% концентрации. Высшие дозы для взрослых внутрь: разовая 0,03 г, суточная 0,1 г.
Хранение и формы выпуска
Этилморфина гидрохлорид хранится по списку А, с соблюдением правил хранения наркотических веществ. Порошок хранится в хорошо укупоренных банках оранжевого стекла, таблетки — в защищенном от света месте.
Формы выпуска: порошок; таблетки по 0,01 и 0,015 г.
Другие производные морфинана.
В качестве болеутоляющих средств в медицине используются также и другие, современные, производные морфинана. От морфина они отличаются главным образом тем, что оказывают свое терапевтическое действие в значительно меньших дозах, и, соответственно, меньше проявляют побочные эффекты: угнетение дыхания, тошноту, рвоту и др.
Препараты данной группы синтетические, получены путем химического видоизменения молекулы морфина, поэтому они проявляют своеобразное действие: являются одновременно и агонистами и антагонистами опиатных рецепторов. Вследствие этого риск возникновения зависимости к этим препаратам значительно ниже, чем при применении морфина.
К препаратам этой группы относятся:
Налорфин (N-аллилнорморфина гидрохлорид)
Пентазоцин, Лексир, Фортрал ((±) 2-Окси-5,9-диметил-2-(3,3-диметилаллил)-6,7-бензоморфинан
Нальбуфин (17-(Циклобутил)-4,5-эпоксиморфинан-3,6,14-триол гидрохлорид)
Бупренорфин (17-(Циклогексилпропилметил)-7,8-дигидро-7-[(1S)-2-гидрокси-3,3-диметилбутил-2]-6-метокси-0-метил-6,17-этано-17-норморфина гидрохлорид)
Буторфанол, Морадол ((–)-17-(Циклобутилметил)-морфинан-3,14-диол гидротартрат)
По химическому строению налорфин близок к морфину и отличается от него лишь наличием аллильного (–CH>2>-CH=CH>2>) остатка вместо метильного при азоте в 17 положении. Эта относительно небольшая модификация структуры морфина привела к получению соединения, оказавшегося не только агонистом, но и антагонистом по отношению к опиатным рецепторам.
П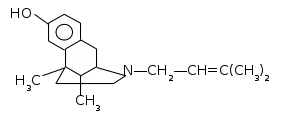
ентазоцин
— синтетическое соединение, содержащее
бензоморфановое ядро молекулы морфина,
на лишенное кислородного мостика и
третьего шестичленного ядра, свойственных
соединениям группы морфина:
Азот в пиперидиновом цикле замещен диметилаллильным радикалом (–CH>2>-CH=C(СН>3>)>2>), что придает молекуле свойства антагониста. Препарат получен по принципу модификации молекулы морфина с учетом, что некоторые, ранее синтезированные, соединения, близкие к морфину, но не содержащие кислородного мостика, такие как леворфанол, леморан (исключены из Госреестра), обладают высокой анальгетической активностью, превышающей анальгетическую активность морфина; вместе с тем диметилаллильный остаток является важной частью молекулы налорфина, обладающего в значительной мере свойствами антагониста морфина. Предполагалось, что такая модификация молекулы морфина приведет к получению соединения с более высокой анальгетической активностью, чем у налорфина, но с меньшими побочными эффектами, свойственными морфину. Пентазоцин в определенной степени удовлетворяет этим требованиям. В настоящее время получены агонисты–антагонисты, более эффективные, чем пентазоцин — нальбуфин и др.
Нальбуфин и буторфанол по химической структуре напоминают морфин, однако характерной особенностью молекулы нальбуфина и буторфанола является наличие вместо метильной группы при азоте в 17 положении метилциклобутильного радикала. Фармакологически, нальбуфин является агонистом–антагонистом опиатных рецепторов. Анальгезирующее действие связано главным образом с агонистическим влиянием на –рецепторы, но вместе с тем препарат является антагонистом –рецепторов, в связи с чем не оказывает выраженного эйфорического действия. По анальгетической активности препарат не уступает морфину при меньших побочных эффектах и меньшей способности к развитию толерантности и физической зависимости.
Производные пиперидина.
Идея создания наркотических анальгетиков, производных пиперидола, возникла в результате исследования химического строения фенантренизохинолиновой структуры морфина и других алкалоидов, содержащихся в опии. Общая формула анальгетиков, производных пиперидола, может быть рассмотрена как синтетический аналог фенил-N-метилпиперидиновой части молекулы морфина.
К производным пиперидина относятся:
Промедол (1,2,5-триметил-4-пропионилокси-4-фенилпиперидина гидрохлорид)
Фентанил (1-(2-фенилэтил)-4-(N-пропионилфениламино)-пиперидина цитрат)
Лоперамид, Имодиум (4-(4-хлорфенил)-4-окси-N,N-диметил--дифенил-1-пиперидин-бутанамида гидрохлорид)
Пиритрамид, Дипидолор (1’-(3-циано-3,3-дифенилпропил)-[1,4’-дипиперидин]-4’-карбоксамид)
Производные пиперидина несколько отличаются по своим фармакологическим эффектам от группы морфинана. Промедол лучше переносится, чем морфин; оказывает некоторый спазмолитический эффект, в связи с чем может быть применен для купирования болевого синдрома, связанного со спазмом гладкой мускулатуры. Фентанил оказывает сильный, но непродолжительный эффект. Лоперамид не оказывает выраженного анальгетического эффекта, но вместе с тем он активно тормозит перистальтику кишечника, что является одной из характерных особенностей опиатов.
Промедол
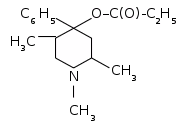
Промедол
является синтетическим производным
фенилпиперидина и по химическому
строению может рассматриваться как
аналог фенил-N-метилпиперидиновой
части молекулы морфина:
Промедол представляет собой белый кристаллический порошок, легко растворимый в воде и спирте.
Фармакологические эффекты
Промедол обладает сильной анальгетической активностью. По влиянию на ЦНС промедол близок к морфину; он уменьшает восприятие ЦНС болевых импульсов, угнетает условные рефлексы. Подобно другим наркотическим анальгетикам, понижает суммационную способность ЦНС, усиливает анестезирующее действие новокаина и других местных анестетиков. Промедол оказывает снотворный эффект, связанный, преимущественно, со снятием болевого синдрома.
По сравнению с морфином, промедол меньше угнетает дыхательный центр, меньше возбуждает центр блуждающего нерва и рвотный центр. Оказывает умеренное спазмолитическое действие на гладкую мускулатуру внутренних органов, но при этом повышая тонус миометрия и усиливая его сокращения.
Фармакокинетика
Действие промедола наступает через 10-20 мин и продолжается после однократной дозы в течение 3-4ч.
Показания к назначению, дозировка
Применяют промедол как болеутоляющее средство при травмах и различных заболеваниях, сопровождающихся болевыми ощущениями; при подготовке к операциям; в послеоперационном периоде и др.
Промедол весьма эффективен при язвенной болезни желудка и двенадцатиперстной кишки, стенокардии, инфаркте миокарда, кишечных печеночных и других видах колик, дискинетических запорах и др. заболеваниях, при которых болевой синдром связан со спазмами гладкой мускулатуры внутренних органов и кровеносных сосудов.
В акушерской практике промедол применяют для обезболивания и ускорения родов, т.к. в терапевтических дозах промедол не оказывает влияния на организм плода.
При болях, связанных со спазмами гладкой мускулатуры, промедол обычно сочетают с холинолитическими и спазмолитическими средствами: атропином, метацином, папаверином и др.
Промедол может применяться в комбинации с нейролептическими, антигистаминными препаратами и транквилизаторами при общей и местной анальгезии.
Назначается промедол подкожно, внутримышечно и внутрь. При парентеральном применении эффект более выражен. При необходимости можно вводить промедол также и внутривенно.
Внутрь назначают взрослым по 0,025-0,05 г, подкожно — по 1 мл 1% или 2% раствора, при сильных болях (особенно в онкологии) до 2 мл 2% раствора. Детям старше 2 лет назначают по 0,003-0,01 г в зависимости от возраста; у детей до 2 лет промедол не применяют.
Высшие дозы для взрослых внутрь: разовая 0,05 г, суточная 0,2 г; парентерально: разовая 0,04 г, суточная 0,16 г.
Противопоказания и побочные эффекты
Промедол обычно хорошо переносится. Из побочных эффектов могут быть легкая тошнота, головокружение, слабость, ощущение легкого опьянения. Эти явления проходят самостоятельно. Если побочные эффекты наблюдаются при повторном применении препарата, необходимо уменьшить дозу.
При применении промедола могут возникнуть явления привыкания и пристрастия (как и к другим наркотическим анальгетикам).
Промедол противопоказан при угнетении дыхания.
Хранение и формы выпуска
Хранится промедол по списку А, соблюдая правила для хранения наркотических анальгетиков, в хорошо укупоренной таре. Выпускается в таблетках по 0.025 г, в ампулах и шприц–тюбиках в виде 1% и 2% раствора.
Фентанил.
Фентанил является синтетическим анальгетиком, производным фенилпиперидина. По химической структуре частично схож с промедолом.
Фентанил представляет собой белый кристаллический порошок, практический нерастворимый в воде, легко растворимый в спирте. Выпускается в виде соли с лимонной кислотой (в виде цитрата).
Фармакокинетика
Фентанил является очень активным анальгетиком. Его анальгетическая активность превосходит морфин приблизительно в 200 раз. Оказывает сильное, но кратковременное (при разовом введении) действие.
После внутривенного введения максимальный эффект развивается через 1-3 мин и продолжается 15-30 мин. После внутримышечного введения эффект наступает через 3-10 мин.
Показания к назначению, дозировка
Применяют фентанил главным образом в сочетании с нейролептиками для нейролептанальгезии и премедикации. Фентанил является составной частью комбинированного препарата «Таламонал».
Для подготовки к наркозу вводят фентанил в дозе 0,05-0,1 мг внутримышечно за полчаса до начала операции. Для достижения нейролептанальгезии предварительно вводят нейролептик (дроперидол), а затем фентанил из расчета 1 мл 0,005% раствора на 5 кг массы тела больного. При необходимости введение препарата можно повторять через каждые 20-40 мин.
Хранение и формы выпуска
Фентанил хранится по списку А, с соблюдением правил хранения наркотических анальгетиков. Выпускается в виде 0,005% раствора в ампулах по 2 и 5 мл.
Производные циклогексана.
Производные циклогексана — довольно молодая группа наркотических анальгетиков, успевшая, однако, зарекомендовать себя с лучшей стороны. Препараты этой группы являются агонистами–антагонистами опиатных рецепторов, что снижает риск возникновения зависимости и привыкания.
К препаратам этой группы относятся:
Трамадол, Трамал ((±)-транс-2-[(диметиламино)-метил]-1-(м-метоксифенил)-циклогексанола гидрохлорид)
Тилидин, Валорон (этиловый эфир DL-транс-2-диметиламино-1-фенил-3-циклогексен-1-карбоновой кислоты)
Трамадол.
Трамадол по химической структуре несколько напоминает промедол. Особенность структуры трамадола заключается в том, что он содержит азот не в пиперидиновом цикле, как другие наркотические анальгетики, а в виде диметиламино–группы (ациклический азот) во втором положении циклогексанового кольца:
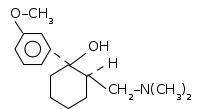
В
медицине трамадол используется в виде
гидрохлорида. Трамадола гидрохлорид
представляет собой бесцветные кристаллы
или белый кристаллический порошок,
легко растворимый в воде.
Трамадол обладает сильной анальгетической активностью, уступая, однако, по активности морфину приблизительно в 10 раз. Препарат хорошо переносится, не вызывая в обычных дозах выраженного угнетения дыхания и существенно не влияет на кровообращение и ЖКТ. Применяется при сильных острых и хронических болях: в послеоперационном периоде, при травмах, у онкологических больных и т.п.
Является одним из самых доступных препаратов наркотических анальгетиков, поскольку не относится к препаратам списков А и Б. Хранится с соблюдением правил хранения для наркотических анальгетиков.
Производные дифенилэтоксиуксусной кислоты.
Наркотические анальгетики, не содержащие циклогексанового или пиперидинового кольца были открыты в 40 годах XX века и широко использовались как дешевые заменители морфина (в военное время). В настоящее время препараты данной группы (метадон, декстроморамид) исключены из Госреестра. Исключение составляет лишь эстоцин, препарат, сочетающий в себе свойства наркотических анальгетиков и м-холиноблокаторов.
Эстоцин.

Эстоцин
представляет собой -диметиламинового
эфира ,-дифенил-
-этоксиуксусной
кислоты гидрохлорид:
По физико-химическим свойствам эстоцин представляет собой белый кристаллический порошок, растворимый в воде и спирте. рН 2% водного раствора 4.0–5.5.
Эстоцин — синтетический наркотический анальгетик. По химическому строению имеет сходство с рядом м-холиноблокаторов.
По анальгетическому эффекту эстоцин значительно слабее морфина и промедола, но меньше угнетает дыхание, не повышает тонуса блуждающего нерва; оказывает умеренное спазмолитическое и холинолитическое действие, уменьшает спазмы кишечника и бронхов.
Используется эстоцин при болях, связанных со спазмами гладкой мускулатуры, в предоперационном и послеоперационном периодах, при небольших травмах, для обезболивания родов.
Хранится по списку А в сухом месте, соблюдая правила хранения наркотических анальгетиков.
1 Сачков В.И., Сухонощенко Л.М. и др. Длительная перидуральная анальгезия морфином в остром периоде инфаркта миокарда. Кардиология. –1985, №9, стр. 80-83.
2 Павлова З.В., Сидоркин В.А. и др. Перидуральная анальгезия морфином у онкологических больных. Сов. мед. –1986, №5, стр. 92-97.
3 Дзизинский А.А., Тумак В.Н., Жаткин С.И. Влияние пролонгированной морфинной эпидуральной анальгезии на клиническое течение и величину зоны некроза у больных острым инфарктом миокарда. Тер. арх. –1991, №12, стр. 35-37.
4 Жоров В.И. Морфилонг. ЭИ. Новые лекарственные препараты. –1988, №4, стр. 9–13.