Строение атома (работа 4)
Строение атома
1. Ядро и электроны
Развитие естествознания на границе XIX-XX веков показало, что помимо химических превращений существует целый ряд процессов, в которых атомы выступают как сложные объекты, состоящие из положительно заряженной части - ядра и отрицательно заряженных электронов, суммарный заряд которых в точности компенсирует заряд ядра. В результате работ английского физика Дж. Дж. Томсона и американского физика Р.С. Малликена было установлено, что электрон имеет массу 9,1•1031 кг, или 1/1837 массы атома водорода, и заряд 1,6•10 19 Кл. Основная масса атома сосредоточена в ядре, которое занимает очень малую часть его объема: диаметр ядра порядка 1СГ14 м, он составляет лишь около 10 4 диаметра атома. Наглядно это соотношение размеров можно представить себе, если увеличить атом в 1011 раз: тогда ядро диаметром 1 мм разместится внутри атома диаметром 10 метров!
Позднее было показано, что атомные ядра состоят из положительно заряженных частиц - протонов и незаряженных частиц - нейтронов. Протон имеет заряд, равный заряду электрона, но со знаком плюс, его масса практически равна массе нейтрона. Отметим, что в химии принято выражать заряды ионов в единицах заряда электрона с соответствующим знаком, например Н+, Mg2+, СГ.
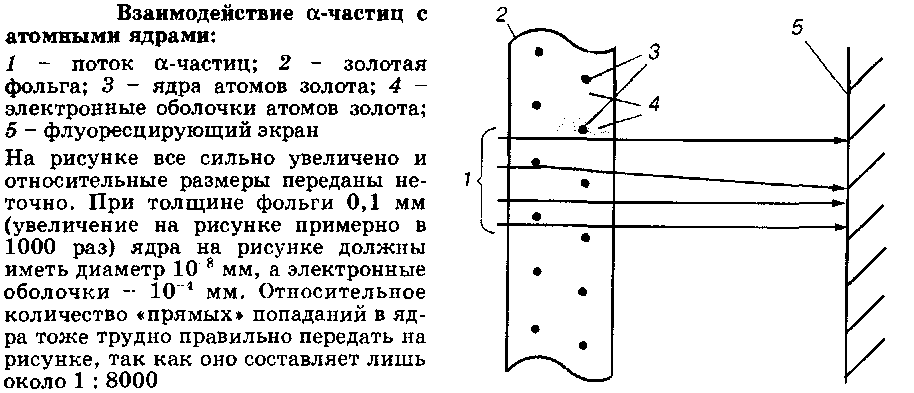
Таким образом, число протонов в ядре определяет его заряд и порядковый номер, а сумма чисел протонов и нейтронов - округленную общую массу ядра в атомных единицах, или массовое число атома. Очевидно, что в электронейтральном атоме число протонов в атомном ядре равно числу электронов в электронной оболочке атома.
2. Атомный номер элемента. изотопы
Порядковый номер элемента принято называть его атомным номером и обозначать буквой Z. Атомный номер лежит в основе систематизации химических элементов и определяет их положение в периодической системе.
При определенном атомном номере, т.е. при определенном числе протонов, в ядре могут находиться разные числа нейтронов, поэтому могут существовать отличающиеся по массе разновидности атомов одного и того же элемента - изотопы.
Например, природный водород представляет собой смесь изотопов с массовыми числами 1 и 2, а.
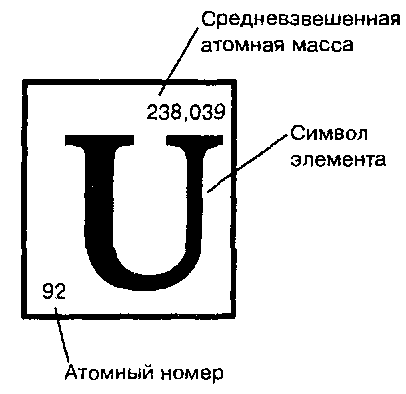
Клетка периодической таблицы
В ядре атома урана 92 протона, а в его электронной оболочке - 92 электрона
В периодической таблице, элементы расположены в порядке увеличения заряда ядра, а в отдельных клеточках таблицы принято приводить средневзвешенные атомные массы, поэтому они часто сильно отличаются от целочисленных.

Рис. 2.3, а. Масс-спектрометр.
Газ вводится в вакуумированный прибор через трубку (i) и подвергается ионизации потоком электронов из электронной пушки (2). Заряженные пластины (3) и (4) разгоняют поток полученных положительных ионов, который проходит через щель в пластине (4) и попадает в поле магнита (5), отклоняющее отдельные ионы в соответствии с отношением заряд: масса. За второй щелью (в) расположен детектор (7), который регистрирует число частиц, прошедших через щель. Меняя напряженность магнитного поля, можно последовательно регистрировать относительное количество ионов с различной массой, получая масс-спектр.
В масс-спектрометре молекулы газа превращаются в ионы. Показана часть масс-спектра, соответствующая нонам ТЮ+ и ТЮ>2>. Отдельные полосы отвечают пяти изотопам титана с массой 46, 47, 48, 49, 50 значений масс атомов и разделение изотопов стало возможным в результате создания масс-спектрометрии - метода, основанного на воздействии магнитного поля на направленные пучки заряженных частиц.
3. Ядерная модель атома
Первая модель атома была предложена в начале XX века Э. Резерфордом, новозеландцем, работавшем в Англии. Она предполагала, что электроны движутся с большой скоростью по круговым орбитам вокруг ядра, подобно планетам по отношению к Солнцу. По представлениям классической электромагнитной теории в таком атоме электрон должен приближаться по спирали к ядру, непрерывно излучая энергию. Через короткое время электрон неизбежно должен упасть на ядро. Это очевидное несоответствие фактам было не единственным недостатком модели Резерфорда: плавное изменение энергии электронов в атоме не согласовывалось с появившимися наблюдениями над спектрами атомов. Одним из достижений второй половины XIX века была разработка атомного спектрального анализа - точного и чувствительного метода, сыгравшего важнейшую роль в открытии новых элементов и послужившего экспериментальной основой изучения строения атомов. Метод основан на испускании света свободными атомами, получающимися при сильном нагреваний вещества; при этом атомы переходят из основного состояния с минимальной энергией в возбужденные состояния с более высокими энергиями.
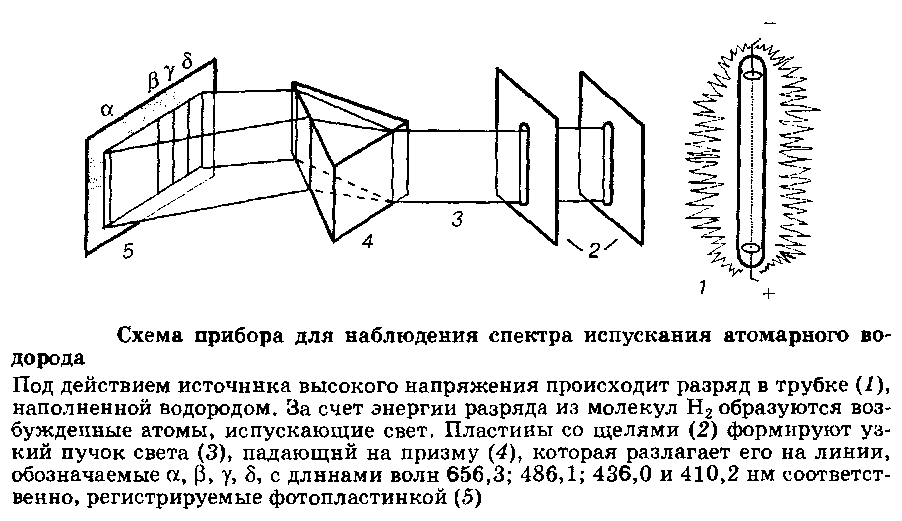
Возвращаясь в основное состояние, атомы излучают свет. Оказалось, что атомные спектры излучения состоят из отдельных линий, отвечающих только определенным длинам волн.
Чтобы объяснить линейчатый характер атомных спектров и устойчивость атомов, знаменитый датский физик Нильс Бор предложил два постулата, выходящие за рамки классической физики:
Из бесконечного числа орбит, возможных с точки зрения классической механики, допустимы лишь определенные орбиты, по которым электрон движется не излучая.
Частота поглощаемого или испускаемого атомом излучения при переходе из одного разрешенного состояния в другое определяется разностью энергий этих состояний.
При этом Бор опирался на идею Макса Планка о квантовании энергии. Планк установил, что, хотя свет, испускаемый раскаленным телом, кажется сплошным, световая энергия поглощается или излучается отдельными порциями - квантами Е = hv, пропорциональными частоте светового электромагнитного колебания. Коэффициент пропорциональности h = 6,6252 • 10 34 Дж • с был назван постоянной Планка. Таким образом в науку было введено понятие кванта света, или некоторого светового пакета - фотона, отражающее не только волновую, но и корпускулярную природу света.
Модель Бора позволила рассчитать точные значения энергии атома водорода и любых одноэлектронных ионов, но оказалась непригодной для объяснения наблюдаемых энергетических характеристик атомов с двумя и более электронами; главный же ее недостаток заключался в том, что она не давала логического обоснования природы квантования и устойчивости не меняющихся во времени состояний атома. Однако, несмотря на эти недостатки, сами идеи Бора о квантовании и стационарных состояниях легли в основу современного описания строения атома с позиций квантовой механики.
4. Волновые свойства электрона
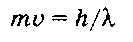
Вскоре после 1920 г. был сделан следующий важный шаг в познании микромира: было установлено, что не только световые кванты, но и любые микрочастицы, в том числе электроны, обладают двойственной природой - частицы как таковой и волны.
Например, электрону при скорости 3 • 10е м/с отвечает длина волны
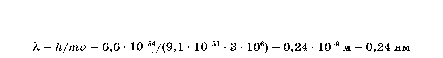
В частности, удалось обнаружить дифракцию электронов на периодической решетке кристаллов и на молекулах газов. Частице с массой покоя т, движущейся со скоростью v, соответствует длина волны X, которая может быть найдена из уравнения де Бройля: сопоставимая с размерами атома. В то же время можно говорить и об импульсе и даже о массе движущегося фотона, хотя, конечно, его масса покоя равна нулю. Это обстоятельство существенным образом влияет на характер информации, которую дает спектроскопия. При столкновении фотона с электроном меняются импульс фотона и частота света, тем самым давая экспериментатору информацию об импульсе электрона. Однако, поскольку импульсы фотона и электрона сопоставимы, при этом меняется и импульс электрона, который надо определить. Ситуация в какой-то степени подобна попытке измерить скорость бегуна с помощью наблюдателя, который прыгает ему на плечи с разбега. Математически эти соображения описываются принципом неопределенности Гейзенберга, согласно которому возможность одновременного определения положения микрочастицы в пространстве и ее импульса ограничена постоянной Планка. Это, в частности, означает, что если мы хотим определить с большой точностью энергию электрона в атоме, то мы не сможем столь же точно определить его положение по отношению к ядру.
5. Квантово-механическая модель атома
Представления о стационарных состояниях атома и двойственной природе электрона, а также требования принципа неопределенности были использованы австрийским физиком Эрвином Шредингером, который в 1926 г. предложил модель, описывающую электрон в атоме как своего рода стоячую волну, причем вместо точного положения электрона в пространстве рассматривалась вероятность его пребывания в определенном месте.
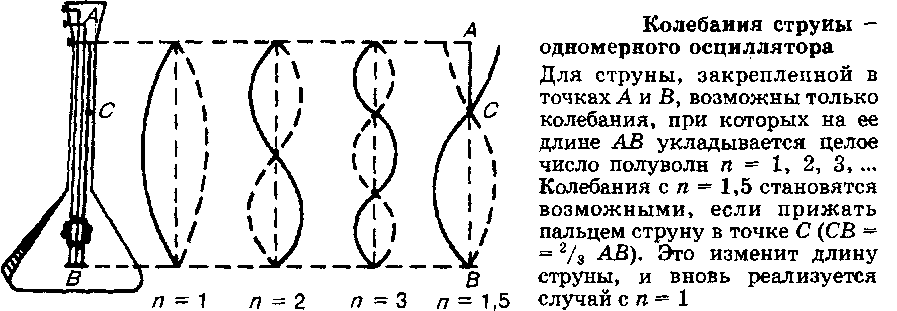
Для того чтобы представить себе электрон в виде трехмерной стоячей волны, остановимся сначала на более простой одномерной модели стоячей волны, в качестве которой можно взять струну, закрепленную на концах. Струна способна издавать звуки только определенных частот, так как на ее длине может уложиться лишь целое число полуволн - это и есть квантование энергии колебаний струны. Для описания характера стоячих волн одномерной системы достаточно одного числа п, которое однозначно определяет длину волны и число узловых точек, в которых струна неподвижна, как и на закрепленных концах.
Моделью двумерной системы, испытывающей стационарные колебания, может служить круглая мембрана, закрепленная по периметру, например, в телефонной трубке. Здесь также возможны лишь определенные, квантованные колебания, для описания которых необходимы уже два числа.
Теперь очевидно, что для описания пространственного движения электрона в атоме как трехмерной стоячей волны необходимы и достаточны три числа, получившие название квантовых чисел. Квантово-механическое описание атома не требует никаких дополнительных постулатов, квантование энергии электрона естественным образом возникает из природы самого атома или так называемых граничных условий, которые сводятся к тому, что электрон не покидает атом и способен двигаться с конечной скоростью.
В волновой механике электрон, как и любая микрочастица, описывается с помощью волновой функции. Его движение определяется уравнением, предложенным Шредингером, - знаменитым уравнением Шредингера. Решением этого уравнения является волновая функция \|/, которая соответствует разрешенной энергии электрона и описывает зависимость амплитуды стационарной волны, соответствующей электрону, от трех его пространственных координат. Квадрат волновой функции определяет вероятность пребывания электрона в некоторой пространственной области. Здесь мы как раз встречаемся со случаем точного знания энергии электрона и вероятностного описания его положения в пространстве. Во многих случаях удобно рассматривать электрон как размытое в пространстве облако отрицательного заряда. Плотность такого электронного облака в любой точке пропорциональна V) /2. Модель электронного облака наглядно описывает распределения электронной плотности в пространстве, хотя она физически несовершенна, так как одноименно заряженные части облака должны отталкиваться друг от друга, вызывая его рассеивание. На самом же деле электрон не отталкивается "сам от себя". Это обстоятельство несколько ограничивает аналогию между электроном и облаком, но не мешает нам говорить об электронных облаках во всех случаях, когда мы не интересуемся деталями, связанными с их потенциальной энергией. Представлением об электронных облаках мы будем широко пользоваться в этой книге.
6. Одноэлектронный атом. квантовые числа
В случае атома водорода и одноэлектронных ионов уравнение Шредингера может быть решено точно.
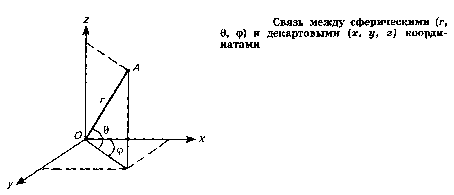
Таким образом может быть получен набор волновых функций электрона или атомных орбиталей. Словом "орбиталь", в отличие от "орбиты", подчеркивается волновая природа электрона. Каждая АО зависит от трех пространственных координат электрона и характеризуется определенными значениями трех квантовых чисел п, I, т.д.ля описания одноэлектронного атома, в котором электрон принимает участие в единственном взаимодействии - с ядром, обладающим сферически-симметричным электростатическим полем, удобно использовать не декартову систему координат с переменными х, у, г, а сферическую с переменными.
Для наших целей нет необходимости заниматься математической стороной решения сложного дифференциального уравнения Шредингера, однако для дальнейших химических выводов важно, что в сферических координатах возможно разделение переменных, и само его решение \j/>n> приобретает более удобный для дальнейшего анализа вид:
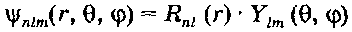
Здесь R>nt> - радиальная составляющая волновой функции, зависящая от единственной переменной г - расстояния электрон - ядро и характеризуемая только двумя квантовыми числами п и I, а Y>lm> - угловая составляющая волновой функции, описывающая зависимость распределения электронной плотности от углов 9 и ф, т.е. форму и ориентацию АО, и характеризуемая квантовыми числами I и т. Рассмотрим последовательно физический смысл квантовых чисел п, I, ти характер различных АО.
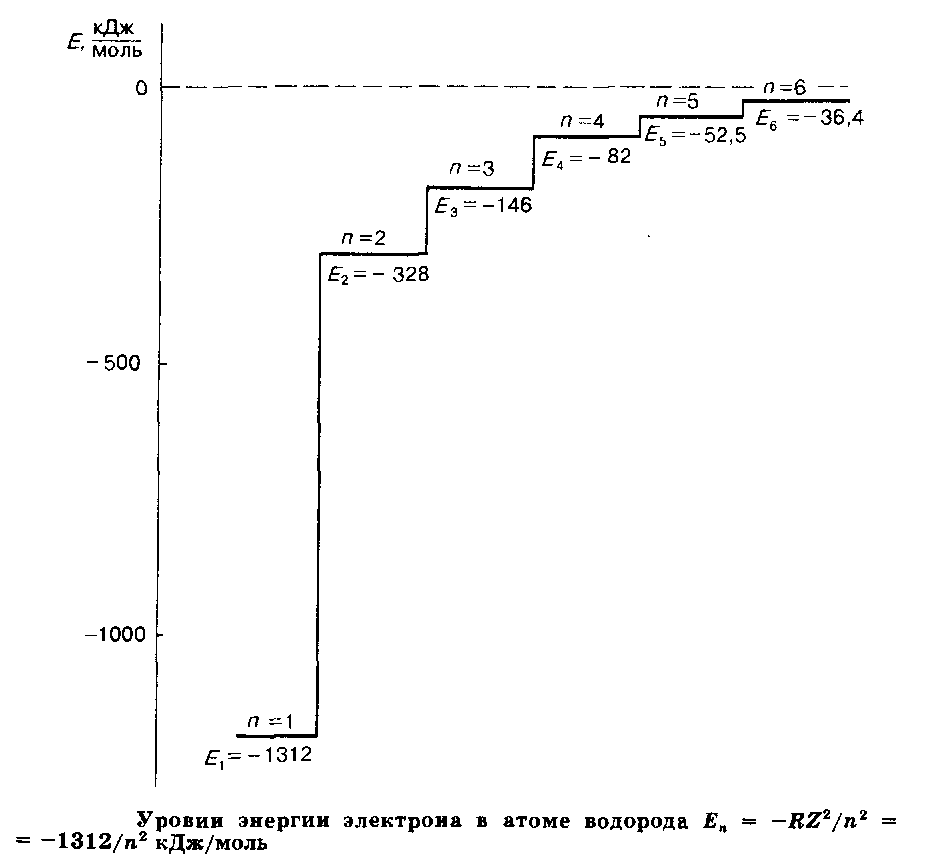
Квантовое число п называется главным квантовым числом. Величина п определяет номер электронного слоя: чем меньше п, тем прочнее электрон связан с ядром и тем ближе, в среднем, он находится к ядру. Главное квантовое число может принимать целочисленные положительные значения 1, 2, 3 и т.д. Набор АО с одинаковым п составляет слой. Основному состоянию атома водорода соответствует п = 1, при этом Е>1> = - 1312 кДж. Такое количество энергии выделится при образовании одного моля атомов водорода из протонов и электронов, находящихся на бесконечном удалении друг от друга. В одноэлектронном атоме или в одноэлектронном ионе с зарядом ядра Z главное квантовое число однозначно определяет энергию электрона Е>п>:
Е>п> = - Rtf/a2
Здесь R - постоянный множитель, равный 1312 кДж, если энергия отнесена к 1 молю атомов и заряд Z измеряется в единицах заряда электрона.
Второе квантовое число I называется орбитальным, оно определяет возможные квантованные величины орбитального момента количества движения электрона. Число I может принимать целочисленные значения от 0 до п - 1.
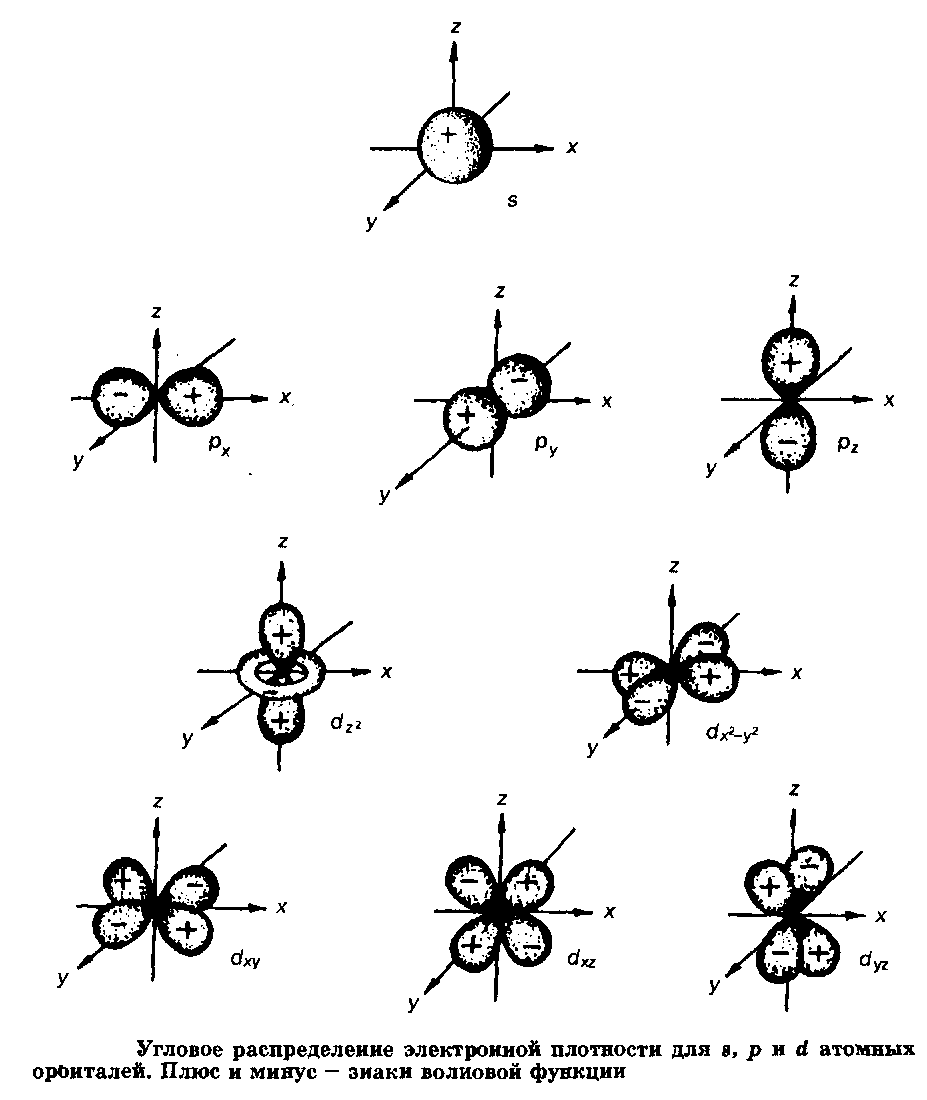
По традиции, сложившейся в процессе изучения атомных спектров, значения I обычно обозначают буквами: s, р, d, f и далее по английскому алфавиту вместо 0, 1, 2, 3 и т.д. Для нас самое главное то, что при описании электрона в виде облака число I определяет его форму. Так, s-электроны имеют шарообразные, сферически симметричные облака, лишь в этом случае волновая функция \|/ не зависит от углов Э и ф; р-электроны {I = 1) имеют гантелеобразные облака, d-электроны образуют облака еще более сложной формы.
Вернемся к уравнению, в котором при R>M> стоят индексы nl. Как уже отмечалось, это значит, что первое и второе квантовые числа вместе полностью определяют характер радиальной части волновой функции. Рассмотрим, как меняется плотность электронного облака с расстоянием от ядра. На рис.2.10 по оси ординат отложена вероятность нахождения электрона в пространстве, заключенном между сферами с радиусами г и г + dr. Из рисунка видно, что все эти кривые, которые называются кривыми радиального распределения электронной плотности, проходят через один или несколько максимумов. Если максимумов несколько, то они разделены узловыми точками, в которых плотность равна нулю. Последний от ядра максимум - самый большой, главный. Число максимумов равно п - I, число узловых точек равно - 1. Таким образом, с учетом углового и радиального распределения облако, соответствующее ls-электрону, можно представить себе как диффузный шар переменной плотности, имеющей один максимум и постепенно сходящей на нет при удалении от центра. Облако 2"-электрона подобно сфере с двумя сгущениями плотности и т.д.
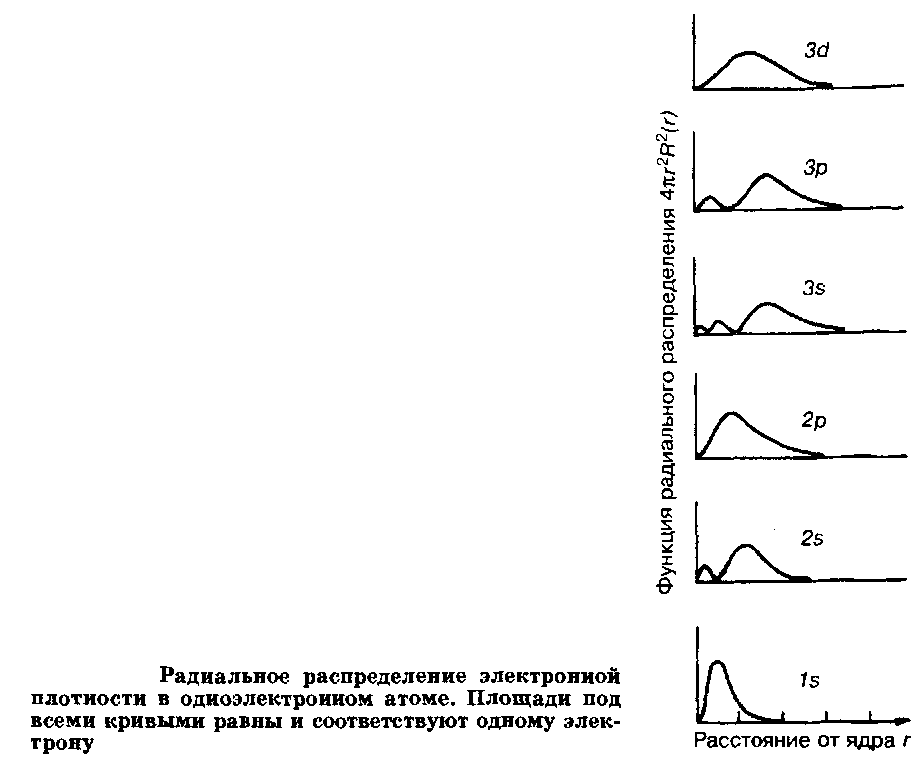
Видно, что среднее расстояние электрона от ядра существенно различно для разных атомных орбиталей: оно растет с увеличением п, а при равных п - с уменьшением I. Чем меньше I при одинаковых п, тем дальше от ядра и тем ниже главный максимум и тем большая часть электронной плотности находится ближе к ядру за счет внутренних максимумов.
Третье квантовое число т - магнитное - определяет направление орбитального момента электрона, а с точки зрения модели электронного облака - ориентацию его в пространстве. Магнитное квантовое число может принимать целочисленные значения от - I до +1, что соответствует разрешенным квантовой механикой значениям проекции орбитального момента на заданное направление в пространстве. Следует отметить, что определенное направление может быть задано внешним полем - электрическим или магнитным. В отсутствие внешнего поля все разрешенные ориентации электронного облака равновероятны.
Поскольку облако s-электронов сферически симметрично, вопрос о его ориентации просто не имеет смысла. В случае р-электронов возможны три значения магнитного квантового числа - 1,0 и +1 и, соответственно, разрешены три взаимно перпендикулярные ориентации гантелеобразного облака. У d-электронов возможны пять значений т, у /электронов - семь.
Итак, три квантовых числа - главное, орбитальное и магнитное - позволяют задать атомную орбиталъ и достаточно подробно охарактеризовать одноэлектронный атом: мы точно знаем энергию электрона и можем качественно описать электронное облако - его форму, ориентацию в присутствии внешнего поля, число сгущений электронной плотности и число внутренних узловых поверхностей, где плотность сходит к нулю.
Однако тремя квантовыми числами не исчерпываются данные, необходимые для полного описания состояния электрона в атоме. Детальное исследование атомных спектров показало, что электрон обладает собственным моментом количества движения, который получил название спинового момента или спина. При вероятностном описании электрона как стоячей волны или как электронного облака спин не имеет классических аналогий - это просто свойство микрочастиц.
Спин электрона характеризуется спиновым квантовым числом m>s>, которое может иметь два значения +1/2 и - 1/2, т.е. спин может иметь два противоположных направления.
Таким образом, для полной характеристики состояния электрона в атоме необходимы четыре квантовых числа. Первые три из них определяют распределение его плотности в пространстве, а четвертое - его спин. Знание смысла и возможных значений квантовых чисел имеет исключительное значение для химика, поэтому ниже мы приводим краткую сводку важнейших сведений такого рода.

Решение уравнения Шредингера для атома водорода позволяет, в принципе, рассчитать его основные характеристики с любой точностью, даже точнее, чем их дает эксперимент. Наиболее важными экспериментальными характеристиками любых атомов являются энергии отрыва и присоедниения электронов. Энергию отрыва электрона от атома, молекулы или иона не совсем правильно принято называть потенциалом ионизации. Потенциал ионизации обозначают обычно буквой / и измеряют в электрон-вольтах. Экспериментально измеренный потенциал ионизации водорода равен 13,6 эВ* или как раз 1312 кДж.
Другой важной энергетической характеристикой атома является сродство к электрону - энергия, которая выделяется при присоединении к нему дополнительного электрона. Сродство обычно обозначают буквой А с указанием частицы, например для водорода А>н> = 73 кДж/моль. Знак "плюс" здесь говорит о том, что атом водорода приобретает второй электрон с выделением энергии, образуя ион Н.
7. Многоэлектронные атомы
При переходе от одноэлектронного атома к многоэлектронному в дополнение к взаимодействию электрон - ядро появляется новый тип взаимодействий - электронов друг с другом. Взаимодействие любого электрона с остальными зависит от состояния каждого электрона и не может быть точно учтено, если неизвестны волновые функции всех остальных электронов, которые, в свою очередь, не могут быть рассчитаны, если неизвестно взаимодействие данного электрона с остальными. Получается замкнутый круг, который принципиально не дает возможности точно решить уравнение Шредингера для многоэлектронного атома. Эта трудность, к счастью, может быть преодолена посредством приближенного решения, суть которого заключается в следующем. Каждый электрон рассматривается отдельно таким образом, как будто он находится в одноэлектронном атоме, заряд ядра которого частично экранирован усредненным сферически-симметричным полем остальных электронов. Отдельный электрон при этом испытывает только кулоновское притяжение центра, состоящего из ядра и остальных электронов, т.е. действие некоторого центрально-симметричного положительного эффективного заряда, меньшего, чем заряд ядра. При таком подходе для многоэлектронных атомов сохраняют смысл понятия атомной орбитали и четырех квантовых чисел, только истинный заряд ядра заменяется эффективным.
Рассмотрим для примера с этой точки зрения атом гелия в основном состоянии. Если бы в нем совсем не было межэлектронного взаимодействия, то оба электрона находились бы на орбитали с п = 1 в поле заряда Z = +2 и по формуле имели бы энергию Е = = - 13,6 • 4 = - 54,4 эВ, равную экспериментально определенному потенциалу ионизации одноэлектронного иона Не+. Другой крайний вариант - идеальное экранирование заряда ядра одним электроном по отношению к другому, который тогда испытывал бы действие заряда ядра, уменьшенного ровно на единицу, т.е. ядра с Z = +1. Тогда мы получаем точно такую же ситуацию, как в атоме водорода, и потенциал ионизации должен быть равен 13,6 эВ.
Для реального атома гелия истина лежит где-то между этими крайностями, действительно, его потенциал ионизации составляет 24,6 эВ. По формуле можно подсчитать заряд Z*, который должен испытывать на себе электрон с этой энергией в одноэлектронном атоме: Z* = ^24,6/13,6 = 1,34. Это и есть тот самый эффективный заряд, который действует на каждый электрон в атоме гелия.
В общем случае эффективный заряд ядра Z* - это положительный заряд, который "чувствует" электрон в многоэлектронном атоме на заданной АО. Пользуясь эффективными зарядами ядер, мы можем оценивать энергию атомных орбиталей в многоэлектронном атоме.
8. Электронная конфигурация атома
Распределение электронов по АО называют электронной конфигурацией атома. Порядок заполнения АО электронами определяется двумя важнейшими принципами.
Согласно принципу минимума энергии наиболее устойчивому состоянию атома отвечает размещение электронов на орбиталях с наименьшей энергией, т.е. обеспечивается минимум потенциальной энергии системы, состоящей из электронов с ядром.
Согласно принципу Паули любые два электрона в атоме во избежание бесконечно большого взаимного отталкивания должны отличаться друг от друга хотя бы одним квантовым числом. Так, если два электрона находятся на одной АО, то они должны иметь противоположные спины.
В соответствии с указанными принципами атом гелия в основном состоянии имеет электронную конфигурацию Is2, при которой оба электрона находятся на ls-орбитали и имеют противоположные спины. Суммарный спин атома равен нулю. Схематически эту ситуацию можно изобразить в виде ячейки с двумя стрелками:
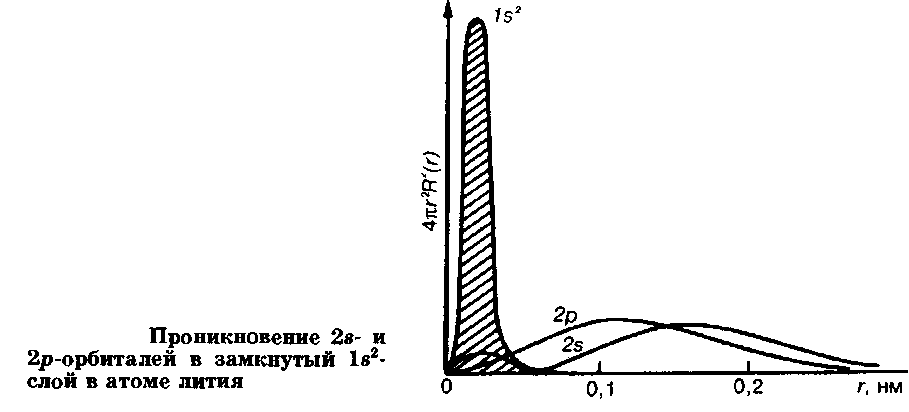
Атом лития, следующий за гелием в периодической системе, содержит три электрона. По принципу минимума энергии два из них расположатся, как и в атоме гелия, на ls-орбитали. Третий электрон в соответствии с принципом Паули должен располагаться на АО с п = 2. Однако таких возможностей две - 2s - и 2р-орбитали, и электрон будет иметь меньшую энергию на той из них, где он будет испытывать действие более высокого эффективного заряда. Рассмотрим с этой точки зрения кривые распределения электронной плотности в атоме лития в зависимости от расстояния от ядра. Из этих кривых хорошо видно, что замкнутый слой Is расположен гораздо ближе к ядру, чем основная плотность 2s - или 2р-электрона. Однако внутренний максимум 2в-электрона практически полностью проникает в ls-электронную плотность в близкой к ядру области, и определенная часть его плотности "чувствует" на себе почти полный заряд ядра Z=+3. Единственный максимум 2р-электрона далек от ядра, а в области сосредоточения ls-электронов находится лишь незначительная его часть. Следовательно, в атоме лития электрон на 2в-орбитали испытывает на себе действие несколько более высокого эффективного заряда, он несколько хуже экранирован от ядра ls-электронами, чем электрон на 2р-орбитали, и прочнее связан с ядром. Соответственно, в основном состоянии атом лития будет иметь электронную конфигурацию ls22s1, а конфигурация ls22p1 отвечает возбужденному состоянию.
Рассматривая одноэлектронный атом, мы пришли к заключению, что при одинаковых п за счет внутренних максимумов ближе к ядру находится большая часть плотности того электрона, который расположен на орбитали с меньшим значением I. Это в основном и определяет тот важнейший для всей химии факт, что в одном слое s-электроны испытывают на себе самый большой эффективный заряд, р-электроны - меньший, d-электроны - еще меньше и т.д.
Другими словами, res-электроны наиболее прочно связаны с ядром и находятся на наиболее низком энергетическом уровне, далее следуют яр-электроны, а затем - red-электроны. Таким образом, энергия электронов в многоэлектронных атомах зависит не только от п, но и от I; при равных п она возрастает в порядке увеличения I. Порядок заполнения АО для любого атома описывается эмпирическими правилами Клечковского:
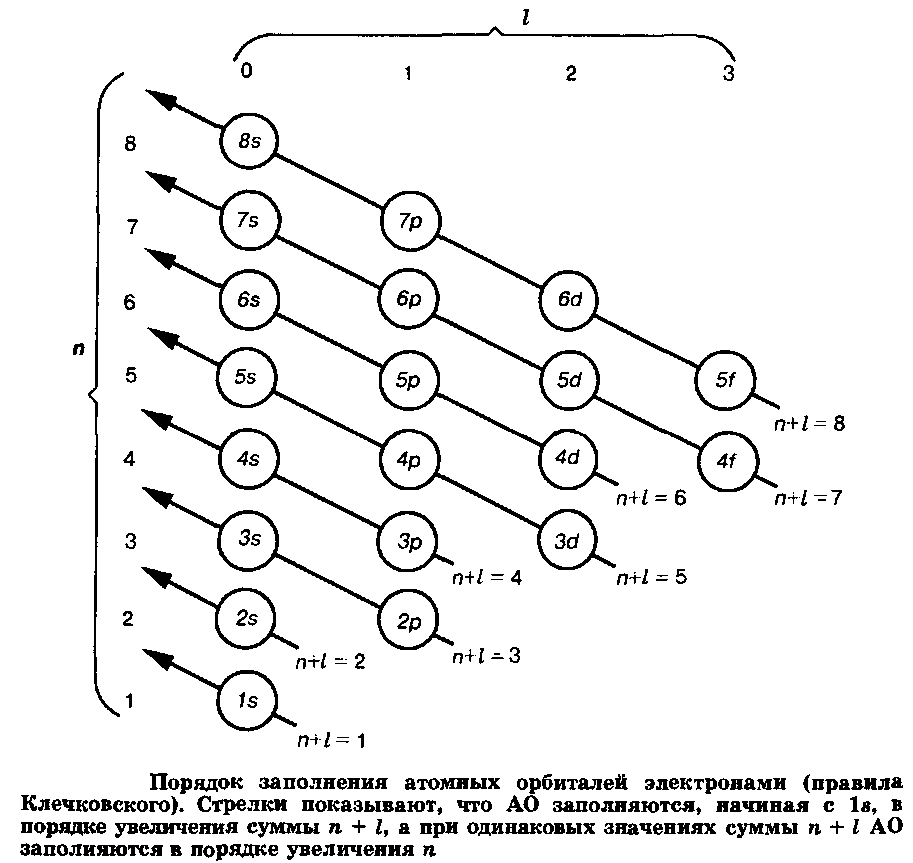
АО заполняются в порядке увеличения суммы п + I. При одинаковых значениях суммы п + I АО заполняются в порядке увеличения п.
Отметим, что одному и тому же Сочетанию значений п и I могут отвечать несколько атомных орбиталей, различающихся значениями магнитного квантового числа т. Например, 2р-электрон может находиться в любой из трех ячеек с т, равным - 1, 0 или +1:
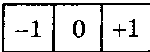
Во всех этих трех случаях электрон будет иметь одну и ту же энергию, но разные волновые функции. В таких случаях говорят, что состояние электрона вырождено.
В данном случае оно трижды вырождено, т.е. три состояния имеют одинаковую энергию. Если в атоме появляется второй р-электрон, го межэлектронное отталкивание будет минимальным, когда оба электрона находятся в разных ячейках и имеют одинаковые спины.

В общем случае при определении электронной конфигурации основного состояния атома удобно пользоваться правилом Хунда: минимальной энергии отвечает максимальный суммарный спин.
Например, основному состоянию атома азота отвечает электронная конфигурация:
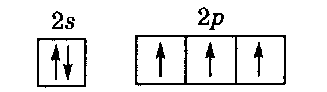
Указанные принципы позволяют легко определить электронную конфигурацию любого атома; для основных состояний электронные конфигурации атомов приведены в табл.2.1
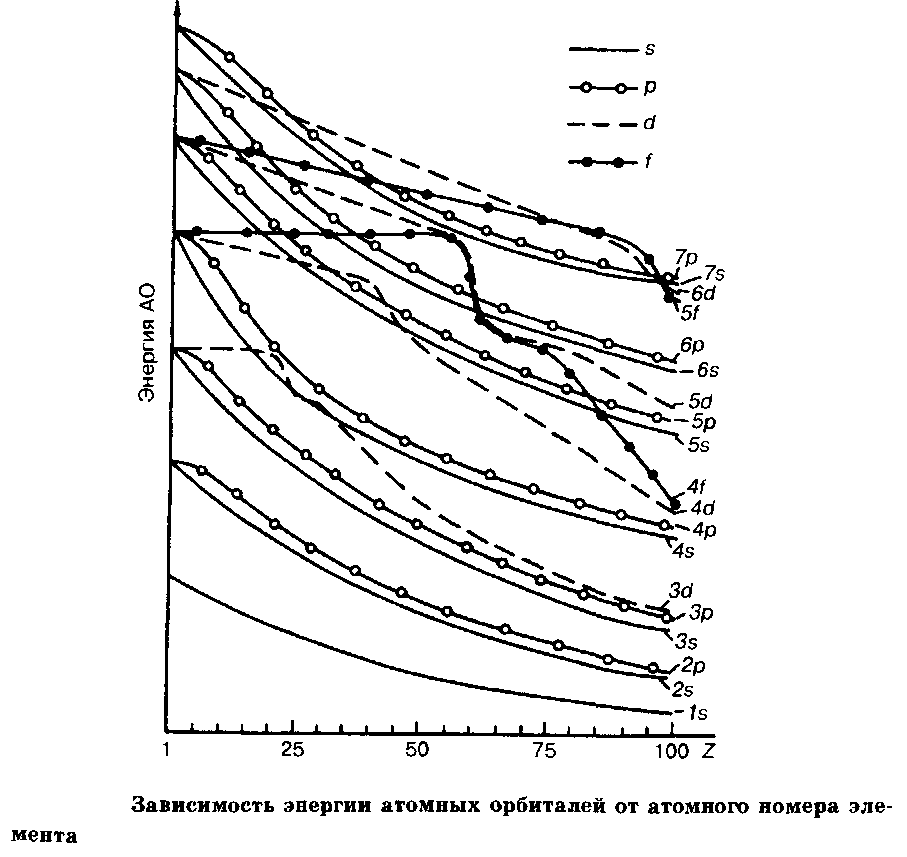
Энергия электронов, находящихся на различных орбиталях атома, которую для краткости принято называть энергией атомных орбиталей, показана на рис. в зависимости от атомного номера. При Z = 1 число энергетических уровней соответствует числу значений п. При Z > 1 уровни расщепляются на подуровни с разными значениями I, причем энергия подуровней увеличивается в порядке возрастания I. Хотя ход отдельных кривых довольно сложен, но в целом он разумно объясняется в терминах эффективных зарядов таким же образом, как и различие 2s - и 2р - подуровней.
Электронные конфигурации атомов в основном состоянии
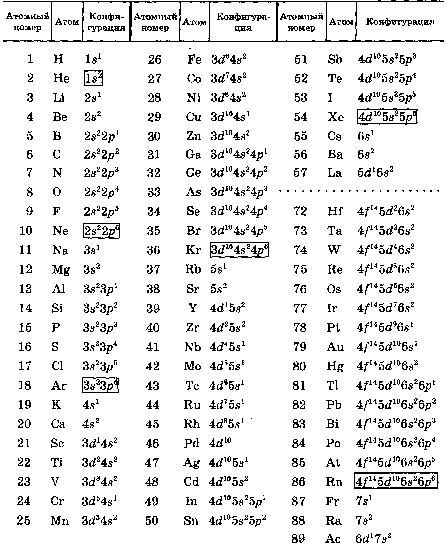
Возвращаясь к литию, отметим, что этот элемент в какой-то степени аналогичен водороду из-за того, что его атом содержит один 2в-электрон, и литий легко образует ион Li+. Однако первый потенциал ионизации лития /i = 5,39 эВ существенно меньше, чем у водорода, здесь уже сказывается рост главного квантового числа). Поэтому литий легко реагирует с большинством неметаллов, хорошо растворяется в кислотах, теряя электрон и переходя в ион Li*, т.е. проявляет свойства типичного активного металла.
Второй потенциал ионизации лития I>2> = 75,7 эВ очень велик, так как его ls-электроны расположены гораздо ближе к ядру, чем 2в-электрон. На этом примере хорошо видно, что электроны внутренних замкнутых слоев не распространяются на периферию атома и настолько прочно связаны с ядром, что, как правило, непосредственно не затрагиваются в химических процессах. В химии оказывается очень полезным разделение электронов на внешние, или валентные, и внутренние, или основные. "Химическая" роль последних сводится к участию в формировании эффективного заряда, действующего на валентные электроны.
9 Электроотрицательность
Идея эффективного заряда лежит в основе оценки ряда полезных характеристик атомов, которыми мы будем широко пользоваться в этой книге. Среди них особенно важна электроотрицательность, которая представляет собой обобщенную характеристику элемента, связанную не с электронами на отдельных орбиталях, а с внешними электронами вообще. Под электроотрицательностью понимают усредненную характеристику способности атома, находящегося в соединении, притягивать электрон. При этом пренебрегают разницей в состояниях атомов в различных соединениях. В отличие от потенциала ионизации и сродства к электрону, электроотрицательность - не строго определенная физическая величина, а полезная условная характеристика.
В табл.2.2 приведены значения электроотрицательности элементов по шкале Олреда - Рохова, основанной на вычислении силы кулоновского притяжения, действующей на внешний электрон. Отметим, что весь диапазон значений ЭО элементов заключен между 0,9 для наименее электроотрицательных металлов 1-й и 2-й групп и 4,1 для наиболее электроотрицательного фтора.