Инертные газы
Британская Международная Школа
Реферат по химии
“Инертные газы и их свойства”
Ученика 9б класса
Соколенко Алексея
Руководитель:
Чернышева И.В.
Москва
2003
Содержание:
I Вступление……………………………………………………………………………2
Инертные газы – элементы VIIIА группы……………………………………...2
Аргон на земле и во вселенной………………………………………………….5
II История открытия газов…………………………………………………..................7
2.1 Аргон………………………………………………………………………………7
2.2 Гелий…………………..…………………………………………………………..8
2.3 Криптон………………………………………………………..…………………..9
2.4 Неон……………………………………………………………..…………………9
2.5 Ксенон……………………………………………………………….…………….9
2.6 Радон………………………………………………………………..…………….10
III Свойства инертных газов и их соединений…………………………………….....10
3.1 Физические свойства инертных газов………………………………………….10
3.2 Химические свойства инертных газов……………………………………….....11
3.3 Получение Аргона…………………………………………………...…………..14
3.4 Физиологические свойства инертных газов……………………………………15
IV Применение инертных газов…………………………………………………..…..16
Список использованной литературы………………………………………………....18
I Вступление.
Везде и по всюду нас окружает атмосферный воздух. Из чего он состоит? Ответ не составляет труда: из 78,08 процента азота, 20,9 процента кислорода, 0,03 процента углекислого газа, 0,00005 процента водорода, около 0,94 процента приходится на долю так называемых инертных газов. Последние были открыты всего лишь в конце прошлого столетия.
Радон образуется при радиоактивном распаде радия и в ничтожных количествах встречается в содержащих уран материалах, а также в некоторых природных водах. Гелий являющийся продуктом радиоактивного α-распада элементов, иногда в заметном количества содержится в природном газе и газе, выделяющемся из нефтяных скважин. В огромных количествах этот элемент содержится на Солнце и на других звездах. Это второй элемент по распространенности во вселенной (после водорода).
Инертные газы – элементы 8А группы.
Конфигурация внешнего электронного слоя атомов гелия 1s2, остальных элементов подгруппы VIII – ns2np6.


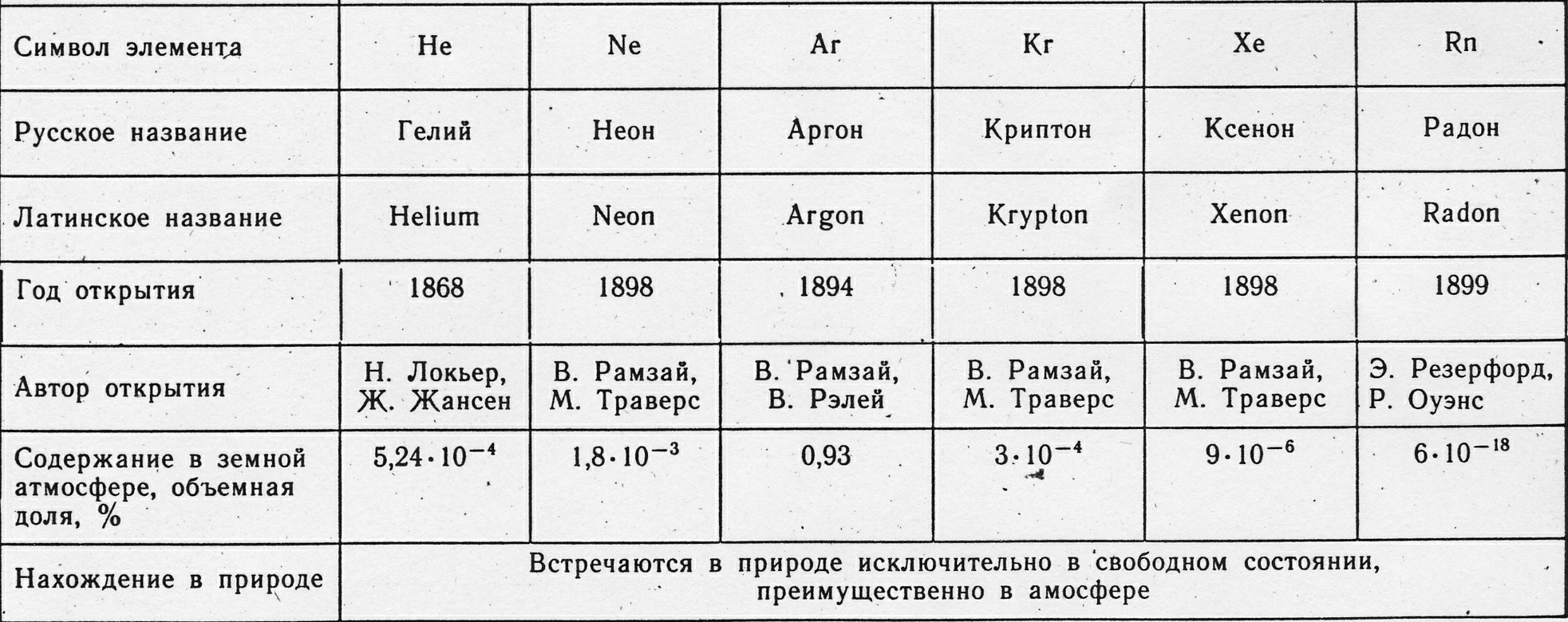
1.2 Аргон на земле и во вселенной.
На Земле аргона намного больше, чем всех прочих элементов его группы, вместе взятых. Его среднее содержание в земной коре (кларк) в 14 раз больше, чем гелия, и в 57 раз больше, чем неона. Есть аргон и в воде, до 0,3 см3 в литре морской и до 0,55 см3 в литре пресной воды. Любопытно, что в воздухе плавательного пузыря рыб аргона находят больше, чем в атмосферном воздухе. Это потому, что в воде аргон растворим лучше, чем азот... Главное «хранилище» земного аргона – атмосфера. Его в ней (по весу) 1,286%, причем 99,6% атмосферного аргона – это самый тяжелый изотоп – аргон-40. Еще больше доля этого изотопа в аргоне земной коры. Между тем у подавляющего большинства легких элементов картина обратная – преобладают легкие изотопы. Причина этой аномалии обнаружена в 1943 г. В земной коре находится мощный источник аргона-40 – радиоактивный изотоп калия 40К. Этого изотопа на первый взгляд в недрах немного – всего 0,0119% от общего содержания калия. Однако абсолютное количество калия-40 велико, поскольку калий – один из самых распространенных на нашей планете элементов. В каждой тонне изверженных пород 3,1 г калия-40. Радиоактивный распад атомных ядер калия-40 идет одновременно двумя путями. Примерно 88% калия-40 подвергается бета распаду и превращается в кальций-40. Но в 12 случаях из 100 (в среднем) ядра калия-40 не излучают, а, наоборот, захватывают по одному электрону с ближайшей к ядру К-орбиты («К-захват»). Захваченный электрон соединяется с протоном – образуется новый нейтрон в ядре и излучается нейтрино. Атомный номер элемента уменьшается на единицу, а масса ядра остается практически неизменной. Так калий превращается в аргон. Период полураспада 40К достаточно велик – 1,3 млрд лет. Поэтому процесс образования 40Аr в недрах Земли будет продолжаться еще долго, очень долго. Поэтому, хотя и чрезвычайно медленно, но неуклонно будет возрастать содержание аргона в земной коре и атмосфере, куда аргон «выдыхается» литосферой в результате вулканических процессов, выветривания и перекристаллизации горных пород, а также водными источниками. Правда, за время существования Земли запас радиоактивного калия основательно истощился – он стал в 10 раз меньше (если возраст Земли считать равным 4,5 млрд лет.). Соотношение изотопов 40Аr: 40К и 40Ar: 36Аr в горных породах легло в основу аргонного метода определения абсолютного возраста минералов. Очевидно, чем больше эти отношения, тем древнее порода. Аргонный метод считается наиболее надежным для определения возраста изверженных пород и большинства калийных минералов. За разработку этого метода профессор Э.К. Герлинг в 1963 году удостоен Ленинской премии. Итак, весь или почти весь аргон-40 произошел на Земле от калия-40. Поэтому тяжелый изотоп и доминирует в земном аргоне. Этим фактором объясняется, кстати, одна из аномалий периодической системы. Вопреки первоначальному принципу ее построения – принципу атомных весов – аргон поставлен в таблице впереди калия. Если бы в аргоне, как и в соседних элементах, преобладали легкие изотопы (как это, по-видимому, имеет место в космосе), то атомный вес аргона был бы на две-три единицы меньше... Теперь о легких изотопах. Откуда берутся 36Аr и 38Аr? Не исключено, что какая-то часть этих атомов реликтового происхождения, т.е. часть легкого аргона пришла в земную атмосферу из космоса при формировании нашей планеты и ее атмосферы. Но большая часть легких изотопов аргона родилась на Земле в результате ядерных процессов. Вероятно, еще не все такие процессы обнаружены. Скорее всего некоторые из них давно прекратились, так как исчерпались короткоживущие атомы-«родители», но есть и поныне протекающие ядерные процессы, в которых рождаются аргон-36 и аргон-38. Это бета-распад хлора-36, обстрел альфа-частицами (в урановых минералах) серы-33 и хлора-35:
36>17>Cl β–→ 36>18>Ar + 0>–1>e + ν.
33>16>S + 4>2>He → 36>18>Ar + 1>0>n.
35>17>Cl + 4>2>He → 38>18>Ar + 1>0>n + 0>+1>e.
В материи Вселенной аргон представлен еще обильнее, чем на нашей планете. Особенно много его в веществе горячих звезд и планетарных туманностей. Подсчитано, что аргона в космосе больше, чем хлора, фосфора, кальция, калия – элементов, весьма распространенных на Земле. В космическом аргоне главенствуют изотопы 36Аr и 38Аr, аргона-40 во Вселенной очень мало. На это указывает масс-спектральный анализ аргона из метеоритов. В том же убеждают подсчеты распространенности калия. Оказывается, в космосе калия примерно в 50 тыс. раз меньше, чем аргона, в то время как на Земле их соотношение явно в пользу калия – 660 : 1. А раз мало калия, то откуда же взяться аргону-40?!
II История открытия инертных газов.
К концу 18 века были обнаружены многие из известных газов. К ним относились: кислород – газ, поддерживающий горение; углекислый газ – его можно было легко обнаружить по весьма примечательному свойству: он мутил известковую воду; и, наконец, азот, горение не поддерживающий и на известковую воду не действующий. Таков был представлении химиков того времени состав атмосферы, и некто, кроме известного английского ученого лорда Кавендиша, не сомневался в этом.
И у него был повод для сомнения.
В 1785 году он проделал довольно простой опыт. Прежде всего он удалил из воздуха углекислый газ. На оставшуюся смесь азота и кислорода он подействовал электрической искрой. Азот, реагируя с кислородом, давал бурные пары оксидов азота, которые, растворяясь в воде, превращались в азотную кислоту. Эта операция повторялась многократно.
Однако немного менее одной сотой части объема воздуха, взятого для опыта, оставалась неизменной. К сожалению, этот эпизод был забыт не многие годы.
2.1 Аргон.
В 1785 г. английский химик и физик Г. Кавендиш обнаружил в воздухе какой-то новый газ, необыкновенно устойчивый химически. На долю этого газа приходилась примерно одна сто двадцатая часть объема воздуха. Но что это за газ, Кавендишу выяснить не удалось. Об этом опыте вспомнили 107 лет спустя, когда Джон Уильям Стратт (лорд Рэлей) натолкнулся на ту же примесь, заметив, что азот воздуха тяжелее, чем азот, выделенный из соединений. Не найдя достоверного объяснения аномалии, Рэлей через журнал «Nature» обратился к коллегам-естествоиспытателям с предложением вместе подумать и поработать над разгадкой ее причин...Спустя два года Рэлей и У. Рамзай установили, что в азоте воздуха действительно есть примесь неизвестного газа, более тяжелого, чем азот, и крайне инертного химически. Когда они выступили с публичным сообщением о своем открытии, это произвело ошеломляющее впечатление. Многим казалось невероятным, чтобы несколько поколений ученых, выполнивших тысячи анализов воздуха, проглядели его составную часть, да еще такую заметную – почти процент! Кстати, именно в этот день и час, 13 августа 1894 г., аргон и получил свое имя, которое в переводе с греческого значит «недеятельный». Его предложил председательствовавший на собрании доктор Медан. Между тем нет ничего удивительного в том, что аргон так долго ускользал от ученых. Ведь в природе он себя решительно ничем не проявлял! Напрашивается параллель с ядерной энергией: говоря о трудностях ее выявления, А. Эйнштейн заметил, что нелегко распознать богача, если он не тратит своих денег... Скепсис ученых был быстро развеян экспериментальной проверкой и установлением физических констант аргона. Но не обошлось без моральных издержек: расстроенный нападками коллег (главным образом химиков) Рэлей оставил изучение аргона и химию вообще и сосредоточил свои интересы на физических проблемах. Большой ученый, он и в физике достиг выдающихся результатов, за что в 1904 г. был удостоен Нобелевской премии. Тогда в Стокгольме он вновь встретился с Рамзаем, который в тот же день получал Нобелевскую премию за открытие и исследование благородных газов, в том числе и аргона.
2.2 Гелий.
|
|
Вскоре Размай послал своих помощников в лондонские химические магазины за урановым минералом клевеитом. Было куплено 30 грамм клевеита, и в тот же день Размай со своим помощником Метьюзом извлек несколько кубических сантиметров газа. Размай подверг этот газ спектраскопическому исследованию. Он увидел яркую желтую линию, очень похожую на линию натрия и в тоже время отличающуюся от нее по своему положению в спектре. Размай был на столько удивлен, что разобрал спектроскоп, почистил его, но при новом опыте снова обнаружил яркую желтую линию, не совпадавшую с линей натрия. Размай просмотрел спектры всех элементов. Наконец он вспомнил о загадочной линии в спектре солнечной короны.
|
|
Он назвал этот гипотетический элемент гелием, то есть “солнечным”. Но на земле он обнаружен не был. Физики и химики им не заинтересовались: на Солнце, мол, совершенно другие условия, там и водород сойдет за гелий.
Так неужели в его руках этот самый гелий? Размай почти уверен в этом, но он хочет услышать подтверждение от известного спектроскописта Крукса. Размай посылает ему газ на исследование и пишет о том, что нашел какой-то новый газ, названый им криптоном, по-гречески означает “скрытый”. Телеграмма от Крукса гласила: “Криптон есть гелий”.
2.3 Криптон.
|
|
И неизвестно, обнаружил бы ученый новые инертные газы, если бы во время его поисков Линде в Генмании и Хемпсон в Англии не взяли одновременно патент на машину, сжижжающую воздух.
Эта машина словно была специально создана для обнаружения инертных газов. Принцип ее действия основан на известном физическом явлении, если сжать воздуж, в затем дать ему быстро расшириться, он охлаждается. Охлажденным воздухом охлаждают новую порцию воздуха , поступающую в машину, и т.д., пока воздух не превратится в жидкость.
Испарив почти весь азот и кислород, Размай оставшийся жидкий воздух поместил в газометр. Он думал найти в нем гелий, так как считал, что этот газ испаряется медленнее, чем кислород и азот. Он очистил газ в газометре от примеси кислорода и азота и снял спектр, в котором снял две ранее не известных линии.
Далее Размай поместил 15 литров аргона в баллоне в жидкий воздух. Для того чтобы найти инертный газ, по расчетам, более легкий, чем аргон и криптон, Размай собрал первые порции испарения аргона. Получился новый спектр с ярко-красными линиями. Размай назвал выделенный газ неоном, что по-гречески означает “новый”.
2.4 Неон.
Далее Размай поместил 15 литров аргона в баллоне в жидкий воздух. Для того чтобы найти инертный газ, по расчетам, более легкий, чем аргон и криптон, Размай собрал первые порции испарения аргона. Получился новый спектр с ярко-красными линиями. Размай назвал новый газ неоном, что по-гречески означает “новый”.
2.5 Ксенон.
В 1888 году помощник Размая Треверс построил машину способную давать температуру -2530С. С помощью ее был получен твердый аргон. Были отогнаны все газы, кроме криптона. И уже в неочищенном криптоне был найден ксенон (“чужой”). Для того чтобы получить 300 кубических сантиметров ксенона, ученым пришлось в течении 2 лет переработать 77,5 миллиона литров атмосферного воздуха.
2.6 Радон.
Уже было сказано, что гелий присутствует в урановых минералах. Чем больше в клевеите урана, тем больше гелия. Размай долго пытался найти взаимосвязь между содержанием урана и гелия, но это ему не удалось. Разгадка пришла с другой стороны; она была связана с открытием радиоактивности.
Обнаружили, что радий выделяет газообразное вещество, названное эманацией. 1 грамм радия в сутки выделял один кубический миллиметр эманации. В 1903 году Размай и известный физик Содди занялись изучением эманации. Они имели в своем распоряжении всего 50 миллиграммов бромистого радия; одновременно у них было не более 0.1 кубического миллиметра эманации.
Для выполнения работ Размай построил сверхчувствительные весы, показывающие четыре миллиардные доли грамма. Вскоре исследователи выяснили, что эманация является последним представителем семейства инертных газов .
Им долго не удавалось рассмотреть спектр эманации. Как-то, оставив трубку с эманацией на несколько дней, они поставили ее в спектроскоп и были удивлены, увидев в спектроскопе известные линии гелия.
Этот факт подтвердил предположение Резерфорда и Содди о том, что радиоактивное превращение связано с превращением атомов. Радий, самопроизвольно распадался, превращался в эманацию и выделял ядро атома гелия. Один элемент превращался в другой.
Ученым
стало понятно, почему гелий обнаруживается
в урановых материалах; он один из
продуктов распада урана. В 1923 году по
решению Международного комитета по
химическим элементам эманация была
переименована в радон.
III Свойства инертных газов и их соединений.
3.1 Физические свойства инертных газов.
Благородные газы – бесцветные одноатомные газ без цвета и запаха.
Инертные газы обладают более высокой электропроводностью по сравнению с другими газами и при прохождении через них тока ярко светятся: гелий ярко-жёлтым светом, потому что в его сравнительно простом спектре двойная жёлтая линия преобладает над всеми другими; неон огненно красным светом, так как самые яркие его линии лежат в красной части спектра.
Насыщенный характер атомных молекул инертных газов сказывается и в том, что инертные газы имеют более низкие точки сжижения и замерзания, чем другие газы с тем же молекулярным весом. Из подгруппы тяжелых инертных газов аргон самый легкий. Он тяжелее воздуха в 1,38 раза. Жидкостью становится при – 185,9°C, затвердевает при – 189,4°C (в условиях нормального давления).
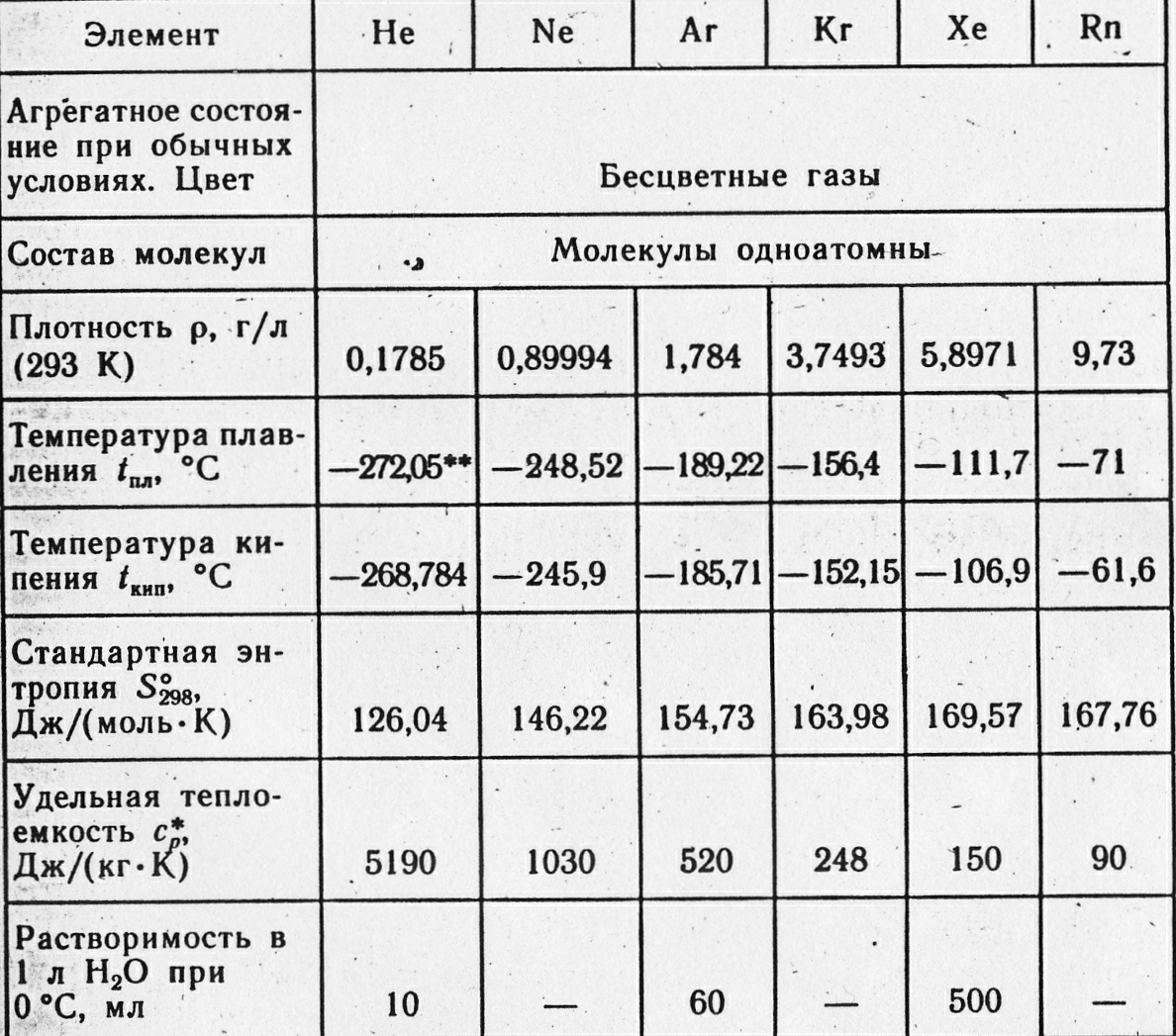
В отличие от гелия и неона, он довольно хорошо адсорбируется на поверхностях твердых тел и растворяется в воде (3,29 см3 в 100 г воды при 20°C). Еще лучше растворяется аргон во многих органических жидкостях. Зато он практически нерастворим в металлах и не диффундирует сквозь них.
3.2 Химические свойства инертных газов.
Долгое время не находили условий, при которых благородные газы могли бы вступать в химическое взаимодействие. Они не образовывали истинных химических соединений. Иными словами их валентность равнялась нулю. На этом основании было решено новую группу химических элементов считать нулевой. Малая химическая активность благородных газов объясняется жёсткой восьмиэлектронной конфигурацией внешнего электронного слоя. Поляризуемость атомов растёт с увеличением числа электронных слоёв. Следовательно, она должна увеличиваться при переходе от гелия к радону. В этом же направлении должна увеличиваться и реакционная способность благородных газов.
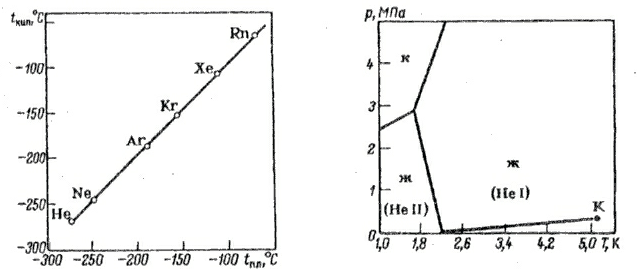
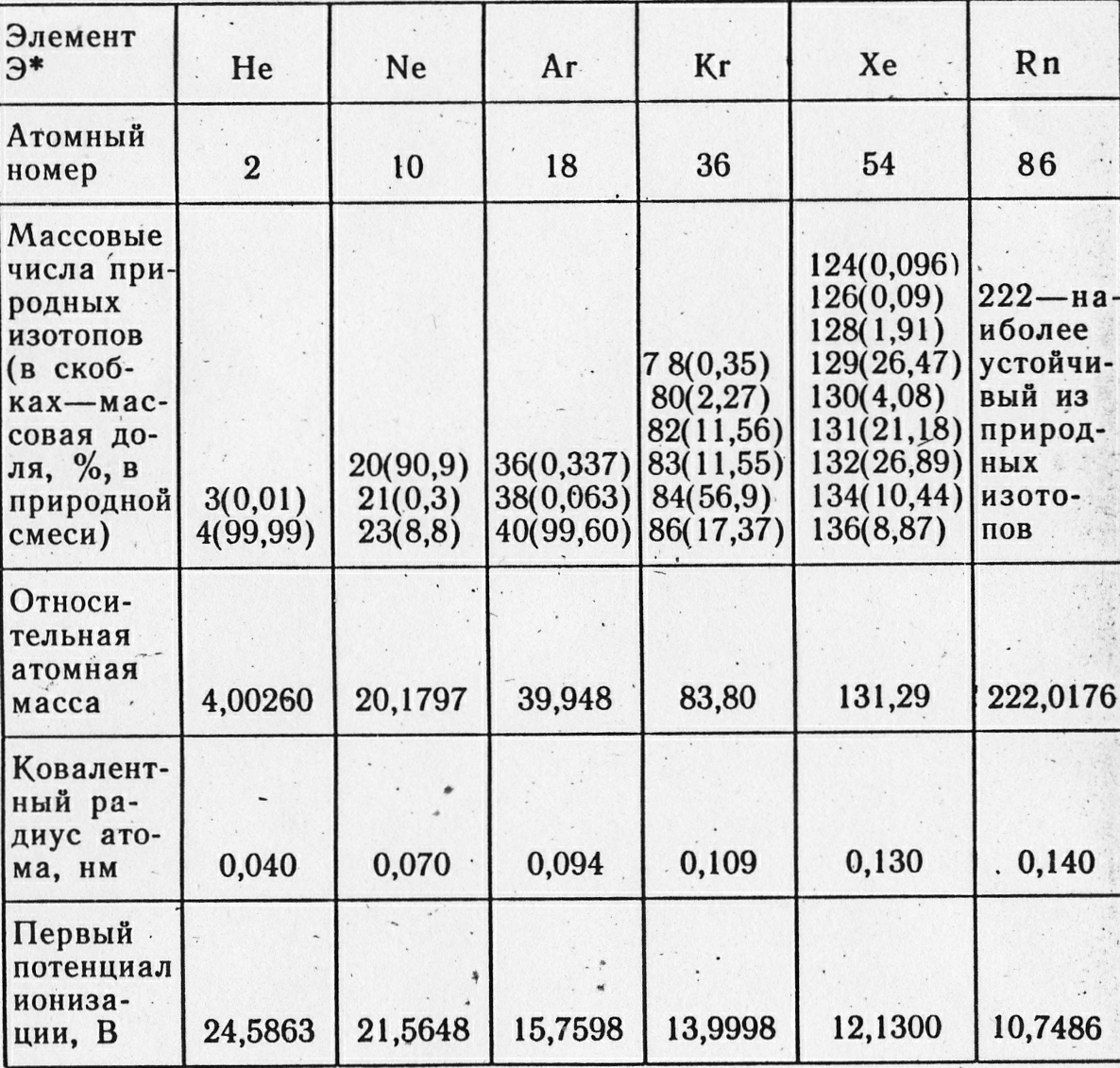

Так, уже в 1924 году высказывалась идея, что некоторые соединения тяжелых инертных газов (в частности, фториды и хлориды ксенона) термодинамически вполне стабильны и могут существовать при обычных условиях. Через девять лет эту идею поддержали и развили известные теоретики — Полинг и Оддо. Изучение электронной структуры оболочек криптона и ксенона с позиций квантовой механики привело к заключению, что эти газы в состоянии образовывать устойчивые соединения с фтором. Нашлись и экспериментаторы, решившие проверить гипотезу, но шло время, ставились опыты, а фторид ксенона не получался. В результате почти все работы в этой области были прекращены, и мнение об абсолютной инертности благородных газов утвердилось окончательно.
Однако в 1961 году Бартлетт, сотрудник одного из университетов Канады, изучая свойства гексафторида платины, соединения более активного, чем сам фтор, установил, что потенциал ионизации у ксенона ниже, чем у кислорода (12, 13 и 12, 20 эв соответственно). Между тем кислород образовывал с гексафторидом платины соединение состава O>2>PtF>6>... Бартлетт ставит опыт и при комнатной температуре из газообразного гексафторида платины и газообразного ксенона получает твердое оранжево - желтое вещество — гексафторплатинат ксенона XePtF>6>, поведение которого ничем не отличается от поведения обычных химических соединений. При нагревании в вакууме XePtF>6> возгоняется без разложения, в воде гидролизуется, выделяя ксенон:
2XePtF>6> + 6Н>2>О = 2Хе + О>2> + 2PtО>2> + 12HF
Последующие работы Бартлетта позволили установить, что ксенон в зависимости от условий реакции образует два соединения с гексафторидом платины: XePtF>6> и Xe (PtF>6>) >2>; при гидролизе их получаются одни и те же конечные продукты. Убедившись, что ксенон действительно вступил в реакцию с гексафторидом платины, Бартлетт выступил с докладом и в 1962 году опубликовал в журнале “Proceedings of the Chemical Society” статью, посвященную сделанному им открытию. Статья вызвала огромный интерес, хотя многие химики отнеслись к ней с нескрываемым недоверием. Но уже через три недели эксперимент Бартлетта повторила группа американских исследователей во главе с Черником в Аргоннской национальной лаборатории. Кроме того, они впервые синтезировали аналогичные соединения ксенона с гексафторидами рутения, родия и плутония. Так были открыты первые пять соединений ксенона: XePtF>6>, Xe (PtF>6>)>2>, XeRuF>6>, XeRhF>6>, XePuF>6> — миф об абсолютной инертности благородных газов развеян и заложено начало химии ксенона. Настало время проверить правильность гипотезы о возможности прямого взаимодействия ксенона с фтором.
Смесь газов (1 часть ксенона и 5 частей фтора) поместили в никелевый (поскольку никель наиболее устойчив к действию фтора) сосуд и нагрели под сравнительно небольшим давлением. Через час сосуд быстро охладили, а оставшийся в нем газ откачали и проанализировали. Это был фтор. Весь ксенон прореагировал! Вскрыли сосуд и обнаружили в нем бесцветные кристаллы XeF>4>. Тетрафторид ксенона оказался вполне устойчивым соединением, молекула его имеет форму квадрата с ионами фтора по углам и ксеноном в центре. Тетрафторид ксенона фторирует ртуть:
ХеF>4> + 2Hg = Хe + 2HgF>2>
|
> Кристаллы XeF>4> |
Интересно в химии ксенона то, что, меняя условия реакции, можно получить не только XeF>4>, но и другие фториды—XeF>2>, XeF>6>.
Советские химики В. М. Хуторецкий и В. А. Шпанский показали, что для синтеза дифторида ксенона совсем не обязательны жесткие условия. По предложенному ими способу смесь ксенона и фтора (в молекулярном отношении 1:1) подается в сосуд из никеля или нержавеющей стали, и при повышении давления до 35 атм начинается самопроизвольная реакция.
XeF>2> — единственный фторид ксенона, который можно получить, не пользуясь элементарным фтором. Он образуется при действии электрического разряда на смесь ксенона и четырехфтористого углерода. Возможен, конечно, и прямой синтез. Очень чистый ХеF>2> получается, если смесь ксенона и фтора облучить ультрафиолетом. Растворимость дифторида в воде невелика, однако раствор его — сильнейший окислитель. Постепенно он саморазлагается на ксенон, кислород и фтористый водород; особенно быстро разложение идет в щелочной среде. Дифторид имеет резкий специфический запах. Большой теоретический интерес представляет метод синтеза дифторида ксенона, основанный на воздействии на смесь газов ультрафиолетового излучения (длина волн порядка 2500—3500 А). Излучение вызывает расщепление молекул фтора на свободные атомы. В этом и заключается причина образования дифторида: атомарный фтор необычайно активен. Для получения XeF>6> требуются более жесткие условия: 700° С и 200 атм. В таких условиях в смеси ксенона и фтора (отношение от 1:4 до 1:20) практически весь ксенон превращается в XeF>6>. Гексафторид ксенона чрезвычайно активен и разлагается со взрывом. Он легко реагируете фторидами щелочных металлов (кроме LiF):
XeF>6> + RbF = RbXeF>7>,
но при 50° С эта соль разлагается:
2RbXeF>7> = XeF>6> + Rb>2>XeF>8>
Сообщалось также о синтезе высшего фторида XeF>8>, устойчивого лишь при температуре ниже минус 196° C.
Синтез первых соединений ксенона поставил перед химиками вопрос о месте инертных газов в периодической системе. Прежде благородные газы были выделены в отдельную нулевую группу, что вполне отвечало представлению об их валентности. Но, когда ксенон вступил в химическую реакцию, когда стал известен его высший фторид, в котором валентность ксенона равна восьми (а это вполне согласуется со строением его электронной оболочки), инертные газы решили перенести в VIII группу. Нулевая группа перестала существовать.
Заставить ксенон вступить в реакцию без участия фтора (или некоторых его соединений) пока не удалось. Все известные ныне соединения ксенона получены из его фторидов. Эти вещества обладают повышенной реакционной способностью. Лучше всего изучено взаимодействие фторидов ксенона с водой. Гидролиз ХеF>4> в кислой среде ведет к образованию окиси ксенона ХеО>3> — бесцветных, расплывающихся на воздухе кристаллов. Молекула ХеО>3> имеет структуру приплюснутой треугольной пирамиды с атомом ксенона в вершине. Это соединение крайне неустойчиво; при его разложении мощность взрыва приближается к мощности взрыва тротила. Достаточно несколько сотен миллиграммов ХеО>3>, чтобы эксикатор разнесло в куски. Не исключено, что со временем трехокись ксенона будут использовать как взрывчатое вещество дробящего действия. Такая взрывчатка была бы очень удобна, потому что все продукты взрывной реакции — газы. Пока же использовать для этой цели трехокись ксенона слишком дорого — ведь ксенона в атмосфере меньше, чем золота в морской воде, и процесс его выделения слишком трудоемок. Напомним, что для получения 1 м3 ксенона нужно переработать 11 млн. м3 воздуха. Соответствующая трехокиси неустойчивая кислота шестивалентного ксенона H>6>XeO>6> образуется в результате гидролиза XeF>6> при 0° С:
XeF>6> + 6H>2>О = 6HF + H>6>XeO>6>
Если к продуктам этой реакции быстро добавить Ва (ОН)>2>, выпадает белый аморфный осадок Ва>3>ХеО>6>. При 125° С он разлагается на окись бария, ксенон и кислород. Получены аналогичные соли—ксенонаты натрия и калия. При действии озона на раствор ХеО>3> в одномолярном едком натре образуется соль высшей кислоты ксенона Na>4>ХеО>6>. Перксенонат натрия может быть выделен в виде бесцветного кристаллогидрата Na4XeO6 · 6Н>2>О. К образованию перксенонатов приводит и гидролиз XeF>6> в гидроокисях натрия и калия. Если твердую соль Na>4>XeO>6> обработать раствором нитрата свинца, серебра или уранила, то получаются соответствующие перксенонаты: PbXeO>6> и (UO>2>) 2XeO>6> желтого цвета и Ag>4>XeO>6> — черного. Аналогичные соли дают калий, литий, цезий, кальций.
Окисел, соответствующий высшей кислоте ксенона, получают взаимодействием Na>4>XeO>6> с безводной охлажденной серной кислотой. Это четырехокись ксенона ХеO>4>. В ней, как и в октафториде, валентность ксенона равна восьми. Твердая четырехокись при температуре выше 0° С разлагается на ксенон и кислород, а газообразная (при комнатной температуре) — на трехокись ксенона, ксенон и кислород. Молекула ХеO>4> имеет форму тетраэдра с атомом ксенона в центре. В зависимости от условий гидролиз гексафторида ксенона может идти двумя путями; в одном случае получается тетраоксифторид XeOF>4>, другом — диоксифторид XeO>2>F>2>. Прямой синтез из элементов приводит к образованию оксифторида ХеОF>2>. Все это бесцветные твердые вещества, устойчивые в обычных условиях.
Очень интересна изученная недавно реакция дифторида ксенона с безводной НС1O>4>. В результате этой реакции получено новое соединение ксенона ХеСlO>4> — чрезвычайно мощный окислитель, вероятно, самый сильный из всех перхлоратов.
Синтезированы также соединения ксенона, не содержащие кислорода. Преимущественно это двойные соли, продукты взаимодействия фторидов ксенона с фторидами сурьмы, мышьяка, бора, тантала: XeF>2> · SbF>5>, ХеF>6> · AsF>3>, ХеF>6> · ВF>3> и ХеF>2> · 2ТаF>5>. И наконец, получены вещества типа XeSbF>6>, устойчивые при комнатной температуре, и XeSiF>6> — нестойкий комплекс.
В распоряжении химиков имеются весьма незначительные количества радона, тем не мене удалось установить, что он также взаимодействует с фтором, образуя нелетучие фториды. Для криптона выделены и изучены дифторид KrF2 и тетрафторид KrF>4> по свойствам, напоминающим соединения ксенона.
3.3 Получение Аргона.
Земная атмосфера содержит 66 · 1013 т аргона. Этот источник аргона неисчерпаем, тем более что практически весь аргон рано или поздно возвращается в атмосферу, поскольку при использовании он не претерпевает никаких физических или химических изменений. Исключение составляют весьма незначительные количества изотопов аргона, расходуемые на получение в ядерных реакциях новых элементов и изотопов. Получают аргон как побочный продукт при разделении воздуха на кислород и азот. Обычно используют воздухоразделительные аппараты двукратной ректификации, состоящие из нижней колонны высокого давления (предварительное разделение), верхней колонны низкого давления и промежуточного конденсатора-испарителя. В конечном счете азот отводится сверху, а кислород – из пространства над конденсатором. Летучесть аргона больше, чем кислорода, но меньше, чем азота. Поэтому аргонную фракцию отбирают в точке, находящейся примерно на трети высоты верхней колонны, и отводят в специальную колонну. Состав аргонной фракции: 10...12% аргона, до 0,5% азота, остальное – кислород. В «аргонной» колонне, присоединенной к основному аппарату, получают аргон с примесью 3...10% кислорода и 3...5% азота. Дальше следует очистка «сырого» аргона от кислорода (химическим путем или адсорбцией) и от азота (ректификацией). В промышленных масштабах ныне получают аргон до 99,99%-ной чистоты. Аргон извлекают также из отходов аммиачного производства – из азота, оставшегося после того, как большую его часть связали водородом. Аргон хранят и транспортируют в баллонах емкостью 40 л, окрашенных в серый цвет с зеленой полосой и зеленой надписью. Давление в них 150 атм. Более экономична перевозка сжиженного аргона, для чего используют сосуды Дюара и специальные цистерны. Искусственные радиоизотопы аргона получены при облучении некоторых стабильных и радиоактивных изотопов (37Cl, 36Аr, 40Аr, 40Са) протонами и дейтонами, а также при облучении нейтронами продуктов, образовавшихся в ядерных реакторах при распаде урана. Изотопы 37Аr и 41Аr используются как радиоактивные индикаторы: первый – в медицине и фармакологии, второй – при исследовании газовых потоков, эффективности спетом вентиляции и в разнообразных научных исследованиях. Но, конечно, не эти применения аргона самые важные.
4Физиологическое действие инертных газов.
Естественно было ожидать, что столь химически инертные вещества, как инертные газы, не должны влиять и на живые организмы. Но это не так. Вдыхание высших инертных газов (конечно в смеси с кислородом) приводит человека в состояние, сходное с опьянением алкоголем. Наркотическое действие инертных газов обуславливается растворением в нервных тканях. Чем выше атомный вес инертного газа, тем больше его растворимость и тем сильнее его наркотическое действие.
Теперь о влиянии аргона на живой организм. При вдыхании смеси из 69% Ar, 11% азота и 20% кислорода под давлением 4 атм возникают явления наркоза, которые выражены гораздо сильнее, чем при вдыхании воздуха под тем же давлением. Наркоз мгновенно исчезает после прекращения подачи аргона. Причина – в неполярности молекул аргона, повышенное же давление усиливает растворимость аргона в нервных тканях. Биологи нашли, что аргон благоприятствует росту растений. Даже в атмосфере чистого аргона семена риса, кукурузы, огурцов и ржи выкинули ростки. Лук, морковь и салат хорошо прорастают в атмосфере, состоящей из 98% аргона и только 2% кислорода.
IV Применение инертных газов.
Гелий является важным источником низких температур. При температуре жидкого гелия тепловое движение атомов и свободных электронов в твердых телах практически отсутствует, что позволяет изучать многие новые явления, например сверхпроводимость в твердом состоянии.
Газообразный гелий используют как легкий газ для наполнения воздушных шаров. Поскольку он негорюч, его добавляют к водороду для заполнения оболочки дирижабля.


Так как гелий хуже растворим в крови, чем азот, большие количества гелия применяют в дыхательных смесях для работ под давлением, например при морских погружениях, при создании подводных тоннелей и сооружений. При использовании гелия декомпрессия (выделение растворенного газа из крови) у водолаза протекает менее болезненно, менее вероятна кессонная болезнь, исключается такое явление, как азотный наркоз, – постоянный и опасный спутник работы водолаза. Смеси He–O>2> применяют, благодаря их низкой вязкости, для снятия приступов астмы и при различных заболеваниях дыхательных путей.
Гелий используют как инертную среду для дуговой сварки, особенно магния и его сплавов, при получении Si, Ge, Ti и Zr, для охлаждения ядерных реакторов.
Другие применения гелия – для газовой смазки подшипников, в счетчиках нейтронов (гелий-3), газовых термометрах, рентгеновской спектроскопии, для хранения пищи, в переключателях высокого напряжения. В смеси с другими благородными газами гелий используется в наружной неоновой рекламе (в газоразрядных трубках). Жидкий гелий выгоден для охлаждения магнитных сверхпроводников, ускорителей частиц и других устройств. Необычным применением гелия в качестве хладагента является процесс непрерывного смешения 3He и 4He для создания и поддержания температур ниже 0,005 K
Области применения ксенона разнообразны и порой неожиданны. Человек использует и его инертность и его чудесную способность вступать в реакцию со фтором. В светотехнике признание получили ксеноновые лампы высокого давления. В таких лампах светит дуговой разряд в ксеноне, находящемся под давлением в несколько десятков атмосфер. Свет в ксеноновых лампах появляется сразу после включения, он ярок и имеет непрерывный спектр — от ультрафиолетового до ближней области инфракрасного. Ксеноном пользуются и медики — при рентгеноскопических обследованиях головного мозга. Как и баритовая каша, применяющаяся при просвечивании кишечника, ксенон сильно поглощает рентгеновское излучение и помогает найти места поражения. При этом он совершенно безвреден. Активный изотоп элемента № 54, ксенон - 133, используют при исследовании функциональной деятельности легких и сердца.
Продувкой аргона через жидкую сталь из нее удаляют газовые включения. Это улучшает свойства металла.
|
|
Неон и аргон используются, как наполнители в неоновых лампах и лампах дневного свата Криптоном наполняют обычные лампы с целью уменьшения испарения и увеличения яркости свечения вольфрамовой нити. Ксеноном наполняют кварцевые лампы высокого давления, являющиеся наиболее мощными источниками света. Гелий и аргон используется в газовых лазерах.

Список использованной литературы
1. Петров М.М., Михилев Л.А., Кукушкин Ю.Н. “Неорганическая химия”
2. Гузей Л.С. Лекции по общей химии”
3. Ахметов Н.С. “Общая и неорганическая химия”
4. Некрасов Б.В. “Учебник общей химии”
5. Глинка Н.Л. “Общая химия
6. Ходаков Ю.В. “Общая и неорганическая химия”



 >
>