Характеристика антитіл та імуноглобулінів
Зміст
Вступ
1. Будова і властивості антитіл
2. Характеристика імуноглобулінів різних класів
2.1 Імуноглобулін А
2.2 Імуноглобулін Е
2.3 Імуноглобулін G
2.4 Імуноглобулін М
Висновок
Список використаних джерел
Вступ
Імуноглобуліни (антитіла) мають здатність специфічно з'єднуватись з антигеном і є найважливішими молекулами імунологічної системи. Тому докладне вивчення їх будови, властивостей і утворення є передумовою розуміння імунологічних механізмів.
Є чотири риси гуморальної імунної відповіді, що вражають і, на перший погляд, взаємно виключають одна одну:
1) універсальність: антитіла можуть бути виробленими проти будь-якого хімічного угрупування. Важко уявити, скільки повинно бути варіантів антитіл, якщо вважати, що кожний антиген потребує окремого антитіла;
2) специфічність: антитіла розрізняють о- чи р-положення функціональних груп, стереоізомери, білки, що відрізняються на один амінокислотний залишок;
3) гетерогенність: на один антиген виробляється багато типів (популяцій) антитіл, інколи більше 100 на одну антигенну детермінанту;
4) поліфункціональність: одне антитіло здатне зв'язувати більш, ніж один антиген.
1. Будова і властивості антитіл
Імуноглобуліни знаходяться в біологічних рідинах всіх хребетних. Молекула імуноглобуліну збудована з чотирьох поліпептидних ланцюгів (рис. 1): 2 легких L (light) і 2 важких Н (heavy), поєднаних між собою дисульфідними зв'язками. Залежно від відмінностей будови важких ланцюгів: а (альфа), 8 (дельта), є (епсілон), у (гамма), і \х (мю), імуноглобуліни можна розділити відповідно на 5 класів: IgA, IgD, IgE, IgG, IgM (табл. 1). Легкі ланцюги можуть існувати у двох варіантах: типу к (каппа) і типу λ (лямбда). Відповідно до незначної різниці у будові важких ланцюгів у межах одного класу виділяють підкласи, наприклад igGl, IgG2, IgG3, IgG4. Існують аналогічні різновиди легких ланцюгів λ. Такі варіанти будови ланцюгів важких (класи, підкласи) і легких (типи, підтипи) називаються ізотипічними варіантами антитіл. Імуноглобуліни можуть існувати як в мономерпій (чотири ланцюги), так і в полімерній формі. IgA у сироватці крові присутній в основному як мономер, а в виділеннях екзокринних залоз - як димер. Натомість IgM завжди є у формі пентамеру (рис. 2). Полімерні форми мають додатковий зв'язуючий поліпептидний ланцюг J (joining). Він є білком з масою 15 kDa, що містить 8 залишків цистеїну. В утворенні полімерних форм бере участь сульфгідрильна оксидаза, що окислює групу SH. Ланцюг J не є необхідним для виникнення полімерних форм імуноглобулінів, оскільки можна виявити полімери імуноглобулінів, позбавлені ланцюга J. Його відсутність не впливає на утворення гексамерів замість пентамерів IgM. Ланцюг J не має нічого спільного з геном (або ділянкою) j, що кодує відтинок змінної частини легкого або важкого ланцюга.
У легких і важких ланцюгах антитіл можна виділити змінні частини (V), що лежать у кінцевому N відрізку (вільні амінні групи поліпептидних ланцюгів), а також постійні частини (С), що займають С-кінці (вільні карбоксильні групи поліпептидних ланцюгів).
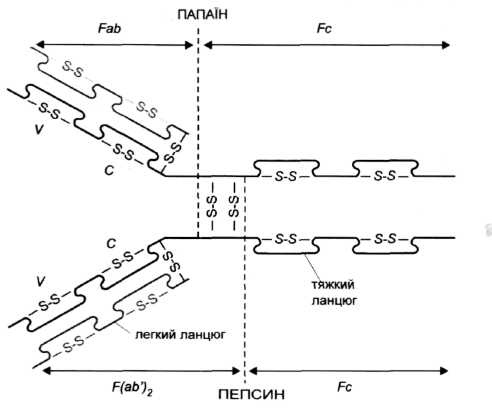
Рис. 1. Схема будови імуноглобуліму. Fab - фрагмент, що зв'язує антиген, Fc - кристалізуючий фрагмент, V- варіабельна частина, С-стабільна частина, S-S - дисульфідні містки. Пунктиром позначено місця гідролізу папаїном і пепсином
У результаті дії папаїну молекула IgG розпадається на два фрагменти Fab (який містить центри, що зв'язують антиген) і на фрагмент Fc (рис. 1). Частина важкого ланцюга, що міститься у фрагменті Fab, позначається символом Fd. Фрагмент антитіла, що зв'язує антиген, називається паратопом. Він просторово відповідає антигенній детермінанті - епітопу. Близько від місця розщеплення під дією папаїну знаходиться так звана рухлива ділянка, що робить можливим зміни кутів розташування Fab по відношенню до себе і до Fc. У цій ділянці знаходяться дисульфідні зв'язки, що з'єднують обидва важкі ланцюги між собою. їх може бути від 2 (IgGl) до 11 (IgG3). У фрагменті Fc антитіл знаходяться ділянки, відповідальні за активацію комплементу, а також за зв'язування з клітинними рецепторами для фрагмента Fc антитіл (FcR).
Внаслідок гідролізу IgG, пепсином утворюється фрагмент F(ab')., і фрагмент Fc'. Руйнування дисульфідного звязку в фрагменті F(ab') призводить до утворення 2 фрагментів Fab'. До складу фрагментів Fab, Fab', F(ab')>2 >входять цілі легкі ланцюги і фрагменти важких ланцюгів зі змінною ділянкою і частиною незмінної ділянки. Так званий фрагмент Fv складається виключно із змінних частин важкого і легкого ланцюга.
Специфічність антитіла безпосередньо залежить від просторової конфігурації змінних ділянок важких і легких ланцюгів. Ця конфігурація залежить від порядкового розміщення амінокислот у цих частинах ланцюгів. Змінні ділянки, що входять до складу фрагмента Fab антитіл, різні в антитіл, що зв'язують різні епітопи, а незмінні ділянки однакові у всіх антитіл даного класу і підкласу.
Серед антитіл одної специфічності, що зв'язують той самий епітоп, можуть ще бути відмінності за рівнем відповідності, тобто спорідненості антитіла до антигену. Від рівня цієї відповідності залежить сила зв'язування антигену антитілом.
Антитіла, що реагують перехресно, - це такі антитіла, які зв'язують як антиген А, так і антиген В. Причиною цього може бути подібність епітопів антигенів або те, що антигени мають багато різних епітопів, а частина їх однакова для обох антигенів. Цьому сприяє факт певної еластичності ділянки, що зв'язує антиген, яка може пристосуватися до дещо просторово різних антигенів.
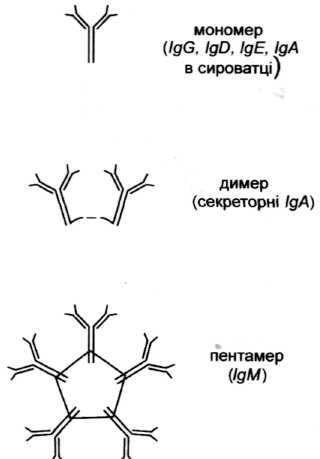
Рис. 2. Мономерна форма і полімерні форми імуноглобулінів
Змінна частина кожного з ланцюгів складається з трьох ділянок дуже змінних і з чотирьох різних ділянок, які прилягають до них (frame region - FR). Антитіла різної специфічності в основному відрізняються послідовністю амінокислот у дуже змінних ділянках. Ці ділянки визначають специфічність антитіл, бо вони власне утворюють місце зв'язування антигену. З цього приводу ці ділянки деколи називають регіонами, що визначають відповідність (complementarity determining regions - CDR). Ці ділянки є ніби "гарячими" місцями імуноглобулінів (рис. 3, 4).
Таблиця 1
Основні властивості імуноглобулінів різних класів у людини
|
Властивості |
IgG |
IgА |
IgM |
IgD |
IgE |
|
Форма |
мономер |
мономер димер |
пентамер |
мономер |
мономер |
|
Підкласи |
IgGl-IgG4 |
IgA1, IgA2 |
- |
- |
- |
|
Інші ланцюги |
- |
J, секре-торний фрагмент |
J |
- |
|
|
Період півіснування (дні) |
23 |
5,8 |
5,1 |
2,8 |
2,5 |
|
Синтез (мг/кг маси/день) |
33 |
65 |
6,7 |
0,4 |
0,016 |
|
Середня концентрація в сироватці |
8-16 |
1,4-4 |
0,5-2 |
0,04 |
1,7 х10-5-4,5 х 10-4 |
|
Активація комплементу (класичний шлях) |
+ а) |
- |
+ |
- |
- |
|
Проходження крізь плаценту |
+ |
- |
- |
- |
- |
|
Зв'язування з людськими мастоцитами |
-а) |
- |
- |
- |
+ |
|
Молекулярна маса (х 103) |
150 |
160 і димер |
970 |
185 |
190 |
|
Число основних 4-ланцюгових одиниць |
1 |
1 або 2 |
5 |
1 |
1 |
|
Відсоток серед імуноглобулінів сироватки |
80 |
13 |
6 |
0-1 |
0,002 |
|
Відсоток вуглеводів |
2-3 |
7-11 |
12 |
9-14 |
12 |
В традиційних викладах і схемах у підручниках місце зв'язування антигену в молекулі імуноглобуліну представляється як рівчик або кишеня, в яку занурений антиген. Однак кристалографічні дослідження з використанням рентгенівського випромінювання змінили точку зору на це питання. Як виявилось, тільки дуже малі антигени після зв'язування з антитілом можуть бути заглиблені у ділянку Fab. При зв'язуванні великих білкових антигенів поверхня контакту між фрагментом Fab антитіла і антигеном розтягнута і більш плоска, хоч має багато нерівностей. Деколи навіть можна побачити на поверхні фрагмента Fab виступи, що входять в молекули антигену. "Малий" антиген, наприклад флюоресцеїн, може бути заглиблений у фрагмент Fab на 94 %, а деякі великі білкові антигени контактують з молекулою антитіла лише кількома процентами своєї поверхні.
Детальні дослідження зв'язування мишачим антитілом великого білкового антигену (лізоцим курячого яйця) показали, що антитіло контактує з антигеном через 17 амінокислот. З них 10 належало важкому ланцюгу, а 6 - легкому. Вони належали до всіх дуже змінних ділянок антитіла, а особливо до ділянки CDR3 важкого ланцюга. Дві амінокислоти належали також до ділянок "зрізу". Площа контакту близько 7,5 нм2, що становило 11 % доступної поверхні антигену.
Тепер вважають, що лише зв'язування антигену певного імуноглобуліну може в деяких випадках зв'язувати два цілком різні епітопи у двох різних "закутках" цього місця. Це відкриття похитнуло один з дотеперішніх канонів імунології, який вважав, що один імуноглобулін може зв'язувати тільки один специфічний епітоп.
Завдяки повторенню лінійної послідовності амінокислот як легкі, так і важкі ланцюги містять так звані гомологічні зони або домени, які охоплюють близько 110 амінокислот і петлі, закриті дисульфідними зв'язками (близько 60 амінокислот). Змінні ділянки легких і важких ланцюгів і стабільні ділянки легких ланцюгів містять тільки по одному домену. Постійні ділянки важких ланцюгів IgA, IgG, IgD містять по 3 домени, a IgE, IgM no чотири домени, оскільки замість рухливої ділянки останні імуноглобулі-ни мають додатковий домен.
Домени незмінних ділянок мають характерну конфігурацію, яку називають складкою Ig. Вона складається з розташованих паралельно двох "гофре" β, з'єднаних дисульфідним зв'язком, одне з яких містить 3, а друге - 4 пасма β. Домени змінних ділянок мають 8 пасм β замість 7.
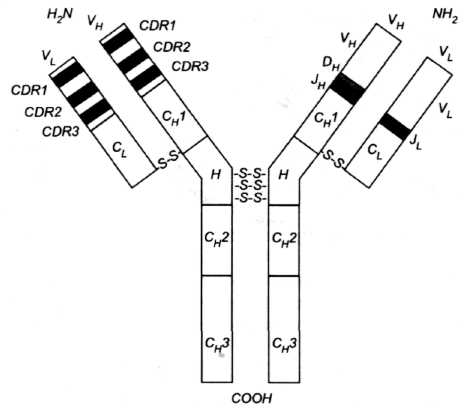
Рис. 3. Імуноглобулін. З лівого боку схеми у варіабельних частинах тяжких і легких ланцюгів позначено гіперваріабельні регіони (CDR) - темні поля і регіони зрізу -світлі поля, які прилягають до ділянок CDR. З правого боку схеми позначено відрізки, які відповідають генам У, D і J, котрі кодують варіабельні частини. У стабільних частинах позначено гомологічні зони, тобто домени, один для легкого ланцюга (С>;>) і три для тяжкого ланцюга (С>Н>1, С>І{>2 і С>ІП>). Н - регіон завіс.

Рис. 4. Спрощена схема просторової будови місця зв'язування антигену. CDR - гіперваріабельні ділянки, FR -регіони зрізу
У IgA, IgD, IgM ще додатково є хвостові ділянки (tail pieces). У IgA та IgM вони беруть участь в утворенні полімерних форм.
За перші дослідження структури антитіл Едельман і Портер в 1972 р. отримали Нобелівську премію.
Крім вільних (циркулюючих) імуноілобулінів В-лімфоцити виробляють також імуноглобуліни, які вбудовані в їхню клітинну оболонку С-кінцем і є рецепторами, що зв'язують антиген.
Всі імуноглобуліни містять приєднані полісахаридні ланцюги. Наприклад, людські IgG мають два або три N-зв'язані олігополісахариди. Два з них зв'язані з аспарагінами в позиції 294 фрагмента Fc. Відсутність цих олігосахаридів порушує з'єднання IgG з рецепторами для ділянки Fc-фрагмента антитіл на макрофагах і моноцитах.
Імуноглобуліни мають три різних види антигенних маркерів, що дозволяє їх класифікувати. Цими маркерами є:
• ізотипні (обумовлені певними суттєвими відмінностями в будові легких і важких ланцюгів - поділ на класи і типи). Здорові особи мають, як правило, всі ізотипні різновиди.
• алотипні - залежать від наявності в важких і легких ланцюгах (в основному в стабільних ділянках) різних амінокислот у певній позиції поліпептидного ланцюга. У різних представників одного виду можна знайти різні алотипні варіанти. Гени, що кодують незмінні ділянки імуноглобулінів, є поліалельними генами. Алотипні варіанти, тобто алотипи, є у важких ланцюгів γ (усіх підкласів), μ і α, а також легких ланцюгів к іλ. Найліпше вивчено алотипи ланцюга у, яких є кільканадцять і позначаються вони символом Gm та черговою цифрою. Імунізація проти алотипних детермінант відбувається при переливанні крові, вагітності, алогенній трансплантації;
• ідіотипні - пов'язані з відмінностями будови змінних ділянок поліпептидних ланцюгів. Антитіла одної специфічності мають однакові ідіотипні маркери.
2. Характеристика імуноглобулінів різних класів
2.1 Імуноглобулін А
Наш організм виробляє більше IgA порівняно з іншими імуноглобулінами, разом взятими. Організм дорослої людини з масою тіла 70 кг виробляє за добу 3 г IgG і 3,6-9,2 г IgA. Хоча в сироватці IgA менше, ніж IgG, слід пам'ятати, що більшість IgA виробляється місцево на слизових оболонках і виділяється з організму слизово-серозними виділеннями. Секреторний IgA є головним елементом захисту слизових оболонок від нападу мікроорганізмів, а слизові потенційно є найбільшими воротами захисту від інфекцій.
Крім виконання своїх захисних функцій у слизово-серозних виділеннях IgA може також брати участь у протиінфекційному імунітеті вже всередині епітеліальних клітин слизових, через які він транспортується (трансцитоз) до просвіту органа (наприклад кишківника). У випадку зараження епітеліальних клітин вірусами IgA, що транспортується крізь ентероцити, може нейтралізувати віруси вже всередині ентероцитів.

Рис. 5. Схема будови IgA.
A. Мономер IgA 1 із сироватки. Він нагадує будовою IgG, але містить хвостові відрізки і видовжений регіон завіс з приєднанами вуглеводневими групами і дисульфідними містками, який охоплює відрізки доменів Сα2.
B. Секреторний димер IgA. J-ланцюг, що нагадує домен Ig, зв'язує хвостові відрізки двох мономерів IgA через дисульфідні містки. Секреторний фрагмент, який нагадує п'ять доменів Ig, нековалентно з'єднується з Fс-фрагментом та J-ланцюгом і утворює поодинокий дисульфідний місток з одним із мономерів IgA
У плазмі людини IgA на 80-95 % знаходиться у мономерній формі, а решту складають полімерні форми, що містять з'єднуючий ланцюг J: димери, меншою мірою тримери і тетрамери. Ланцюг J з'єднується дисульфідними зв'язками з хвостовою частиною IgA.
У слизових і слизово-серозних виділеннях, таких як сльози, піт, виділення залоз шлунково-кишкового тракту, дихальних, сечовивідних, статевих шляхів, IgA присутній у формі димерів, зв'язаних додатково з так званим секреторним фрагментом (рис. 5). Це секреторні IgA або S-IgA (secretory IgA). S-IgA становить також 5-10 % від загальної кількості полімерного IgA в сироватці крові. Існує два його підкласи: IgA1 і lgA2.
Антитіла підкласу IgAl мають видовжену, збудовану з 20 амінокислот рухливу ділянку, а в підкласу IgA2 ця ділянка значно коротша, бо містить лише 7 амінокислот. IgAl в сироватці становить 80-90 % від загальної кількості IgA, а в слизово-серозних виділеннях два підкласи присутні в більш-менш рівних кількостях. Скорочена рухлива ділянка IgA1 робить його невразливим до дії бактерійних протеаз, які можуть перетяти і пошкодити IgA1. Слід пам'ятати, що IgA2 присутній саме у просвіті шлунково-кишкового тракту, де власне і є різні протеази. Хоча в людини є два гени а, у більшості тварин є лише один ген (відсутні підкласи), а у кроля їх аж 13.
У більшості антитіл IgA легкі ланцюги зв'язані дисульфідним зв'язком між собою, а не з важкими ланцюгами. Тому Fab фрагмента дуже зближені між собою і рухливість одного стосовно другого є обмежена.
2.2 Імуноглобулін Е
IgE, так само як і IgM, містить аж 4 домени у незмінній ділянці важкого ланцюга, але не має рухливої ділянки. На відміну від IgM, IgE не містить хвостової ділянки. Імуноглобуліни цього класу зв'язуються з відповідними рецепторами FcR на мастоци-тах, викликаючи після приєднання антигену дегрануляцію (вивільнення вмісту гранул) цих клітин, що лежить в основі анафілаксії.
Міститься у сироватці крові, концентрація невелика. Основна функція - індукція гострої реакції запалення шляхом звільнення медіаторів запалення: вазоактивних амінів - гістаміну та серотоніну - із тучних клітин. Цей процес запускається після взаємодії IgE з антигеном. В нормі медіатори запалення викликають приток у місце інфекції IgG антитіл, комплементу, нейтрофілів, еозинофілів, що сприяє подоланню інфекції. Однак у цьому цілком нормальному механізмі часто трапляється збій, і тоді організм починає раптово відповідати надто сильно, неадекватно, на якийсь незначний і не небезпечний антиген типу пилку рослин чи бджолиної отрути. Тоді виникає алергічна реакція: анафілактичний шок, сінна лихоманка, бронхіальна астма. IgE - головні медіатори алергії.
2.3 Імуноглобулін G
Всі підкласи IgG містять рухливу ділянку, а у IgG3 вона дуже видовжена (62 амінокислоти), що робить його подібним до IgD. У рухливій ділянці gG3 аж 11 дисульфідних зв'язків, які з'єднують важкі ланцюги. IgG1, IgG2, IgG4 з'єднуються Fc-фрагментом з А-білком золотистого стафілококу.
Багато клітин мають рецептори до фрагмента Fc антитіл IgG (FcyR). Ці рецептори виконують багато різних функцій. Завдяки цим рецепторам К-клітини здатні вбивати клітини, обгорнуті IgG, у реакції антитілозалежної клітинної цитотоксичності. У свою чергу фагоцитуючі клітини, наприклад макрофаги і нейтрофіли, завдяки присутності на їх поверхні FcyR енергійно фагоцитують клітини і покриті антитілами частинки у процесі, що називається імунофагоцитозом.
IgG є дуже важливими імуноглобулінами в боротьбі з мікроорганізмами, що проникають у наші тканини. їх концентрація в сироватці найбільша порівняно з антитілами інших класів. Вони представлені у людини 4 підкласами. При довготривалій антигенній стимуляції спочатку переважає утворення IgG І, а потім починає домінувати IgG4.IgG (за вийнятком lgG4) і IgM започатковують класичний шлях активації комплементу, завдяки чому можуть ініціювати процес знищення розпізнаних ними мікроорганізмів, а також заражених вірусом клітин.
IgG активно транспортуються від організму матері до дитини через плаценту завдяки рецепторам FcR. Тому плазма здорового доношеного новонародженого містить IgG навіть у більшій концентрації, ніж плазма матері. Через плаценту проходять усі підкласи IgG. Препарати людських IgG, що вироблені з крові багатьох донорів, призначаються при імунодефіцитах та важких вірусних і бактерійних захворюваннях. Еквівалентом і попередником IgG у птахів, плазунів і земноводних є так звані антитіла lg Y.
2.4 Імуноглобулін М
Антитіла цього класу синтезуються в початковій фазі імунної відповіді; також ці антитіла перші синтезуються в онтогенезі. При первинній імунній відповіді першими виділяються IgM, але їх спорідненість до антигену загалом мала, бо їх вивільнення проходить ще до дозрівання спорідненості. Однак, маючи аж 10 Fab фрагментів, IgM захланно (з великою авідністю) з'єднується з антигеном, що має багато епітопів.
Форму вільної молекули IgM, яка є пентамером, можна порівняти до форми сніжинки. Однак якщо вона зв'яже антиген, що має велику кількість однакових лінійно розташованих епітопів, то приймає форму краба (рис. 6). Таке переміщення мономерів у пентамерній молекулі IgM експонує фрагмент Fc і сприяє активації комплементу і зв'язуванню рецепторів FcR на фагоцитах та фагоцитозу. Отже, нічого дивного, що IgM у 100-400 разів ефективніше активує комплемент, ніж IgG. Цей фагоцитоз найправдоподіб-ніше відбувається за посередництвом рецепторів для комплементу на фагоцитах, а не за посередництвом рецепторів для фрагмента Fc IgM (FcμR), хоча останні рецептори також присутні на деяких клітинах.
IgM містить додаткові вуглеводні ланцюги в доменах Cμ1, Cμ2 і Сμ3 і хвостові ділянки. При полімеризації, що призводить до виникнення пентамерів, важливу роль відіграють дисульфідні зв'язки, але точне розміщення цих зв'язків є дискусійною темою.
Близько 5 % IgM плазми знаходиться в формі гексамерів. Цікаво, що гексамери IgM активують комплемент у 20 разів ефективніше, ніж пентамери, і що продукція гексамерів посилюється у відповідь на бактерійні ліпополісахариди.
Дуже невелику частину IgM сироватки становлять мономери. Збільшення їх концентрації може зростати при деяких хворобах (наприклад, ревматоїдний артрит і системний червоний вовчак).
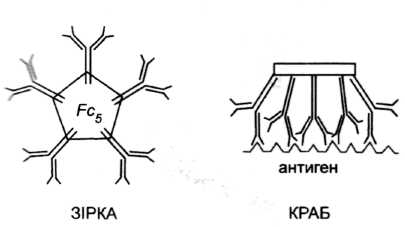
Рис. 6. Форми IgM.
Вільний IgM (не зв'язаний з антигеном) може набувати форми зірки, натомість IgM, зв'язаний з антигеном, що містить лінійно повторювані епітопи, набуває форми краба.
Висновок
Антитіла за своєю природою є імуноглобулінами. Вони мають симетричну будову молекули, яка складається із двох типів ланцюгів: важкого і легкого. Ділянки ланцюгів замкнено в домени, які фактично є одиницями структури цих білків. Розрізняють варіабільні і константні домени. Варіабільні утворюють активний центр антитіла, що відповідає за зв'язування антигену. Константні домени відповідають за ефекторні функції антитіл, преципітацію токсинів і аглютинацію бактерій, опсонізацію, активацію комплементу, дегрануляцію тучних клітин. Активний центр антитіла - це порожнина, заглиблена в Fv-фрагмент, яка може зв'язувати структурно різні антигени.
Виявляється, що саме поліфункціональність антитіл сприяє універсальності імунної відповіді, а гетерогенність - її високій специфічності.
Імуноглобуліни, в залежності від виконуваної функції поділяються на декілька класів: імуноглобулін А міститься переважно у секретах слизових оболонок, імуноглобулін М є першим бар`єром на шляху інфекції, імуноглобулін G – головний клас сироваткових антитіл при вторинній імунній відповіді, імуноглобулін Е – міститься в сироватці крові, індукує гострі запалення шляхом звільнення медіаторів запалення.
Список використаних джерел
Вершигора А.Ю. Основы иммунологии. — К.: Вища шк. Головное изд-во, 1980. — 504 с.
Земское В.М. Основы общей микробиологии, вирусологии и иммунологии. — М.: Колос, 1977. — 311 с.
Петров Р.В. Иммунология. — М.: Медицина, 1982. — 368 с.
Скок М.В. Основи імунології. Курс лекцій. – К.: Фітосоціоцентр, 2002. – 152 с.
Якобисяк М. Імунологія. – Вінниця: Нова книга, 2004. – 672 с.