Всероссийская Проверочная Работа ВПР Химия 11 класс – Вариант 2
Всероссийская Проверочная Работа ВПР Химия 11 класс Вариант 2 – Всероссийская Проверочная Работа
Вариант подготовлен учительницей химии Гимназии-интернат №4 Корневой Лилией Федоровной
Инструкция по выполнению работы
Проверочная работа включает в себя 15 заданий. На выполнение работы по химии отводится 1 час 30 минут (90 минут).
Оформляйте ответы в тексте работы согласно инструкциям к заданиям. В случае записи неверного ответа зачеркните его и запишите рядом новый.
При выполнении работы разрешается использовать следующие дополнительные материалы:
– Периодическая система химических элементов Д.И. Менделеева;
– таблица растворимости солей, кислот и оснований в воде;
– электрохимический ряд напряжений металлов;
– непрограммируемый калькулятор.
При выполнении заданий Вы можете использовать черновик. Записи в черновике проверяться и оцениваться не будут.
Советуем выполнять задания в том порядке, в котором они даны. Для экономии времени пропускайте задание, которое не удаётся выполнить сразу, и переходите к следующему. Если после выполнения всей работы у Вас останется время, Вы сможете вернуться к пропущенным заданиям.
Баллы, полученные Вами за выполненные задания, суммируются. Постарайтесь выполнить как можно больше заданий и набрать наибольшее количество баллов.
Желаем успеха!
1. В лабораторных условиях собрать газ можно двумя методами: вытеснением воды и вытеснением воздуха. На рисунках 1-3 представлены примеры использования некоторых из этих способов
Какой из названных способов можно использовать для собирания:
- Кислорода
- Углекислого газа
Запишите в таблицу номер рисунка и название соответствующего способа собирания газа.
| Газ | Номер рисунка | Способ собирания газа |
| Кислород | ||
| Углекислый газ |
| Газ | Номер рисунка | Способ собирания газа |
| Кислород | 1 | методом вытеснения воды |
| Углекислый газ | 2 | методом вытеснения воздуха |
2. На рисунке изображена модель электронного строения аниона некоторого химического элемента.
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, анион которого со степенью окисления -2 имеет такое электронное строение;
2) укажите количество протонов, которые содержит этот элемент;
3) укажите периода и номер группы в Периодической системе химических элементов Д.И.Менделеева, в которых расположен этот элемент.
Ответы запишите в таблицу.
Ответ:
| Символ химического элемента | Количество протонов | № периода | № группы |
| Символ химического элемента | Количество протонов | № периода | № группы |
| S | 16 | 3 | 6 (VI) |
3. Элементы-неметаллы образуют генетический ряд химических соединений, в которых проявляются их неметаллические химические свойства: неметалл — оксид неметалла — гидроксид неметалла (кислородсодержащая кислота). В сложных веществах проявление неметаллических свойств характеризуется понятием кислотность, и говорят, что оксиды и гидроксиды проявляют кислотные свойства. Соответственно, кислотные свойства оксидов и гидроксидов неметаллов в высших степенях окисления сверху вниз по подгруппе уменьшаются, а основные — увеличиваются. Кислотные свойства оксидов и гидроксидов по периоду слева направо также возрастают.
Учитывая эти закономерности, расположите в порядке увеличения кислотных свойств, следующие соединения: Na2O, Cl2O7, Al2O3, SiO2. Запишите соединения в нужной последовательности.
Ответ: ____________________________
Na2O, , Al2O3, SiO2, Cl2O7
4. В таблице перечислены характерные физические свойства веществ с атомной и молекулярной кристаллической решеткой.
|
Характерные физические свойства веществ |
|
| Атомная кристаллическая решетка | Молекулярная кристаллическая решетка |
| ♦ Прочность
♦ Тугоплавкость ♦ Низкая электропроводность ♦ Низкая теплопроводность ♦ Химическая инертность ♦ Нерастворимость в растворителях |
♦ Легкоплавкость
♦ Высокая сжимаемость ♦ Молекулярные кристаллы в твердом виде, а также в растворах и расплавах не проводят ток |
Используя данную информацию, определите, какую кристаллическую решетку имеют вещества углекислый газ CO2 и графит С.
Запишите ответ в отведенном месте:
- Углекислый газ CO2 ………………………………………………..
- Графит С ……………………………………………………………
- Углекислый газ CO2 ……молекулярная……………
- Графит С …………атомная…………………………
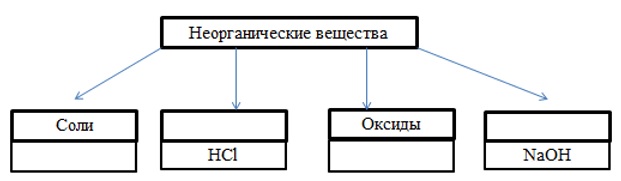
5. Все неорганические вещества можно классифицировать на четыре основные группы, как показано на схеме. В эту схему впишите пропущенные названия групп или химических формул веществ, принадлежащих данной группе.
Прочитайте следующий текст и выполните задания 6–8.
Тысячи тонн соляной кислоты расходуются для растворения железной окалины (Fe3O4) и ржавчины с тех чугунных и стальных изделий, которые собираются никелировать, хромировать, цинковать, золотить и т.д. Ведь на ржавую поверхность изделия при электролизе не произойдет осаждения ни цинка, ни никеля, ни меди. Потому и руль велосипеда перед никелированием, и кухонное ведро перед оцинкованием, и великое множество других изделий приходится «купать» в соляной кислоте.
Много соляной кислоты используют для снятия накипи в паровых котлах и тепловых бойлерах. Накипь – это в основном карбонаты кальция и магния, которые легко растворяются в соляной кислоте.
Правда, при этом кислота «набрасывается» и на металл. Чтобы предохранить его от растворения, в кислоту обычно добавляют ингибиторы коррозии. Эти вещества, адсорбируясь на металле, создают защитную пленку, затрудняющую растворение металла. Растворению карбонатов они практически не мешают.
Такую же ингибированную кислоту нефтяники спускают по трубам в нефтеносные пласты, если там имеются известняки. Образующийся при растворении известняков углекислый газ выдавливает нефть через скважины наверх, заметно увеличивая процент забора нефти из пластов.
6.
1) Составьте молекулярное уравнение растворения железной окалины в растворе соляной кислоты
Ответ: _________________________________________________________________
2) Объясните, зачем используют соляную кислоту перед оцинкованием кухонного ведра?
Ответ: ________________________________________________________________
______________________________________________________________________
Элементы ответа:
- Fe3O4 + 8HCl = FeCl2 + 2FeCl3 + 4 H2O
- Для растворения железной окалины с поверхности стальных и чугунных изделий, так как на ржавую поверхность изделия при электролизе не произойдет осаждения ни цинка, ни никеля, ни меди
7.
1) Составьте молекулярное уравнение реакции взаимодействия карбоната кальция с соляной кислотой, которая упоминалась в тексте.
Ответ: _____________________________________________________
2) Объясните, почему добавляют ингибиторы коррозии в раствор при удалении накипи?
Ответ: ________________________________________________________________ ____________________________________________________________________________
Элементы ответа:
- CaCO3 + 2HCl = CaCl2 + CO2 + H2O
- Ингибиторы, адсорбируясь на металле, создают защитную пленку, затрудняющую растворение металла поверхности паровых котлов и тепловых бойлеров.
8.
1) Составьте сокращенное ионное уравнение реакции взаимодействия карбоната кальция с соляной кислотой.
Ответ: _____________________________________________________________
2) Объясните, какие особенности этой реакции используются при добычи нефти?
Ответ: ________________________________________________________________ ____________________________________________________________________________
Элементы ответа:
- CaCO3 + 2H+ = Ca2+ + CO2 + H2O
- Если нефтеносные пласты содержат известняки, при добавлении соляной кислоты происходит растворение известняков, углекислый газ выдавливает нефть через скважины наверх, заметно увеличивая процент забора нефти из пластов.
9. Дана схема окислительно-восстановительной реакции
Cu + H2SO4 (конц) → CuSO4 + SO2 + H2O
1) Составьте электронный баланс этой реакции
__________________________________________________________________
2) Укажите окислитель и восстановитель
__________________________________________________________________
3) Расставьте коэффициенты в уравнении реакции
__________________________________________________________________
Элементы ответа:
1) Составлен электронный баланс:
Cu0 -2 ē → Cu+2 1
S+6 + 2 ē → S+2 1
2) Указано, что Cu0 является восстановителем,
а H2SO4 за счет S+6 является окислителем;
3) Составлено уравнение реакции:
Cu + 2 H2SO4 (конц) → CuSO4 + SO2 + 2H2O
10. Дана схема превращений: Na → NaOH → NaCl → NaNO3
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения
- ___________________________________________________________
- ___________________________________________________________
- ___________________________________________________________
Написаны уравнения реакций, соответствующие схеме превращений:
Na → NaOH → NaCl → NaNO3
- 2 Na + 2H2O → 2NaOH + H2
- NaOH + HCl → NaCl + H2O
- NaCl + AgNO3 → NaNO3 + AgCl
11. Установите соответствие между названием органического вещества и его гомологом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА
А) Толуол Б) Пропин В) Этаналь |
ГОМОЛОГ
1) Ацетилен 2) Этилбензол 3) Муравьиный альдегид 4) Метан
|
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ:
| А | Б | В |
| А | Б | В |
| 2 | 1 | 3 |
12. В предложенные схемы химических реакций вставьте формулы пропущенных веществ и расставьте коэффициенты
1) Al4C3 + H2O → …….. + ……………….
| H2SO4 | |
| 2) CH3C ≡ CH + H2O | ———> ………………………….. |
1) Al4C3 + 12H2O → 3 CH4 + 4 Al(OH)3
| H2SO4 | ||
| 2) CH3C ≡ CH + H2O | ———> |  |
13. Ацетилен – основной горючий газ, используемый при газовой сварке, а также широко применяется для газовой резки (кислородной резки). Температура ацетилено-кислородного пламени может достигать 3300°C. Благодаря этому ацетилен по сравнению с более доступными горючими газами (пропан-бутаном, природным газом и др.) обеспечивает более высокое качество и производительность сварки. В промышленности ацетилен обычно получают из карбида кальция (CaC2) при разложении последнего водой. Определите объем ацетилена (н.у.), который можно получить из 128 кг технического карбида кальция, содержащего 5% примесей.
Запишите подробное решение задачи.
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Элементы ответа:
1) Составлено уравнение реакции
CaC2 + 2 H2O = Ca(OH)2 + HC≡ CH
2) m (CaC2)чист = 128 кг * 0,95 = 121,6 кг
n(CaC2) = m(CaC2)/ M(CaC2) = 121,6 кг/ 64 кг/кмоль = 1,9 кмоль
n(CaC2) = n (C2H2) = 1,9 кмоль
3) V (C2H2) = n* Vm = 1,9 кмоль * 22,4м3/кмоль = 42,56 м3
14. Первое упоминание о практическом применении уксусной кислоты относится к III веку до н. э. Греческий учёный Теофраст впервые описал действие уксуса на металлы, приводящее к образованию некоторых используемых в искусстве пигментов. Уксус применялся для получения свинцовых белил, а также ярь-медянки (зелёной смеси солей меди, содержащей помимо всего ацетат меди).
Ранними промышленными методами получения уксусной кислоты были окисление ацетальдегида и бутана. Ацетальдегид окислялся в присутствии ацетата марганца (II) при повышенной температуре и давлении. Выход уксусной кислоты составлял около 95 % при температуре 50—60 °С.
Оба метода базировались на окислении продуктов крекинга нефти. В результате повышения цен на нефть оба метода стали экономически невыгодными, и были вытеснены более совершенными каталитическими процессами карбонилирования метанола монооксидом углерода.
Составьте уравнения реакций получения уксусной кислоты, описанные в тексте. При написании уравнений реакций используйте структурные формулы органических веществ.
1) _________________________________________________________
2) _________________________________________________________
3) _________________________________________________________
Написаны уравнения реакций, соответствующие схеме превращений:
- 2 CH3CHO + O2 → 2 CH3COOH ( в присутствии ацетата марганца (II)
- 2CH3CH2CH2CH3 + 5O2 → 4 CH3COOH + 2H2O (каталитическое окисление)
- CH3OH + CO → CH3COOH
15. 0,25% раствор сульфат цинка ZnSO4 применяется в качестве глазных капель. Сколько (г) воды нужно добавить к 25 г раствора с массовой долей ZnSO4, равной 3%, чтобы приготовить глазные капли?
Запишите подробное решение задачи.
Ответ:__________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
- m(ZnSO4 )=
-w%(ZnSO4)}{100%}.png) = 25.0,03 = 0,75 г;
= 25.0,03 = 0,75 г; - w% (ZnSO4) =
-100%}{m(p-paZnSO4)+m(H_20)}.png)
0,25 =}.png)
300 = 25 + m(H2O)
m(H2O) = 275 г
Ответ: 275 г