Задание с ответами: химия. ЕГЭ — 2018
Химическое равновесие в системе
С4H10(г) 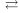 С4H6(г) + 2H2(г) − Q
С4H6(г) + 2H2(г) − Q
сместится в сторону исходных веществ при
1) использовании катализатора
2) понижении давления
3) охлаждении системы
4) добавлении бутана
По принципу Ле Шателье — если на систему, находящуюся в состоянии химического равновесия, воздействовать извне, изменяя какое-либо из условий равновесия (температура, давление, концентрация), то в равновесие в системе сдвинется в сторону, уменьшающую воздействие.
Введение катализатора на положение равновесия влиять не будет.
При понижении давления или добавлении бутана равновесие сместится в сторону продуктов.
А вот при охлаждении системы равновесие эндотермической реакции сдвинется в сторону исходных веществ.
Правильный ответ: 3