Задание с ответами: химия. ЕГЭ — 2018
При нагревании образца нитрата цинка часть вещества разложилась, при этом выделилось 5,6 л газов (в пересчете на н. у.). Остаток массой 64,8 г полностью растворили в минимальном объеме 28%-ного раствора гидроксида натрия. Определите массовую долю нитрата натрия в конечном растворе. В ответе напишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления.
При разложении нитрата цинка (соли амфотерного металла) образуются оксид цинка, бурый газ — диоксид азота (IV) и кислород:

Поскольку в условии задачи речь идет о полном растворении остатка, состоящего из оксида и нитрата цинка, то в итоге образуется комплексная соль цинка — тетрагидроксоцинкат натрия:


Вычислим количество смеси газов — 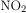 и
и 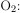

По уравнению реакции 

Вычисли массу и количество вещества оставшегося нитрата цинка:


По уравнениям реакции взаимодействия оксида цинка и нитрата цинка со щелочью, количество вещества и масса гидроксида натрия равно:


Вычислим массу щелочного раствора:

Вычислим количество вещества и массу нитрата натрия:


Вычислим массу образовавшегося раствора и массовую долю нитрата натрия в нем:


Правильный ответ: 19,26%.