Запоры в клинической практике
Запоры в клинической практике
П.Я. Григорьев, Э.П. Яковенко, Н.А. Агафонова
Запор – это нарушение опорожнения кишечника различной этиологии и патогенеза.
Наличие или отсутствие запора определяется следующими характеристиками: частота стула, продолжительность натуживания при акте дефекации, качество, консистенция и форма кала, ощущение полной или неполной эвакуации содержимого кишки, наличие или отсутствие анальных или перианальных болей (болезненность при акте дефекации), абдоминальные боли, использование пальцевой помощи в процессе акта дефекации.
Термин «запор», часто используемый пациентами и врачами, трактуется ими по–разному. Частота стула у здоровых людей варьирует от 3 раз в день до 3 раз в неделю. У большинства взрослых (70%), придерживающихся западного стиля диеты, стул бывает 1 раз в день. Частота актов дефекации достоверно реже у женщин. Консистенция и форма кала обусловлены содержанием в нем воды, которое у здоровых составляет 70%, а при запоре – около 60%. У мужчин консистенция фекалий более мягкая, чем у женщин.
Для описания формы и консистенции кала целесообразно пользоваться Бристольской шкалой, по которой для запоров характерна форма кала 1–2–го типов (табл. 1). У здоровых людей масса фекалий за сутки в среднем составляет 110 г, но могут отмечаться колебания от 40 до 260 г [5]. У мужчин и у молодых лиц масса кала больше, чем у женщин и у пожилых. Количество фекалий вариабельно и зависит от многих причин: особенностей диеты, социальных условий, перемены обычного режима дня, климата, объема потребления жидкости, гормонального цикла (menses). Все указанные характеристики акта дефекации зависят от времени транзита кишечного содержимого через желудочно–кишечный тракт. При изучении времени транзита с использованием контрастных маркеров или радиоактивных изотопов установлено, что у здоровых людей оно составляет около 60 ч: у женщин – 72 ч, у мужчин – 55 ч.
У пациентов с запорами среднее время транзита колеблется от 67 до 120 ч [5]. В норме последовательное продвижение содержимого по толстой кишке обеспечивается различными типами ее сокращения. По данным исследования миоэлектрической активности моторика толстой кишки представлена как сегментарными сокращениями (единичные или организованные групповые фазовые сокращения), так и пропульсивными – специальные пропульсивные сокращения [2,10]. Толстой кишке присущи циркадные и дневные ритмы моторной функции. Во время сна ее моторная активность ингибируется [3]. В течение дня сегментарная и пропульсивная активность толстой кишки значительно увеличивается, особенно при утреннем пробуждении и после приема пищи. Возбуждение моторной активности происходит в течение 1–3 мин после приема пищи и длится до 3 ч [8].
Моторика толстой кишки зависит от состава съеденной пищи . Жиры и углеводы стимулируют, а аминокислоты и белки подавляют моторную активность толстой кишки. В проксимальных отделах пищевой химус перемешивается, накапливается и тесно контактирует с кишечными бактериями. Сахаролитические бактерии (бифидо– и лактобактерии, Enterococcus faecalis ) ферментируют целлюлозу и гемицеллюлозу, содержащиеся в кожуре овощей и фруктов и оболочке зерновых, до конечных продуктов распада – короткоцепочечных жирных кислот (молочная, пропионовая и др.) и газов (метан, водород, диоксид углерода), которые стимулируют перистальтику кишки. Кроме того, неперевариваемая клетчатка удерживает в просвете кишки воду, увеличивая объем кишечного содержимого. Слабительное действие пищевых волокон комплексное и связано с увеличением объема кишечного содержимого благодаря удержанию молекул воды, увеличению бактериальной массы и раздражению рецепторов толстой кишки.
Протеолитические бактерии, в частности, представители родов Bacteroides , Proteus , Clostridium , а также Escherichia coll расщепляют белки до аммония, фенолов, меркаптопуринов и пуринов. При нормальном микробиоценозе протео– и сахаролитические бактерии работают содружественно, расщепляя белки и углеводы до конечных продуктов распада. Изменения состава кишечной микрофлоры могут привести к нарушению метаболизма (дисбаланс витаминов, электролитов) и транзита по толстой кишке. Дистальные отделы толстой кишки продвигают фекальные массы к прямой кишке. В этих отделах окончательно абсорбируются электролиты и вода (около 2 л/сут). Акт дефекации начинается при достаточном заполнении сигмовидной ободочной кишки. Результаты 24–часовой манометрии толстой кишки показали, что акту дефекации предшествует увеличение частоты высокоамплитудных и перистальтических сокращений [8].
Рефлекс дефекации возникает при остром растяжении прямой кишки. Если супраспинальные центры способствуют этому процессу, то при сокращении сигмовидной ободочной и прямой кишки увеличивается давление в ампуле прямой кишки, сглаживается ректосигмоидальный угол. В результате расслабления внутреннего и наружного анального сфинктеров каловые массы эвакуируются. В регуляции указанной функции участвуют нервные центры поясничного и крестцового отделов позвоночника. Позыв к дефекации можно усилить за счет увеличения внутрибрюшного давления с помощью приема Вальсальвы (натуживание) или подавить путем сокращения поперечно–полосатых мышц тазовой диафрагмы и наружного анального сфинктера. Частое подавление позывов к дефекации может привести к хроническому растяжению прямой кишки, снижению тонуса и хроническому запору.
Важной причиной, приводящей к утрате моторно–эвакуаторных свойств кишки, является нарушение чувствительности биорецепторов кишечной стенки . При запоре нарушение передачи нервного сигнала может быть обусловлено нейропатией крестцового отдела позвоночника после повреждения афферентных и эфферентных парасимпатических нервных волокон в нижнем гипогастральном сплетении. При утрате афферентной фазы дефекационного рефлекса различного генеза прямая кишка увеличивается в объеме и развивается атония ее стенки. Вследствие этого позыв возникает только после большого скопления в ней кала (мегаректум, или инертная прямая кишка). У пациентов с хроническими запорами при манометрии толстой кишки значительно снижены количество и продолжительность высокоамплитудных перистальтических сокращений, а также подавлен или отсутствует «гастроколитический» ответ на прием пищи во всех сегментах толстой кишки [4]. Таким образом, при запорах может быть нарушен транзит химуса преимущественно по толстой кишке либо в аноректальной зоне, либо имеется комбинация этих расстройств.
Запоры могут быть органической или функциональной природы. Согласно Римскимкритериям II (1999), диагноз функционального запора может быть поставлен при наличии 2 или более нижеуказанных симптомов, сохраняющихся не менее 12 необязательно последовательных недель на протяжении 12 мес: – частота актов дефекации менее 3 в неделю; – натуживание при акте дефекации, занимающее не менее 25% его времени; – фрагментированный и (или) твердый кал не менее чем при 1 из 4 актов дефекации; – ощущение неполной эвакуации кишечного содержимого не реже чем при 1 из 4 актов дефекации; – ощущение препятствия при прохождении каловых масс не реже чем при 1 из 4 актов дефекации; – необходимость проведения пальцевых манипуляций, облегчающих акт дефекации более чем при 1 из 4 актов дефекации. В основе формирования запоров лежит гипотоническая, или спастическая дискинезия кишки. Патофизические механизмы, обусловливающие первичные расстройства толстой кишки, недостаточно изучены.
Предполагается роль дисбаланса в системе гастроинтестинальных гормонов, стимулирующих (гастрин, холецистокинин, субстанция Р, энкефалины, мотилин) или замедляющих моторику кишки, в частности, глюкагон, вазоактивный интестинальный полипептид (ВИП), серотонин, изменения чувствительности рецепторного аппарата толстой кишки к различным стимулам. Также придается значение нарушению функции нервно–рецепторного аппарата кишечной стенки, ответственного за ее моторную активность. В практике врача чаще встречаются запоры, обусловленные вторичными моторными расстройствами кишечника. Этиологические факторы хронического запора многообразны [1]. Традиционно наиболее частой причиной нарушений кишечного транзита считается нерациональное питание (нерегулярный прием пищи, низкое потребление жидкости и пищевых волокон). Однако сравнительный анализ характера питания лиц с запором и с нормальным стулом свидетельствует об отсутствии различий в употреблении балластных веществ. В то же время у больных с запором масса фекалий оказалась меньше, а время кишечного транзита значительно больше, чем у лиц с нормальным стулом, независимо от того, употребляли они пищу с клетчаткой или нет [6]. Нередко запоры возникают вследствие привычного подавления позывов к дефекации, обусловленного стилем жизни (утренняя спешка, особенности режима работы, отсутствие условий в туалете).
Запоры сопровождают многие эндокринные болезни (сахарный диабет, гипотиреоз, ожирение). Болезнь Паркинсона, паралитический синдром, рассеянный склероз и психические расстройства (депрессия, стресс, деменция) также могут сопровождаться запорами. Тормозить моторную активность толстой кишки могут многие лекарственные препараты, при этом одновременный прием нескольких препаратов может усиливать и поддерживать запор: – антациды, содержащие гидроксид алюминия или карбонат кальция; – антихолинергические препараты (спазмолитики); – антидепрессанты; – нестероидные противовоспалительные средства; – наркотические анальгетики; – противоэпилептические средства; – гипотензивные средства (b–блокаторы, антагонисты кальция, антиадренергические препараты центрального действия, блокаторы рецепторов ангиотензина II, ингибиторы ангиотензинпревращающего фермента); – противотуберкулезные средства; – антибиотики (ингибиторы гиразы, цефалоспорины); – системные антифунгицидные средства (кетоконазол); – препараты железа (его соли); – гестагены; – диуретики; – липидоснижающие препараты (ионообменные); – нейролептики (фенотиазины); – транквилизаторы; – мышечные релаксанты; – урологические препараты (для лечения болезней простаты); – препараты, применяемые при глаукоме. Запоры, связанные с нарушением аноректального транзита, обусловливаются или первичными расстройствами моторики прямой кишки и мышц тазового дна, или их структурными изменениями.
Следует иметь в виду, что выявленные анатомические нарушения не всегда являются причиной запоров, а могут быть их следствием или обусловливаться сопутствующими болезнями. О нарушении моторики аноректальной зоны свидетельствуют запоры с неполным опорожнением прямой кишки даже после сильного натуживания, с наличием болей в нижней части живота, в анальной и перианальной областях и недержанием кала. Несмотря на то, что запоры и недержание кала, кажется, исключают друг друга, нередко обусловливающие их механизмы оказываются одинаковыми. Так, повторные и продолжительные натуживания при запорах повреждают слизистую оболочку прямой кишки, крестцовые нервы и мышцы тазового дна. В конечном итоге эти обстоятельства вызывают нарушение функции анальных сфинктеров и недержание кала. Кроме того, с образованием при запорах каловых пробок происходит разжижение фекалий в вышележащих отделах кишки, которые обтекают плотные каловые массы и обильно выделяются из ануса – так называемая парадоксальная диарея.
Запор может быть симптомом болезней верхних отделов желудочно–кишечного тракта, толстой и прямой кишки. Поэтому при появлении запора требуется тщательное обследование для установления причин его развития. Детальный анализ клинических проявлений запора позволяет предположить основные механизмы их развития (табл. 2).
Обследование пациентов с запорами включает два этапа. На первом этапе диагностический поиск нацелен на исключение органической патологии. Больным проводятся: общеклинические исследования; пальцевое исследование прямой кишки; ректороманоскопия; ирригоскопия, при необходимости – колоноскопия; осмотр гинекологом (для женщин) и урологом (для мужчин). Выявленные органические изменения требуют соответствующего лечения, часто хирургического.Особенно тщательного обследования требуют пациенты с запорами и симптомами «тревоги»: немотивированная потеря массы тела, ночная симптоматика (боли), постоянные и интенсивные боли в животе, начало «заболевания» в пожилом возрасте, рак толстой кишки у родственников, лихорадка, кровь в кале, лейкоцитоз, анемия, увеличение СОЭ, изменение биохимического статуса, гепато– и спленомегалия. После исключения органической патологии на втором этапе обследования уточняется уровень стаза кишечного содержимого, устанавливается тип моторных нарушений (гипер– или гипокинетический), выявляется сопутствующая патология желудочно–кишечного тракта, эндокринной и нервной систем. Измерение времени транзита может быть проведено рентгенологическим методом с пассажем бария или радиоизотопными маркерами по толстой кишке. При этом может быть выявлен не только уровень стаза в кишечнике, но и тип моторных нарушений в том или ином сегменте кишки.
Результаты обследования также должны ответить на вопрос: является ли запор первичным или вторичным функциональным нарушением кишечника. Поэтому в протокол исследования следует включить: ультразвуковое исследование органов брюшной полости, лабораторные тесты для исключения гипотиреоза, сахарного диабета, дегидратации, гипокалиемии и гиперкальциемии; исследование микрофлоры кала; психоневрологическое обследование. При стазе содержимого в прямой кишке могут использоваться особые исследования в специализированных медицинских центрах (анометрия, дефекография, электромиография мышц тазового дна и т.д.).
Лечение запоров преследует цель достижения регулярного опорожнения кишечника и нормализации консистенции кала. Если запор является симптомом какой–либо болезни, то ее лечение значительно повышает эффективность мероприятий, предпринимаемых для ликвидации запора [1]. На первом этапе лечения проводят просветительскую беседу с пациентом о причинах запоров и дают рекомендации по изменению образа жизни и питания. Прежде необходимо разъяснить больному, что ежедневная дефекация не является физиологической необходимостью. Если опорожнение кишечника полное, то стул может быть и 1 раз в 2–3 дня. Важную роль в лечении запоров играет диета . Питание должно быть четырехразовым. Если нет противопоказаний, в рацион при запоре включают больше продуктов и блюд, ускоряющих опорожнение кишечника: богатые растительной клетчаткой морковь, свеклу, кабачки, тыкву, хлеб из ржаной и пшеничной муки грубого помола, диетические сорта хлеба с добавлением пшеничных отрубей, каши из пшеничной, гречневой, перловой и овсяной круп. Стимулируют работу кишечника также органические кислоты и сахара, содержащиеся в овощах, фруктах и ягодах. Поэтому при запорах назначают фруктовые и овощные соки, инжир, финики, чернослив, курагу, бананы, некислые яблоки. Обязательно следует употреблять молочнокислые продукты: свежий кефир, простоквашу, ацидофилин. Общее количество поступающей в организм жидкости – не менее 2 л/сут. Больным следует исключить из рациона питания хлеб из муки высших сортов, сдобное тесто, жирные сорта мяса, копчености, консервы, острые блюда, шоколад, крепкие кофе и чай, ограничить употребление каши из манной крупы и риса, вермишель, картофель; не рекомендуются продукты, вызывающие повышенное газообразование (бобовые, капуста, щавель, шпинат, яблочный и виноградный соки), а при спастической диспесии – также продукты, содержащие эфирные масла: репу, редьку, лук, чеснок, редис.
При запоре со спастической дискинезией для предотвращения усиления спазмов под влиянием пищевых волокон лечение начинают с бесшлаковой диеты с примесью жиров, постепенно добавляя в нее вареные, а затем и сырые овощи. В качестве стимуляторов кишечной моторики можно использовать пшеничные отруби: начинают с 3 чайных ложек в день и постепенно увеличивают дозу до 3~6 столовых ложек. Больным с запором показаны минеральные воды «Ессентуки», «Баталинская», «Славяновская», «Джермук». Более минерализированнную воду, в частности, «Ессентуки №17», назначают при запорес гипомоторной дискинезией по 150–200 мл в холодном виде 2–3 раза в день; менее минерализированную – в таких же дозах в теплом виде, например, «Ессентуки №4» – при гипермоторной дискинезии. Пациентам с запорами рекомендуется увеличить физическую нагрузку (ходьба, плавание, физические упражнения, в том числе для укрепления мышц тазового дна и брюшного пресса). Утром пациент должен предусмотреть время (15–30 мин) для дефекации после обильного завтрака. Стакан воды комнатной температуры или сока также может быть достаточен для возбуждения гастрокишечного рефлекса. При отсутствии дефекации в первые дни могут использоваться слабительные свечи. Диету и физические упражнения можно усилить физиотерапевтическими процедурами.
Для электростимулирующей терапии используют пороговые и экспоненциальные электроимпульсы. Этот метод в комбинации с диетой дает положительный эффект у многих пациентов с гипокинетическими запорами [7]. Медикаментозную терапию назначают с учетом характера моторных нарушений толстой кишки. При гипомоторной дискинезии толстой кишки используют прокинетики, при спастической дискинезии – спазмолитики миотропного действия. В последние годы значительный прогресс достигнут в уточнении механизмов, контролирующих моторную функцию пищеварительного тракта, и создании новых лекарственных препаратов для коррекции моторных расстройств. Моторика желудочно–кишечного тракта регулируется деятельностью центральной и вегетативной нервной системы [9]. В кишечнике ведущая роль принадлежит вегетативной иннервации, представленной интрамуральными (автономными) и вставочными нейронами, объединенными в подслизистое и мышечное сплетения.
К интрамуральным нейромедиаторам относят: ацетилхолин – для холинергических нейронов; серотонин – для серотонинергических нейронов; АТФ – для пуринергических нейронов (пуринергическая система ингибирует тонус гладкомышечных волокон). К интрамуральным медиаторам относятся также нейропептиды: ВИП, который может активировать и ингибировать функцию нейронов мышц; соматостатин, ингибирующий и стимулирующий интрамуральныенейроны; субстанция Р, возбуждающая интрамуральные нейроны; энкефалины, модулирующие активность интрамуральных нейронов. Усиление моторики наблюдается при стимуляции холинорецепторов (через ацетилхолин), ряда опиатных (ОР 1 и ОР 3 ) и серотониновых рецепторов, ослабление – при стимуляции адренорецепторов, дофаминовых, пуриновых и других опиатных (ОР 2 ) рецепторов [1,8]. К прокинетикам относятся следующие группы препаратов: агонисты 5–гидрокситриптамин (5НТ 4 )–рецепторов (цизаприд, тегасерод, прукалоприд, мосаприд); агонисты 5НТ–рецепторов (суматриптан); антагонисты дофаминовых Д 2 –рецепторов (метоклопрамид, домперидон). Из перечисленных групп только агонисты 5НТ 4 –рецепторов оказывают эффективное пропульсивное действие на толстую кишку.
Цизаприд, как установлено, ускоряет транзит по толстой кишке, стимулирует ее моторную активность и уменьшает порог чувствительности прямой кишки к дефекации. Эффективная доза цизаприда – не менее 30 мг/сут. Однако использование этого препарата сопряжено с развитием побочных явлений. Описаны случаи аритмий сердца и внезапной смерти пациентов, получавших цизаприд (синдром удлиненного интервала Q–Т). В связи с этим в ряде стран его применение ограниченно. Перед началом лечения следует проводить оценку «польза–риск», особенно у пожилых пациентов с исходным удлинением интервала Q~T, гипокалиемией и гипомагниемией. Однако другие производные бензамида, такие как мосаприд, не имеют подобного побочного действия на функцию сердца. Тегасерод – один из новых прокинетиков, который является высокоселективным агонистом 5НТ 4 –рецепторов. Показано, что он может сокращать время транзита при синдроме разраженной кишки с преобладанием запора [9]. Продолжаются клинические исследования этого препарата.
В связи с отсутствием эффективного и безопасного прокинетика в лечении запоров, обусловленных гипо– или атонией толстой кишки, используются слабительные средства . Часто пациенты сами подбирают себе слабительный препарат методом проб или по совету друзей и знакомых. Существуют большое количество слабительных средств и различное их деление на группы. По механизму действия слабительные препараты условно разделяются на четыре группы: 1) вызывающие химическое раздражение рецепторов слизистой оболочки кишечника: антрахиноны (производные сенны, крушины, ревеня, алоэ), дифенолы (бисакодил, пикосульфат натрия), касторовое масло; 2) обладающие осмотическими свойствами: солевые (натрия или магния сульфат, карлварская соль), дисахариды (лактулоза), многоатомные спирты (маннитол, сорбитол), макрогол; 3) увеличивающие объем содержимого кишечника – балластные вещества (агар–агар, метилцеллюлоза, отруби, семя льна); 4) способствующие размягчению кала (жидкий парафин, масло вазелиновое, макрогол).
Действующим веществом растительных экстрактов являются ди– или тригидроксилантрахиноны в форме антрахиноновых гликозидов. Из экстрактов алоэ, сенны, крушины и ревеня в толстой кишке высвобождаются активные производные антрахинона, которые стимулируют перистальтику толстой кишки, ингибируют всасывание воды и электролитов. Действие препаратов этой группы зависит от времени опорожнения желудка, пассажа по толстой кишке и наступает спустя 6 ч при приеме их перед едой. По выраженности слабительного эффекта препараты располагаются в следующей последовательности: листья сенны > плоды сенны > кора крушины > корень ревеня. При длительном применении они вызывают меланоз слизистой оболочки кишки. Часто возникает привыкание к данным препаратам, поэтому при длительном употреблении требуется увеличение их дозы. Так, через 5 лет приема на то же слабительное средство отвечает каждый 2–й пациент, а через 10 лет – каждый 10–й [3]. Производное дифенилметана – бисакодил – по частоте применения занимает 1–е место среди препаратов этой группы. Он выпускается в двух лекарственных формах: в драже и свечах. В отличие от препаратов, содержащих антрахиноны, бисакодил при приеме внутрь находится в активной форме уже в желудке. Поэтому его прием, особенно при увеличении дозы, часто сопровождается спастическими болями в верхней части живота.
При использовании в свечах бисакодил увеличивает пропульсивную активность толстой кишки, и слабительный эффект наступает через 1 ч. Эту форму препарата применяют для быстрой очистки кишечника при подготовке пациента к срочной операции или инструментальному исследованию. В тонкой кишке бисакодил частично всасывается и, вступая в системный кровоток, увеличивает возможность токсического действия и развития аллергических реакций. Из препаратов, обладающих осмотическими свойствами , наибольшее распространение получили лактулоза и макрогол. Солевые слабительные (натрия сульфат, магния сульфат) для лечения хронических запоров практически не используют из–за болей в животе и формирования жидкого кала, что при частом употреблении приводит к водно–электролитным расстройствам.
Лактулоза – синтетический неадсорбируемый дисахарид, состоящий из лактозы и фруктозы. В неизменном виде она поступает в толстую кишку. В подвздошной кишке лактулоза расщепляется с образованием молочной и других кислот. Вследствие этого снижается рН в просвете кишки, что вызывает раздражение ее рецепторов и стимулирует моторику. Положительным эффектом лактулозы является ее пребиотический эффект, способствующий росту нормальных сахаролитических бактерий. Однако в лечении запоров требуются более высокие дозы препарата, чтобы сопровождается вздутием и распиранием живота. Это обстоятельство вынуждает пациентов отказываться от длительного приема лактулозы.
Макрогол – препарат с молекулярной массой 4000 является гидрофильным полимером, не проникающим через биологические мембраны кишечной стенки; способен образовывать устойчивые связи с молекулами воды и удерживать ее в просвете кишки. Увеличение объема содержимого на всем протяжении толстой кишки способствует ее перистальтической активности. Препарат не взаимодействует с лекарственными препаратами, не изменяет водно–электролитный обмен. Макрогол не метаболизируется, не абсорбируется, не изменяет рН кишечного химуса и действует независимо от состава бактерий кишки. Может использоваться даже у беременных. Слабительное действие наступает через 24–48 ч после приема. Стойкий эффект наблюдается через 2 недели регулярного его приема. Препарат не вызывает побочных явлений, к нему не развивается привыкания.
К слабительным средствам, увеличивающим объем содержимого кишечника , относят пищевые волокна овощей, фруктов и зерновых, целлюлозосодержащие препараты и мукофальк. Увеличение в рационе доли продуктов, богатых клетчаткой, нередко становится причиной диспептических расстройств (метеоризм, боли в животе). В этих случаях используют целлюлозосодержащие препараты. Они не всасываются, абсорбируют воду, набухают и, вызывая растяжение кишки, усиливают ее перистальтику [2]. Однако при запорах, обусловленных атонией толстой кишки, препараты этой группы эффективны лишь у 25% больных, а при нарушении дефекации – у 30%.
Препараты, размягчающие каловые массы (жидкий парафин и вазелиновое масло) имеют ограниченное применение. Они не усиливают перистальтику, но снижают напряжение при дефекации. Этими же свойствами обладают масляные микроклизмы. При неоднократном применении внутрь вазелиновое масло снижает всасывание жирорастворимых витаминов и может обусловливать их дефицит в организме. Прием слабительных препаратов различных групп приводит к развитию ряда побочных эффектов:
1. Нарушение всасывания: – подавление всасывания витаминов, солей, питательных веществ; – стимулирование секреции на фоне потери воды и солей.
2. Патологические эффекты и системные поражения: – псевдомеланоз прямой, сигмовидной ободочной и толстой кишки; – токсический гепатит; – парафиномы; – синдром недостаточности калия и натрия; – вторичный или третичный альдостеронизм; – интоксикация, обусловленная гипермагниемией.
3. Функциональные расстройства желудочно–кишечного тракта: – интолерантность в желудке (тошнота, рвота); – абдоминальные боли; – отрыжка, метеоризм, ощущение переполнения; – кишечная непроходимость, вызванная «слабительными препаратами, увеличивающими объем»; – нарушение состава кишечной микрофлоры.
4. Влияние слабительных средств на метаболические процессы: – замедление или снижение абсорбции нутриентов; – увеличение выделения с мочой ионов Na + и К + ; – тахифилаксия.
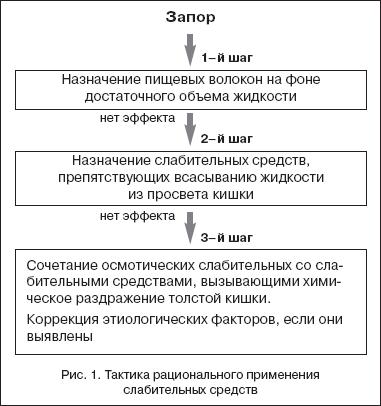
Электролитные расстройства возникают у 25–35% пациентов, регулярно принимающих слабительные средства. В большей степени они отмечаются при приеме препаратов сенны, алоэ, бисакодила и натрия пикосульфата, которые чаще используются пациентами и назначаются врачами. Основное нарушение электролитного баланса – дефицит калия, способствующий усилению запора [7]. Гипокалиемия может привести к повреждению почечных канальцев. Вследствие этого увеличивается потеря калия через почечный барьер. Дефицит калия обусловливает нарушение сокращения мышц кишки (формирование инертной кишки) и к увеличению дозы слабительных препаратов. По этой причине следует избегать длительного приема слабительных средств указанных групп, особенно в высоких дозах. При выборе слабительного средства следует придерживаться определенной тактики (рис. 1). Начинать лечение следует с препаратов, увеличивающих объем содержимого кишки (наполнители и осмотические слабительные). Среди этих слабительных преимущество имеет макрогол, который при оценке эффективности по шкале 0–100 мм (0 – отсутствие эффекта, 100 – высокая эффективность) получил 89,5 мм, по мнению врачей, и 78,3 мм – при оценке пациентами. В среднем положительный индекс составил 77,3 мм. Даже при длительном применении макрогол не вызывал побочных эффектов.
При выраженной гипотонии или атонии кишки следует сочетать препараты, увеличивающие объем содержимого в кишке: макрогол с прокинетиками или слабительными средствами, вызывающими химическое раздражение кишки. При этом необходимо индивидуальное дозирование (как можно меньше, но столько, сколько нужно; избегать диареи). Ежедневный прием стимуляторов моторики не обязателен. Например, 2 пакетика макрогола принять утром с интервалом в 1 ч (в 8 или 9 ч) ежедневно и дополнительно 2 раза в неделю во 2–й пакетик добавить 15 капель натрия пикосульфата. Целесообразно делать перерывы в приеме слабительных средств, чтобы определить, прошел ли запор. Благодаря комбинации стимуляторов моторики с препаратами, обеспечивающими объем кишечного содержимого, можно надежно нормализовать деятельность кишечника (рис. 2).
Для лечения запоров, обусловленных спастической дискинезией и сопровождающихся болями в животе, следует использовать спазмолитики . Препараты должны обладать высокой избирательностью действия на спазмированные участки кишки, не нарушать ее перистальтическую активность, эффективно купировать болевой синдром, не влиять на функцию других органов. Из миотропных спазмолитиков наиболее эффективно купируют болевой синдром в кишке пинаверия бромид, мебеверина гидрохлорид, отилония бромид и препараты, обладающие прямым действием на внутриклеточные процессы в миоците. Однако, по данным мета–анализа 26 клинических исследований, спазмолитики миотропного действия в виде монотерапии существенно не влияли на купирование запоров [3]. Поэтому для получения регулярного стула их следует принимать со слабительными средствами, увеличивающими объем кала и размягчающими его консистенцию (рис. 3). Схема лечения запоров, обусловленных функциональной аноректальной обструкцией, представлена в табл (рис. 4). При сниженной чувствительности слизистой оболочки прямой кишки назначают свечи, освобождающие углекислый газ, индуцирующий дефекационный рефлекс (лецикарбон).
Для выработки позыва на дефекацию можно назначать микроклизмы объемом до 200 мл ежедневно утром. В специализированных центрах лечения этого вида запоров успешно применяется методика биологической обратной связи – biofeedback . Biofeedback –тренинг оказался эффективным у 85% пациентов с функциональной обструкцией аноректальной зоны [5]. При всех видах запоров в комплексное лечение следует включать препараты, восстанавливающие кишечный биоценоз. И хотя эффект пробиотиков при запоре с научной точки зрения доказан недостаточно убедительно, их применение позволяет уменьшить газообразование в кишечнике и нередко снизить дозу слабительных препаратов. Итак, эффективное лечение запоров достигается благодаря совместному взаимодействию врача и пациента при выборе оптимальной схемы терапии, улучшающей качество жизни больного.




Список литературы
1. Григорьев П.Я, Яковенко Э.П. Запор: от симптома к диагнозу и адекватному лечению // Тер. арх. – 1996. – Т. 68, № 2. – С. 27–30.
2. Румянцев В.Г. Хронические запоры: подходы к диагностике и терапии // Моторика толстой кишки. Патофизиологические и терапевтические аспекты / ГНЦ колопроктологии МЗ РФ. – М., 1997.
3. Синдром раздраженного кишечника. Для тех кто лечит // Здоровье. – 2001. –№ 6, прил.
4. Bazzocchi S., Ellis J., Villanueva–Meyer et al. Postprandial colonic transit and motor activity in chronic constipation // Gastro–enterology. – 1990. – Vol. 98. – P. 686–693.
5. CummingsJ.H. Diet and transit through the gut // J. Plant. Foods. – 1978. – Vol.. – P. 83–95.
6. Finke S. Ballaststofte in der Ernahrung // Biol. Med. – 1991. – №1. – S. 456–463.
7. Fusgen I. Constipation. Practical geriatrics series. – Munchen: MMV Med.–Verlag, 1993.
8. Marvin M., Michael D., Kenneth L. Gastrointestinal motility in Health and Disease. – 2002.
9. Prather C.M., Camilleri M., Zinsmeis–ter A.R. et al. Tegaserod accelerates orocecal transit in patient with constipation predominant irritable bowel syndrome // Gastroenterology. – 2000. – Vol. 1 18. – P. 463–468.
10. Sarna S.K. Physiology and pathophysiology of colonic motor activity. Part I // Dig. Dis. Sci. – 1991. – Vol. 36. – P. 827–862.