Кристалохімія атомних дефектів у напівпровідниках структури сфалериту і в'юрциту.
Міністерство освіти і науки України
КРИСТАЛОХІМІЯ АТОМНИХ ДЕФЕКТІВ У НАПІВПРОВІДНИКАХ
СТРУКТУРИ СФАЛЕРИТУ І В’ЮРЦИТУ
Кваліфікаційна робота
м. Івано-Франківськ
2007
ЗМІСТ
Вступ 3
Моделі структур в халькогенідах кадмію і цинку 5
Області існування структур сфалериту і в’юрциту 8
Радіуси тетраедричних і октаедричних порожнин для сфалериту і в’юрциту 10
Кристалічна структура і антиструктура в телуриді кадмію 15
Кристалоквазіхімічний аналіз 17
Процеси легування 17
Утворення твердих розчинів 20
Обговорення результатів 21
Висновки 23
Література 24
Вступ
В останні роки інтерес до сполук А2В6, до яких відносяться халькогеніди цинку і кадмію, непохитно зростає в зв’язку з все більш чітко виявленими широкими можливостями їх практичного використання. Більшість цих сполук кристалізуються в двох структурних типах: сфалериту і в’юрциту, один з яких стабільний [1-3].
Структури сфалериту і в’юрциту досліджувались досить давно, проте область їх існування для окремих сполук, умови фазових переходів, уточнення дефектної підсистеми, кристалічної будови, кристалохімія вимагає і сьогодні.
В роботі на основі літературних джерел зроблена узагальнена характеристика структур сфалериту і в’юрциту для халькогенідів цинку і кадмію, запропонована дефектна модель, уточнено різні типи радіусів елементів в цих структурах, розраховано радіуси тетраедричних і октаедричних порожнин. За об’єкт дослідження із халькогенідного ряду цинку і кадмію було вибрано широкозонний напівпровідник телурид кадмію, який може кристалізуватися як в структурі сфалериту так і в’юрциту.
Актуальність вивчення поведінки домішок у телуриді кадмію обумовлена широким його використанням в оптоелектроніці, при створені модулів сонячних елементів, детекторів іонізуючого випромінювання, які працюють при кімнатній температурі [13-15].
Ширина області гомогенності в CdTe збагачена як Cd, так і Te, складає ~ 10-1 ат.%, при цьому на кожен заряджений дефект припадає 100 електрично неактивних дефектів. Переважаючими видами дефектів в телуриді кадмію, збагаченому Сd є електрично неактивні вакансії телуру, а з сторони Те – вакансії кадмію, що дає можливість припустити наявність в CdTe поряд з дефектами Френкеля дефектів Шоткі. Введення в основну матрицю телуриду кадмію як стехіометричного складу так і при нестехіометрії домішок дозволяє одержати матеріал з різною дефектною підсистемою, яка визначає тип провідності і концентрацію носіїв струму матеріалу. Так, надлишкові відносно стехіометричного складу атоми кадмію вкорінюються в міжвузля решітки і є донорами. При надлишку телуру утворюються вакансії кадмію, які є акцепторами з рівнем 0,15 еВ над валентною зоною [16].
Ряд елементів (Ga, In, Al) III групи в CdTe проявляють донорні властивості, тобто дають можливість одержати матеріал n-типу провідності [17]. Елементи VII групи, а саме хлор, утворює в телуриді кадмію малі донорні рівні і займає в кристалічній решітці позицію атомів телуру. Однак також відомо, що хлор поводить себе як акцептор, утворюючи з вакансіями кадмію комплекси (V>Cd>>->>Cl>) [15].
В роботі на основі кристалоквазіхімічних підходів [18] запропоновані кристалоквазіхімічні моделі процесів нестехіометрії та легування телуриду кадмію киснем, хлором, індієм; утворення твердих розчинів з ізовалентним і гетеровалентним заміщенням.
1. Моделі структур в халькогенідах кадмію і цинку
Кристалографія сполук А2В6, утворених із елементів II i VI груп періодичної системи, дещо ускладнена внаслідок того, що вони здатні кристалізуватися в різних поліморфних модифікаціях.
Цинкова обманка ZnS (сфалерит) – кубічна структура, в’юрцит – гексагональна, характеризуються тетраедричним розміщенням атомів. Крім того, вони утворюють ряд близьких за структурою політипів, які характеризуються також тетраедричним розміщенням атомів. Тип зв’язку в цих кристалах може змінюватися від чисто іонного характеру до ковалентного і змішаного [2].
Моделі структур сфалериту і в’юрциту показані на рис.1(а,б), параметри гратки в таблицях 1,2. Всі халькогеніди цинку і кадмію і в частковості CdTe, ZnTe і ZnSe кристалізуються в структурі цинкової обманки типу (В3). Структура сфалериту характеризується щільною трьохшаровою кубічною упаковкою шарів, в’юрциту - двохшаровою гексагональною. В структурі в’юрциту (В4) кристалізуються майже всі халькогеніди цинку і кадмію[2].


а) б)
Рис.1. Моделі структур: а – сфалериту, б – в’юрциту
Слід відмітити, що атомами будь-яких ідеальних щільних упаковок простір заповнюється на 74.05%. Т.чином ¼ всього простору упаковки належить пустотам [3]. Розрізняють два види пустот: пустоти оточені чотирьма атомами – тетраедричні , оточені шістьма атомами – октаедричні. Щільноупакованні аніонні решітки мають одну октаедричну і дві тетраедричні порожнини. На рис.2(а,б) і 3(а,б) графічно показано розміщення цих порожнин (дефектів) в елементарній комірці сфалериту і в’юрциту. Із яких видно, що октаедричні пустоти в них не заповнені, а тетраедричні на половину. На основі розрахованої кількості розміщення атомів в елементарній комірці розрахували, що на одну комірку сфалериту припадає 4 октаедричні і 8 тетраедричних порожнин, в’юрциту – 12 тетраедричних, 6 октаедричних. Так як тетраедричні порожнини в цих структурах заповнені наполовино металом, а октаедричні не заповнені, то дефектна підсистема буде утворена тетраедричними і октаедричними кристалічними вакансіями і міжвузловими атомами металу в тетраедричних поржнинах.


а) б)
Рис 2. Графічне розміщення тетраедричних порожнин (ТП) для структур: а – сфалериту, б – в’юрциту
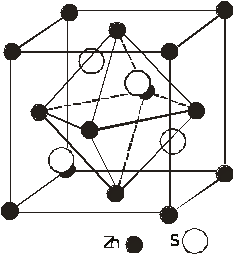

а) б)
Рис 3. Графічне розміщення октаедричних порожнин (ОП) для структур: а – сфалериту, б – в’юрциту
2. Області існування структур сфалериту і в’юрциту
Cтруктура в’юрциту для ZnS – стійка при високих температурах. Фазовий перехід із гексагональної модифікації ZnS в кубічну проходить при температурах 1020 і 1150 0С [2]. В [4] показані поліморфні пари, зв’язані переходом під тиском, які зачіпають зміну першої координації для ZnO тиск переходу 100 кбар: низькотемпературна форма – в’юрцит, перша координація 4:4; високотемпературна форма – NaCl, перша координація 6:6. Для СdS тиск переходу 20 кбар: низькотемпературна форма – сфалерит,перша координація 4:4; високотемпературна форма – NaCl, перша координація 6:6. Зміна другої координації для CdS проходить при тиску 160-200 кбар, при низькому тиску структурний тип сфалерит; привисокому тиску в’юрцит. Для CdSструктурна зміна при збільшені тиску обернена тій, яка викликається пониженням температури. Перехід із тетраедричної до октаедричної координації супроводжується зменшенням об’єму приблизно на 20 %. Незалежно від того чи має вихідний матеріал структуру в’юрциту чи цинкової обманки, при зворотньому переході до атмосферного тиску зберігається структура цинкової обманки [2].
Можливість зв’язати тип стабільної структури А2В6 з співвідношенням іонності і ковалентності хімічного зв’язку розроблено авторами [5] (табл. 3).
Таблиця 3
Зв’язок стабільні структури А2В6 з коефіцієнтом іонності
|
А2В6 |
,% |
Стабільна структура |
(с/а) |
А2В6 |
,% |
Стабільна структура |
(с/а) |
|
ZnO |
82 |
W |
-293 |
ZnSe |
33 |
S |
+65 |
|
CdS |
45 |
W |
-103 |
CdTe |
21 |
S |
+68 |
|
CdSe |
40 |
W |
-24 |
ZnTe |
16 |
S |
+81 |
|
ZnS |
40 |
S |
+33 |
Як відомо, різниця в енергіях двох поліморфних модифікацій – в’юрцита і сфалерита, яка б мала вона не була, буде обумовлена різним вкладом іонності, про що свідчить порівняння їх констант Маделунга. Вони є мірою електростатичної взаємодії між іонами решітки, для структурного типу в’юрциту і сфалериту і рівні 1,641;1,638, яка є більшою для решітки в’юрциту [6]. Звідси можна зробити два висновки. По-перше, якщо сполуки А2В6 можуть кристалізуватися в двох модифікаціях, одна з яких метастабільна, то тоді характер зв’язку в гексагональній модифікації повинен бути більш іонним, чим у кубічній. Більший іонний характер структури в’юрциту експериментально доказаний вимірюванням ширини забороненої зони, яка для деяких сполук А2В6 виявилася дещо більшою, ніж ширина забороненої зони тих же сполук, які мають структуру сфалериту [7-9]. По-друге, в ряді сполук А2В6 з збільшенням долі іонності зв’язку () повинен спостерігатися перехід від стабільної структури сфалериту S до стабільної структури в’юрциту W (табл. 3).
3. Радіуси тетраедричних і октаедричних порожнин для сфалериту і в’юрциту
Коли необхідно підкреслити зв’язок атомів в сполуках використовують для одного і того ж атома різні радіуси: ковалентні, іонні, тетраедричн і октаедричні ковалентні радіуси атомів в сполуках. Для атомів халькогенідного ряду цинку і кадмію вони приведені в таблиці 4.
Таблиця 4
Радіуси елементів в халькогенідах цинку і кадмію
|
Елементи, r, Å |
Zn |
Cd |
S |
Se |
Te |
Література |
|
Атомний, r>a> |
1,53 |
1,71 |
1,09 |
1,22 |
1,42 |
|
|
Ковалентний, r>k> |
1,25 |
1,48 |
1,02 |
1,16 |
1,36 |
|
|
Іонний, r>i> |
0,83 |
0,99 |
1,82 |
1,93 |
2,11 |
|
|
Тетраедричний, r>t> |
1,31 |
1,48 |
1,04 |
1,14 |
1,32 |
[2] |
|
Октаедричний, r>o> |
1,20 |
1,38 |
1,35 |
1,45 |
1,64 |
[10] |
Повернемося до відомої теорії структур щільної упоковки, яка дозволяє в рамках цього підходу визначити всі необхідні геометричні характеристики кристалічних структур напівпровідників А2В6. В цій теорії під кристалічною будовою розуміють послідовну шарову упаковку твердих сфер з утворенням тетра- і октапорожнин [12].
Якщо вважати структури сфалериту і в’юрциту щільноупаковані по аніону тоді необхідне виконання наступних двох умов:
топологія аніонної підрешітки співпадає з топологією кількості щільноупакованих сфер, причому катіони розміщуються тільки в тетраєдричних і октаедричних міжвузлях цієї підрешітки;
потенціали міжатомної взаємодії U>мх>, U>хх> i U>мм>, відповідають нерівності (1)
U>мх>>U>хх>>U>мм> , (1)
де М – метал, Х – неметал
Із простих геометричних уявлень можна одержати сукупність величин, які характеризують тетраедр, октаедр і елементарну комірку г.ц.к. решітки. Ці величини, однозначно зв’язані з радіусом сфер будови, тобто радіусами атомів кристалічної решітки, а відповідно і з параметром решітки (а,с) для сфалериту і в’юрциту показані в таблиці 5.
Таблиця 5
Зв’язок величин, які характеризують тетраедр і октаедр в г.ц.к. решітці з радіусом атома і періодом решітки для сфалериту і в’юрциту
|
Параметр |
Позначення |
f (R) |
|
Сфалерит |
||
|
1. Радіус атома |
R |
|
|
2. Період кристалічної решітки |
a |
a = 2R2 |
|
3. Ребро тетраедра |
a>1> |
a>1 >= 2R = 0,71a |
|
4. Висота тетраедра |
h |
h = 2R2/3 = 0,578a |
|
5. Відстань від центра тетраедра до його основи |
z |
z = R/6 = 0,41R= 0,145 a |
|
6. Відстань центра тетраедра від вершини |
y>t> |
y>t>=h-z = (3/6)R = 0,433 a |
|
7. Відстань центра октаедра від вершини |
y>o> |
y>o> = R2 |
|
8. Мінімальний радіус сфери, вписаної в тетрапорожнину |
rt>min> |
rt>min> = y>t>-R = 0,225 R |
|
9. Мінімальний радіус сфери, вписаної в октапорожнину |
ro>min> |
ro>min > = y>o>- R = 0,414 R |
|
10. Максимальний радіус сфери, вписаної в тетрапорожнину |
rt>max> |
rt>max> = 0,5 R |
|
11. максимальний радіус сфер, вписаних в октапорожнину |
ro>max> |
ro>max> = 0,732 R |
|
В’юрцит |
||
|
1. Період кристалічної решітки |
a, c |
a =1/2 √2 а(куб.) c = 2/3 √3 а(куб.) |
|
2. Ребро тетраедра |
a>1> |
a>1 =>[1/3a2 + 1/4c2]1/2 |
|
3. Висота тетраедра |
h |
h = c/2 |
|
4. Відстань центра тетраедра від вершини |
y>t> |
y>t> = 2/3 h = c/3 |
|
5. Відстань центра октаедра від вершини |
y>o> |
y>o> = [1/4a2 + 3/16c2]1/2 |
|
6. Мінімальний радіус сфери, вписаної в тетрапорожнину |
rt>min> |
rt>min> = y>t >– R |
|
7. Мінімальний радіус сфери, вписаної в октапорожнину |
ro>min> |
ro>min> = y>o> - R |
|
8. Максимальний радіус сфери, вписаної в тетрапорожнину |
rt>max> |
rt>max> = rt>min √3/2> |
|
9. Максимальний радіус сфери, вписаної в октапорожнину |
ro>max> |
ro>max> = ro>min √3/2> |
Елементарний тетраедр і октаедр, утворені з щільної упаковки шарів халькогену або металу показані на рис. 4. Для сфалериту і в’юрциту кристалічна решітка складається з двох підрешіток утворених із атомів II i VI груп періодичної системи. В такій решітці виникають вже два типи тетрапорожнин (t>1,> t>2>) і два типи октапорожнин (o>1, >o>2>), які відрізняються оточенням, тому розраховували радіуси ТП і ОП в оточені телуру і металу.

Рис. 4. Елементарний тетраедр (а), октаедр (б), утворені аніонною і катіонною упаковкою шарів: Т – центр тетраедра, О – центр октаедра, а>1> – ребро тетраедра, h – висота тетраедра.
Геометричні характеристики тетра- і октапорожнин дозволяють визначити радіуси сфер (атомів) rt>min>, ro>min> (табл. 5), які в них можуть бути вписані. Існує обмеження на rt, ro, тобто радіуси вписаних сфер не можуть приймати значення, яке перевищує rt>max>, ro>max>. Їх можна визначити із порушення щільної упаковки сфер, коли вони не дотикаються одна до одної. Тоді проходить ніби збільшення ефективних розмірів сфер основної будови настільки, що, висота утвореного ними нового тетраедра h>1> буде рівна або перевищить 2R. Так як h = 2r2/3, тоді прирівнюючи h = 2R, одержимо r = r3/2. Звідси можна знайти гранично допустиме значення радіусів сфер вписаних в порожнини rt>max> і ro>max>.[12].
В результаті такого геометричного представлення, враховуючи тип зв’язку в ряді досліджуваних сполук, тобто ковалентні і іонні (умовно) радіуси атомів, які приймають участь в утворені щільної упаковки визначили числові значення (мінімальні) тетраедричних і октаедричних порожнин на основі характеристик приведених в таблиці 5. Для сфалериту і в’юрциту одежані результати показані в табл. 6.
Таблиця 6
Розраховані радіуси тетраедричних і октаедричних порожнин для сфалериту і в’юрциту Оточення – халькоген
|
Сполука |
а, Ао |
с, Ǻ |
y>t>, Ǻ |
rt>к>, Ǻ |
rt>і>, Ǻ |
y>o>, Ǻ |
rо>к>, Ǻ |
rо>і>, Ǻ |
|
СФАЛЕРИТ |
||||||||
|
ZnS |
5,4093 |
2,3422 |
1,3222 |
0,5222 |
2,7046 |
1,6846 |
0,8846 |
|
|
ZnSe |
5,668 |
2,4545 |
1,2945 |
0,5245 |
2,8343 |
1,6743 |
0,9043 |
|
|
ZnTe |
6,1037 |
2,6429 |
1,2829 |
0,5329 |
3,0518 |
1,6918 |
0,9418 |
|
|
CdS |
5,820 |
2,5200 |
1,530 |
0,73 |
2,91 |
1,550 |
1,09 |
|
|
CdSe |
6,05 |
2,6196 |
1,4596 |
0,6895 |
3,025 |
1,865 |
1,095 |
|
|
CdTe |
6,481 |
2,8063 |
1,4463 |
0,6963 |
3,2405 |
1,8805 |
1,1305 |
|
|
В’ЮРЦИТ |
||||||||
|
ZnS |
3,820 |
6,280 |
2,693 |
1,673 |
0,873 |
3,323 |
2,303 |
1,053 |
|
ZnSe |
4,003 |
6,540 |
2,18 |
1,16 |
0,36 |
3.468 |
2,308 |
1,538 |
|
ZnTe |
4,31 |
7,09 |
2,363 |
1,343 |
0,543 |
3,751 |
2,391 |
1,641 |
|
CdS |
4,1362 |
6,714 |
2,238 |
1,218 |
0,418 |
3,568 |
2,548 |
1,748 |
|
CdSe |
4,300 |
7,007 |
2,336 |
1,316 |
0,516 |
3,719 |
2,559 |
1,789 |
|
CdTe |
4,57 |
7,48 |
2,493 |
1,473 |
0,673 |
3,96 |
2,600 |
1,85 |
Оточення – метал
|
Сполука |
а, Ǻ |
с, Ǻ |
y>t>, Ǻ |
rt>к>, Ǻ |
rt>і>, Ǻ |
y>o>, Ǻ |
rо>к>, Ǻ |
rо>і>, Ǻ |
|
СФАЛЕРИТ |
||||||||
|
ZnS |
5,4093 |
2,3422 |
1,062 |
1,512 |
2,7046 |
1,425 |
1,875 |
|
|
ZnSe |
5,668 |
2,4545 |
1,174 |
1,624 |
2,8343 |
1,554 |
2,004 |
|
|
ZnTe |
6,1037 |
2,6429 |
1,363 |
1,813 |
3,0518 |
1,772 |
2,222 |
|
|
CdS |
5,820 |
2,5200 |
1,04 |
1,53 |
2,91 |
1,43 |
1,92 |
|
|
CdSe |
6,05 |
2,6196 |
1,139 |
1,629 |
3,025 |
1,545 |
2,035 |
|
|
CdTe |
6,481 |
2,8063 |
1,326 |
1,816 |
3,2405 |
1,761 |
2,251 |
|
|
В’ЮРЦИТ |
||||||||
|
ZnS |
3,820 |
6,280 |
2,693 |
1,413 |
1,863 |
3,323 |
2,043 |
2,493 |
|
ZnSe |
4,003 |
6,540 |
2,18 |
0,9 |
1,35 |
3.468 |
2,188 |
2,638 |
|
ZnTe |
4,31 |
7,09 |
2,363 |
1,083 |
1,533 |
3,751 |
2,471 |
2,921 |
|
CdS |
4,1362 |
6,714 |
2,238 |
0,758 |
1,248 |
3,568 |
2,088 |
2,578 |
|
CdSe |
4,300 |
7,007 |
2,336 |
0,856 |
1,346 |
3,719 |
2,239 |
2,729 |
|
CdTe |
4,57 |
7,48 |
2,493 |
1,013 |
1,503 |
3,96 |
2,48 |
2,97 |
4. Кристалічна структура і антиструктура в телуриді кадмію
Телурид кадмію кристалізується в структурах сфалериту (S – кубічна структура В3), і в’юрциту (W – гексагональна структура В4) із однаковим числом атомів як в першій, так і в другій координаційних сферах [2, 9]. При кімнатній температурі і тиску 3,3-3,6 ГПа в телуриді кадмію проходить фазовий перехід із структури типу сфалерит в’юрцит у структуру типу NaCl, що супроводжується різким зменшенням електропровідності [20-22].
Із кристалічної будови цих структур відомо, що вони характеризуються тетраедричним оточенням атомів двох видів, і тетраедричними (ТП) та октаедричними (ОП) порожнинами яким належить ¼ всього простору упаковки атомів [3]. На рис. 2 (а,б) і 3 (а,б) представлено розміщення ТП і ОП в елементарній комірці структур сфалериту і в’юрциту. На одну комірку сфалериту припадає 4 ОП, 8 ТП; в’юрциту – 6 ОП, 12 ТП. Із рис. 2, 3 видно, що ТП в обох структурах заповнені наполовину, а ОП повністю не заповнені.
На основі геометричних уявлень, враховуючи тип зв’язку в CdTe (21% іонності) [5], тобто ковалентні (rк) та іонні (ri) радіуси оточуючих атомів [10] розрахували радіуси ТП (r>т>) і ОП (r>o>) порожнин для оточення телуру і кадмію, які приведені в таблиці 7.
Таблиця 7
Радіуси тетраедричних (ТП) і октаедричних (ОП) порожнин для структур сфалериту та в’юрциту в підрешітці телуру (1), кадмію (2)
|
Сполука |
Структура |
a, Å |
c, |
rк, Å |
ri, Å |
rк>т>, Å |
ri>т>, Å |
rк>о>, Å |
ri>о>, Å |
|
СdTe CdTe |
S W |
6,48 4,57 |
7,48 |
1,36 1,36 |
2,11 2,11 |
1,446 1,473 |
0,696 0,673 |
1,881 2,60 |
1,131 1,85 |
|
CdTe CdTe |
S W |
6,48 4,57 |
7,48 |
1,48 1,48 |
0,99 0,99 |
1,326 1,013 |
1,816 1,503 |
1,761 2,48 |
2,251 2,97 |
Кристалоквазіхімічні підходи до запису хімічних формул і рівнянь грунтуються на правильному виборі антиструктури для даного класу сполук [18]. Для халькогенідів кадмію антиструктурою може бути природня “цинкова обманка” сульфід цинку, який кристалізуватися як в структурі сфалериту, так і в’юрциту.
Новизна кристалоквазіхімічного
методу полягає в тому, що антиструктуру
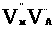 – сфалерит) накладають (суперпозиція,
резонанс) на кристалохімічну формулу
сполуки
– сфалерит) накладають (суперпозиція,
резонанс) на кристалохімічну формулу
сполуки
 .
Де
.
Де
 – двократно іонізовані негативні і
позитивні тетраедричні вакансії металу
(М) і аніону (А). Заряди дефектів в
кристалоквазіхімії позначаються як: х
– нейтральні, –
позитивні,
– негативні кількість цих знаків
відповідає кратності іонізації, e'
– концентрація електронів, h·
– концентрація дірок.
– двократно іонізовані негативні і
позитивні тетраедричні вакансії металу
(М) і аніону (А). Заряди дефектів в
кристалоквазіхімії позначаються як: х
– нейтральні, –
позитивні,
– негативні кількість цих знаків
відповідає кратності іонізації, e'
– концентрація електронів, h·
– концентрація дірок.
Така суперпозиція дає можливість ефективно аналізувати як самі процеси нестехіометрії, так і легування, утворення твердих розчинів, тощо. Розглянемо їх детальніше.
4.1. Кристалоквазіхімічний аналіз:
Нестехіометрія. При надлишку
кадмію антиструктура стехіометричного
сфалериту
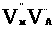 утворює кластер з катіонними вакансіями
утворює кластер з катіонними вакансіями
 (4.1)
(4.1)
Тоді при суперпозиції отриманого кластеру із квазіхімічною формулою стехіометричного складу отримаємо:

 (4.2)
(4.2)
Тут - мольні долі. Стає очевидним, що надлишок кадмію приводить до утворення донорних рівнів і обумовлює електронну провідність матеріалу.
При надлишку халькогену відповідно:
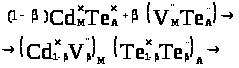
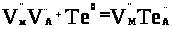 (4.3.)
(4.3.)
 (4.4)
(4.4)
Таким чином, надлишок телуру обумовлює утворення акцепторних рівнів і додаткових дірок, тобто, матеріалу р-типу.
Одержані результати визначення типу провідності для процесів нестехіометрії узгоджується із експериментальними приведеними в роботі [16].
Процеси легування
а) легування киснем. При суперпозиції антиструктури з киснем отримаємо такий кристалоквазіхімічний кластер:
 (4.5)
(4.5)
Суперпозиція матриці з даним кристалоквазіхімічним кластером приведе до наступного:
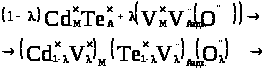
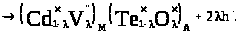 (4.6)
(4.6)
Отже, легування (адсорбція) телуриду кадмію киснем приводить до заміщення вакансії халькогена киснем з утворенням акцепторних центрів , що і обумовлює діркову провідність.
б) легування хлором. При суперпозиції антиструктури з хлором отримаємо такий кристалоквазіхімічний кластер за механізмом заміщення:
 (4.7)
(4.7)
С
уперпозиція
матриці з даним кристалоквазіхімічним
кластером приведе до наступного:
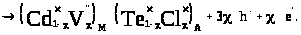 (4.8)
(4.8)
У випадку вкорінення хлору одержимо такий кластер:
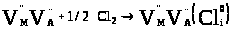 (4.9)
(4.9)
Так як
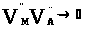 ,
тоді при суперпозиції основної матриці
з кластером (4.9) отримаємо:
,
тоді при суперпозиції основної матриці
з кластером (4.9) отримаємо:

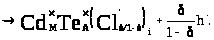 (4.10)
(4.10)
Отже, легування телуриду кадмію
хлором приводить до заміщення вакансій
телуру хлором і часткового проникнення
хлору в ОП підгратки аніону з утворенням
акцепторних центрів і діркової
провідності. Одержані кристалоквазіхімічні
результати не підтверджують донорну
дію хлору в CdTe
наведену в роботі [23]. Це
пояснюється можливим утворенням
акцепторних комплексів
 і нейтральних
і нейтральних
 ,
тоді як ізольованих
,
тоді як ізольованих
 залишається дуже мало, що і обумовлює
донорну дію хлору.
залишається дуже мало, що і обумовлює
донорну дію хлору.
в) легування індієм. З врахуванням донорної дії In в CdTe [23], кристалоквазіхімічний аналіз досліджували за механізмом заміщення атомів індію вакансій кадмію в основній матриці (механізм заміщення) та вкорінення індію у міжвузля, тобто в ТП або ОП порожнини (механізм вкорінення).
Механізм заміщення. Суперпозиція індію із антиструктурою основної матриці утворює кластер:
 (4.11)
(4.11)
Враховуючи електронну конфігурацію 4d105s25p1(In) і його зарядовий стан (In+1, In+3, 2In+2In+3 + In+1) отримаємо:
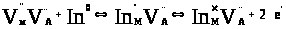 (4.12)
(4.12)
 (4.12')
(4.12')
При суперпозиції основної матриці з кластером (4.11) одержимо наступні вирази. Кластер (4.12') для спрощення запису опускаємо:

 (4.13)
(4.13)
Таким чином, утворений матеріал (5.13) характеризується електронною провідністю, яка обумовлена вакансіями в аніонній підгратці.
За механізмом вкорінення легуючий кластер має вигляд:
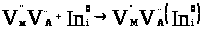 (4.14)
(4.14)
При суперпозиції одержимо:

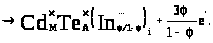 (4.15)
(4.15)
Механізм вкорінення індію (4.15) як і заміщення (4.13) підтверджує його донорну дію. При цьому припускається, що вкорінений індій може знаходитися в зарядовому стані (In+3), займаючи ТП чи ОП основної матриці.
Утворення твердих розчинів
Розглянемо криствлоквазіхімічний механізм утворення твердого розчину CdTe-ZnTe з ізовалентним заміщенням. Легуючий кластер має вигляд:
 (5.1)
(5.1)
При накладані матеріалу р-типу на кластер (5.1) одержимо:

 (5.2)
(5.2)
З виразу (5.2) видно, що цинк буде займати тетраедричні вакансії металу внаслідок чого зменшиться кількість вакансій металу і концентрація основних носіїв.
У випадку утворення твердого розчину CdTe-K>2>Te з гетеровалентним заміщенням одержимо кластер:
 (5.3)
(5.3)
Накладання основної матриці на кластер (5.3) приведе до наступного:
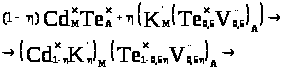
 (5.4)
(5.4)
Отже, утворений твердий розчин характеризується вакансіями в аніонній підгратці і n-типом провідності матеріалу.
Обговорення результатів
Згідно одержаних кристалоквазіхімічних рівнянь, що описують процеси нестехіометрії (4.2), (4.4) встановлено, що при відхилені від стехіометрії на боці кадмію одержуємо матеріал n-типу, а на боці телуру – p-типу.
Кисень згідно одержаного виразу (4.6) проявляє в телуриді кадмію акцепторні властивості з утворенням матеріалу p-типу.
Легування кристалів телуриду кадмію хлором дає можливість одержати матеріал p-типу із заміщенням тетраедричних вакансій телуру і вкоріненням хлору в ОП підгратки аніону або ТП підгратки металу. Механізм вкорінення хлору підтверджується співставленням іоного радіусу хлору (табл.8) з радіусом ОП підгратки аніону для в’юрциту (ri>о>= 1,85 Å).
Таблиця8
Електронна конфігурація та радіуси кадмію, індію, хлору, телуру [10]
|
Елементи |
Електронна конфігурація |
Радіуси, Å |
||||
|
атомні |
ковалентні |
іонні |
r>T> |
r>O> |
||
|
Cd |
4d103s2 |
1,71 |
1,48 |
0,99(2+) |
1,48 |
1,38 |
|
Іn |
4d105s25p1 |
1,55 |
1,58 |
0,94(3+) |
- |
1,65(I), 1,27(III) |
|
Cl>2> |
3s23p5 |
1,00 |
0,99 |
1,67(-) |
1,06 |
- |
|
Те |
4d105s25p4 |
1,42 |
1,36 |
2,11(2-) |
1,34 |
1,64 |
Імовірним є те, що хлор буде вкорінюватися і в ТП підгратки металу двох структур (ri>т>=1,8163 Å, ri>т>=1,503 Å) де він може проявляти донорну дію. Радіуси ОП і ТП наведені в табл. 7.
При легуванні телуриду кадмію індієм одержують матеріал n-типу як за механізмом заміщення так і вкорінення. Вкорінюється In3+ (r>In>3+=0,94 Å) при порівняні з радіусами ОП і ТП аналогічно хлору.
Розглянуті механізми утворення твердих розчинів з ізовалентним заміщенням (5.2) і гетеровалентним заміщенням (5.4) вказують на можливість заміщення вакансій металу досліджуваної матриці елементами Zn і К з утворенням матеріалів p- і n-типів.
Висновки
Згідно одержаних кристалоквазіхімічних механізмів процесів не стехіометрії, легування, утворення твердих розчинів в телуриді кадмію встановлено:
При процесах нестехіометрії на боці кадмію одержуємо матеріал n-типу провідності, на боці телуру – р-типу.
Адсорбція кисню на поверхні CdTe приводить до заміщення вакансій телуру киснем з утворенням матеріалу р-типу.
Легування CdTe хлором і індієм проходить за двома механізмами заміщення і вкорінення, що дає можливість одержати матеріал р-типу при легуванні хлором та n-типу при легуванні індієм, як за механізмом заміщення так і вкорінення.
При утворені твердих розчинів CdTe-ZnTe, CdTe-K>2>Te одержують матеріал р-типу з ізовалентним заміщенням і n-типу з гетеровалентним заміщенням.
Література
А. Верма, П. Кришка. Полиморфизм и политипизм в кристаллах. «Мир». М., 1969.
Физика и химия соединений АIIBVI. «Мир». М., 1970.
Г.М. Попов., И.И. Шафрановский. Кристаллография. М., «Высшая школа», 1972.
М.Дж. Бюргер. Фазовые переходы // Кристаллография.Том 16, в.6, 1971, с.1084.
К.В. Шалимова, В.А. Дмитриев. Изменение типа стабильной структуры в ряду соединений АIIBVI // Кристаллография, Том 17, в.3, 1972, с.541.
Л. Паулинг. Природа химической связи. М. – Л., 1947.
J.S. Park, F.I. Chan, J.Appl. Phys, 36, 800,1965.
G.F. Neumark. Phus. Rev., 125.838,1962.
O. Brafman, G. Schachar, I.T. Steinberger. J.Appl. Phys. 36.668,1965.
C.А. Семилетова. Тетраедрические и октаедрические ковалентные радиусы // Кристаллография. Том 21, в.4, 1976, с.752-754.
Д.М. Фреїк, В.В. Прокопів, У.М. Писклинець, І.М. Ліщинський. Вплив технологічних факторів і легуючої домішки індію на дефектну систему і тип провідності у телуриді кадмію // Фізика і хімія твердого тіла Т.3. №1 (2002) с. 526-530.
В.Й. Фистуль. Примеси переходных металлов в полупроводниках – М.: Металлургия, 1983, с.192.
F.V. Wald. Application of CdTe. A Review // Rev Phys. Appl. 12 (12). P.277-290 (1977).
G.C. Morris, S.K. Das, P.G. Tanner. Some Factors Aftecting Efficiencies of n-CdS/p-CdTe Thin Film Solar Cells // j. Cryst. Growth. 117. P.929-934 (1992).
S. Seto, A. Tanaka, Y. Mosa, M. Kawashima. Clorine – Related Photoluminescence Lines in High-Resistivitg Cl-Doped CdTe // j. Cryst. Growth. 117. P.271-275 (1992).
С.А. Медведев, С.Н. Максимовский, К.В. Киселева, Ю.В. Клевков, Н.Н. Сентгорина. О природе точечных дефектов в нелегированом СdTe // Изв. АН СССР. Неорганические материалы, IX (3), сс. 356-360 (1973).
О.Э. Панчук, П.И. Фейчук, Л.П. Щербак, П.М. Фочук, Р.Ф. Бойчук. Распределение Ga в CdTe // Изв. АН СССР. Неорганические материалы, 21 (7), сс.1118-1120 (1985).
С.С. Лисняк. Кристаллоквазихимическая модель исследований в химии твердого тела // Изв. АН СССР. Неорганические материалы, 29 (9), сс.1913-1917 (1992).
В.Г. Яковлева. Структура и свойства соединений АIIВVI. - В сб.: Современное состояние аналитической химии полупроводниковых соединений типа АIIВVI (Тр. Моск. ин-та стали и сплавов). М.: Изд. МИСиС, с. 151 (1983).
Н.Х. Абрикосов, В.Ф. Банкина, Л.В Порецкая, Е. В. Скуднова, С.Н. Чижевская. Полупроводниковые халькогениды и сплавы на их основе. М., Наука, с.220 (1975).
В.В. Матлак, М.И. Илащук, О.А. Парфенюк, П.А. Павлин, А.В. Савицкий. Електропроводность полуизолирующего СdTe // Физика и техника полупроводников, 16 (10), сс.89-92 (1982).
К. Руманс. Структурные исследования некоторых окислов и других халькогенидов при нормальных и высоких давлениях. М.: Мир, (1969).
Д.В. Корбутяк, С.В. Мельничук, П.М. Ткачук. Домішково-дефектна структура CdTe:Cl – матеріалу для детекторів іонізуючого випромінювання // Укр. Фіз. Журн., 44 (6), сс.730-737 (1999).