Исследование процессов испарения и конденсации жидких капель
Содержание:
Введение
Предисловие
Экологический аспект проблемы
О дисперсных системах
Атмосферные аэрозоли
Классификация и размер аэрозолей
Основная характеристика частиц дисперсной фазы – функция распределения частиц по размерам
Обратно-степенное распределение
Гамма распределение
Логарифмически-нормальное распределение
Состояние проблемы и постановка задачи
Газокинетические процессы в дисперсной системе
Непрерывная и дискретная динамика.
Непрерывный режим.
Свободно - молекулярный (кинетический) режим.
Переходный режим
Подведение итогов
Постановка задачи
Решение задачи и результаты исследования
Линеаризованное уравнение Больцмана для сферической
геометрии в односкоростном приближении.
Основные уравнения
Формальное решение уравнения для функции распределения
Точные результаты решения уравнений
Пограничный слой
Приближение скачка концентрации на поверхности частицы
Численные результаты
Выводы и заключение
Список литературы
Введение
1.1 Предисловие
Испарение и конденсация частиц представляют собой наиболее существенный фактор, изменяющий спектр размеров аэродисперсной системы. В особенности это касается жидких частиц. Это проблема очень актуальна как в различных технологических приложениях, так и в окружающей нас природе. Достаточно сказать, что круговорот воды в природе происходит через фазы испарения и объемной конденсации. Дисперсный состав аэрозольных частиц при испарении оказывается определяющей характеристикой системы в целом. Именно распределение по размерам ответственно за радиационный баланс солнечного излучения, достигающего поверхности земли и определяющего все земные процессы. В карбюраторных и дизельных двигателях распределение по размерам частиц топлива определяет скорость их горения, а значит и процесс работы двигателя. Конденсационные туманы не только паров воды образуются при сгорании различных топлив, при этом образуется множество ядер конденсации, которые могут служить центрами конденсации для других паров, в том числе и воды. Конденсация пересыщенных паров воды на ионах, которые образуются при радиоактивном распаде различных элементарных частиц, служит индикацией этих элементарных частиц в камерах Вильсона.
Этот беглый обзор может служить убедительным доказательством актуальности проблемы.
1.2 Экологический аспект проблемы
Осознание важности экологических проблем, связанных с влиянием жизнедеятельности человека на атмосферу и гидросферу Земли, является одним из наиболее серьезных стимулов к изучению процессов, управляющих поведением дисперсных систем в целом и аэрозолей в частности. Сейчас уже понятно, что мы живем в эпоху серьезного кризиса технократических идей, подразумевающих неограниченное воздействие человека на среду обитания. Прагматично-потребительское отношение к природе оказывается настолько недальновидным, что во многих случаях речь идет буквально о выживании человечества в преобразованном им природном мире. Особенно показательными в этом отношении становятся различного рода техногенные аварии и катастрофы, участившиеся в последнее время.
Экология - далеко не единственная сфера, где имеют дело с дисперсными системами. Можно назвать массу природных объектов и множество технологических процессов, которые связаны с присутствием и применением аэрозолей:
межзвездные и допланетные облака;
вулканические выбросы;
атмосферные процессы формирования и выпадения осадков;
двухфазные течения, используемые в технологических процессах и установках;
дисперсные среды для нужд пищевой и автомобильной промышленности, медицины и сельского хозяйства.
Это разнообразие физических проблем и технических приложений, а также целая совокупность необычных физических и химических свойств фактически позволяют отнести дисперсные системы к отдельному агрегатному состоянию вещества, которому внимание стало уделяться лишь в последнее время.
Очень важной причиной повышающегося интереса к аэрозолям является разнообразие и фундаментальный характер задач, которые возникают в физике дисперсных систем. Физическая кинетика, оптика, физика атмосферы, многофазная газодинамика, теория турбулентности - все эти разделы механики и физики необходимы для квалифицированного физика-аэрозолыцика и широко используются в классических работах Максвелла, Томсона, Айткена, Смолуховского, Эйнштейна, Колмогорова, Чандрасекара, Френкеля, Зельдовича и работах современных исследователей по физике дисперсных систем. Значительный прогресс в моделировании процессов формирования и динамики переноса аэрозольных примесей достигнут в последнее время, благодаря применению быстродействующих ЭВМ и использованию методологии численного эксперимента.
1.3 О дисперсных системах
Дисперсные системы - системы, представляющие собой механическую смесь частиц дисперсной фазы со средой-носителем. Такие системы являются широко распространенным объектом в природе и повседневной деятельности человека. Образование облаков и выпадение осадков, формирование аэрозольной компоненты земной атмосферы, эволюция допланетного роя и частиц межзвездной пыли, миграция дефектов в твердых телах, двухфазные течения в физических и промышленных установках, перенос в атмосфере различного рода промышленных и радиоактивных загрязнений - все это далеко не полный круг явлений, в которых решающую роль играют процессы, происходящие с дисперсными системами.
Обычно дисперсные системы подразделяют, исходя из агрегатного состояния частиц дисперсной фазы и среды-носителя. Ряд дисперсных систем получил отдельные названия:
аэрозоли (взвесь твердых или жидких частиц в газовой среде, обычно в воздухе);
эмульсии (жидкие частицы, обычно стабилизированные защитными оболочками, в жидкой среде)
коллоиды (взвесь твердых частиц в жидкой среде);
астрозоли (твердые или жидкие частицы в вакууме)
Кроме того, существуют дисперсные системы без устоявшихся названий: ансамбли газовых пузырьков в твердом теле или жидкости, ансамбли жидких капель в твердом теле и т. д.
Дисперсные системы обладают многими необычными физическими свойствами, которые требуют отдельного изучения и сказываются на практике. Так, отдельно взятая молекула вещества в газовом состоянии имеет одни свойства, в сплошном состоянии – другие свойства, а в состоянии аэрозоли (дисперсная фаза) уже совсем другие свойства, которые являются плавным переходом от газообразной к твёрдой фазе. Можно назвать своеобразную газодинамику, обусловленную различным движением среды-носителя и частиц дисперсной фазы; необычные оптические свойства, вызванные сравнимостью размеров частиц с длинами волн света и влиянием формы частиц; повышенную способность к взаимодействиям, вызванную чрезвычайно развитой поверхностью частиц. Особое место среди дисперсных систем занимают аэрозоли.
1.4 Атмосферные аэрозоли
Обычно классификация атмосферных аэрозолей проводится на основе их разделения по способам создания, материалам и характерным размерам частиц. При этом к аэрозолям обычно относят частицы со скоростями осаждения не больше, чем у капелек воды диаметром 100 мкм (крупные дождевые капли и осадки тем самым относят к отдельному классу).
Пыли состоят из твердых частиц, диспергированных в результате механического измельчения твердых тел (взрывы, горные работы и т. д.) или высыхания капелек с растворенными веществами или частицами (солевые частицы над океаном). В обыденном понятии пылью называют осадок твердых частиц на различных поверхностях, который легко переходит во взвешенное состояние. Материалы пыли самые различные, а размеры также колеблются в широких пределах - от субмикронных (0,01 мкм) до микроскопических (100 мкм).
Дымы образуются при горении или возгонке летучих веществ, а также в результате химических и фотохимических реакций. Размеры дымовых частиц - от субмикронных до 5 мкм.
Туманы состоят из капелек жидкости, образующихся при конденсации пара или распылении жидкости. Сюда также включаются капли с растворенными веществами или содержащимися в них частицами. Природные туманы обычно состоят из капелек с диаметром до 10 мкм и более.
Капельки, а также частицы различных атмосферных загрязнений и пыли иногда называют дымкой, которая, на самом деле представляет собой комбинацию из трех названных выше основных классов аэрозолей. Систему, образующуюся в результате взаимодействия природного тумана с газообразными загрязнениями, называют смогом. Размеры частиц дымки и смога обычно - 1 мкм.
Промышленные аэрозоли, образующиеся при получении и обработке горючих материалов, способны за счет развитой поверхности к более интенсивному воспламенению, чем исходные вещества. При скоплении мелкодисперсной пыли таких материалов в замкнутых помещениях и наличии источников воспламенения может произойти взрыв.
В целом использование технологических процессов и работа производств, связанных с выходом аэрозолей в рабочие помещения или атмосферу, требует тщательной оценки экологической опасности и применения различных средств очистки. Особая чистота внутри помещений требуется при работе с радиоактивными материалами и в микроэлектронике. Допустимое содержание аэрозолей регламентируется при этом соответствующими нормативными документами. Ряд средств очистки и принципы их работы описаны в изданиях (Спурный и др., 1964; Грин, Лейн, 1972; Петрянов-Соколов, Сутугин, 1989).
Частицы атмосферных аэрозолей играют важную роль в процессах конденсации водяного пара и тем самым в формировании осадков. В метеорологии их просто называют ядрами конденсации, независимо от физических и химических свойств, а классификацию проводят по характерным размерам:
частицы Айткена -
 r
< 0,1 мкм;
r
< 0,1 мкм;
большие частицы - r = 0,1 + 1 мкм;
гигантские частицы - r > 1 мкм.
Источники атмосферных аэрозолей принято делить на:
естественные (вулканические извержения, конденсация водяного пара в атмосфере, выветривание пород, разбрызгивание капелек воды над океаном, космическая пыль)
Для иллюстрации приведем некоторые цифры (Хргиан, 1986). За счет космической пыли на Землю поступает в год (1,4-2,0)·107 т вещества при общей массе атмосферы 5·1015 т. При пылевых бурях концентрация пыли в пустынных районах может достигать 300 мкг/м3, в Подмосковье до 30 мкг/м3 , в районах Урала свыше 5 мкг/м3. За счет разбрызгивания капелек воды при ветре со скоростью порядка 12 м/с над океаном образуется до 500 мкг/м3 солевых частиц - вполне ощутимые количества.
антропогенные - источники, обусловленные жизнедеятельностью человека (промышленные выбросы из дымовых труб, токсичные выбросы от автомобилей, пожары, взрывы, выветривание почвы в результате земледелия и открытой добычи ископаемых).
Это дает поступление (3-4)·108 т аэрозолей в атмосферу за год. Концентрация аэрозольного смога, обусловленная фотохимическими реакциями с выхлопными газами, в промышленных центрах достигает 200 мкг/м3 (Хргиан, 1986), что вполне сравнимо с последствиями пылевых бурь. Промышленные и аварийные выбросы вредных веществ в атмосферу представляют собой непосредственную опасность для окружающей среды и населения. Во-первых, процессы переноса примесей в атмосфере настолько динамичны, что последствия таких выбросов сказываются практически сразу. Во-вторых, при выбросах в атмосферу загрязняется приземный слой воздуха и подстилающая поверхность (почва, водоемы, растительность), что приводит к непосредственному воздействию на окружающую среду и представляет собой последующую угрозу поступления вредных веществ в организм человека и животных.
Мощные или регулярные выбросы в атмосферу могут иметь и глобальные последствия. Поступление в атмосферу окисей серы, азота и хлора приводит к образованию водяных капель, содержащих кислоту, и к выпадению кислотных осадков. Выбросы окисей углерода сказываются на теплообмене в нижних слоях атмосферы и способствуют глобальному потеплению климата. Проведенный в 40-60-х годах воздушные ядерные взрывы на десятилетия изменили баланс радиоактивных веществ в атмосфере и вызвали выпадения радиоактивных осадков (Юнге, 1965; Стыро, 1968; Грин, Лейн, 1972; Кароль, 1972). Широкое применение хлор-(бром)-содержащих фреонов, а также выброс соединений азота повлияли на состав аэрозолей в тропосфере и озонового слоя земной атмосферы (Петрянов-Соколов, Сутугин, 1989; Владимиров и др., 1991). Выбросы радиоактивных веществ в результате Кыштымской и Чернобыльской аварий надолго нарушили нормальную жизнедеятельность в районах этих аварий (Владимиров и др., 1991; Кабакчи, Путилов, 1995). Из этих примеров видно, что экологическая опасность различного рода газообразных и аэрозольных выбросов в атмосферу заключается не только в непосредственном влиянии вредных выбрасываемых веществ на здоровье человека, но и имеет глобальный аспект, связанный с долговременными процессами изменения химического и дисперсного состава загрязнений, переносом веществ в тропосфере и стратосфере, влиянием загрязнений на массовые балансы веществ и температурные режимы в атмосфере.
Однако не следует полагать, что аэрозоли наносят только вред и должны применяться лишь с известными мерами предосторожности. Они широко используются в технологических процессах пищевой промышленности, применяются в медицине, служат для борьбы с сельскохозяйственными вредителями, являются необходимым элементом в физических установках и промышленных процессах, используются для изготовления материалов со многими полезными свойствами [33]. Интересную историю имеет деятельность, связанная с применением аэрозолей для активного воздействия на облачные процессы (засев облаков) и борьбы с засухой. В основе этой идеи лежало желание использовать неустойчивость и огромные запасы энергии атмосферных облачных систем путем засева облаков искусственными ядрами конденсации. Однако после постоянного применения засева облаков в течение нескольких лет этот метод перестал приносить результаты и даже наблюдалась обратная картина с повышением длительности засушливых периодов.
1.5 Классификация и размеры аэрозолей.
По типу происхождения и по размерам аэрозоли обычно подразделяют на две большие группы: микро и макрочастицы [1]. Микрочастицы радиуса меньше 0,5-1,0 мкм образуются в процессах конденсации и коагуляции, тогда как макрочастицы возникают в основном при дезинтеграции поверхности Земли.
Возможно, также классифицировать частицы просто в зависимости от размера. Напомним, что размер средней по величине молекулы или атома составляет, колеблется в районе 0,1 нм. Концентрация частиц радиуса порядка 1 нм обычно измеряется при помощи расширительных камер (камеры Вильсона), первая конструкция которых была предложена Айткеном, поэтому частицы называются ядрами, или частицами Айткена. Они были измерены экспериментально, и, по мнению ряда авторов, представляют собой наименьшие, но размеру частицы, которые могут быть обнаружены с помощью таких камер. Частицы таких размеров в значительной степени подвержены броуновскому движению, что позволяет им достичь стенок любой камеры разумных размеров в течение нескольких секунд или, в крайнем случае, минут. Поэтому для них трудно отобрать представительную пробу, при консервации проб наблюдаются значительные потери. Частицы малых размеров очень быстро коагулируют с частицами больших размеров. При рассмотрении судьбы частиц следует иметь в виду, что частицы, достигшие стенок камеры, остаются на них вследствие действия сил адгезии. Это отличает поведение частиц от поведения молекул, однако классификация на такой основе не получила развития из-за малой изученности природы адгезионных взаимодействий.
Размер 10-6 см характеризует частицы более стабильные, для них коагуляция при атмосферных условиях протекает достаточно медленно, поэтому консервация проб возможна. Из экспериментальных методов для прямых наблюдений за такими частицами, обычно используют электронную микроскопию.
Частицы размером 10-5 см называют "большими" (в контексте атмосферных аэрозолей). На такие аэрозоли одинаково слабое воздействие оказывают как броуновское движение, так и гравитационное осаждение. Частицы таких размеров, по-видимому, характеризуются наибольшим временем жизни. Интересно отметить, что "большие" частицы трудно получить непосредственно как при измельчении твердого тела (обычно размеры частиц при самом тонком помоле больше), так и при конденсации из газовой фазы (где, за исключением случая наиболее летучих соединений, размер образующихся частиц меньше).
Размер 10-4 см (1 мкм) - это, на жаргоне специалистов по атмосферным аэрозолям, "хвост" фракции "гигантских" частиц в атмосфере. Скорость падения под действием силы тяжести частиц размером 1 мкм приблизительно равна 0,2 мм/с, но даже такое медленное осаждение за 1 сутки представляет собой уже 20м. Скорость оседания возрастает пропорционально квадрату радиуса частицы для частиц таких размеров. Такие частицы легко наблюдать на поверхности при небольшом увеличении, но точно измерить их трудно.
Размер 10-3 см (10 мкм) - это приблизительный размер ядер облака, которые представляют собой очень важную специальную подгруппу атмосферных аэрозолей. Скорость падения 10 мкм частицы плотности 2 г/см3 при нормальных условиях составляет величину 2 см/с, поэтому в течение нескольких минут в стандартной комнате большинство таких частиц осело бы на пол. Частицы таких размеров можно увидеть невооруженным глазом на контрастной поверхности, а их размеры могут быть определены обычным оптическим микроскопом.
Размер 10-2 см (100 мкм) - размер капель измороси (скорость оседания 1 м/с). Повседневный опыт показывает, что в хорошую погоду частицы таких размеров в атмосфере отсутствуют или очень редки, за исключением пыльных бурь и других подобных явлений антропогенных или природных. Частицы таких размеров характерны для морских аэрозолей, но быстро оседают и практически не наблюдаются далеко от источника образования.
Размер 10-1 см (1 мм) - типичный размер дождевых капель. В атмосфере в год образуется приблизительно 4·1022 дождевых капель, что составляет 104 капель на 1см2 поверхности Земли. В среднем дожде, однако, их объемная концентрация невелика - 10-5 см3 (или 10 капель на 1 кубический метр воздуха). В нижних слоях атмосферы средняя концентрация меньше на два порядка.
Размер 1 см. Падающие капли дождя из-за гидродинамических эффектов разбиваются до диаметра 0,5 см, и поэтому жидких аэрозолей такого размера не наблюдается. Однако, град и снежинки (твердые гидрометеориты) могут достичь таких размеров.
Размер 10 см. Имеются сообщения о граде такого размера. Легко оценить масштабы наносимого им вреда.
Размер > 10 см. Можно сказать, что 10 см - верхний предел размеров атмосферных частиц. Конечно, самолеты, метеориты и пепел при извержении вулканов могут достигать и больших размеров.
Итак, даже самая краткая классификация по размерам занимает область от 10-8 см до 10 см. Если исключить экстремальные случаи, то останется: область в шесть порядков - от 10-7 см до нескольких миллиметров. Если перейти к массовым или объемным характеристикам, то получится разброс в 20 порядков, а для такой характеристики, как концентрация, ситуация еще более впечатляющая. Крайне важно понять, что область от 1 мкм до размера молекулы так же велика, как от 1 мкм до градины больших размеров. Поэтому такие макрохарактеристики, как "концентрация частиц аэрозоля" или "средний размер частиц аэрозоля" должны быть определены очень осторожно.
Основная характеристика частиц дисперсной фазы – функция распределения частиц по размерам.
Отдельные частицы характеризуются так называемыми морфологическими признаками: размер, плотность, форма, структура, химический состав. По форме различают три вида частиц:
• изометрические (с приблизительно одинаковыми размерами в трех направлениях),
• пластинки (с одним размером, гораздо меньшим, чем два других),
• волокна или цепочки (протяженные в одном направлении).
Форму пластинок обычно имеют частицы пыли, цепочечные агрегаты часто образуются при горении. Твердые аэрозольные частицы в основном имеют неправильную форму, и им приписывается некий средний размер, например, по объему или по проекционной площади.
Очень полезным является понятие эквивалентного аэродинамического диаметра, за который принимается диаметр сферической частицы плотностью 1г/см3, имеющей такую же скорость осаждения, как и данная частица. Это означает, что частицы различной плотности и формы имеют один и тот же аэродинамический диаметр, если их скорости осаждения равны. Применение этой величины удобно для расчетов выпадения частиц в поле тяжести, например, применительно к переносу аэрозолей в атмосфере.
Химический состав частиц может быть самым разнообразным и определяется как исходными материалами, так и способами создания этих частиц. В некоторых случаях приходится иметь дело с композитными частицами, составленными из нескольких химических веществ. Например, кислотные осадки состоят из раствора кислоты в воде; радиоактивные частицы, образующиеся при авариях с диспергированием ядерных материалов, включают в себя не только радиоактивные вещества, но и материалы теплоносителя или грунт и т. д.
В действительности, сферическую форму имеют жидкие частицы и субмикрочастицы, наблюдаемые с помощью электронной микроскопии. Как правило, твёрдые частицы имеют отличную от сферической форму. На уровне молекулярных образований сферические молекулярные кластеры тоже встречаются довольно редко. Несмотря на это, теоретические построения трактуют аэрозоли как сферические образования и часто характеризуют их радиусом или диаметром, о котором было сказано выше.
Аэрозольные частицы, наблюдаемые под микроскопом, также различают по цвету, структуре, степени однородности, растворимости в воде и сорбционным характеристикам.
Если поставить перед исследователем задачу описать каждую аэрозольную частицу, содержащуюся в 1 см3 городского воздуха, то на это потребуется целая жизнь. Работа такого типа лишена смысла еще и потому, что система является неравновесной и подвергается изменениям в результате испарения и конденсации, коагуляции, адсорбции и десорбции, а также химических процессов в массе и на поверхности. Следовательно, необходимо снизить наши требования к классификации и попытаться значительно упростить ее, группируя частицы по единственному параметру - размеру.
Сущность понятия "размер" в отношении аэрозолей весьма расплывчата. В одних случаях можно определить массу или объем частицы и из них рассчитать радиус эквивалентной сферы. В других случаях фундаментальной характеристикой, определяющей распределение частиц по размеру, является измеряемый коэффициент диффузии. Тогда частицу описывают как сферу, характеризующуюся этим коэффициентом диффузии. Дополнительные трудности возникают и вследствие того, что частицы радиусом от 10-7 до 10-4 см различаются по массе на девять порядков. Если взять весь диапазон частиц, описываемых как аэрозоли, то есть включить в рассмотрение туман, дождь и снег, то различия в массах могут достичь 24 порядков для частиц радиусом от 10-7 до 1 см. Приходится сводить воедино результаты, полученные различными методами. При этом измеряемая одними методами масса и, например, измеряемая другими методами подвижность не связаны между собой взаимно однозначными соотношением (электрическая подвижность не зависит от плотности). Тем не менее, плотности веществ, входящих обычно в состав аэрозолей, различаются между собой не очень сильно (приблизительно от 0,7 до 4 г/см3). Таким образом, искусственный прием сведения результатов всех этих измерений к радиусу частицы является вполне разумным.
Итак, в дальнейшем мы постараемся описать аэрозоли с точки зрения того, сколько частиц обладает радиусом (в широком толковании этого термина), попадающим в заданный нами интервал. Остается тем не менее, еще ряд возможностей даже при таком ограниченном выборе описания. Наиболее очевидно использовать функцию распределения по радиусам v(r), которая предполагает, что v(r)∆r - частиц имеет радиус в интервале (r, r + ∆r). Функция v(r) проста для понимания, но имеет ряд принципиальных недостатков. Покажем это на примере. Пусть в пробе воздуха объемом 1 см3 содержится 5·103 частиц радиуса r<10-6 см, 5·103 частиц в диапазоне радиусов (10-6 – 10-5) см и одна частица с r>0,1 мкм. Попытка графического распределения на листе с линейной шкалой 20 см, соответствующей максимальному радиусу 5 мкм, приведет к тому, что на первом миллиметре абсциссы появится большая малоинформативная клякса. Поэтому вводятся полулогарифмические координаты log(r) = x и соответствующая им функция распределения n(x) = n(log(r)), которая предполагает, что n(log(r))∆log(r) частиц имеют логарифмический радиус в интервале (log(r), log(r) + ∆log(r)). В дальнейшем будем использовать натуральные логарифмы, хотя это непринципиальный момент.
Ясная и «естественная» функция распределения v(r), отнесенная к
единичному объему, может быть легко найдена из соотношений:
n(x) · ∆x = v(r) · ∆r, (1.1)
∆x = ∆ln(r) = r-1 · ∆r. (1.2)
Отсюда следует, что
n(x) = r · v(r), (1.3)
v(r) = e-x · n(x). (1.4)
В теоретических работах по конденсации очень удобно использовать объем, а не ln(r) в качестве измеряемого параметра, но в практических целях в качестве шкалы для измерения масштаба это крайне неудобно.
Совершенно по-другому можно использовать объем, введя объемное распределение V(x), которое показывает, что в единичном объеме воздуха частный объем V(x) ∆x представлен частицами с радиусами в диапазоне (x, x +∆x).
Между численными значениями n(x) и v(r) разница значительна, поэтому графическое представление результатов или их табличное оформление представляет значительные сложности. Гораздо легче интерпретировать интегральные распределения, несмотря на то, что в зависимости от их определения они могут убывать или возрастать, оставаясь монотонными (то есть необходимо всегда четко представлять себе, как определено данное распределение).
Интегральное распределение характеризует общее число частиц в единичном объеме воздуха, размер которых больше или меньше заданной величины. Последнее алгебраически несколько легче и симбатно изменению размера.
Введя для интегрального распределения обозначение N(r),получим:
 , (1.5)
, (1.5)
 . (1.6)
. (1.6)
Для заданного граничного размера N(r) и N(x) численно равны, поэтому их можно обозначить просто N . Однако для обработки экспериментальных данных более информативным является распределение вида:
 , (1.7)
, (1.7)
 , (1.8)
, (1.8)
характеризующее общее число частиц с размерами, более заданной величины. Обусловлено это следующими причинами:
в природе встречается значительно больше мелких частиц, чем крупных, поэтому если проводить интегрирование, то на верхней границе будут очень малые изменения, особенно в логарифмических координатах;
строго говоря, соответствующий
(1.5) интеграл должен быть записан как
 ,
и тогда определение того, какую величину
считать r>min>
для аэрозолей, влияет на величину
интеграла. Между тем, как уже упоминалось
ранее, среди исследователей не существует
единого мнения по поводу r>min>.
,
и тогда определение того, какую величину
считать r>min>
для аэрозолей, влияет на величину
интеграла. Между тем, как уже упоминалось
ранее, среди исследователей не существует
единого мнения по поводу r>min>.
Аналогично (1.7) можно определить
и интегральные объемные распределения
как
 или
или
 ,
причем интегрирование проводится от r
до ∞, либо от
r>min>
до r
в зависимости от того, какое из определений
(больше, чем или меньше, чем) принято.
Рассмотрим теперь наиболее часто
используемые в работах по атмосферным
аэрозолям типы распределений.
,
причем интегрирование проводится от r
до ∞, либо от
r>min>
до r
в зависимости от того, какое из определений
(больше, чем или меньше, чем) принято.
Рассмотрим теперь наиболее часто
используемые в работах по атмосферным
аэрозолям типы распределений.
1.6.1 Обратно-степенное распределение.
Экспериментальные наблюдения за атмосферными аэрозолями позволили сформулировать ряд эмпирических закономерностей, описывающих их распределение.
В работах Юнга (Junge), выполненных в конце 40-х - начале 50-х годов, было показано, что для атмосферных аэрозолей размером от десятых долей микрометра до нескольких десятков микрометров величина ∆V/∆ln(r) остается постоянной. Это значит, что общий объем ∆V, занимаемый частицами, с радиусами от 0,4 до 0,6мкм или от 0,6 до 0,9 мкм, от 1 до 1,5 мкм или от 4 до б мкм, примерно одинаков. Поскольку физический объем частицы радиусом 4-6 мкм в 103 раз больше объема частицы с радиусом 0,4-0,6мкм, постоянство ∆V/∆ln(r) требует, чтобы концентрация частиц большего радиуса была в 103 раз меньше. Хотя встречается большое число отклонений от данного правила, тем не менее, общепринято в настоящее время, что для природных аэрозолей, образовавшихся в основном в результате дезинтеграции земной поверхности, справедлива формула:
 (1.9)
(1.9)
Парциальный объем частиц, приходящихся на единичный интервал радиусов, пропорционален, таким образом, r-4. Более поздние исследования показали, что показатель степени при r может быть в общем случае как больше 3, так и меньше 3. Любое распределение, которое может быть линеаризовано в логарифмических координатах, описывается таким обратным степенным распределением:
 ,
(1.10)
,
(1.10)
либо
 ,
(1.11)
,
(1.11)
где B = const. Распределения такого типа используют весьма широко, но ими также часто злоупотребляют. Поэтому обсудим некоторые их достоинства и недостатки.
• Общее число частиц.
Для его определения необходимо вычислить
 ,
который расходится при любых a.
Если задать нижний предел как r>min>
(трудности такого шага были обсуждены
выше), то получим:
,
который расходится при любых a.
Если задать нижний предел как r>min>
(трудности такого шага были обсуждены
выше), то получим:
 (1.12)
(1.12)
Таким образом, общая концентрация определяется величиной r>min>. Для a = 3 рассчитанное общее число частиц возрастает в 8 раз при двукратном уменьшении r>min>.
• Средний радиус. Интеграл в этом случае также расходится, поэтому необходимо ввести r>min> . Тогда получим:
 (1.13)
(1.13)
Если a = 3, то средний радиус близок к r>min>. Если a = 1, то интеграл расходится и средний радиус неопределим.
• Общий объем частиц. Общий объем частиц задается величиной
 (1.14)
(1.14)
которая не определена при a = 3. Хотелось бы отметить, что именно a = 3 было предсказано на основании постоянства ∆V/∆ln(r). Если взять интеграл от r>min> до r>m>>ax> , то общий объем частиц составит:
 . (1.15)
. (1.15)
Если a > 3, то получим:
 . (1.16)
. (1.16)
А если a < 3, то:
 . (1.17)
. (1.17)
Если r>min> много меньше r>max>,тогда из уравнения (16) следует, что объем
пропорционален
 и весьма слабо зависит от r>min>.
Если a
< 3, то общий объем в основном определяется
r>min>.
Следовательно, если состав систематически
меняется с изменением размера, то в
зависимости от тангенса угла наклона
a
средний состав аэрозоля будет меняться
очень сильно.
и весьма слабо зависит от r>min>.
Если a
< 3, то общий объем в основном определяется
r>min>.
Следовательно, если состав систематически
меняется с изменением размера, то в
зависимости от тангенса угла наклона
a
средний состав аэрозоля будет меняться
очень сильно.
• Общая площадь. В некоторых случаях эта характеристика очень важна. В зависимости от того, a < 2 или a > 2, доминируют большие или меньшие частицы. Коэффициент оптической экстинкции в грубом приближении пропорционален площади поверхности частицы вплоть до r>min >≈ 0.5λ, где λ - длина волны. Состав частиц (из оптических измерений) будет определяться концом интервала радиусов для a ≈ 3 (то есть оптическое поведение системы будет определяться размером в десятые доли мкм). Если a < 2, то происходит сдвиг в сторону больших частиц.
1.6.2 Гамма-распределение.
Закон распределения имеет вид:
 , (1.18)
, (1.18)
он обеспечивает экстремум функции распределения при r>extr> = b-1 и убывание функции - медленное при уменьшении радиуса и экспоненциально быстрое при r > r>extr>. Однако теоретическое исследования в области сухих аэрозолей и экспериментальные данные подтверждают, что при r < r>extr> функция распределения также убывает по экспоненте. Лучшее приближение к экспериментальным данным можно получить, если в качестве аргумента взять обратный радиус или какую-либо другую отрицательную степень.
Такие распределения, известные как гамма - распределения, удобны для машинных расчетов, однако представляют всего лишь удобную аппроксимацию экспериментальных данных и не имеют под собой никакой теоретической основы.
Можно легко получить выражение для определения первого момента гамма - распределения. Если принять, что
 , (1.19)
, (1.19)
то легко взять интеграл вида
 , (1.20)
, (1.20)
где Г - соответствующее значение γ-функции:
 (1.21)
(1.21)
в точке
 .
Это очень удобное свойство позволяет
выбирать функцию
.
Это очень удобное свойство позволяет
выбирать функцию
 таким образом, чтобы удовлетворить
экспериментально найденным среднему
значению, моде, ширине и кривизне, или
любым трем моментам, выбрав соответствующим
образом b, β и
λ.
таким образом, чтобы удовлетворить
экспериментально найденным среднему
значению, моде, ширине и кривизне, или
любым трем моментам, выбрав соответствующим
образом b, β и
λ.
1.6.3 Логарифмически-нормальное распределение.
Гауссово (нормальное) распределение симметрично относительно своего среднего значения (которое одновременно является модой и медианой) и принимает ненулевые значения, когда модуль аргумента стремится к бесконечности. Нормальная кривая, в которой аргументом является радиус, по вышеупомянутой, а также по ряду других причин плохо аппроксимирует распределения по размерам, наблюдаемые в природных и искусственных аэрозолях. Здесь и заложена логическая причина, по которой используют логарифмический аргумент. Другая причина может быть сформулирована следующим образом. Пусть мы решаем задачу синтеза искусственного аэрозоля, состав которого задан средним размером частиц. Из изложенного в предыдущих разделах следует, что при среднем размере частиц в 1 мкм невозможно ожидать равномерного образования частиц с радиусом 0,1 мкм и 1,9 мкм. Несомненно, в большей степени одинакова вероятность найти частицы с радиусом ar и a1r. Таким образом, нормальное логарифмическое распределение - это просто нормальная кривая, аргументом которой является ln(r). Нормальное распределение по аргументу x, которое задается формулой:
 , (1.22)
, (1.22)
где N>0>
- общее число частиц; σ
- стандартное отклонение, может быть
записано в единицах r.
Заметим, что σ,
будучи средним ln(x),
в единицах радиуса соответствует
отношению r.
Так σ = 0, 3
означает, что точки с
 располагаются на расстоянии
располагаются на расстоянии
 и
и
 ,
где
,
где
 ,
и, таким образом,
,
и, таким образом,
 представляет собой среднее геометрическое
радиуса. Если использовать радиус в
качестве аргумента, то нормальное
логарифмическое распределение будет
иметь вид:
представляет собой среднее геометрическое
радиуса. Если использовать радиус в
качестве аргумента, то нормальное
логарифмическое распределение будет
иметь вид:
 (1.23)
(1.23)
Природные аэрозоли в большинстве случаев не характеризуются симметрией, присущей нормальному логарифмическому распределению. Искусственные системы хорошо им описываются, поскольку при получении искусственных аэрозолей обычно преследуется одна цель - получить частицы определенного среднего размера в рамках узкой фракции.
Еще раз подчеркнем, что распределения Юнга основано на экспериментальных данных о природных аэрозолях. Математические операции с такими распределениями чаще всего возможны только с определенным приближением, а решения уравнений являются численными. Математически строгие обратно-степенное, гамма, и логарифмическое нормальное распределения удобны с точки зрения математической обработки, но, за исключением этого смысла, их использование не обосновано ни экспериментально, ни теоретически. Распределение Юнга, особенно в случае, если a - переменная величина и нижняя граница r>min> минимальна, обеспечивает достаточно гибкое представление с хорошими коэффициентами корреляции.
Состояние проблемы и постановка задачи.
2.1 Газокинетические процессы в дисперсной системе
2.1.1 Непрерывная и дискретная динамика.
Исследование динамики аэрозолей в среде (в том числе в воздухе), необходимо определить, с точки зрения процессов переноса. В свободно - молекулярном режиме молекулы среды перемещаются по прямой, пока не столкнутся с другой молекулой, после чего, молекула изменяет направление, до того момента, пока вновь не столкнётся с другой молекулой, и так далее. Среднее расстояние, пройденное молекулой между столкновениями с другими молекулами, называется длиной свободного го пробега. В зависимости от относительного размера частицы, находящейся в среде и средней длины свободного пробега, отличают два случая.
Если размер частицы намного больше, чем средняя длина свободного пробега окружающих молекул, система ведет себя, как непрерывная среда. Движение такой частицы подчиняется законам диффузии.
В другом случае, если частица намного меньше, чем средняя длина свободного пробега окружающих молекул, то она (частица) ведёт себя как большая молекула. В этом случае говорят о свободно - молекулярный режим.
Ключевой в нашем случае, безразмерный параметр, который определяет характерные свойства среды относительно частицы, - число Кнудсена.
 (2.1)
(2.1)
где λ- длина свободного пробега, D – диаметр частицы, а R, соответственно, её радиус. Таким образом, число Кнудсена - отношение двух метрических параметров.
Прежде, чем обсуждать роль числа
Кнудсена, мы должны рассмотреть вычисление
средней длины свободного пробега для
пара. Так же необходимо вычислить среднюю
длину свободного пробега для чистого
газа и для газов, составленных из смесей
нескольких компонентов. Заметим, что
воздух, в основном, состоит из смеси
кислорода с азотом, однако общепринято
говорить о средней длине свободного
пробега воздуха,
 ,
как будто воздух - отдельная химическая
разновидность.
,
как будто воздух - отдельная химическая
разновидность.
Начнём с самого простого случая,
когда частица, находится в чистом газе
B.
Если нас интересует природа газа –
носителя, то мы должны рассчитать средний
путь свободного пробега, который
появляется при определении числа
Кнудсена, -
 .
Индекс обозначает, что мы интересуемся
столкновениями молекул B друг с другом.
Длина свободного пробега была определена,
как среднее расстояние, которое проходит
молекула B между столкновениям с другой
молекулой B. Средняя скорость газовых
молекул B, -
.
Индекс обозначает, что мы интересуемся
столкновениями молекул B друг с другом.
Длина свободного пробега была определена,
как среднее расстояние, которое проходит
молекула B между столкновениям с другой
молекулой B. Средняя скорость газовых
молекул B, -
 (Moore,
1962):
(Moore,
1962):
 , (2.2)
, (2.2)
где M>B> - молекулярный вес молекулы B. Отметим, что большие молекулы перемещаются более медленно, в то время как средняя скорость газа увеличивается с температурой. Средняя скорость молекулы азота при температуре 298К, согласно (8.2) равна 474 м/c, а кислорода – 444 м/c.
Давайте оценим то, что случается с молекулой B в течение единицы времени, скажем, секунды. В течение этой секунды молекула перемещается, в среднем, на расстояние, равное этому промежутку времени (секунда), умноженному на скорость молекулы. Если в течение той секунды молекула подвергается некоторому числу столкновений – Z>bb>, то ее средняя длина свободного пробега будет равна, по определению,
 (2.3)
(2.3)
Таким образом, чтобы вычислить
среднюю длину свободного пробега
молекулы, мы должны сначала вычислить
число столкновений Z>bb>.
Пускай,
 - диаметром молекулы B. За 1 секунду
молекула перемещается на дистанцию
- диаметром молекулы B. За 1 секунду
молекула перемещается на дистанцию
 и сталкивается со всеми молекулами,
центры которых находятся в цилиндре
радиуса
и сталкивается со всеми молекулами,
центры которых находятся в цилиндре
радиуса
 и высоты
и высоты
 .
Отметим, что две молекулы диаметра
.
Отметим, что две молекулы диаметра
 сталкиваются тогда и только тогда, когда
расстояние между их центрами
сталкиваются тогда и только тогда, когда
расстояние между их центрами
 .
Если
.
Если
 - число молекул B в единице объёма, то
число молекул в вышеупомянутом цилиндре
-
- число молекул B в единице объёма, то
число молекул в вышеупомянутом цилиндре
-
 .
Итак, мы вычислили число столкновений,
предполагающих, что одна молекула B
перемещается, в то время как остальные
молекулы неподвижны, в результате чего
недооценили частоту столкновений.
Вообще, все частицы перемещаются в
случайных направления, и мы должны
описать это движение, оценивая их
относительную скорость. Если две частицы
перемещаются в противоположных
направлениях, их относительная скорость
- 2
.
Итак, мы вычислили число столкновений,
предполагающих, что одна молекула B
перемещается, в то время как остальные
молекулы неподвижны, в результате чего
недооценили частоту столкновений.
Вообще, все частицы перемещаются в
случайных направления, и мы должны
описать это движение, оценивая их
относительную скорость. Если две частицы
перемещаются в противоположных
направлениях, их относительная скорость
- 2 .
Если они двигаются в одном направлении,
их относительная скорость - ноль, в то
время как при движении под углом в 90°
их относительная скорость -
.
Если они двигаются в одном направлении,
их относительная скорость - ноль, в то
время как при движении под углом в 90°
их относительная скорость -
 .
Можно доказать, что последняя ситуация
определяет среднее число, таким образом:
.
Можно доказать, что последняя ситуация
определяет среднее число, таким образом:
 (2.4)
(2.4)
и средняя длина свободного пробега:
 (2.5)
(2.5)
Видно, что чем больше размер
молекулы,
 ,
и выше газовая концентрация, тем меньшее
значение принимает средняя длина
свободного пробега.
,
и выше газовая концентрация, тем меньшее
значение принимает средняя длина
свободного пробега.
К сожалению, даже притом, что
(2.5) обеспечивает достаточно неплохую
зависимость длины свободного пробега
от газовой концентрации и размера
молекулы, она не удобна для использования,
потому что необходимо знать диаметр
молекулы
 ,
так же, большинство молекул вовсе не
являются сферическими. Окончательно
всё усугубляет то, что средняя длина
свободного пробега газа не может быть
измерена непосредственно. Однако, она
может быть теоретически связана с
измеримыми газовыми макроскопическими
свойствами, типа вязкости, коэффициента
теплопроводности, или молекулярного
коэффициента диффузии. Таким образом,
можно использовать вышеупомянутые
газовые свойства, чтобы оценить
теоретически среднюю длину свободного
пробега в газе. Например, длина свободного
пробега чистого газа может быть связана
с газовой вязкостью, соотношением, что
следует из кинетической теории газов:
,
так же, большинство молекул вовсе не
являются сферическими. Окончательно
всё усугубляет то, что средняя длина
свободного пробега газа не может быть
измерена непосредственно. Однако, она
может быть теоретически связана с
измеримыми газовыми макроскопическими
свойствами, типа вязкости, коэффициента
теплопроводности, или молекулярного
коэффициента диффузии. Таким образом,
можно использовать вышеупомянутые
газовые свойства, чтобы оценить
теоретически среднюю длину свободного
пробега в газе. Например, длина свободного
пробега чистого газа может быть связана
с газовой вязкостью, соотношением, что
следует из кинетической теории газов:
 (2.6)
(2.6)
где
 -
газовая вязкость, p
- газовое давление, и M>B>
- молекулярный вес B.
-
газовая вязкость, p
- газовое давление, и M>B>
- молекулярный вес B.
Таким образом, для стандартных
атмосферных условий, если диаметр
частицы является большим, чем приблизительно
0.2 ,
Kn < 1, и с точки зрения атмосферных
свойств, частица находится в непрерывном
режиме. В этом случае применимы уравнения
механики сплошной среды. Когда диаметр
частицы является меньшим, чем 0.01
,
Kn < 1, и с точки зрения атмосферных
свойств, частица находится в непрерывном
режиме. В этом случае применимы уравнения
механики сплошной среды. Когда диаметр
частицы является меньшим, чем 0.01 ,
частица существует в более или менее
разреженной среде, и ее свойства переноса
должны быть получены из кинетической
теории газов. Этот режим, когда Kn >>
1 называют свободно молекулярным режимом.
Промежуточное звено, когда размер
частицы заключён между этими двумя
значениями (0.01
,
частица существует в более или менее
разреженной среде, и ее свойства переноса
должны быть получены из кинетической
теории газов. Этот режим, когда Kn >>
1 называют свободно молекулярным режимом.
Промежуточное звено, когда размер
частицы заключён между этими двумя
значениями (0.01
 и 0.2
и 0.2 )
называют переходным режимом.
)
называют переходным режимом.
Теперь перейдём к рассмотрению
более интересного случая – определению
длины свободного пробега газа в бинарной
смеси. Если мы интересуемся диффузией
молекулы пара к частице, которые
содержатся в фоновом газе B (например,
в воздухе), тогда описание диффузионного
процесса, зависит от значения числа
Кнудсена, определение которого основано
на среднем длине свободного пробега
 .
Отметим, что, если концентрация молекул
A –
на несколько порядков ниже чем концентрация
молекул фонового газа B (воздух),
столкновениями между молекулами А можно
пренебречь. Столкновения между молекулами
А и B фактически равны общему количеству
столкновений. Число Кнудсена определяют
так:
.
Отметим, что, если концентрация молекул
A –
на несколько порядков ниже чем концентрация
молекул фонового газа B (воздух),
столкновениями между молекулами А можно
пренебречь. Столкновения между молекулами
А и B фактически равны общему количеству
столкновений. Число Кнудсена определяют
так:
 (2.7)
(2.7)
теперь мы должны оценить .
Джинс (Jeans)
показал, что средняя длина свободного
пробега молекул A,
.
Джинс (Jeans)
показал, что средняя длина свободного
пробега молекул A,
 ,
в бинарной смеси A и B - (Davis,
1983)
,
в бинарной смеси A и B - (Davis,
1983)
 (2.8)
(2.8)
где
 и
и
 - молекулярные концентрации частиц A и
B,
- молекулярные концентрации частиц A и
B,
 и
и
 - ударные диаметры для бинарных
столкновений между молекулами A и
молекулами A и B, соответственно, где
- ударные диаметры для бинарных
столкновений между молекулами A и
молекулами A и B, соответственно, где
 (2.9)
(2.9)
и
 - отношение молекулярных масс A и B. Первый
член в знаменателе (8.9) отвечает за
столкновения между молекулами А, в то
время как второй - за столкновения между
молекулами A и молекулами B. Если
концентрация молекул A очень низка (в
действительности, в атмосферных
приложениях, так и есть),
- отношение молекулярных масс A и B. Первый
член в знаменателе (8.9) отвечает за
столкновения между молекулами А, в то
время как второй - за столкновения между
молекулами A и молекулами B. Если
концентрация молекул A очень низка (в
действительности, в атмосферных
приложениях, так и есть),
 и (8.9) может быть упрощена, фактическим
пренебрежением столкновениями между
молекулами А:
и (8.9) может быть упрощена, фактическим
пренебрежением столкновениями между
молекулами А:
 (2.10)
(2.10)
Отметим, что молекулярная
концентрация
 может легко быть вычислена из уравнения
Клайперона
может легко быть вычислена из уравнения
Клайперона
 ,
где p - давление системы. Средний{скупой}
путь свободного пробега газа проекции
прямой на заднем плане газ не зависит
от концентрации непосредственно. Это
не удивительно, поскольку мы предположили,
что концентрация A настолько низка, что
молекулы никогда не сталкиваются и не
взаимодействуют друг с другом. Далее
мы сосредотачиваемся на взаимодействиях
частиц с единственным газом - воздухом,
где средняя длина свободного пробега
задана формулой (2.6).
,
где p - давление системы. Средний{скупой}
путь свободного пробега газа проекции
прямой на заднем плане газ не зависит
от концентрации непосредственно. Это
не удивительно, поскольку мы предположили,
что концентрация A настолько низка, что
молекулы никогда не сталкиваются и не
взаимодействуют друг с другом. Далее
мы сосредотачиваемся на взаимодействиях
частиц с единственным газом - воздухом,
где средняя длина свободного пробега
задана формулой (2.6).
2.1.2 Непрерывный режим.
Неустановившаяся диффузия
молекул вида A к поверхности частицы
радиуса
 :
:
 (2.11)
(2.11)
где c(r,t)
– концентрация молекул А, а
 -
молярный поток (количество молей падающих
на единицу площади в единицу времени)
в любом радиальном положении r.
Это уравнение - просто выражение массового
баланса в бесконечно малой сферической
ячейке, вокруг частицы. Молярный поток
молекул A дается согласно закону Фика
(Бирд и др., 1960),
-
молярный поток (количество молей падающих
на единицу площади в единицу времени)
в любом радиальном положении r.
Это уравнение - просто выражение массового
баланса в бесконечно малой сферической
ячейке, вокруг частицы. Молярный поток
молекул A дается согласно закону Фика
(Бирд и др., 1960),
 (2.12)
(2.12)
где
 - молекулярная фракция частиц A,
- молекулярная фракция частиц A,
 - радиальный поток воздуха в положении
r, и
- радиальный поток воздуха в положении
r, и
 - коэффициент диффузии молекул А в
воздухе. Так как выделенных направлений
нет,
- коэффициент диффузии молекул А в
воздухе. Так как выделенных направлений
нет,
 во всех r.
Принимая во внимание предположение,
применимое в большинстве атмосферных
состояний -
во всех r.
Принимая во внимание предположение,
применимое в большинстве атмосферных
состояний -
 ,
, (2.12) может быть переписана как
(2.12) может быть переписана как
 (2.13)
(2.13)
Теперь, комбинируя (2.11) и (2.13), получим:

 (2.14)
(2.14)
Если
 - концентрация молекул А вдали от частицы,
а
- концентрация молекул А вдали от частицы,
а
 -
концентрация паровой фазы на поверхности
частицы, и частица первоначально
находится в атмосфере частиц А с
концентрацией, равной
-
концентрация паровой фазы на поверхности
частицы, и частица первоначально
находится в атмосфере частиц А с
концентрацией, равной
 ,
начальные, и граничные условия для
(11.4) записываются так:
,
начальные, и граничные условия для
(11.4) записываются так:
 (2.15)
(2.15)
 (2.16)
(2.16)
 (2.17)
(2.17)
решение (2.14) в граничных условиях (2.5) - (2.17), будет выглядеть так:
 (2.18)
(2.18)
Временная зависимость концентрации в любом радиальном положении r дается третьим членом на правой стороне (2.18). Отметим, что для больших значений t, значение верхнего предела интегрирования приближается к нулю и профиль концентрации приближается к установившемуся состоянию, задаваемому
 (2.19)
(2.19)
Полный поток молекул А (молей в секунду) к частице обозначен Jc, индекс c показывает, что режим непрерывный (continuum), и задаётся, как:
 (2.20)
(2.20)
или, используя (2.19) и (2.13), как
 (2.21)
(2.21)
Если
 ,
поток молекул A - к частице, а если
,
поток молекул A - к частице, а если
 - наоборот. Вышеупомянутый результат
был впервые получен Максвеллом (1877), и
(11.11) часто называется потоком
Максвела.
- наоборот. Вышеупомянутый результат
был впервые получен Максвеллом (1877), и
(11.11) часто называется потоком
Максвела.
Массовый баланс на растущей или испаряющейся частице:
 (2.22)
(2.22)
где
 - плотность частицы и
- плотность частицы и
 молекулярный вес A. Объединяя (2.21) с
(2.22) получим,
молекулярный вес A. Объединяя (2.21) с
(2.22) получим,
 (2.23)
(2.23)
Когда
 и
и
 постоянны, (2.23) можно проинтегрировать,
что даст:
постоянны, (2.23) можно проинтегрировать,
что даст:
 (2.24)
(2.24)
Использование независимого от времени установившегося профиля, заданного (2.19), для вычисления размера частицы во времени (11.24) может казаться противоречивым. Использование установившегося диффузионного потока, для вычисления темпа роста частицы подразумевает, что профиль концентрации пара около частицы достигает установившейся величины прежде, чем произойдёт заметное изменение величины молекулы. Так как рост действительно происходит в сотни раз медленнее чем диффузия, профиль около частицы фактически всегда остается в ее стационарном значении.
2.1.3 Свободно - молекулярный (кинетический) режим.
В трёхмерном случае число
столкновений молекул с единицей
поверхности в единицу времени равно
 (Moore,
1962)
(Moore,
1962)
 , (2.25)
, (2.25)
где
 -
скорость молекул:
-
скорость молекул:
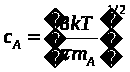 . (2.26)
. (2.26)
Учитывая это, молярный поток
 (молей в единицу времени) на частицу
радиусом
(молей в единицу времени) на частицу
радиусом
 :
:
 (2.27)
(2.27)
где
 - вероятность прилипания. Отношение
молекулярного потока в кинетическом
режиме к потоку в непрерывном режиме,
равно:
- вероятность прилипания. Отношение
молекулярного потока в кинетическом
режиме к потоку в непрерывном режиме,
равно:
 (2.28)
(2.28)
2.1.4 Переходный режим.
Установившийся поток молекул
пара к сфере, когда частица является
достаточно большой по сравнению со
средней длинной свободного пробега
молекул пара, задаётся уравнением
Максвелла (2.20). Так как это уравнение
основано на решении уравнения переноса
в непрерывном режиме, оно перестаёт
действовать, когда средняя длина
свободного пробега молекул пара
становится сопоставимым диаметру
частицы. В другом случае, выражение,
основанное на кинетической теории газов
(2.27) также не справедливо в этом случае,
где
 .
Когда
.
Когда
 ,
явления, как говорят, лежат в переходном
режиме.
,
явления, как говорят, лежат в переходном
режиме.
Распределение концентрации
диффузионных молекул и фонового газа
в переходном режиме строго описывается
уравнением Больцмана. К сожалению, не
существует общего решения уравнения
Больцмана, справедливого для всего
диапазона чисел Кнудсена. Как следствие,
большинство исследований явлений
переноса избегает решать непосредственно
уравнение Больцмана и ограничивают
себя подходом, основанным на так
называемом методе
подгонки потоков. Подгонка потоков
предполагает, что кинетические эффекты
ограничены областью
 ,
а вне этой области имеет место непрерывный
режим.
,
а вне этой области имеет место непрерывный
режим.
Расстояние
 имеет порядок средней длины свободного
пробега
имеет порядок средней длины свободного
пробега
 .
Предполагают, что в пределах этой
внутренней области применима простая
кинетическая теория газов.
.
Предполагают, что в пределах этой
внутренней области применима простая
кинетическая теория газов.
• Теория Фукса
Соответствие непрерывных и
свободномолекулярных потоков молекулы
относится ко времени Николая Альбертовича
Фукса, который предложил, что подгонкой
двух потоков в
 ,
можно получить граничное условие к
уравнению диффузии. Предположим,
коэффициент прилипания равен единице,
,
можно получить граничное условие к
уравнению диффузии. Предположим,
коэффициент прилипания равен единице,
 (2.29)
(2.29)
Тогда решая стационарное уравнение переноса для разбавленной системы,
 (2.30)
(2.30)
используя как граничные условия
(11.27) и
 ,
получаем решение:
,
получаем решение:
 (2.31)
(2.31)
где поправочный коэффициент
 :
:
 (2.32)
(2.32)
Связав бинарную диффузию и
среднюю длину свободного пробега,
используя
 ,
и
,
и
 ,
получим:
,
получим:
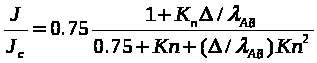 (2.33)
(2.33)
Заметим, что определение средней
длины свободного пробега
 подразумевает, что для a=
1,
подразумевает, что для a=
1,
 (2.34)
(2.34)
и отношение Фукса (2.33) преобразуется, используя (2.34),
 (2.35)
(2.35)
Значение
 ,
используемого в выражениях выше не было
определено в теории и должно быть выбрано
опытным путем или оценено в соответствии
с независимой теорией. Несколько выборов
для
,
используемого в выражениях выше не было
определено в теории и должно быть выбрано
опытным путем или оценено в соответствии
с независимой теорией. Несколько выборов
для
 были предложены: самое простое, самим
Фуксом,
были предложены: самое простое, самим
Фуксом,
 =0.
Другие предложения по этой теме высказаны
Дэвисом , в 1983 году:
=0.
Другие предложения по этой теме высказаны
Дэвисом , в 1983 году:
 ,
,
 .
.
• Подход Фукса и Сутугина.
Фукс и Сутугин в 1971 году последовали
решению уравнения Больцмана, данного
Сахни в 1966 году, для
 ,
где
,
где
 -
отношение молекулярного веса
диффундирующего вещества и воздуха,
для создания следующей интерполяционной
формулы переходного режима.
-
отношение молекулярного веса
диффундирующего вещества и воздуха,
для создания следующей интерполяционной
формулы переходного режима.
 (2.36)
(2.36)
Уравнение (2.36) основано на
результатах для
 и поэтому непосредственно применимо,
чтобы описать молекулы в более тяжелом
фоновом газе. Средняя длина свободного
пробега, включенная в определение числа
Кнудсена в (2.36):
и поэтому непосредственно применимо,
чтобы описать молекулы в более тяжелом
фоновом газе. Средняя длина свободного
пробега, включенная в определение числа
Кнудсена в (2.36):
 .
.
• Подход Дахнеке.
Дахнеке(Dahneke)
в 1983 использовал поток, соответствующий
подходу Фукса, но, предполагая что -
 и
и
 ,
получил,
,
получил,
 (2.37)
(2.37)
где
 .
Средняя длина свободного пробега
свободного пробега, включенного в
определение числа Кнудсена в (2.37):
.
Средняя длина свободного пробега
свободного пробега, включенного в
определение числа Кнудсена в (2.37):

• Подход Лоялки. Лоялка в 1983 построил улучшенные интерполяционные формулы для переходного режима, решая линеаризованное уравнения Больцмана с помощью БГК модели (Bhatnagar, Gross, Krook - 1954):
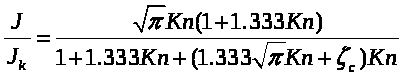 (2.38)
(2.38)
Средняя длина свободного пробега,
используемая Лоялкой:
 ,
коэффициент скачка концентрации имел
значение
,
коэффициент скачка концентрации имел
значение
 .
Виллиамс и Лоялка в 1991 году указали, что
(2.38) не работает вблизи свободно -
молекулярного режима.
.
Виллиамс и Лоялка в 1991 году указали, что
(2.38) не работает вблизи свободно -
молекулярного режима.
2.2 Подведение итогов
Для получения возможно более точных результатов по испарению и конденсации частиц применяются самые разные подходы: от полуэмпирических, некоторые из которых перечислены выше, до достаточно обоснованных с математической точки зрения. К этим работам, в частности, относится серия работ [16] - [21]. В основе этих работ лежит расчет потока пара на частицу интегрированием функции распределения, полученной в результате решения линеаризованного уравнения Больцмана:
 (2.39)
(2.39)
здесь:
 - одночастичная функция распределения
по скоростям и координатам i-ого
газового компонента,
- одночастичная функция распределения
по скоростям и координатам i-ого
газового компонента,
 - телесный угол,
- телесный угол,
 - вектор относительной скорости,
- вектор относительной скорости,
 - сечение столкновений,
- сечение столкновений,
 - скорость молекулы, которая сталкивается
с рассматриваемой молекулой - для которой
записывается уравнение Больцмана,
суммирование производится по всем
газовым составляющим. Вообще говоря, в
левой части уравнения (2.39) следует
добавить слагаемое -
- скорость молекулы, которая сталкивается
с рассматриваемой молекулой - для которой
записывается уравнение Больцмана,
суммирование производится по всем
газовым составляющим. Вообще говоря, в
левой части уравнения (2.39) следует
добавить слагаемое -
 ,
где
,
где
 сила, действующая на молекулу, m
- ее масса,
сила, действующая на молекулу, m
- ее масса,
 - ее ускорение. Предполагается, что
силовое поле отсутствует. В таком виде
уравнение Больцмана слишком сложное,
чтобы для него можно было найти решение,
кроме самых простых случаев, например,
для равновесного распределения по
скоростям. В таком виде оно используется
для исследования ее решений. Правая
часть этого уравнения называется
интегралом столкновения, вся сложность
поиска решений связана именно с этим
интегралом столкновений. В частности
существует принцип Гильберта [26], [27], в
соответствии с которым решение уравнения
(2.39) можно найти в виде разложения по
моментам распределения в начальный
момент времени. На этом основан метод
моментов Греда. Однако этот метод более
применим к задачам гидродинамики,
нежели, к проблемам кинетики. Основные
приближения, которые используются для
получения решения уравнения (2.39) сводятся
к тому, чтобы упростить интеграл
столкновений. При этом предполагается,
что распределение по скоростям мало
отличается от равновесного распределения.
Таким образом конструируется уравнение
для функции, описывающей отклонение
распределения от равновесного. Этот
подход аналогичен методам, описанным
в работе Черчиньяни [21], [22]. В конечном
счёте этот метод приводит к интегральному
уравнению Фредгольма первого или второго
рода - в зависимости от выбранной формы
аппроксимации. Дополнительные осложнения
возникают при постановке граничных
условий. Наибольшие продвижения возможны
в этом направлении при сферической
форме испаряющихся капель. Попытки
получить точное решение приводят к
довольно сложным зависимостям, с которыми
сложно работать и сопоставлять с
экспериментальными данными. Кроме
этого, приходится делать предположение
скачка концентраций на поверхности
частицы. Для диффузионного и около
диффузионного режима столкновений
молекул пара с частицей, когда задачу
можно свести к решению уравнения
диффузии, авторам [17] удалось создать
метод расчета конденсации и испарения
для несферических частиц, используя
формализм функций Грина - задача сводится
к решению соответствующего интегрального
уравнения, при этом могут быть использованы
численные методы - аналитические
зависимости в этом случае получить не
удается. Еще сложнее описать процессы
испарения и конденсации частиц, в среде,
состоящей из нескольких летучих
компонентов [23]. Предполагалось, что
процесс стационарный, испаряющиеся
компоненты химически инертны, пары
представляют собой идеальный газ. Для
переходного режима использовалась
формула Фукса - Сутугина. По сути, этот
подход представлял собой применение
ранее разработанных моделей для бинарной
смеси. Сопоставление модельных расчетов
с экспериментальными результатами
испарения смеси азотной кислоты с водой
показало, что при различных внешних
условиях (соотношениях компонент и
относительной влажности) большинство
моделей можно применять, если подогнать
соответствующим образом модельные
параметры, например, вероятность
прилипания.
- ее ускорение. Предполагается, что
силовое поле отсутствует. В таком виде
уравнение Больцмана слишком сложное,
чтобы для него можно было найти решение,
кроме самых простых случаев, например,
для равновесного распределения по
скоростям. В таком виде оно используется
для исследования ее решений. Правая
часть этого уравнения называется
интегралом столкновения, вся сложность
поиска решений связана именно с этим
интегралом столкновений. В частности
существует принцип Гильберта [26], [27], в
соответствии с которым решение уравнения
(2.39) можно найти в виде разложения по
моментам распределения в начальный
момент времени. На этом основан метод
моментов Греда. Однако этот метод более
применим к задачам гидродинамики,
нежели, к проблемам кинетики. Основные
приближения, которые используются для
получения решения уравнения (2.39) сводятся
к тому, чтобы упростить интеграл
столкновений. При этом предполагается,
что распределение по скоростям мало
отличается от равновесного распределения.
Таким образом конструируется уравнение
для функции, описывающей отклонение
распределения от равновесного. Этот
подход аналогичен методам, описанным
в работе Черчиньяни [21], [22]. В конечном
счёте этот метод приводит к интегральному
уравнению Фредгольма первого или второго
рода - в зависимости от выбранной формы
аппроксимации. Дополнительные осложнения
возникают при постановке граничных
условий. Наибольшие продвижения возможны
в этом направлении при сферической
форме испаряющихся капель. Попытки
получить точное решение приводят к
довольно сложным зависимостям, с которыми
сложно работать и сопоставлять с
экспериментальными данными. Кроме
этого, приходится делать предположение
скачка концентраций на поверхности
частицы. Для диффузионного и около
диффузионного режима столкновений
молекул пара с частицей, когда задачу
можно свести к решению уравнения
диффузии, авторам [17] удалось создать
метод расчета конденсации и испарения
для несферических частиц, используя
формализм функций Грина - задача сводится
к решению соответствующего интегрального
уравнения, при этом могут быть использованы
численные методы - аналитические
зависимости в этом случае получить не
удается. Еще сложнее описать процессы
испарения и конденсации частиц, в среде,
состоящей из нескольких летучих
компонентов [23]. Предполагалось, что
процесс стационарный, испаряющиеся
компоненты химически инертны, пары
представляют собой идеальный газ. Для
переходного режима использовалась
формула Фукса - Сутугина. По сути, этот
подход представлял собой применение
ранее разработанных моделей для бинарной
смеси. Сопоставление модельных расчетов
с экспериментальными результатами
испарения смеси азотной кислоты с водой
показало, что при различных внешних
условиях (соотношениях компонент и
относительной влажности) большинство
моделей можно применять, если подогнать
соответствующим образом модельные
параметры, например, вероятность
прилипания.
С точки зрения корректности постановки задачи и нахождения ее решения следует отметить работу Сахни [24]. Вообще говоря, эта работа относится к расчету потока нейтронов - в замедлителе реактора с учетом поглощения их черными сферами. Тем не менее, она полностью применима для испарения и конденсации частиц сферической формы. По сути дела эта работа - решение задачи Милна для сферической геометрии. Эта задача была сведена к интегральному уравнению первого рода, затем преобразовано к сингулярному уравнению типа Коши, которое было затем решено численными методами. Эти результаты, в частности, были использованы Фуксом и Сутугиным [8] для получения аппроксимационной формулы переходного режима. Очевидно, что для получения точных соотношений для потока молекул на поверхность частицы, необходимо решать уравнение для функции распределения Больцмана. Все определяется тем, в каком виде брать правую часть этого уравнения, ниже мы вернемся к этому.
2.2 Постановка задачи.
Наука об аэрозольных частицах началась c решения проблемы испарения в газообразной среде.
Предположим, нам известен радиус
частицы – a,
и концентрация молекул пара вокруг этой
частицы – n(r),
где r
– радиус-вектор, построенный из точки
начала координат (центр частицы).
Требуется найти зависимость радиуса
частицы от времени – a(t).
Итак, массу частицы можно выразить как
 ,
где ρ –
плотность частицы, площадь поверхности
частицы -
,
где ρ –
плотность частицы, площадь поверхности
частицы -
 ,
тогда будет справедливо уравнение:
,
тогда будет справедливо уравнение:
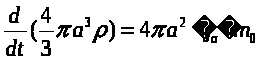 , (2.39)
, (2.39)
где j – плотность потока конденсирующихся молекул пара, m>0 >– масса молекулы. Продифференцировав левую часть и упростив уравнение (2.39) получим:
 (2.40)
(2.40)
Проинтегрировав это выражение, получим:
 (2.41)
(2.41)
Видно, что для расчета скорости испарения или конденсации, что и составляет нашу задачу, необходимо знать величину потока молекул пара на поверхность частицы. Впервые ее записал Максвелл в конце 19-го века:
 (2.42)
(2.42)
здесь j
- это плотность потока конденсирующихся
молекул пара (количество молекул
осаждающихся на единице площади частиц
в единицу времени); D - коэффициент
диффузии молекул пара в газе-носителе,
 -
концентрация пара на далеких от частицы
расстояниях и у поверхности частицы
соответственно; а
- радиус частицы. Этот результат и его
модификации справедливы для сравнительно
крупных частиц, размер которых существенно
превышает длину свободного пробега
конденсирующихся молекул.
-
концентрация пара на далеких от частицы
расстояниях и у поверхности частицы
соответственно; а
- радиус частицы. Этот результат и его
модификации справедливы для сравнительно
крупных частиц, размер которых существенно
превышает длину свободного пробега
конденсирующихся молекул.
Другой предельный случай был
получен значительно позже для свободно
молекулярного режима: конденсационный
поток пропорционален произведению
тепловой скорости молекул
 и поперечному сечению частицы (квадрату
радиуса частицы)
и поперечному сечению частицы (квадрату
радиуса частицы)
 (2.43)
(2.43)
Как уже отмечалось выше, для переходного режима, когда уравнение для потока молекул преобразуется из вида (33) к форме (34), предложено довольно много подходов [2] - [11]. Из этих формул можно выделить выражение, предложенное Фуксом и Сутугиным, поскольку оно наиболее часто цитируется:
 , (2.44)
, (2.44)
где х = а/l и l относительная и размерная длина свободного пробега. Если ввести термин - эффективность конденсации а - то задача будет сведена к нахождению этой величины, через которую определяется поток молекул на поверхность частицы:
 (2.45)
(2.45)
Таким образом, все усилия экспериментаторов и теоретиков сводились к определению именно этой величины.
Предлагаемый ниже подход основан на расчете эффективности конденсации а при помощи распределения молекул пара по скоростям и координатам, как это было сделано у Сахни [24]. Для получения этой функции распределения необходимо решать уравнение Больцмана. Чтобы упростить получение этого решения, правая часть уравнения Больцмана - интеграл столкновения - был линеаризован. Такой прием был предпринят Бхатнагаром, Гроссом и Круком [27] - так называемое БГК приближение. В этом БГК приближении используются наиболее простые граничные условия. Предполагается, что частично молекулы испытывают зеркальное отражение, а некоторые из молекул осаждаются на поверхности. В этом приближении интеграл столкновений представлен в довольно простом виде:
 (2.46)
(2.46)
здесь
 - не зависящая от скорости частота
столкновений, эта величина имеет порядок
- не зависящая от скорости частота
столкновений, эта величина имеет порядок
 ,
где а - радиус
частицы, n
- концентрация молекул пара, <
v > - средняя скорость
относительного движения молекул.
Несмотря на то, что складывается
впечатление, что сделано довольно грубое
приближение - сложный интеграл столкновений
заменен довольно простым слагаемым - в
такой форме уравнение Больцмана сохраняет
основные свои свойства, и, как будет
видно ниже, эта простота кажущаяся.
Можно легко показать, что решение
уравнения (2.46)
,
где а - радиус
частицы, n
- концентрация молекул пара, <
v > - средняя скорость
относительного движения молекул.
Несмотря на то, что складывается
впечатление, что сделано довольно грубое
приближение - сложный интеграл столкновений
заменен довольно простым слагаемым - в
такой форме уравнение Больцмана сохраняет
основные свои свойства, и, как будет
видно ниже, эта простота кажущаяся.
Можно легко показать, что решение
уравнения (2.46)
удовлетворяют уравнениям сохранения массы, импульса и энергии;
удовлетворяет Н - теореме.
Простота уравнения (2.46) обманчива.
Это уравнение имеет сильную нелинейность,
таким образом, локальные параметры -
масса, импульс и энергия должны
определяться через одночастичную
функцию распределения
 ,
поэтому, как будет видно ниже, в то время
как удалось уйти от одних проблем,
возникли другие. При построении
приближений следует принимать во
внимание, что вид уравнения (2.46) дает
два характерных времени -
,
поэтому, как будет видно ниже, в то время
как удалось уйти от одних проблем,
возникли другие. При построении
приближений следует принимать во
внимание, что вид уравнения (2.46) дает
два характерных времени -
 - характерное время микроскопической
релаксации, время за которое
- характерное время микроскопической
релаксации, время за которое
 заметно меняется. Кроме этого, из-за
наличия
заметно меняется. Кроме этого, из-за
наличия
 возникает второе характерное время -
возникает второе характерное время - .
Легко показать, что
.
Легко показать, что
 .
Полученный конденсационный поток
выражен через пространственную
концентрацию конденсирующегося пара.
Показано, что минимальной информации
о профиле концентрации достаточно для
получения точного аналитического
выражения для молекулярного потока при
произвольном режиме конденсации и
произвольной вероятности прилипания.
Это и есть основной результат предложенного
подхода. Следует несколько слов сказать
о соотношении между равновесной
концентрацией пара и концентрацией
пара у поверхности частицы. Вообще
говоря, предполагается, что
.
Полученный конденсационный поток
выражен через пространственную
концентрацию конденсирующегося пара.
Показано, что минимальной информации
о профиле концентрации достаточно для
получения точного аналитического
выражения для молекулярного потока при
произвольном режиме конденсации и
произвольной вероятности прилипания.
Это и есть основной результат предложенного
подхода. Следует несколько слов сказать
о соотношении между равновесной
концентрацией пара и концентрацией
пара у поверхности частицы. Вообще
говоря, предполагается, что
 ,
где
,
где
 - равновесная концентрация пара вблизи
поверхности частицы. В то же время это
не совсем так. Например, при неединичной
вероятности прилипания (β),
концентрация вблизи поверхности частицы
отличается от
- равновесная концентрация пара вблизи
поверхности частицы. В то же время это
не совсем так. Например, при неединичной
вероятности прилипания (β),
концентрация вблизи поверхности частицы
отличается от
 и определяется кинетикой процесса
переноса массы к частице. То же самое
относится к переходному режиму
конденсации, где скачок концентрации
(также возникающий благодаря динамике
переноса массы) заставляет поверхностную
концентрацию отличаться от хорошо
известного значения
и определяется кинетикой процесса
переноса массы к частице. То же самое
относится к переходному режиму
конденсации, где скачок концентрации
(также возникающий благодаря динамике
переноса массы) заставляет поверхностную
концентрацию отличаться от хорошо
известного значения
 .
На самом деле концентрацию
.
На самом деле концентрацию
 саму необходимо находить из решения
динамики столкновения, что ограничивает
применение соотношения
саму необходимо находить из решения
динамики столкновения, что ограничивает
применение соотношения
 .
Более детально эта проблема будет
обсуждаться в рамках ВГК модели наряду
с проблемой скачка концентрации.
.
Более детально эта проблема будет
обсуждаться в рамках ВГК модели наряду
с проблемой скачка концентрации.
Решение задачи и результаты исследования
3.1 Линеаризованное уравнение Больцмана для сферической геометрии в односкоростном приближении.
Рассмотрим получение левой части
уравнения для функции распределения
Больцмана - найдем выражение оператора
 .
Для решения уравнения введем новую
систему ортогональных координат
.
Для решения уравнения введем новую
систему ортогональных координат
 .
Эта система координат очень похожа на
сферическую систему координат -
.
Эта система координат очень похожа на
сферическую систему координат -
 .
.
Связь вводимой системы координат - она также ортогональна - с декартовой может быть представлена системой уравнений:
 (3.1)
(3.1)
Для вычисления градиента в этой системе координат найдем метрический тензор:
 (3.2)
(3.2)
После простых вычислений можно получить:
 (3.3)
(3.3)
Тогда для градиента произвольной функции в этой системе координат:
 (3.4)
(3.4)
Где
 - соответствующие орты в направлениях
- соответствующие орты в направлениях
 .
Тогда производная в направлении вектора
.
Тогда производная в направлении вектора
 может быть представлена в форме:
может быть представлена в форме:
 (3.5)
(3.5)
Для рассматриваемой функции распределения Больцмана, как это было сделано в односкоростном приближении, соответствующим задаче Милна:
 (3.6)
(3.6)
Тогда левая часть уравнения для функции распределения Больцмана в системе координат, описанной ранее, будет выглядеть следующим образом:
 (3.7)
(3.7)
3.2 Основные уравнения
Предположим, что имеется
сферическая частица (капля жидкости),
которая окружена молекулами газа-носителя,
концентрация которых
 -
концентрации пара, который может как
конденсироваться на капле, так и
испаряться. Для того чтобы найти поток
пара на частицу и распределение
концентрации его вокруг частицы,
необходимо рассчитать функцию
распределения пара по координатам и
ско5ростям. Для этого, вообще говоря,
необходимо решить уравнение Больцмана.
Будем считать, что линейная форма
уравнения Больцмана дает хорошие
результаты для рассматриваемого случая:
-
концентрации пара, который может как
конденсироваться на капле, так и
испаряться. Для того чтобы найти поток
пара на частицу и распределение
концентрации его вокруг частицы,
необходимо рассчитать функцию
распределения пара по координатам и
ско5ростям. Для этого, вообще говоря,
необходимо решить уравнение Больцмана.
Будем считать, что линейная форма
уравнения Больцмана дает хорошие
результаты для рассматриваемого случая:

 (3.8)
(3.8)
Здесь
 - функция распределения, зависящая от
- функция распределения, зависящая от
 и r,
а r
расстояние от центра частицы до r
и
и r,
а r
расстояние от центра частицы до r
и
 - угол между радиальным направлением и
направлением скорости молекулы. Другие
обозначения: l
- средняя длина свободного пробега и
- угол между радиальным направлением и
направлением скорости молекулы. Другие
обозначения: l
- средняя длина свободного пробега и
 (3.9)
(3.9)
это численная концентрация молекул пара. Для простоты будем работать в системе единиц, где l = 1.
 (3.10)
(3.10)
При интегрировании (3.8) по
 получается уравнение непрерывности:
получается уравнение непрерывности:
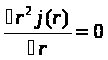 (3.11)
(3.11)
Функцию распределения удобно разбить на две части:

 (3.12)
(3.12)
где
 -
единичная функция Хевисайда. С учетом
(3.12) уравнение (3.8) дает два спаренных
уравнения для
-
единичная функция Хевисайда. С учетом
(3.12) уравнение (3.8) дает два спаренных
уравнения для
 и
и
 :
:
 (3.13)
(3.13)
 (3.14)
(3.14)
Функции
 и
и
 описывают молекулы пара двигающиеся
по направлению к поверхности частицы
и от частицы
описывают молекулы пара двигающиеся
по направлению к поверхности частицы
и от частицы
 .
Численная концентрация молекул и их
поток может быть выражен через эти
функции:
.
Численная концентрация молекул и их
поток может быть выражен через эти
функции:
 (3.15)
(3.15)
 (3.16)
(3.16)
Система уравнений (3.13) и (3.14) должна быть дополнена граничными условиями:
 (3.17)
(3.17)
Это наиболее простые граничные
условия, устанавливающие связь между
функциями
 и
и
 с помощью вероятности прилипания
молекулы пара к поверхности частицы.
Формула (3.9) означает, что доля налетающих
на частицу молекул пара, которые остаются
на ее поверхности, составляет
с помощью вероятности прилипания
молекулы пара к поверхности частицы.
Формула (3.9) означает, что доля налетающих
на частицу молекул пара, которые остаются
на ее поверхности, составляет
 ,
остальные молекулы, доля которых
,
остальные молекулы, доля которых
 ,
зеркально отражаются от поверхности.
Ниже будут представлены более общие
граничные условия, которые не внесут
существенных изменений в дальнейшее
решение.
,
зеркально отражаются от поверхности.
Ниже будут представлены более общие
граничные условия, которые не внесут
существенных изменений в дальнейшее
решение.
3.3 Формальное решение уравнения для функции распределения.
Введем новые переменные
 ,
которые связаны с
,
которые связаны с
 соотношениями:
соотношениями:
 (3.18)
(3.18)
В этих переменных уравнения (3.6) и (3.7) принимают форму:
 (3.19)
(3.19)
 (3.20)
(3.20)
Предположим, что
 -
это известная функция координат, тогда
решение уравнения (3.19) можно получить
в виде:
-
это известная функция координат, тогда
решение уравнения (3.19) можно получить
в виде:
 (3.21)
(3.21)
где
 .
Правая часть уравнения (3.21) содержит
растущую с r
экспоненту, от которой следует избавиться
выбором функции
.
Правая часть уравнения (3.21) содержит
растущую с r
экспоненту, от которой следует избавиться
выбором функции
 .Окончательный
результат приобретает вид:
.Окончательный
результат приобретает вид:
 (3.22)
(3.22)
В переменных
 (3.22) имеют форму:
(3.22) имеют форму:
 (3.23)
(3.23)
Теперь
 принимает
вид:
принимает
вид:
 (3.24)
(3.24)
3.4 Точные результаты решения уравнений
Дальнейшие шаги связаны с
получением явного вида решения (3.24). Для
этого необходимо получить зависимость
 .
Введем новую функцию
.
Введем новую функцию
 уравнением:
уравнением:
 (3.25)
(3.25)
Эта функция предназначена для
того, чтобы плавно перейти от значений
концентрации пара на поверхности частицы
к концентрации на далеких от частицы
расстояниях. Естественно,
 .
При подстановке выражения (3.24) в (3.25)
получаем:
.
При подстановке выражения (3.24) в (3.25)
получаем:
 (3.26)
(3.26)
Здесь введены обозначения
 .
Первый интеграл в правой части (3.26) легко
посчитать:
.
Первый интеграл в правой части (3.26) легко
посчитать:
 (3.27)
(3.27)
Второй тоже легко привести к
удобному для использования виду, для
этого введем замену переменных:
 ,
,
 :
:
 (3.28)
(3.28)
В результате для
 получим удобное выражение:
получим удобное выражение:
 (3.29)
(3.29)
Теперь выражения для распределения
концентрации
 и потока молекул j
принимают форму:
и потока молекул j
принимают форму:
 (3.30)
(3.30)
 (3.31)
(3.31)
Здесь введены следующие обозначения
 и
и
 (3.32)
(3.32)
В соответствии с уравнением
(3.11) можно записать, что
 ,
а также
,
а также
 ,
откуда с учетом (3.25) при
,
откуда с учетом (3.25) при

 для потока у поверхности частицы получим:
для потока у поверхности частицы получим:
 (3.33)
(3.33)
где D коэффициент
диффузии (D=1/3
в БГК приближении) и введем обозначение
 .
Таким образом, найдена связь между
потоком у поверхности частицы с
параметрами распределения концентрации
пара на далеком удалении от нее.
.
Таким образом, найдена связь между
потоком у поверхности частицы с
параметрами распределения концентрации
пара на далеком удалении от нее.
Чтобы установить форму этой
зависимости,
 представим в виде двух слагаемых, каждое
из которых определяет поведение
концентрации у поверхности и вдали от
частицы:
представим в виде двух слагаемых, каждое
из которых определяет поведение
концентрации у поверхности и вдали от
частицы:

 (3.34)
(3.34)
Здесь функция
 равна единице при
равна единице при
 и ничтожно мала на расстояниях порядка
длины свободного пробега молекул пара
и более (r
порядка 1 в наших единицах). Тогда
и ничтожно мала на расстояниях порядка
длины свободного пробега молекул пара
и более (r
порядка 1 в наших единицах). Тогда
 , (3.35)
, (3.35)
где
 (3.36)
(3.36)
и
 (3.37)
(3.37)
При подстановке соотношения (3.34) в уравнения (3.30) и (3.31) можно получить:
 (3.38)
(3.38)
 (3.39)
(3.39)
где .
Уравнение (3.33) позволяет исключить
комбинацию
.
Уравнение (3.33) позволяет исключить
комбинацию
 при помощи линейной системы уравнений
для
при помощи линейной системы уравнений
для
 и
и
 :
:
 (3.40)
(3.40)
 (3.41)
(3.41)
Решение этих уравнений можно представить через детерминанты:
 (3.42)
(3.42)
 (3.43)
(3.43)
 (3.44)
(3.44)
Окончательно получим:
 (3.45)
(3.45)
Можно получить и явную форму этих выражений:
 (3.46)
(3.46)
3.5 Пограничный слой.
Следует учитывать, что, несмотря
на то, что все выше полученные выражения
точные, пока нет рецепта, как считать
интегралы, входящие в выражения (3.42-
3.44). Для этого надо понять, как выбрать
конкретный вид функции
 .
Вообще говоря, это может быть сделано
при нахождении точного решения уравнения
(3.8). Однако на данном этапе это невозможно.
На самом деле известны свойства функции
.
Вообще говоря, это может быть сделано
при нахождении точного решения уравнения
(3.8). Однако на данном этапе это невозможно.
На самом деле известны свойства функции
 ,
поэтому ее можно подобрать, используя
подгоночные параметры пробных функций.
Для этого необходимо с помощью этой
функции суметь подобрать правильный
профиль концентрации паров вокруг
частицы. Такой функцией может быть
зависимость вида:
,
поэтому ее можно подобрать, используя
подгоночные параметры пробных функций.
Для этого необходимо с помощью этой
функции суметь подобрать правильный
профиль концентрации паров вокруг
частицы. Такой функцией может быть
зависимость вида:
 (3.47)
(3.47)
где величина параметра
 -
это характерное расстояние, на котором
свободно молекулярный режим переходит
в непрерывный. Множитель
-
это характерное расстояние, на котором
свободно молекулярный режим переходит
в непрерывный. Множитель
 - описывает профиль концентрации
конденсирующихся паров в безстолкновительном
режиме, когда поток пропорционален
плотности, а не ее градиенту. Поскольку
поток пропорционален
- описывает профиль концентрации
конденсирующихся паров в безстолкновительном
режиме, когда поток пропорционален
плотности, а не ее градиенту. Поскольку
поток пропорционален
 ,
то
,
то
 .
Экспоненциальный множитель аппроксимирует
переход от свободно молекулярного
режима к непрерывному. Таким образом,
вместо уравнения (3.36) получается:
.
Экспоненциальный множитель аппроксимирует
переход от свободно молекулярного
режима к непрерывному. Таким образом,
вместо уравнения (3.36) получается:
 (3.48)
(3.48)
Представленная интерпретация
достаточно прямолинейна, чувствительность
окончательного результата к величине
 будет позже исследована. На рисунке 1
показан профиль концентрации при
различных значениях величины
будет позже исследована. На рисунке 1
показан профиль концентрации при
различных значениях величины
 .
Вообще говоря,
.
Вообще говоря,
 может быть найдена при помощи вариационных
расчетов.
может быть найдена при помощи вариационных
расчетов.

Рис. 1. Профиль
концентрации вблизи поверхности частицы
(см. уравнения (3.25), (3.34) и (3.47)). Концентрации
нормированы на 1, расстояние измерено
в длинах свободного
пробега. Кривые 1-4
рассчитаны
для
 = 1, 3, 10,
= 1, 3, 10,
 соответственно как функции расстояния
от центра
частицы. Радиус частицы а=1.
Последняя
кривая соответствует приближению скачка
профиля концентрации:
сам профиль концентрации получен из
уравнения Фика, а граничные условия для
концентрации
пара - из решения кинетического уравнения
(см. уравнение
(3.59)).
соответственно как функции расстояния
от центра
частицы. Радиус частицы а=1.
Последняя
кривая соответствует приближению скачка
профиля концентрации:
сам профиль концентрации получен из
уравнения Фика, а граничные условия для
концентрации
пара - из решения кинетического уравнения
(см. уравнение
(3.59)).
Итак, найдём параметр
 .
Для этого построим функционал и
минимизируем его численными методами
с помощью ЭВМ. Итак, вспомним уравнение
(3.13). Оно и станет основой для нашего
функционала:
.
Для этого построим функционал и
минимизируем его численными методами
с помощью ЭВМ. Итак, вспомним уравнение
(3.13). Оно и станет основой для нашего
функционала:
 (3.49)
(3.49)
В результате преобразования получим:
 (3.50)
(3.50)
Теперь можно записать функционал,
который надо минимизировать относительно
параметра
 :
:
 (3.51)
(3.51)
где
 (3.52)
(3.52)
 ,
,
 (3.53)
(3.53)
 ,
,
 (3.54)
(3.54)
 ,
(3.55)
,
(3.55)
 (3.55)
(3.55)
 (3.56)
(3.56)
 (3.57)
(3.57)
 (3.58)
(3.58)
Вышеописанная модель была реализована в двух видах: в качестве программы на языке C с использованием библиотеки GSL, а так же в виде приложения пакета Mathcad. Рассмотрим полученные результаты:

Рис. 2. Значение
функционала (3.51) в диффузионном
(непрерывном) режиме
 .
.

Рис. 3. Значение
функционала (3.51) в переходном режиме
 .
.

Рис. 4. Значение
функционала (3.51) в свободномолекулярном
(кинетическом) режиме
 .
.
Мы видим, что функционал уменьшается
с ростом
 .
Это соответствует скачку концентрации
на поверхности частицы. Таким образом,
модель оказалась чувствительной к
скачку концентрации, то есть оправдывающей
приближение, описанное ниже.
.
Это соответствует скачку концентрации
на поверхности частицы. Таким образом,
модель оказалась чувствительной к
скачку концентрации, то есть оправдывающей
приближение, описанное ниже.
Рассмотрим влияние параметра на окончательный результат:

Рис. 5.
Зависимость потока конденсирующихся
паров
 .
Потоки
нормированы на 1, расстояния измерены
в длинах свободного пробега: а) - полная
вероятность
прилипания, кривая 1
соответствует
.
Потоки
нормированы на 1, расстояния измерены
в длинах свободного пробега: а) - полная
вероятность
прилипания, кривая 1
соответствует
 = 1, кривая
2 соответствует скачку концентрации (
= 1, кривая
2 соответствует скачку концентрации ( ), показано
также и отношение этих потоков; б) - при
уменьшении
), показано
также и отношение этих потоков; б) - при
уменьшении
 приближение скачка концентрации
дает лучшую точность
приближение скачка концентрации
дает лучшую точность
Из рисунка 5 видно, что окончательный
результат не сильно зависит от параметра
 .
Максимальное отклонение между граничными
значениями
.
Максимальное отклонение между граничными
значениями
 и
и
 не превышает 10% и уменьшается при
уменьшении
не превышает 10% и уменьшается при
уменьшении
 .
.
3.6. Приближение скачка концентрации на поверхности частицы
Рассмотрим случай, когда
 .
При больших
.
При больших
 функция
функция
 ведет себя довольно резко (на расстояниях
порядка
ведет себя довольно резко (на расстояниях
порядка
 ),
при этом она изменяется от
),
при этом она изменяется от
 до
до
 (см. рис. 1). На предельном значении
(см. рис. 1). На предельном значении
 это изменение соответствует скачку
концентрации между значениями
это изменение соответствует скачку
концентрации между значениями
 и
и
 .
Интегралы
.
Интегралы
 находятся в этом пределе. Конечно, это
приближение оставляет правильным
асимптотическое поведение потока при
больших и малых значениях а. Если
пренебречь выражением, пропорциональным
находятся в этом пределе. Конечно, это
приближение оставляет правильным
асимптотическое поведение потока при
больших и малых значениях а. Если
пренебречь выражением, пропорциональным
 ,
то можно из уравнений (3.40) и (3.41) получить:
,
то можно из уравнений (3.40) и (3.41) получить:
 (3.59)
(3.59)
 (3.60)
(3.60)
 (3.61)
(3.61)
При выводе этих уравнений было
использовано то, что
 .
.
3.7 Численные результаты
Зависимости j
от вероятности прилипания
 показаны на рисунке 6 для различных
размеров частиц а.
показаны на рисунке 6 для различных
размеров частиц а.

Рис. 6.
Зависимость относительного потока
конденсирующихся
паров (
 ,где
,где
 -
поток при свободно
молекулярном режиме при
-
поток при свободно
молекулярном режиме при
 )
от вероятности прилипания
)
от вероятности прилипания
 .
Расстояния измерены в длинах свободного
пробега. При расчетах использовалась
система уравнений
(3.38).
.
Расстояния измерены в длинах свободного
пробега. При расчетах использовалась
система уравнений
(3.38).
Поток
 был найден из уравнения (3.59), а после
этого был сопоставлен с формулой
Фукса-Сутунгина, которая для произвольных
был найден из уравнения (3.59), а после
этого был сопоставлен с формулой
Фукса-Сутунгина, которая для произвольных
 может быть переписана в форме уравнения
(3.59) с
может быть переписана в форме уравнения
(3.59) с
 ,
замененным на
,
замененным на
 ([10]):
([10]):
 (3.62)
(3.62)
Соответствие между формулами,
как можно видеть из рисунков 8 и 9, не
требует комментариев за исключением
того, что при малых
 это соответствие становится хуже.
это соответствие становится хуже.

Рис. 7.
Поток конденсирующихся паров: сравнение
приближения
скачка концентрации с формулой
Фукса-Сутугина
при вероятности прилипания
 =1.
Потоки
вблизи поверхности частицы нормированы
на 1, расстояния
измерены в длинах свободного пробега.
Кривая 1:
формула
Фукса-Сутугина. Кривая 2: приближение
скачка концентрации (уравнение (3.59)).
=1.
Потоки
вблизи поверхности частицы нормированы
на 1, расстояния
измерены в длинах свободного пробега.
Кривая 1:
формула
Фукса-Сутугина. Кривая 2: приближение
скачка концентрации (уравнение (3.59)).

Рис. 8.
Поток конденсирующихся паров: сравнение
приближения скачка концентрации с
формулой Фукса-Сутугина
при вероятности прилипания
 = 0.1. Потоки
вблизи поверхности частицы нормированы
на 1, расстояния
измерены в длинах свободного пробега.
Кривая 1:
формула
Фукса-Сутугина. Кривая 2: приближение
скачка концентрации (уравнение (3.59)).
= 0.1. Потоки
вблизи поверхности частицы нормированы
на 1, расстояния
измерены в длинах свободного пробега.
Кривая 1:
формула
Фукса-Сутугина. Кривая 2: приближение
скачка концентрации (уравнение (3.59)).
График роста частицы для различных вероятностей прилипания представленная на рисунке 9 и рисунке 10 была найдена из уравнений (2.41) и (3.59).

Рис. 9. Размер частицы a(t), найденный из уравнений (2.41) и (3.59). Масса и плотность налетающих частиц взяты равными единице.

Рис. 10. Размер частицы a(t), найденный из уравнений (2.41) и (3.59). Масса и плотность налетающих частиц взяты равными единице.
4. Выводы и заключение.
В результате работы над дипломом было сделано:
Исследован процесс конденсации при различных числах Кнудсена.
Для расчета плотности потока молекул пара на частицу было использовано решение линеаризованного уравнения Больцмана.
Оценено значение параметра решения уравнения Больцмана для широкого диапазона значений чисел Кнудсена.
Выявлено, что модель односкоростного приближения дает скачок концентрации на поверхности. Это означает, что значение параметра решения должно быть очень большим.
Численные эксперименты показали, что наиболее важные величины, поток молекул пара, скорость роста частицы, слабо зависят от значения определяемого параметра.
При малых значениях вероятности прилипания эта зависимость становится еще меньше.
Предложен и реализован алгоритм расчета конденсационного роста частиц при различных числах Кнудсена вероятностях прилипания молекул пара к поверхности частицы.
Список литературы
J.C. Maxwell Collected Scientific Papers, Cambridge, 11, 625, 1890.
Фукс Н.А. Испарение и рост капель в газообразной среде. - Изд. АН СССР, Итоги науки, с. 90, 1958.
Н.Фукс, ЖЭТФ, т.4, вып. 7, 1934.
Li Y.Q., Davidovits P., Shi Q., Jayne J.T., Kolb C.E., Worsnop D.R. Mass and Thermal Accomodation Coefficients of H3O(g) on Liquid Water as Function of Temperatrue. - J.Phys.Chem.A, 105, 29, 10627-10634, 2001.
Heidenreich S., Buttner H. Investigation about the infuence of the Kelvin effect on droplet growth rate. - J.Aerosol Sci., v.26, n.2, 335 - 339, 1995.
Shi Q., Davidovits P., Jayne J.T., Worsnop D.R., Kolb C.E. Uptake of gas-phase ammonia. 1. Uptake by aqueous surfases as function of pH. - Mass and Thermal Accomodation Coefficients of H3O(g) on Liquid J.Phys.Chem.A, 103, 29, 8812-8823, 1999.
Swartz E., Shi Q., Davidovits P., Jayne J.T., Worsnop D.R., Kolb C.E. Uptake of gas-phase ammonia. 2. Uptake by sufuric acid surfaxres J.Phys.Chem.A, 103, 29, 8824-8833 1999
Widmann J.F., Davis E.J. Mathemetical models of the uptake of C1ONO2 and other gases by atmospheric aerosols. - J.AerosoI Sci., v.28, n.2, pp. 87 - 106, 1997.
Fuchs N.A., Sutugin A.G. Highly dispersed aerosols, in Topicsin Current Aerosol Research (Part 2), ed. by CM. Hidy and J.R. Brock, New York, pp. 1-200, 1971.
Dahneke B. Simple kinetic theory of Brownian diffusion in vapor and aerosols, in Theory of Dispersed Multiphase Flow, ed. by R.E. Meyer Academic Press, New York, pp. 97 - 133, 1983.
Loyalka S.K. Modelling of condensation in aerosols. - Prog. Nucl.Energy, v.12, pp.1-? 1983.
Sitarski M., Nowakowski B. Condensation rate of trace vapor on Knudsen aerosols from solution of the Boltzmann equation. - J.Colloid Interface Sci., v.72, pp.113-122, 1979.
Лушников А.А., Загайнов В.А. Кинетические эффекты конденсации при произвольной вероятности прилипания молекул к частицам. - Изв. АН, сер. ФАС), т.38, №2, с. 192 - 199.
К. Черчиньяни. Теория и приложения уравнения Больцмана. - Изд. Мир. Москва, 1978.
Резибуа П., Де Ленер П. Классическая кинетическая теория жидкостей и газов. - Изд. Мир, Москва, 1980.
Bhatnagar P.L., Gross E.P., Krook M. A model for collision processes in gases.
1