Высокоэффективная жидкостная хроматография загрязнителей атмосферного воздуха и воздуха рабочей зоны
«Высокоэффективная жидкостная хроматография загрязнителей атмосферного воздуха и воздуха рабочей зоны»
Содержание
Введение
Глава 1.Измерение и оценка химических загрязнителей
Глава 2. Высокоэффективная жидкостная хроматография
Глава 3. Современное оборудование
Приложение
Литература
Введение
С
точки зрения загрязнения воздух
непромышленных помещений обладает
некоторыми особенностями, отличающими
его от наружного, или атмосферного,
воздуха и воздушной среды промышленных
объектов. Помимо загрязнителей,
содержащихся в атмосферном воздухе,
воздух помещений содержит загрязнители,
вырабатываемые конструктивными
материалами здания, а также являющимися
результатом деятельности внутри
помещения. Концентрация загрязнителей
в воздухе помещений обычно такая же,
как в атмосферном воздухе, или ниже, и
зависит от качества вентиляции;
загрязнители, вырабатываемые
конструктивными материалами, обычно
отличаются от тех, что содержатся в
атмосферном воздухе, и их концентрация
может быть гораздо выше, в то время как
загрязнители, являющиеся результатом
деятельности внутри помещения, зависят
от рода деятельности и могут совпадать
по концентрации с теми, что содержатся
в атмосферном воздухе, например СО и
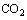 .
.
По этой причине количество загрязнителей, обнаруживаемых в воздухе непромышленных помещений, довольно велико, и уровень концентрации их незначителен (за исключением случаев наличия мощного источника загрязнения); он зависит от атмосферных и климатических условий, типа и характеристик здания, способа вентиляции и рода деятельности внутри помещений.
ГЛАВА 1. ИЗМЕРЕНИЕ И ОЦЕНКА ХИМИЧЕСКИХ ЗАГРЯЗНИТЕЛЕЙ
Методы, доступные для отбора проб воздуха в помещении и для их анализа, можно разделить на две группы: методы, в которых используются непосредственные измерения, и те, в которых собираются пробы для последующего анализа.
В методах, основанных на непосредственных измерениях, взятие пробы воздуха и измерение концентрации загрязнителей происходит одновременно; они быстры, и результаты измерений появляются мгновенно, позволяя получить точные данные при небольших затратах. Эта группа включает в себя колориметрические трубки и специальные контрольно-измерительные устройства.
Принцип
действия колориметрических трубок
основан на изменении цвета определенного
реагента при вступлении в контакт с тем
или иным загрязнителем. Наибольшее
распространение получили трубки с
твердым реагентом, через которые при
помощи ручного насоса прокачивается
воздух. Оценка качества воздуха помещений
при помощи колориметрических трубок
применима только для предварительных
измерений или выявления спорадических
выбросов, поскольку их чувствительность,
как правило, низка, за исключением
чувствительности к некоторым загрязнителям
типа СО или
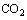 ,
концентрация которых в воздухе помещений
достаточно высока. Важно помнить, что
точность этого метода низка, и на
результат измерения могут влиять другие
загрязнители.
,
концентрация которых в воздухе помещений
достаточно высока. Важно помнить, что
точность этого метода низка, и на
результат измерения могут влиять другие
загрязнители.
В случае применения специальных контрольно-измерительных устройств, обнаружение загрязнителей основано на их физических, электрических, тепловых, электромагнитных и хемоэлектромагнитных свойствах. Большинство этих контрольно-измерительных устройств могут использоваться для длительных и кратковременных измерений и дают возможность составить карту загрязненности данного помещения. Их точность различна у разных производителей, и они требуют периодической калибровки посредством измерения регулируемых составов воздуха или аттестованных газовых смесей. Точность и чувствительность контрольно-измерительных устройств постоянно повышается. Многие из них имеют встроенную память для хранение результатов измерений, которые затем могут быть загружены в компьютер для анализа и создания баз данных.
Методы сбора проб и анализа можно разделить на активные (или динамические) и пассивные.
В активных системах воздух продувается через специальные устройства, в которых собираются и концентрируются загрязнители. Это делается при помощи фильтров, твердых адсорбентов, абсорбирующих или активных растворов, которые помещаются в барботер, или которыми пропитывается пористый материал. Затем анализируют сам загрязнитель или продукты его реакции. Для анализа проб воздуха активным методом необходим собирающий загрязнитель фиксатор, насос, чтобы прокачивать воздух через систему, и устройство для измерения объема - непосредственно или на основе измерений потока и времени.
Значения потока и объема воздуха берутся из справочников или определяются в результате предыдущих измерений и зависят от количества и типа абсорбента или адсорбента, от конкретного загрязнителя, от метода забора проб (эмиссионный или имиссионный), а также от состояния воздушной среды (влажность, температура, давление). Эффективность сбора загрязнителя повышается при уменьшении объема пробы и при увеличении количества фиксатора.
Другой
активный метод отбора проб заключается
в непосредственном сборе образцов
воздуха в специальный мешок или любой
другой инертный и герметичный контейнер.
Этот метод применим для некоторых газов
(СО,
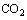 ,
,
 ,
,
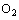 )
и полезен при предварительных измерениях,
когда неизвестен тип загрязнителя.
Недостаток его заключается в том, что
без концентрации образца чувствительность
приборов может оказаться недостаточной,
и потребуются дополнительные исследования
в лаборатории.
)
и полезен при предварительных измерениях,
когда неизвестен тип загрязнителя.
Недостаток его заключается в том, что
без концентрации образца чувствительность
приборов может оказаться недостаточной,
и потребуются дополнительные исследования
в лаборатории.
Пассивные системы
основаны на диффузии или осаждении
загрязнителей на ту или иную основу, в
качестве которой может выступать
адсорбент - чистый или пропитанный
определенным реагентом. Эти системы
более удобны и просты в эксплуатации,
чем активные. Они не требуют насосов
для отбора проб и высококвалифицированного
персонала. Однако сбор образца может
занимать длительное время, и результаты
будут отражать усредненную концентрацию
того или иного загрязнителя. Пассивный
метод неприменим для измерения пиковых
концентраций; для этих целей должны
использоваться активные системы. Для
правильной эксплуатации пассивных
систем необходимо знать скорость сбора
каждого загрязнителя, которая зависит
от скорости диффузии газа или пара и
конструкции измерительного прибора.
Процедуры анализа
Количество загрязнителей в воздухе помещений велико, а концентрация из низка. Доступная методология анализа основана на адаптации методов, используемых для контроля качества атмосферы и воздуха промышленных объектов. Приспособление этих методов к анализу воздуха непромышленных помещений включает в себя изменение диапазона измеряемых величин, увеличение времени выборки и использование большего количества абсорбентов или адсорбентов. Все эти изменения приемлемы только в том случае, если они не ведут к потере достоверности или точности. Анализ смеси загрязнителей обычно дорог, а полученные результаты неточны. Во многих случаях удается получить лишь распределение загрязнителей, которое отражает уровень загрязнения во время сбора проб по отношению к чистому воздуху, атмосферному воздуху, или воздуху других помещений. Для построения распределения загрязнителей используются контрольно-измерительные устройства первичного анализа, хотя в некоторых случаях они могут оказаться слишком громоздкими или шумными. В настоящее время разрабатываются более компактные и бесшумные приборы, имеющие более высокую точность и чувствительность. Таблица 1 отражает современное состояние методов, используемых для определения концентрации различных типов загрязнителей.
Таблица.1 Методы, используемые для анализа химических загрязнителей
|
Загрязняющее вещество |
Измерительные приборы с прямым считыванием* |
Отбор образцов и анализ |
|
Угарный газ |
+ |
+ |
|
Углекислый газ |
+ |
+ |
|
Двуокись азота |
+ |
+ |
|
Формальдегид |
- |
+ |
|
Сернистый газ |
+ |
+ |
|
Озон |
+ |
+ |
|
VOCs |
+ |
+ |
|
Пестициды |
- |
+ |
|
Взвешенные частицы |
+ |
+ |
* ++ = наиболее часто используемый; + = реже используемый; - = неприменимый.
Анализ газов
Для
анализа газов наиболее часто применяются
активные методы, основанные на
использовании твердых адсорбентов и
абсорбирующих жидкостей или на
непосредственном отборе образцов
воздуха при помощи специальных мешков
или других инертных и герметичных
контейнеров.
Для предотвращения потери
части пробы и повышения точности
измерений объем образца должен быть
меньше, а количество абсорбента или
адсорбента больше, чем для других типов
загрязнителей. Необходимо также принять
меры предосторожности при транспортировке
и хранении образца (поддерживать низкую
температуру) и минимизировать время до
его анализа. В настоящее время для
анализа газов широко применяются методы
непосредственных измерений, поскольку
современные контрольно-измерительные
устройства стали гораздо точнее и
чувствительнее. Из-за простоты их
применения, а также качества и удобства
выдаваемой ими информации они все больше
вытесняют традиционные методы анализа.
В таблице 2 представлены минимальные
уровни обнаружения различных газов для
разных методов отбора проб и анализа.
Таблица 2. Минимальные уровни обнаружения некоторых газов с использованием измерительных приборов для оценки качества воздуха помещений
|
Загрязняющий агент |
Измерительные приборы первичного анализа* |
Отбор
образцов и |
|
Угарный газ |
1,0
|
0,05
|
|
Двуокись азота |
2
|
1,5
|
|
Озон |
4
|
5,0
|
|
Формальдегид |
|
5,0
|
* Приборы для измерения углекислого газа с использованием инфракрасной спектроскопии всегда достаточно чувствительны.
**
Пассивные контрольно-измерительные
устройства (продолжительность
воздействия). Эти газы - наиболее
распространенные загрязнители воздуха
помещений. Их концентрация измеряется
непосредственно при помощи
контрольно-измерительных устройств
электрохимическим или инфракрасным
методом. Правда, инфракрасные детекторы
обладают меньшей точностью. Измерения
могут также производиться путем отбора
проб в инертные герметичные контейнеры
и последующего анализа образцов методами
газовой хроматографии с детектором
ионизации пламени, когда газы в результате
каталитической реакции сначала
превращаются в метан. Детекторы
теплопроводности обладают достаточной
чувствительностью для измерения близких
к норме концентраций
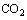 .
.
Двуокись азота
Для
обнаружения двуокиси азота,
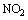 ,
в воздухе помещений были разработаны
специальные методы с использованием
пассивных контрольно-измерительных
устройств и взятием проб воздуха для
последующего анализа, однако для них
характерны проблемы чувствительности,
которые в будущем, вероятно, будут
разрешены. Лучшим из известных методов
является метод трубки Палмеза (Palmes
tube), имеющий чувствительность на уровне
300
,
в воздухе помещений были разработаны
специальные методы с использованием
пассивных контрольно-измерительных
устройств и взятием проб воздуха для
последующего анализа, однако для них
характерны проблемы чувствительности,
которые в будущем, вероятно, будут
разрешены. Лучшим из известных методов
является метод трубки Палмеза (Palmes
tube), имеющий чувствительность на уровне
300
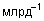 (миллиардных
долей по объему). Для непромышленных
помещений необходимо производить
выборку, как минимум, в течение пяти
дней, чтобы достичь уровня обнаружения
1,5
(миллиардных
долей по объему). Для непромышленных
помещений необходимо производить
выборку, как минимум, в течение пяти
дней, чтобы достичь уровня обнаружения
1,5
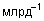 ,
который в три раза превышает нулевой
уровень для недельной экспозиции. Были
разработаны также портативные
контрольно-измерительных устройств
измерения в режиме реального времени,
принцип действия которых основан на
хемилюминисцентной реакции между
,
который в три раза превышает нулевой
уровень для недельной экспозиции. Были
разработаны также портативные
контрольно-измерительных устройств
измерения в режиме реального времени,
принцип действия которых основан на
хемилюминисцентной реакции между
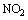 и
специальным реагентом люминолом, но
результаты, полученные данным методом,
в значительной степени зависят от
температуры, а их точность и линейность
зависит от характеристик используемого
люминола. Контрольно-измерительные
устройства с электрохимическими
датчиками обладают лучшей чувствительностью,
но на их показания влияет присутствие
веществ, содержащих серу (Freixa 1993).
и
специальным реагентом люминолом, но
результаты, полученные данным методом,
в значительной степени зависят от
температуры, а их точность и линейность
зависит от характеристик используемого
люминола. Контрольно-измерительные
устройства с электрохимическими
датчиками обладают лучшей чувствительностью,
но на их показания влияет присутствие
веществ, содержащих серу (Freixa 1993).
Диоксид серы
Для
измерения концентрации диоксида серы,
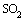 ,
в воздухе помещений применяется
спектрофотометрический метод. Образец
воздуха пропускается через раствор
калия тетрохлоромеркуриата
(tetrachloromercuriate), в результате чего образуется
устойчивое соединение, которое после
реакции с параросанилином (pararosaniline)
подвергается спектрофотометрическому
анализу. Другие способы используют
метод пламенной фотометрии и измерение
пульсаций ультрафиолетового излучения,
а также проведение дополнительных
измерений перед спектральным анализом.
Эти способы обнаружения диоксида серы
не подходят для анализа воздуха помещений
из-за отсутствия необходимых методик
и из-за необходимости вентиляционной
системы для удаления вырабатываемых
при их работе газов. Поскольку в последнее
время выделение
,
в воздухе помещений применяется
спектрофотометрический метод. Образец
воздуха пропускается через раствор
калия тетрохлоромеркуриата
(tetrachloromercuriate), в результате чего образуется
устойчивое соединение, которое после
реакции с параросанилином (pararosaniline)
подвергается спектрофотометрическому
анализу. Другие способы используют
метод пламенной фотометрии и измерение
пульсаций ультрафиолетового излучения,
а также проведение дополнительных
измерений перед спектральным анализом.
Эти способы обнаружения диоксида серы
не подходят для анализа воздуха помещений
из-за отсутствия необходимых методик
и из-за необходимости вентиляционной
системы для удаления вырабатываемых
при их работе газов. Поскольку в последнее
время выделение
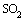 значительно
уменьшилось, диоксид серы больше не
рассматривается в качестве существенного
загрязнителя воздуха помещений, и
поэтому усовершенствование приборов
для его обнаружения продвинулось не
очень далеко. Тем не менее, на рынке
имеются переносные измерительные
приборы для обнаружения
значительно
уменьшилось, диоксид серы больше не
рассматривается в качестве существенного
загрязнителя воздуха помещений, и
поэтому усовершенствование приборов
для его обнаружения продвинулось не
очень далеко. Тем не менее, на рынке
имеются переносные измерительные
приборы для обнаружения
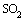 ,
принцип действия которых основан на
детектировании параросанилина
(pararosaniline) (Freixa 1993).
,
принцип действия которых основан на
детектировании параросанилина
(pararosaniline) (Freixa 1993).
Озон
Озон,
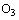 ,
может быть обнаружен только в воздухе
специальных помещений, где происходит
его непрерывная генерация, так как он
быстро разрушается. Его концентрация
измеряется непосредственно при помощи
колориметрических трубок или методами
хемилюминисценции. Его также можно
обнаружить посредством методов,
используемых в промышленной гигиене,
поскольку они легко адаптируются к
условиям непромышленных помещений.
Образец, полученный при помощи
абсорбирующего раствора йодида калия,
затем подвергается спектрофотометрическому
анализу.
,
может быть обнаружен только в воздухе
специальных помещений, где происходит
его непрерывная генерация, так как он
быстро разрушается. Его концентрация
измеряется непосредственно при помощи
колориметрических трубок или методами
хемилюминисценции. Его также можно
обнаружить посредством методов,
используемых в промышленной гигиене,
поскольку они легко адаптируются к
условиям непромышленных помещений.
Образец, полученный при помощи
абсорбирующего раствора йодида калия,
затем подвергается спектрофотометрическому
анализу.
Формальдегид
Формальдегид
является одним из значимых загрязнителей
воздуха в помещении. Из-за его химических
и токсичных свойств рекомендуется
проводить индивидуальный анализ его
присутствия. Существуют различные
методы определения присутствия
формальдегида в воздухе, и все они
основаны на отборе проб для последующего
анализа с использованием активного
связующего вещества или диффузии.
Наиболее подходящий способ связывания
определяется на основе типа пробы
(эмиссионная или иммиссионная) и
чувствительности аналитического метода.
Традиционные методы основаны на
пропускании образца воздуха через
дистиллированную воду или 1% раствор
бисульфата натрия при температуре
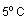 с
последующим его анализом
спектрофлюорометрическими методами.
Храниться образцы должны также при
температуре
с
последующим его анализом
спектрофлюорометрическими методами.
Храниться образцы должны также при
температуре
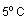 ,
а на результаты измерения могут влиять
вещества, содержащиеся в табачном дыме.
Для анализа воздуха помещений чаще
используются активные системы или
методы сбора загрязнителей посредством
твердых адсорбентов. Основой всех их
служит фильтр или пропитанное реагентом
типа бисульфата натрия или
2-4-дифенилгидразина твердое вещество.
Методы, в основе которых лежит диффузия
загрязнителя, наряду с другими
преимуществами обладают большей
чувствительностью, поскольку время,
требуемое для получения образца, у них
дольше (Freixa 1993).
,
а на результаты измерения могут влиять
вещества, содержащиеся в табачном дыме.
Для анализа воздуха помещений чаще
используются активные системы или
методы сбора загрязнителей посредством
твердых адсорбентов. Основой всех их
служит фильтр или пропитанное реагентом
типа бисульфата натрия или
2-4-дифенилгидразина твердое вещество.
Методы, в основе которых лежит диффузия
загрязнителя, наряду с другими
преимуществами обладают большей
чувствительностью, поскольку время,
требуемое для получения образца, у них
дольше (Freixa 1993).
Обнаружение летучих органических соединений
Методы,
используемые для контроля органические
паров в воздухе помещений, должны
отвечать ряду критериев: они должны
иметь чувствительность порядка
миллиардных и триллионных долей по
объему, инструменты для взятия проб или
проведения непосредственных измерений
должны обладать достаточной точностью,
быть портативными и удобными в
транспортировке, а полученные результаты
точны и воспроизводимы. Существует
большое количество методов, отвечающих
этим критериям, но
наиболее часто для
контроля воздуха помещений используется
отбор проб с последующим анализом.
Методы непосредственного измерения
реализованы на основе портативных
газовых хроматографов с различными
принципами действия. Эти приборы дороги
и сложны в обращении, и с ними может
работать только специально обученный
персонал. Для полярных и неполярных
органических соединений, которые имеют
точку кипения от
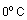 до
до
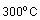 ,
наиболее широко применяются активные
и пассивные системы с активированным
углем. Также используются пористые
полимеры и полимеризованная резина
типа Tenax GC, XAD-2 и Ambersord. Чаще всего
применяется Tenax. Адсорбированные
активированным углем образцы выделяются
при помощи дисульфида углерода, а затем
анализируются газовыми хроматографами
методами пламенной ионизации, электронного
захвата или масс-спектрометрии с
последующим количественным и качественным
анализом. Образцы, адсорбированные при
помощи Tenax, обычно выделяются посредством
тепловой десорбции с гелием и конденсируются
в азотной охлаждаемой ловушке, а затем
помещаются в хроматограф. Другие
распространенные методы включают в
себя непосредственный сбор проб воздуха
при помощи мешков или инертных контейнеров
с последующей прямой подачей воздуха
в газовый хроматограф или предварительной
концентрацией при помощи адсорбента
или охлаждаемой ловушки. Чувствительность
этих методов зависит от типа анализируемого
соединения, от объема пробы, от уровня
фонового загрязнения и чувствительности
используемых приборов. Поскольку
квантификация всех встречающихся
летучих органических соединений
невозможна, ее выполняют по группам,
используя вещества, являющиеся
характерными представителями группы.
При определении наличия летучих
органических соединений в воздухе
помещения особое внимание следует
обращать на чистоту растворителей. При
применении тепловой десорбции очень
важна также чистота используемых газов.
,
наиболее широко применяются активные
и пассивные системы с активированным
углем. Также используются пористые
полимеры и полимеризованная резина
типа Tenax GC, XAD-2 и Ambersord. Чаще всего
применяется Tenax. Адсорбированные
активированным углем образцы выделяются
при помощи дисульфида углерода, а затем
анализируются газовыми хроматографами
методами пламенной ионизации, электронного
захвата или масс-спектрометрии с
последующим количественным и качественным
анализом. Образцы, адсорбированные при
помощи Tenax, обычно выделяются посредством
тепловой десорбции с гелием и конденсируются
в азотной охлаждаемой ловушке, а затем
помещаются в хроматограф. Другие
распространенные методы включают в
себя непосредственный сбор проб воздуха
при помощи мешков или инертных контейнеров
с последующей прямой подачей воздуха
в газовый хроматограф или предварительной
концентрацией при помощи адсорбента
или охлаждаемой ловушки. Чувствительность
этих методов зависит от типа анализируемого
соединения, от объема пробы, от уровня
фонового загрязнения и чувствительности
используемых приборов. Поскольку
квантификация всех встречающихся
летучих органических соединений
невозможна, ее выполняют по группам,
используя вещества, являющиеся
характерными представителями группы.
При определении наличия летучих
органических соединений в воздухе
помещения особое внимание следует
обращать на чистоту растворителей. При
применении тепловой десорбции очень
важна также чистота используемых газов.
Обнаружение пестицидов
Методы обнаружения пестицидов в воздухе помещений обычно включают в себя отбор проб при помощи твердых адсорбентов, хотя не исключено применение барботеров и смешанных систем. В качестве твердого адсорбента чаще всего применяется пористый полимер Хромосорб (Chromosorb) 102, хотя в последнее время все большее распространение получают пенополиуретаны, способные захватывать более широкий спектр пестицидов. Методы анализа зависят от способа сбора образцов и типа пестицида. Обычно используются газовые хроматографы с различными датчиками, от детекторов захвата электронов до масс-спектрографических. Последние обладают большим потенциалом в отношении анализа сложных соединений. При анализе подобных соединений приходится сталкиваться с определенными проблемами, связанными с загрязнением стеклянных частей приборов для отбора проб следами полихлорированных бифенилов, фталатов и пестицидов.
Обнаружение проникающих из окружающей среды пыли или частиц. Для захвата и анализа содержащихся в воздухе частиц известно большое число методов и оборудования, подходящих для оценки качества воздуха помещений.
В контрольно-измерительных устройствах для непосредственного измерения концентрации взвешенных в воздухе частиц применяются детекторы световой диффузии, а методы сбора проб и последующего анализа используют взвешивание и анализ при помощи микроскопа.
В этом случае необходимо наличие циклонного или инерционного сепаратора, чтобы до фильтра отсеять наиболее крупные частицы.
Методы, в которых применяется циклонный сепаратор, могут работать с небольшими объемами, что приводит к увеличению времени взятия проб.
Пассивные контрольно-измерительные устройства обладают высокой точностью, но их показания зависят от температуры, и эти приборы имеют тенденцию завышения результатов при работе с частицами небольших размеров.[1-6]
ГЛАВА 2. ВЫСОКОЭФФЕКТИВНАЯ ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ
Хроматографическое разделение смеси на колонке вследствие медленного продвижения ПФ занимает много времени. Для ускорения процесса хроматографирование проводят под давлением. Этот метод называют высокоэффективной жидкостной хроматографией (ВЖХ)
Модернизация аппаратуры, применяемой в классической жидкостной колоночной хроматографии, сделала ее одним из перспективных и современных методов анализа. Высокоэффективная жидкостная хроматография является удобным способом разделения, препаративного выделения и проведения качественного и количественного анализа нелетучих термолабильных соединений как с малой, так с большой молекулярной массой.
В зависимости от типа применяемого сорбента в данном методе используют 2 варианта хроматографирования: на полярном сорбенте с использованием неполярного элюента (вариант прямой фазы) и на неполярном сорбенте с использованием полярного элюента - так называемая обращенно-фазовая высокоэффективная жидкостная хроматография (ОфВЖХ).
При переходе элюента к элюенту равновесие в условиях ОфВЖХ устанавливается во много раз быстрее, чем в условиях полярных сорбентов и неводных ПФ. Вследствие этого, а также удобства работы с водными и водно-спиртовыми элюентами, ОфВЖХ получила в настоящее время большую популярность. Большинство анализов при помощи ВЖХ проводят именно этим методом.
Аппаратура для ВЖХ
Колонки для ВЖХ выполняют из нержавеющей стали с внутренним диаметром 2-6 мм и длиной 10-25 см. Колонки заполняют сорбентом (НФ). В качестве НФ используются силикагель, оксид алюминия или модифицированные сорбенты. Модифицируют обычно силикагель, внедряя химическим путем в его поверхность различные функциональные группы.
Детекторы. Регистрация выхода из колонки отдельного компонента производится с помощью детектора. Для регистрации можно использовать изменение любого аналитического сигнала, идущего от подвижной фазы и связанного с природой и количеством компонента смеси. В жидкостной хроматографии используют такие аналитические сигналы, как светопоглощение или светоиспускание выходящего раствора (фотометрические и флуориметрические детекторы), показатель преломления (рефрактометрические детекторы), потенциал и электрическая проводимость (электрохимические детекторы) и др.
Непрерывно детектируемый сигнал регистрируется самописцем. Хроматограмма представляет собой зафиксированную на ленте самописца последовательность сигналов детектора, вырабатываемых при выходе из колонки отдельных компонентов смеси. В случае разделения смеси на внешней хроматограмме видны отдельные пики. Положение пика на хроматограмме используют для целей идентификации вещества, высоту или площадь пика - для целей количественного определения.
Качественный анализ
Важнейшие характеристики хроматограммы - время удерживания t>r >и связанный с ней удерживаемый объем -- отражают природу веществ, их способность к сорбции на материале неподвижной фазы и, следовательно, при постоянстве условий хроматографирования являются средством идентификации вещества. Для данной колонки с определенными скоростью потока и температурой время удерживания каждого соединения постоянно (рис), где t>R(a)> - время удерживания компонента А анализируемой смеси с момента ввода в колонку до появления на выходе из колонки максимума пика, t>R(BC)> - время удерживания внутреннего стандарта (первоначально отсутствующее в анализируемой смеси вещество), h - высота пика (мм), a>1/2 >-- ширина пика на половине его высоты, мм.
Для идентификации вещества по хроматограмме обычно используют стандартные образцы или чистые вещества. Сравнивают время удерживания неизвестного компонента t>Rx> с временем удерживания t>RCT> известных веществ. Но более надежна идентификация по измерению относительного времени удерживания
При этом в колонку сначала вводят известное вещество (внутренний стандарт) и измеряют время его удерживания t>R(BC)>, затем хроматографически разделяют (хроматографируют) исследуемую смесь, в которую предварительно добавляют внутренний стандарт.
Количественный анализ
В основе этого анализа лежит зависимость высоты пика h или его площади S от количества вещества. Для узких пиков предпочтительнее измерение h, для широких размытых - S. Площадь пика измеряют разными способами: умножением высоты пика (h) на его ширину (а>1/2>), измеренную на половине его высоты; планиметрированием; с помощью интегратора. Электрическими или электронными интеграторами снабжены современные хроматографы.
Для определения содержания веществ в пробе используют в основном три метода: метод абсолютной градуировки, метод внутренней нормализации и метод внутреннего стандарта.
Метод абсолютной градуировки основан на предварительном определении зависимости между количеством введенного вещества и площадью или высотой пика на хроматограмме. В хроматограмму вводят известное количество градуировочной смеси и определяют площади или высота полученных пиков. Строят график зависимости площади или высоты пика от количества введенного вещества. Анализируют исследуемый образец, измеряют площадь или высоту пика определяемого компонента и на основании градировочного графика рассчитывают его количество.
Метод внутренней нормализации основан на приведении к 100% суммы площадей всех пиков на хроматограмме.
Этот метод дает информацию только об относительном содержании компонента в смеси, но не позволяет определить его абсолютную величину.
Метод внутреннего стандарта основан на сравнении выбранного параметра пика анализируемого вещества с тем же параметром стандартного вещества, введенного в пробу в известном количестве. В исследуемую пробу вводят известное количество такого стандартного вещества, пик которого достаточно хорошо отделяется от пиков компонентов исследуемой смеси.
В последних двух методах требуется введение поправочных коэффициентов, характеризующих чувствительность используемых детекторов к анализируемым веществам. Для разных типов детекторов и разных веществ коэффициент чувствительности определяется экспериментально.
В жидкостной адсорбционной хроматографии используется также анализ фракций растворов, собранных в момент выхода вещества из колонки. Анализ может быть проведен различными физико-химическими методами.
Жидкостную адсорбционную хроматографию применяют в первую очередь для разделения органических веществ. Этим методом весьма успешно изучают состав нефти, углеводородов, эффективно разделяют - транс- и цис- изомеры, алкалоиды и др. С помощью ВЖХ можно определять красители, органические кислоты, аминокислоты, сахара, примеси пестицидов и гербицидов, лекарственных веществ и других загрязнителей в пищевых продуктах.
Аппаратура для жидкостной хроматографии.
В современной жидкостной хроматографии используют приборы различной степени сложности - от наиболее простых систем, до хроматографов высокого класса, снабженных различными дополнительными устройствами. На рис. 1. представлена блок-схема жидкостного хроматографа, содержащая минимально необходимый набор составных частей, в том или ином виде, присутствующих в любой хроматографической системе.
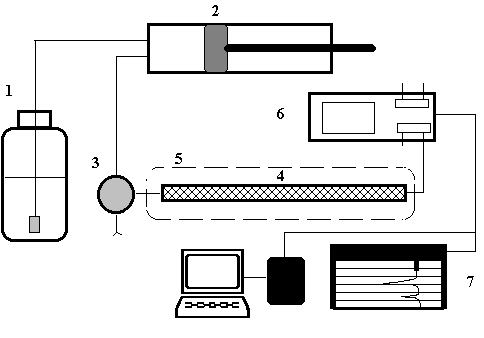
Рис. 1. Блок-схема жидкостного хроматографа.
Насос (2) предназначен для создания постоянного потока растворителя. Его конструкция определяется, прежде всего, рабочим давлением в системе. Для работы в диапазоне 10-500 МПа используются насосы плунжерного (шприцевого), либо пистонного типов. Недостатком первых является необходимость периодических остановок для заполнения элюентом, а вторых - большая сложность конструкции и, как следствие, высокая цена. Для простых систем с невысокими рабочими давлениями 1-5 МПа с успехом применяют недорогие перистальтические насосы, но так как при этом трудно добиться постоянства давления и скорости потока, их использование ограничено препаративными задачами.
Инжектор (3) обеспечивает ввод пробы смеси разделяемых компонентов в колонку с достаточно высокой воспроизводимостью. Простые системы ввода пробы - "stop-flow" требуют остановки насоса и, поэтому, менее удобны, чем петлевые дозаторы, разработанные фирмой Reodyne.
Колонки (4) для ВЭЖХ представляют собой толстостенные трубки из нержавеющей стали, способные выдержать высокое давление. Большую роль играет плотность и равномерность набивки колонки сорбентом. Для жидкостной хроматографии низкого давления с успехом используют толстостенные стеклянные колонки. Постоянство температуры обеспечивается термостатом (5).
Детекторы (6) для жидкостной хроматографии имеют проточную кювету, в которой происходит непрерывное измерение какого-либо свойства протекающего элюента. Наиболее популярными типами детекторов общего назначения являются рефрактометры, измеряющие показатель преломления, и спектрофотометрические детекторы, определяющие оптическую плотность растворителя на фиксированной длине волны (как правило, в ультрафиолетовой области). К достоинствам рефрактометров (и недостаткам спектрофотометров) следует отнести низкую чувствительность к типу определяемого соединения, которое может и не содержать хромофорных групп. С другой стороны, применение рефрактометров ограничено изократическими системами (с постоянным составом элюента), так что использование градиента растворителей в этом случае невозможно.
Регистрирующая (7) система в простейшем случае состоит из дифференциального усилителя и самописца. Желательно также наличие интегратора, позволяющего рассчитывать относительные площади получаемых пиков. В сложных хроматографических системах используется блок интерфейса, соединяющий хроматограф с персональным компьютером (8), который осуществляет не только сбор и обработку информации, но и управляет прибором.
Детекторы для ВЭЖХ
Высокоэффективная жидкостная хроматография (ВЭЖХ) используется для детектирования полярных нелетучих веществ, которые по каким-либо причинам не могут быть переведены в форму удобную для газовой хроматографии, даже в виде производных. К таким веществам, в частности, относят сульфоновые кислоты, водорастворимые красители и некоторые пестициды, например производные фенил - мочевины.
Детекторы:
УФ - детектор на диодной матрице. «Матрица» фотодиодов (их более двухсот) постоянно регистрирует сигналы в УФ- и видимой области спектра, обеспечивая таким образом запись УФ-В-спектров в режиме сканирования. Это позволяет непрерывно снимать при высокой чувствительности неискаженные спектры быстро проходящих через специальную ячейку компонентов.
По сравнению с детектированием на одной длине волны, которое не дает информации о «чистоте» пика, возможности сравнения полных спектров диодной матрицы обеспечивают получение результата идентификации с гораздо большей степенью достоверности.
Флуоресцентный детектор. Большая популярность флуоресцентных детекторов объясняется очень высокой селективностью и чувствительностью, и тем фактором, что многие загрязнители окружающей среды флуоресцируют (например, полиароматические углеводороды).
Электрохимический детектор используются для детектирования веществ, которые легко окисляются или восстанавливаются: фенолы, меркаптаны, амины, ароматические нитро- и галогенпроизводные, альдегиды кетоны, бензидины. [7-9]
Индикат орные
трубки для тест-определения ароматических
аминов в воздухе рабочей зоны[12]
орные
трубки для тест-определения ароматических
аминов в воздухе рабочей зоны[12]
Ароматические амины обладают высокими токсичными свойствами и характеризуются низкими значениями предельно допустимых концентраций в воздушной среде. Склонность к окислительной деградации этих загрязнителей в объектах окружающей среды ограничивает возможность оперативного контроля их содержания в местах локальных выбросов. Это определяет актуальность использования для оценки загрязнения различных сред аналитических систем, основанных на тест-определениях веществ. Тест-методы, к которым относят аналитические устройства с прямым, без дополнительных операций пробоотбора и пробоподготовки анализируемых образцов детектированием аналитического сигнала позволяют наиболее экономично и объективно получать информацию о состоянии окружающей среды.
Цель работы - разработка индикаторных трубок для тест-определения амино соединений в воздухе на основе нового, перспективного класса реагентов для молекулярного органического анализа хлординитрозамещенных бенз-2,1,3-оксадиазола и их N-оксидов.
Окраска образующихся производных зависит от природы определяемого соединения и наблюдаемый батохромный сдвиг полос поглощения определяется степенью замещения аминогруппы и наличием заместителей. Это позволяет использовать в основе тест-метода прямое визуальное детектирование аналитического сигнала. Пределы визуального обнаружения токсикантов достигают 0.05 мг/м3.
Разработанные индикаторные трубки использованы как эффективные хемосорбционные пробоотборники (химические дозиметры) для анализа воздуха, содержащего смесь аминосоединений. Экспериментально была установлена скорость пробоотбора по степени поглощения токсикантов селективным слоем. Состав и количество, например, замещенных анилинов можно определить после элюирования продуктов хемосорбции с силикагеля методом ВЭЖХ. При этом широкий круг потенциальных компонентов промышленных экосистем не влияет на результаты определений.
ГЛАВА 3. СОВРЕМЕННОЕ ОБОРУДОВАНИЕ
Аналитические системы ВЭЖХ Varian основаны на полностью интегрированных автоматизированных модулях ProStar, которые могут работать как самостоятельная система. Фактически, любой из модулей ProStar может быть легко внедрен в уже работающую ВЭЖХ-систему, что очень удобно для создания на базе простой ВЭЖХ станции исследовательского комплекса.
Основные преимущества ВЭЖХ модулей Varian:
- Все основные блоки хроматографов ProStar (автосэмлеры, автоинжекторы, насосы, колонки, блоки термостатирования колонок, распределительные краны, детекторы) производятся на заводах Varian.
- Автоcэмплеры с функцией перемешивания, термостатирования, для работы с обычными количествами пробы и микрообъемами, планшетный автосэмплер вместимостью до 384 проб.
- Перистальтические насосы высочайшей стабильности, от простых изократических до градиентных насосов 4 уровня, не требуют дегазации.
- Лучшие на сегодня хроматографические колонки Chrompack Varian.
- Прецизионные системы термостатирования колонок (от минусовых температур до +990С), распределения потоков.
- Все наиболее распространенные в жидкостной хроматографии детекторы (6 типов), включая самый чувствительный в мире СФ детектор ProStar 325 производства оптического отделения фирмы Varian.
- Удобное программное обеспечение, позволяющее работать как с ВЭЖХ, так и с газовыми хроматографами и хромато-масс-спектрометрами Varian, полностью совместимо с требованиями GLP и протоколами QC/QA.
Ниже приведены наиболее типичные конфигурации, на основе которых, меняя те или иные модули, можно создать системы, максимально удовлетворяющие поставленным задачам.
Изократическая система для рутинных задач
ProStar 340 UV/Vis детектор, 1 длина волны (опция: 310 или 320 UV/Vis)
ProStar 210 насос: аналитический - полупрепаративный (опция: 220 cо скоростью потока от микроколичеств до аналитических)
ProStar 410 автосэмплер
QA/QC система бинарного градиента
ProStar 310 UV/Vis детектор (опция: 320 UV/Vis, 330 диодная матрица, или 345 UV/Vis, две длины волны)
Два ProStar 210 насоса: аналитических – полупрепаративных.
ProStar 410 автосэмплер с переменным объемом ввода (опции: 400 рутинный или 430 многопланшетный от 96 проб).
R&D система тройного градиента (исследования и анализ)
ProStar 330 диодная матрица (опции: 310 UV/Vis, 320 UV/Vis, or 345 UV/Vis, две длины волны)
ProStar 230 насос тройного градиента cо скоростью потока от микроколичеств до аналитических (опция: Три 210 насоса: аналитических - полупрепаративных )
ProStar 410 автосэмплер с переменным объемом ввода (опция: 420 с переменным объемом и разными виалами или 430 многопланшетный от 96 проб)
Профессиональная исследовательская система
ProStar 330 диодная матрица (опция 310 UV/Vis)
ProStar 230 насос тройного градиента cо скоростью потока от микроколичеств до аналитических (опция: Два 215 насоса: аналитических - полупрепаративных)
ProStar 430 автосэмплер многопланшетный от 96 проб с разными планшетами (опция: 420 с разными виалами)
PrepStar 218: бюджетная препаративная система
50-% мощность работы при использовании насоса мощностью 50 или 100 мл/мин
Максимальная производительность с насосом на 200 мл/мин при 3500 psi
Обработка данных и составление отчетов с помощью ПО Galaxie TM
Приложение
МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ. ИЗМЕРЕНИЕ МАССОВЫХ КОНЦЕНТРАЦИЙ АВЕРСЕКТИНА (СМЕСИ ИЗОМЕРОВ) В ВОЗДУХЕ РАБОЧЕЙ ЗОНЫ МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ. МЕТОДИЧЕСКИЕ УКАЗАНИЯ
1. Подготовлены НИИ медицины труда РАМН (Макеева Л.Г., Муравьева Г.В.).
2. Разработаны ООО НБЦ "Фармбиомед" (В.Т. Тер-Симонян, Е.Б. Кругляк), Российским государственным медицинским университетом (Е.Б.Гугля).
3. Рассмотрены на совместном заседании группы Главного эксперта. Комиссии по государственному санитарно-эпидемиологическому нормированию по проблеме "Лабораторно-инструментальное дело и метрологическое обеспечение" и метод бюро подсекции
"Промышленно-санитарная химия" Проблемной комиссии "Научные основы гигиены труда и профпатологии".
4. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию при Министерстве здравоохранения Российской Федерации (протокол N 18 от 27 марта 2003 года).
5. Утверждены и введены в действие Главным государственным санитарным врачом Российской Федерации, Первым заместителем Министра здравоохранения Российской Федерации 16 мая 2003 года.
6. Введены впервые.
1. Общие положения и область применения Настоящие Методические указания устанавливают количественный хроматографический анализ воздуха рабочей зоны на содержание аверсектина C в диапазоне массовых концентраций от 0,025 до 0,5 мг/куб. м.
Методические указания разработаны и подготовлены в соответствии с требованиями ГОСТ 12.1.005-88. ССБТ "Воздух рабочей зоны. Общие санитарно-гигиенические требования", ГОСТ Р 8.563-96 "Государственная система обеспечения единства измерений. Методики выполнения измерений", МИ 2335-95 "Внутренний контроль качества результатов количественного химического анализа", МИ 2336-95 "Характеристика погрешности результатов количественного химического анализа. Алгоритмы оценивания".
Методические указания предназначены для санитарных лабораторий промышленных предприятий, организаций и учреждений, где возможен контакт работающих с аверсектином C, и других лабораторий, аккредитованных в установленном порядке на право проведения таких исследований.
2. Характеристика вещества
2.1. Структурная формула
Аверсектин C представляет собой смесь восьми близких в химическом отношении природных 16-членных макроциклических лактонов, продуктов жизнедеятельности культуры Streptomycis avermitilis (табл. 1). Компоненты A1 и B1 имеют двойную связь в положении 22 - 23 (см.рисунок <*>), у компонентов A2 и B2 эта связь восстановлена. Основные компоненты - авермектины B1 и B2, причем содержание компонента B1a ( 10E,14T,16E,2Z)- (1R,4S,S`,6S,6`R,8R,12S,20R,21R,24S) -6`-[(S)]-sec-бутил ]- 21, 24- гидрокси -S`,11,13,22- тетраметил -2- окс о- 3,7,19 - триоксатетрацикло =[16,6-1]-4,8O,22,24-пентакоза-0,14,16,22-тетраен-6- спиро -2`(5`,6`- дигидро -2Н- пиран )-12- ил --2,6- дидеокси -4-2-(2,60-дидеокси-3-0-метил-альфа-1- арабино= гексапиранозил)-3=0- метил-альфаарабиногекса-пиранозида) в смеси составляет не менее 40%. 2.5. Физико-химические свойства
Аверсектин C - порошок белого или желтовато-белого цвета, легко растворим в хлорированных углеводородах, ацетоне, бензоле, растворим в низших спиртах, практически нерастворим в воде, петролейном эфире. Температуры плавления авермектинов (с разложением) составляют около 150 ёC. Агрегатное состояние в воздухе - аэрозоль.
2.6. Токсикологическая характеристика
Аверсектин C - противопаразитарный препарат, обладает нервно-паралитическим действием.
Предельно допустимая концентрация (ПДК) аверсектина C в воздухе 0,05 мг/куб. м. Класс опасности - первый.
3. Погрешность измерений
Методика обеспечивает выполнение измерений массовых концентраций аверсектина C с погрешностью не более +/- 24% при доверительной вероятности 0,95.
4. Метод измерений
Измерение массовых концентраций аверсектина C основано на получении флюоресцирующих производных авермектинов путем их дериватизации 1-метилимидазолом и трифторуксусным ангидридом.
Последующее количественное определение авермектина B1a, одного из компонентов аверсектина C, проводят методом обращенно-фазовой высокоэффективной жидкостной хроматографии с применением флюоресцентного детектора при длинах волн возбуждения и испускания 365 и 470 нм соответственно.
Отбор проб проводится с концентрированием на фильтр.
Нижний предел измерения содержания авермектина B1a в хроматографируемом объеме раствора 0,004 мкг.
Нижний предел измерения концентрации аверсектина С в воздухе 0,025 мг/куб. м (при отборе 140 куб. дм воздуха).
Определению не мешают другие авермектины.
5. Средства измерений, вспомогательные устройства, материалы, реактивы
5.1. Средства измерений, вспомогательные устройства, материалы
5.1.1 Хроматограф жидкостной Du Pont 8800 (США) с флюоресцентным детектором.
5.1.2 Колонка хроматографическая стальная длиной 250 мм и внутренним диаметром 4 мм, заполненная сорбентом Диасорб-130-С16Т с
размером частиц 5 мкм (фирма БиоХимМак, Россия).
5.1.3 Аспирационное устройство ПУ-3Э, ТУ 4215-000-11696625-95.
5.1.4 Весы аналитические ВЛА-200, ГОСТ 24104-88Е.
5.1.5 Меры массы, ГОСТ 7328-82Е.
5.1.6 Фильтродержатель, ТУ 95.72.05-77.
5.1.7 Набор для фильтрации жидкостей, производство НПФ
"Биохром".
5.1.8 Колбы мерные вместимостью 25 и 100 куб. см, ГОСТ 1770-74Е.
5.1.9 Пипетки вместимостью от 1, 2, 5 и 10 куб. см, ГОСТ
29227-91.
5.1.10. Цилиндр мерный со шлифом вместимостью 100 куб. см, ГОСТ
1770-74Е.
5.1.11 Бюксы 50/30, ГОСТ 25336-82Е.
5.1.12 Пробирки с пришлифованными пробками вместимостью 10 куб.
см, ГОСТ 25336-82Е.
5.1.13 Воронка фильтровальная ВФ-20/16, ГОСТ 25336-82.
5.1.14 Центрифуга низкоскоростная ЦЛС-3, ТУ 5-375-4170-73.
5.1.15. Центрифужные пробирки стеклянные вместимостью 5 куб. см с
полиэтиленовыми пробками.
5.1.16. Ультразвуковой диспергатор УЗДН-А, ТУ 25-7401.0127-88.
5.1.17. Холодильник бытовой, ГОСТ 16317-87.
5.1.18. Вакуумный испаритель ротационный ИР-1М, ТУ 25-11-917-76.
5.1.19. Фильтры АФА-ВП-10, ТУ 95-743-80.
5.2. Реактивы
5.2.1. Авермектин B1, РСО 9340-201-00-494189-99, содержание
авермектина B1a 88,88%.
5.2.2. Аверсектин C, ТУ 9383-009-17266133-97, содержание
авермектина B1a не менее 40%.
5.2.3. Ацетонитрил "для жидкостной хроматографии",
ТУ-6-09-14-2167-84.
5.2.4. Спирт этиловый, х.ч., ТУ 6-0951710-72.
5.2.5. 1-Метилимидазол импортный, фирма Мерк.
5.2.6. Трифторуксусный ангидрид импортный, фирма Мерк.
5.2.7. Спирт метиловый, х.ч., ГОСТ 6995-77.
5.2.8. Вода дистиллированная, ГОСТ 6709-72.
5.3. Допускается применение иных средств измерения, вспомогательных устройств, реактивов и материалов, обеспечивающих показатели точности, установленные для данной МВИ.
6. Требования безопасности
6.1. При работе с реактивами соблюдают требования безопасности,
установленные для работы с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005-88.
6.2. При проведении анализов горючих и вредных веществ соблюдают меры противопожарной безопасности по ГОСТ 12.1.004-76.
6.3. При выполнении измерений с использованием хроматографа соблюдают правила электробезопасности в соответствии с ГОСТ 12.1.019-79 и инструкцией по эксплуатации прибора.
7. Требования к квалификации оператора
К выполнению измерений и обработке результатов допускают лиц с высшим и средним специальным образованием, имеющих навыки работы на жидкостном хроматографе.
8. Условия измерений
8.1. Приготовление растворов и подготовку проб к анализу проводят в нормальных условиях при температуре воздуха (20 +/- 5) ёC, атмосферном давлении 84 - 106 кПа и влажности воздуха не более 80%.
8.2. Измерения на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
9. Подготовка к выполнению измерения
9.1. Приготовление растворов
9.1.1. Стандартный раствор N 1 авермектина B1a для градуировки с концентрацией 88,8 мкг/куб. см готовят путем растворения точной навески 10 мг авермектина B1 в этиловом спирте в мерной колбе объемом 100 куб. см. Раствор хранят не более 2-х месяцев в холодильнике.
9.1.2. Стандартный раствор N 2 авермектина B1 с концентрацией авермектина B1а 3,52 мкг/куб. см готовят путем разведения 4 куб. см стандартного раствора N 1 в мерной колбе на 100 куб. см этиловым спиртом. Раствор хранят не более 2-х недель в холодильнике.
9.1.3. Раствор элюента готовят смешиванием в мерном цилиндре 98куб. см метилового спирта и 2 куб. см дистиллированной воды.
Непосредственно перед измерением раствор фильтруют с помощью набора для фильтрации.
9.1.4. Реакционную смесь готовят из трифторуксусного ангидрида и ацетонитрила в соотношении 1:2 и помещают ее в холодильник при 0 ёC (смесь готовят в день работы и не хранят).
9.2. Подготовка прибора
Общую подготовку прибора осуществляют согласно инструкции по эксплуатации.
9.3. Установление градуировочной характеристики
Градуировочную характеристику, выражающую зависимость площади пика авермектина B1a (в условных единицах) от количества массы (мкг) авермектина B1а в хроматографируемом объеме пробы, устанавливают по методу абсолютной градуировки с использованием градуировочных растворов. Градуировочные растворы устойчивы в течение недели при хранении в холодильнике. Для построения градуировочного графика отбирают по 2,0 куб. см каждого градуировочного раствора, помещают в центрифужные пробирки и упаривают досуха на вакуумном испарителе. В каждую пробирку с сухим остатком вносят по 0,5 куб. см ацетонитрила, пробирку энергично встряхивают и обрабатывают ультразвуком в течение 30 с. Затем пробирку повторно встряхивают и повторно обрабатывают ультразвуком. В каждую пробирку вносят по 0,05 куб. см 1-метилимидазола. Пробирку закрывают, тщательно перемешивают содержимое в течение 5 - 10 с, обрабатывают ультразвуком, центрифугируют и помещают в холодильник при 0 ёC на 10 минут. После охлаждения в пробирку с образцом вносят 0,15 куб. см охлажденной реакционной смеси. Пробирку закрывают и выдерживают в холодильнике в течение 1 часа. Общий объем раствора пробы после проведения реакции - 0,7 куб. см. Растворы помещают в пробоотборное устройство хроматографа. Условия хроматографирования градуировочных смесей и анализируемых проб:
состав элюента метиловый спирт: дистиллированная вода, 98:2
скорость потока элюента 2,0 куб. см/мин.
объем вводимой пробы 10 куб. мм
длины волн флюоресцентного
детектора 365/470 нм
Время удерживания авермектина B1в 9,7 мин. B1a12,2 мин.
На полученной хроматограмме измеряют площадь пика с помощью интегратора хроматографа (в условных единицах) при анализе 6-и растворов разных концентраций и растворителя, проводя не менее 5-и параллельных определений для каждого раствора, и строят градуировочную кривую зависимости площади пика авермектина B1a от количества компонента в пробе (в мкг). Проверку градуировочного графика проводят при изменении условий анализа, но не реже 1 раза в неделю.
9.4. Отбор проб воздуха
Воздух с объемным расходом 20 куб. дм/мин. аспирируют через фильтр АФА ВП-20. Для измерения 1/2 ПДК достаточно отобрать 140 куб. дм. Пробы можно хранить не более десяти суток в защищенном от света месте. Отбор проб сопровождается составлением акта отбора с указанием, при какой температуре и давлении он проводился.
10. Выполнение измерений
Фильтр с отобранной пробой помещают в бюкс и приливают пипеткой 10 куб. см раствора этанола. Периодически встряхивая, выдерживают раствор в течение 10 мин. Экстракт фильтруют через воронку с пористой пластинкой N 1 или N 2 и сливают в пробирку с притертой пробкой.
Степень экстракции с фильтра 93%. Отбирают 2 куб. см раствора, помещают в центрифужную пробирку и упаривают досуха. Далее проводят химическую трансформацию и хроматографический анализ аналогично тому,как описано в п. 9.3 для градуировочных растворов. Количественное определение содержания анализируемого авермектина B1a в растворе проводят по предварительно построенному градуировочному графику.
11. Вычисление результатов измерений Концентрацию аверсектина C "C" (в мг/куб. м) в воздухе вычисляют по формуле:
а x в x г
C = -------------,
К x б x V x д
где:
а - содержание вещества в хроматографируемом объеме пробы, найденное по градуировочному графику, мкг;
б - объем пробы, взятый для хроматографирования, куб. см;
в - общий объем раствора пробы после проведения химической
реакции, куб. см;
г - объем жидкой пробы после экстракции с фильтра, куб. см;
д - объем жидкой пробы, взятый для упаривания, куб. см;
V - объем воздуха, отобранный для анализа и приведенный к
стандартным условиям, куб. дм (см. приложение 1);
К = 0,4 - массовая доля авермектина B1a в аверсектине C согласно
ТУ 9383-009-17266133-97.
12. Оформление результатов анализа
Результат количественного анализа представляют в виде C +/- ДЕЛЬТА мг/куб. м, Р = 0,95, где ДЕЛЬТА - характеристика погрешности, ДЕЛЬТА = 0,20C + 0,0006.
12.1. Оперативный контроль воспроизводимости
Оперативный контроль воспроизводимости выполняют в одной серии с анализом рабочих проб. Отбирают реальные пробы воздуха из одного традиционного места отбора двумя пробоотборниками одновременно.
Анализируют в соответствии с прописью методики, привлекая различных исполнителей и максимально варьируя условия проведения анализа (партии реактивов, набора мерной посуды и т.д.), и получают два результата C1 и C2 анализов. Результаты не должны отличаться друг от друга на величину большую, чем норматив оперативного контроля воспроизводимости D:
|C1 - C2| <= D.
При превышении расхождения между двумя результатами норматива оперативного контроля воспроизводимости эксперимент повторяют. При повторном превышении указанного норматива выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их. Внутренний оперативный контроль воспроизводимости проводят не реже чем 1 раз в неделю.
12.2. Оперативный контроль точности
Оперативный контроль точности выполняют в одной серии с анализом рабочих проб. Отбирают реальные пробы воздуха из одного традиционного места отбора двумя пробоотборниками одновременно. Затем к одной пробе,
отобранной на фильтр, делают добавку анализируемого компонента дельта
C из раствора, нанося его на фильтр. Результаты анализа C1 без добавки и C2 с добавкой получают по возможности в одинаковых условиях: одним аналитиком, с одной партией реактивов, с одним набором посуды и т.д. Величина добавки дельта C должна соответствовать 50 - 150% от содержания компонента в пробе, а величина C2 не должна выходить за верхнюю границу диапазона измерения. Погрешность процедуры отбора проб контролируют путем поверки используемых пробоотборников. Расчет норматива оперативного контроля погрешности К проводят по характеристике погрешности методики за вычетом характеристики погрешности пробоотборника. Решение об удовлетворительной погрешности принимают при выполнении условия:
|C2 - C1 - дельта C| <= К.
13. Нормы затрат времени на анализ
Для проведения серии анализов из 6-и проб при последовательном
проведении анализов воздуха требуется 9 часов.
Литература
Пилипенко А.Т., Пятницкий И.В. Аналитическая химия. В двух книгах: кн..1 – М.: Химия, 1990,-480с.
Пилипенко А.Т., Пятницкий И.В. Аналитическая химия. В двух книгах: кн..2 – М.: Химия, 1990,-480с.
Васильєв В.П. Аналитическая химия. В 2 ч. Ч. 2. Физико – химические методы анализа: Учеб. для Химко – технол. спец. вузов. – М.: Высш. шк., 1989. – 384с.
Столяров Б.В., Савинов И.М., Витенберг А.Г., и др. Практическая газовая и жидкостная хроматография. СПб.: Изд-во С.-Петербург. ун-та, 1998. - 612 с.
Лурье Ю.Ю. Аналитическая химия производственных сточных вод / Ю.Ю. Лурье; М.: ХимияЮ, 1984. - 448с.
Юинг Г. Инструментальные методы химического анализа / Пер. с англ. М.: Мир, 1989. – 235 с.
Стыскин Е.Л., Ициксон Л.Б., Брауде Е.В. Практическая высокоэффективная жидкостная хроматография. М.:Химия. 1986. - 288 с.
Горелик Д.О., Конопелько Л.А., Панков Э.Д. Экологический мониторинг. В 2 т. СПб.: Крисмас. 2000. - 260 с.
Айвазов Б.В. Введение в хроматографию. М.: Высш. шк., - 1983.
Гольдберг К.А., Вигдергауз М.С. Введение в газовую хроматографию. М.: Химия, 1990. – 346 с.
Хубер. Применение диодно-матричного детектирования в ВЭЖХ. – М.: “Мир”. 1993. - 96 с.
12.
П.Е. Белов, Р.Н. Исмаилова
Индикат орные
трубки для тест-определения ароматических
аминов в воздухе рабочей зоны
орные
трубки для тест-определения ароматических
аминов в воздухе рабочей зоны