Важкі метали та їх виявлення в стічних водах підприємств
Зміст
Вступ 3
Розділ 1. Коротка характеристика впливу важких металів на біологічні об’єкти 4
1.1. Поняття важких металів 4
1.2. Токсикологічна характеристика деяких важких металів 5
1.2.1. Залізо 6
1.2.2. Кадмій 6
1.2.3. Кобальт 7
1.2.4. Мідь 8
1.2.5. Нікель 8
1.2.6. Ртуть 9
1.2.7. Свинець 9
1.2.8. Цинк 10
1.3. Забруднення важкими металами стічних вод 10
1.4. Вплив важких металів на біологічні об’єкти 11
Розділ 2. Сучасні методи аналізу 14
2.1 Хімічні методи 15
2.2 Фізико – хімічні методи 16
Розділ 3. Практична частина. Отримання та аналіз важких металів із стічних вод підприємств методом сорбції 20
3.1 Виділення важких металів із стічних вод методом сорбції 21
3.2 Методика виявлення іонів важких металів у розчинах 26
3.2.1 Визначення концентрації міді 28
3.2.2 Визначення концентрації свинцю 28
3.2.3 Визначення концентрації цинку 28
3.2.4 Визначення концентрації нікелю 29
3.2.5 Визначення концентрації кадмію 29
3.2.6 Визначення концентрації кобальту 29
3.2.7 Визначення концентрації ртуті 30
3.2.8 Визначення концентрації заліза 30
Висновки 31
Список використаної літератури. 32
Вступ
Із кожним роком зростає техногенне навантаження на навколишнє середовище. Одним із факторів такого навантаження є зростання кількості побутових та промислових викидів, які вимагають своєї утилізації та захоронення. Проблема утилізації та захоронення промислових та побутових викидів вже давно стала надзвичайно важливою. Для вирішення її будують фабрики по переробці побутового сміття, та очисні споруди. Промислові викиди, якщо порівняти їх із побутовими будуть більш токсичні і чинитимуть більш негативний вплив на навколишнє середовище. Адже до промислових викидів відносяться викиди теплових електростанцій, різноманітних промислових підприємств. Особливо небезпечні по впливу на екологічну систему водойм важкі метали. Їх можна знайти в стічних водах металургійних та металообробних підприємств, гальванічних цехів, автопідприємств. В залежності від виду підприємства буде змінюватися картина викидів, в викидах автопідприємств переважають викиди сполук свинцю, гальванічні цехи скидають в стічні води сполуки цинку, кобальту, кадмію.
Якою б довершеною не була очистка стічних вод, але значна кількість важких металів потрапляє в природне середовище. Адже іноді підприємству вигідніше заплатити штрафи чим побудувати чи модернізувати очисні споруди.
Завданням даної роботи буде розглянути, що ж розуміють під поняттям «важкі метали», якою є їх біологічна роль та вплив на екологічну систему водойм, також розглянемо способи виділення важких металів із стічних вод підприємств методом сорбції, що може бути використано як для аналітичного виявлення важких металів у стічних водах так і як перспективний метод очистки стічних вод. Також одним із завдань роботи буде розгляд основних методів виявлення важких металів в стічних водах підприємств на основі державних стандартів України по якості води та виявленню важких металів: ДСт. 18293 – 72, ДСт. 4152 – 72, ДСт. 4011 – 72, ДСт. 4388 – 72, ДСт. 18963 – 72, ДСт. 4151 – 72.
Розділ 1. Коротка характеристика впливу важких металів на біологічні об’єкти
Розглянемо, що ж розуміють під поняттям «важкі метали», які їх шляхи потрапляння в природне середовище та їх вплив на біологічні об’єкти.
1.1. Поняття важких металів
Поняття «важкі метали» досить часто зустрічається у літературі, але у різних авторів до них відносять різні метали. Тобто трактування цього поняття у різних авторів різне. Тому потрібно визначитися, які ж саме метали відносять до важких, які їхні характеристики є визначальними при їх класифікації.
Термін «важкі метали» пов'язаний з високою відносною атомною масою елемента. Ця характеристика звичайно ототожнюється з уявленням про високу токсичність. Також однією із ознак «важких металів» є їхня густина. У сучасній кольоровій металургії розрізняють важкі кольорові метали – густиною 7,14 – 21,4 г/см3 (цинк, олово, мідь, свинець, хром, кадмій, кобальт й ін.) і легкі кольорові метали - густиною 0,53 – 3,5 г/см3 (літій, берилій й ін.).
Відповідно до однієї класифікації [16], до групи важких металів належить більше 40 елементів з високою відносною атомною масою й густиною більшою 6 г/см3. По іншій класифікації, у цю групу включають кольорові метали із густиною більшою, ніж у заліза (свинець, мідь, цинк, нікель, кадмій, кобальт, олово, сурма, вісмут, ртуть).
Відповідно до відомостей, представлених в довіднику [22] до важких металів віднесені елементи, густина яких більша за 5 г/см3. Якщо виходити їх цього показника, важкими можна вважати 43 з 84 металів Періодичної системи хімічних елементів. Таким чином, до важких металів відносять більше 40 хімічних елементів з відносною густиною більше 6. Число ж небезпечних забруднювачів, якщо враховувати токсичність, стійкість і здатність накопичуватися в зовнішньому середовищі, значно менше.
1.2. Токсикологічна характеристика деяких важких металів
Розглянемо властивості, шляхи попадання, гранично допустимі концентрації деяких важких металів. Насамперед становлять інтерес ті метали, які найбільше широко й у значних об'ємах використаються у виробничій діяльності й у результаті нагромадження в зовнішньому середовищі становлять серйозну небезпеку з огляду їх високої біологічної активності й токсичних властивостей. До них відносять залізо, свинець, ртуть, кадмій, цинк, нікель, мідь.
1.2.1. Залізо
Значні кількості заліза надходять зі стічними водами підприємств металургійної, металообробної, текстильної, лакофарбової промисловості й із сільськогосподарськими стоками.
Фазові рівноваги між формами сполук заліза у розчинах залежать від хімічного складу води, РН, Eh і від температури. Розчинене залізо у стічних та природних водах представлене сполуками, що перебувають в іонній формі, у вигляді гідроксокомплексів й комплексів з розчиненими неорганічними й органічними речовинами природних вод. В іонній формі мігрує головним чином Fe (II), а Fe (III) під час відсутності комплексоутворювачів може в значних кількостях перебувати в розчиненому стані.
У результаті хімічного й біохімічного (при участі залізобактерій) окиснення Fe (II) переходить в Fe (III), іони якого, гідролізуючись, випадають в осад у вигляді Fe(OH)>3>. Як для іонів Fе2+, так і для Fe3+ характерна здатність до утворення гідроксокомплексів типу [Fe(OH)>2>]+, [Fe>2>(OH)>2>]4+, [Fe(OH)>3>]+, [Fe>2>(OH)>3>]3+, [Fe(OH)>3>]– і інших, співіснуючих у розчині в різних концентраціях залежно від РН. Основною формою знаходження Fe3+ у поверхневих водах є комплексні сполуки його з розчиненими неорганічними й органічними комплексоутворювачами, головним чином гумусовими речовинами. При РН = 8,0 основною формою знаходження іонів тривалентного заліза в розчинах є Fe(OH)>3>.
Вміст заліза у воді вище 1 – 2 мг/л значно погіршує органолептичні властивості води, надаючи їй неприємний в'язкий смак, і робить воду малопридатною для використання в технічних цілях. ГДК заліза становить 0,3 мг/дм3 (лімітуючий показник шкідливості – органолептичний).
1.2.2. Кадмій
Сполуки кадмію виносяться в поверхневі води зі стічними водами свинцево-цинкових заводів, гірничо-збагачувальних комбінатів, ряду хімічних підприємств (виробництво сірчаної кислоти), гальванічного виробництва, а також із шахтними водами. Зниження концентрації розчинених сполук кадмію відбувається за рахунок процесів сорбції, випадання в осад гідроксида й карбонатів кадмію.
Розчинені форми кадмію в стічних водах являють собою головним чином мінеральні комплекси. У річкових незабруднених й слабко забруднених водах кадмій утримується в субмікрограммових концентраціях, у забруднених і стічних водах концентрація кадмію може досягати десятків мікрограмів в 1 дм3.
Сполуки кадмію відіграють важливу роль у процесі життєдіяльності тварин і людини. У підвищених концентраціях токсичний, особливо в сполученні з іншими токсичними речовинами [8], [19].
ГДК становить 0.001 мг/дм3 (лімітуюча ознака шкідливості – токсикологічна).
1.2.3. Кобальт
У природні води сполуки кобальту попадають зі стічними водами металургійних, металообробних і хімічних заводів.
Сполуки кобальту в природних водах перебувають у розчиненому й звішеному стані, кількісне співвідношення між якими визначається хімічним складом води, температурою й значеннями РН. Розчинені форми представлені в основному комплексними сполуками. Сполуки двовалентного кобальту найбільш характерні для поверхневих вод. У присутності окислювачів можливе існування в помітних концентраціях тривалентного кобальту [19].
Кобальт відноситься до числа біологічно активних елементів. Входячи до складу вітаміну В>12>, кобальт досить активно впливає на надходження азотистих речовин, збільшення змісту хлорофілу й аскорбінової кислоти, активізує біосинтез і підвищує зміст білкового азоту в рослинах. Разом з тим підвищені концентрації сполук кобальту є токсичними [8].
ГДК становить 0.1 мг/дм3.
1.2.4. Мідь
Мідь – один з найважливіших мікроелементів. Фізіологічна активність міді зв'язана головним чином із включенням її до складу активних центрів окислювально-відновних ферментів. Недостатній зміст міді в ґрунтах негативно впливає на синтез білків, жирів і вітамінів і сприяє безплідності рослинних організмів. Мідь бере участь у процесі фотосинтезу й впливає на засвоєння азоту рослинами. Разом з тим, надлишкові концентрації міді впливають на рослинні й тваринні організми.
У природних водах найбільше часто зустрічаються сполуки Cu(II). Зі сполук Cu(I) найпоширеніші важкорозчинні у воді Cu>2>O, Cu>2>S, CuCl. При наявності у водному середовищі лігандів, поряд з рівновагою дисоціації гідроксида, необхідно враховувати утворення різних комплексних сполук, що перебувають у рівновазі з акваіонами міді.
Основним джерелом надходження міді в природні води є стічні води підприємств хімічної, металургійної промисловості, шахтні води, альдегідні реагенти, використовувані для знищення водоростей. Мідь може з'являтися в результаті корозії мідних трубопроводів й інших споруд. Гранично припустима концентрація міді у воді водойм санітарно-побутового водокористування становить 0,1 мг/дм3 (лімітуюча ознака шкідливості – загальносанітарна) [8].
1.2.5. Нікель
Сполуки нікелю у водні об'єкти надходять також із стічними водами цехів нікелювання, заводів синтетичного каучуку, нікелевих збагачувальних фабрик. Величезні викиди нікелю супроводжують спалювання викопного палива.
Концентрація його може знижуватися в результаті випадання в осад таких сполук, як ціаніди, сульфіди, карбонати або гідроксиди (при підвищенні значень РН) й процесів адсорбції.
У поверхневих водах сполуки нікелю перебувають у розчиненому, звішеному й колоїдному стані, кількісне співвідношення між якими залежить від властивостей води, температури й значень РН. Сорбентами сполук нікелю можуть бути гідроксид заліза, органічні речовини, високодисперсний карбонат кальцію, глини. Розчинені форми являють комплексні іони, найбільше часто з амінокислотами, гуміновими кислотами, а також у вигляді міцного ціанідного комплексу. Найпоширеніші в природних водах сполуки нікелю, у яких він перебуває в ступені окислювання +2.
Сполуки нікелю відіграють важливу роль у кровотворних процесах. Підвищений його вміст впливає на серцево-судинну систему. Нікель належить до числа канцерогенних елементів. Вважається, що вільні іони нікелю (Ni2+) приблизно в 2 рази більш токсичні, чим його комплексні сполуки [8]. ГДК становить 0,1 мг/дм3.
1.2.6. Ртуть
Значні кількості ртуті надходять у водні об'єкти зі стічними водами підприємств, що виготовляють барвники, пестициди, фармацевтичні препарати, деякі вибухові речовини.
У поверхневих водах сполуки ртуті перебувають у розчиненому й звішеному станах. Співвідношення між ними залежить від хімічного складу води й значення РН. Звішена ртуть являє собою сорбовані сполуки ртуті. Розчиненими формами є недисоційовані молекули, комплексні органічні й мінеральні сполуки.
Сполуки ртуті високо токсичні, вони вражають нервову систему людини, викликають зміни з боку слизової оболонки, порушення рухової функції й секреції шлунково-кишкового тракту, зміни в крові й ін. ГДК ртуті становить 0,0005 мг/дм3.
1.2.7. Свинець
Викиди свинцю пов’язані із стічними водами гірничо-збагчувальних комбінатів, деяких металургійних заводів, хімічних виробництв, шахт і т.д. Свинець перебуває в воді у розчиненому й звішеному (сорбованому) стані. У розчиненій формі зустрічається у вигляді мінеральних й органо-мінеральних комплексів, а також простих іонів, у нерозчинній – у вигляді сульфідів, сульфатів і карбонатів.
У річкових водах концентрація свинцю коливається від десятих часток до одиниць мікрограмів в 1 дм3.
Свинець – промислова отрута, здатний при несприятливих умовах виявитися причиною отруєння. В організм людини проникає через органи травлення. Виводиться з організму дуже повільно, внаслідок чого накопичується в костях, печінці й нирках [8]. ГДК свинцю становить 0,03 мг/дм3.
1.2.8. Цинк
Попадає в природні води з стічними водами гірничо-збагачувальних комбінатів та гальванічних цехів, виробництв пергаментного паперу, мінеральних фарб, віскозного волокна й ін.
У воді знаходиться в іонній формі або у формі мінеральних й органічних комплексів. Іноді зустрічається в нерозчинній формі: у вигляді гідроксида, карбонату, сульфіду й ін.
Цинк ставиться до числа активних мікроелементів, що впливають на ріст і нормальний розвиток організмів. У той же час багато сполук цинку токсичні, насамперед його сульфат і хлорид. ГДК Zn2+ становить 1 мг/дм3 .
1.3. Забруднення важкими металами стічних вод
Джерелами забруднення вод важкими металами служать стічні води гальванічних цехів, підприємств гірничодобувної, чорної й кольорової металургії, машинобудівних заводів. Важкі метали входять до складу добрив і пестицидів і можуть попадати у водойми разом зі стоками із сільськогосподарських угідь.
У водних середовищах метали можуть бути присутні в трьох формах: у формі звішених часток, колоїдів й розчинених сполук. Останні представлені вільними іонами й розчинними комплексними сполуками з органічними і неорганічними лігандами. Великий вплив на вміст цих елементів у воді має гідроліз, який визначає форму знаходження елемента у водних середовищах. Значна частина важких металів переноситься поверхневими водами у звішеному стані.
Багато металів утворять досить міцні комплекси з органікою; ці комплекси є однієї з найважливіших форм міграції елементів у природних водах. Більшість органічних комплексів утворюються по хелатному принципу і є достатньо стійкими. Комплекси, утворені ґрунтовими кислотами із солями заліза, алюмінію, титану, урану, ванадію, міді, молібдену й інших важких металів, відносно добре розчинні в умовах нейтрального, слабко кислого і слабко лужного середовищ. Тому металоорганічні комплекси здатні мігрувати в природних водах на досить значні відстані. Так, хелатні форми Cu, Cd, Hg менш токсичні, ніж вільні іони. Для розуміння факторів, які регулюють концентрацію металу в стічних водах, їх хімічну реакційну здатність, біологічну доступність і токсичність, необхідно знати не тільки вміст, але й частку зв'язаних і вільних форм металів.
Підвищення концентрації важких металів у природних водах часто пов'язане з іншими видами забруднення, наприклад, із закисленням. Випадання кислотних опадів сприяє зниженню значення РН і переходу металів із сорбованого на мінеральних й органічних речовинах стану у вільний.
1.4. Вплив важких металів на біологічні об’єкти
Відомо, що такі метали як ванадій, залізо, кадмій, калій, кальцій, кобальт, магній, марганець, мідь, молібден, натрій, нікель, олово, хром, цинк є життєво необхідними.
Токсичність у відповідних концентраціях для людини проявляють алюміній, барій, берилій, кадмій, мідь, миш'як, нікель, селен, свинець, срібло, стронцій, ртуть, хром. Концентрація елемента має суттєве значення, оскільки кадмій, мідь, миш'як, нікель, селен, хром відносяться до життєво необхідних для організму людини елементів. Для нормального функціонування організму людини необхідне досягнення збалансованого обміну мікроелементів, порушення якого призводить до важких захворювань та отруєнь. В таблиці 1 приведені дані для деяких металів в порядку зростання їх летальної дози, вказані також й необхідні дози цих елементів.
Таблиця 1. Добова потреба людини в мікроелементах та їх токсичні концентрації (в розрахунку на масу 70кг, в мг/доба)
|
Елемент |
Доза, мг/кг |
||
|
Нормальна |
Токсична |
Летальна |
|
|
Миш'як |
0,04-1,4 |
5-50 |
50-340 |
|
Ртуть |
0,004-0,02 |
0,4 |
150-300 |
|
Мідь |
0,5-6 |
– |
175-250 |
|
Алюміній |
0,0014-0,08 |
60 |
1300-6200 |
|
Кадмій |
0,07-0,3 |
3-330 |
1500-9000 |
|
Фтор |
0,3-5 |
20 |
2000 |
|
Хром |
0,01-1,2 |
200 |
3000-8000 |
|
Цинк |
5-40 |
150-600 |
6000 |
|
Свинець |
0,06-0,5 |
– |
10000 |
|
Залізо |
6-40 |
200 |
7000-35000 |
Розглянемо вплив деяких металів на метаболічні процеси в організмі людини та тварин. У складі стічних вод металургійних комбінатів можна виявити алюміній. В організм людини алюміній потрапляє у складі питної води. Видалення алюмінію з організму ускладнене, близько половини його початкової кількості затримується в організмі до 300 днів. Накопичуючись в тканинах мозку, печінки, нирок, кісток, викликає їх функціональні порушення. Алюміній викликає порушення в синтезі ряду ферментів, сприяючи видаленню таких біоелементів як P, Mg, Ca, Na, Fe . Постійне вживання питної води з вмістом алюмінію понад 0,2 мг/л призводить до підвищення вірогідності появи таких захворювань як енцефалопатія, хвороби Альцгеймера і Паркінсона, анемії, зниження імунної реактивності та інші.
ГДК залишкового алюмінію в питній воді встановлена на рівні 0,5 мг/л за санітарно-токсикологічною ознакою шкідливості, в той час як в більшості країн Європи рекомендовано вміст алюмінію не більше 0,2 мг/л. Така ж норма встановлена ВОЗ. Новий ДержСанПіН “Вода питна”, встановивши норму 0,2 мг/л, дозволяє концентрацію алюмінію в питній воді на рівні 0,5 мг/л, якщо при водопідготовці використовуються реагенти, що містять алюміній.
Кадмій має токсичні і кумулятивні властивості. При надходженні в організм він накопичується в печінці, нирках і селезінці, а також викликає анемію, знижує вміст кисню в крові. Нирки є основною мішенню токсичної дії кадмію. Метал викликає хворобу ітай-ітай, що проявляється в розм’якшенні кісток, кальцифікації і пієлонефриті нирок. Оскільки кадмій накопичується в органах і має тривалий період напіввиведення (10-30 років), вживання заражених продуктів на протязі тривалого часу може призвести до тих чи інших форм кадмієвої інтоксикації.
Мідь є одним з незамінних елементів для організму людини. В деяких випадках дефіцит міді за симптомами подібний до хронічної її інтоксикації. Споживання міді з їжею звичайно складає 2-3 мг на добу, що підтримує необхідну рівновагу. Звичайно швидкість поглинання, утримання і виведення міді не призводять до підвищеного її вмісту в організмі. Однак, при хворобах, що викликають порушення цього механізму, тривала абсорбція міді може викликати цироз печінки. Є відомості про вплив міді на метаболізм штучно вигодовуваних новонароджених. Зафіксовані гострі отруєння людей при вживанні з питною водою міді при дозі 0,14 мг/кг і вище. Мідь токсична для більшості прісних безхребетних.
Ртуть і її сполуки надзвичайно токсичні для людини, вони акумулюються в нирках, печінці, головному мозку. Основний орган – мішень для неорганічної ртуті – нирки. Летальна доза ртуті при споживанні з питною водою складає 75 – 300 мг на добу. Симптоми ртутної інтоксикації – атаксія, пригнічення периферійного сприйняття і рефлексу кінцівок.
В неорганічній формі ртуть в поверхневих і підземних водах присутня зазвичай в концентрації менше 0,5 мкг/л. Середньодобове споживання ртуті варіюється від 2 до 20 мкг на добу на людину.
Свинець вражає нервову систему, кістковий мозок і кров, судини, генетичний апарат клітки, впливає на синтез білка і проявляє гонадотоксичну і ембріотоксичну дію. За результатами досліджень на тваринах було встановлено, що свинець, що надходить в високій концентрації з кормом, викликає рак нирок. На цій основі МАВР віднесла свинець і його неорганічні сполуки до класу можливих канцерогенів для людини.
Цинк життєво необхідний
для ссавців, бо він грає важливу роль в
біосинтезі нуклеїнових кислот, РНК- і
ДНК-полімераз. Встановлено, що цинк -
обов'язковий складник ферменту крові,
карбоангідрази. Цей фермент міститься
в еритроцитах. Карбоангідраза прискорює
виділення вуглекислого газу в легенях.
Крім того, вона допомагає перетворити
частину СО>2>
в іон
 ,
що грає важливу роль в обміні речовин.
Токсичність цинку для людини залежить
багато в чому від його синергізму або
антагонізму з іншими важкими металами,
особливо з кадмієм. Підвищена акумуляція
важких металів може призводити до
дефіциту цинку в організмі людини, що
виявляється в пригніченні ферментної
активності, а також в більш уповільненому
заживанні ран.
,
що грає важливу роль в обміні речовин.
Токсичність цинку для людини залежить
багато в чому від його синергізму або
антагонізму з іншими важкими металами,
особливо з кадмієм. Підвищена акумуляція
важких металів може призводити до
дефіциту цинку в організмі людини, що
виявляється в пригніченні ферментної
активності, а також в більш уповільненому
заживанні ран.
Розділ 2. Сучасні методи аналізу
Розглянемо основні сучасні методи визначення важких металів у розчинах, які найбільш широко використовують при визначенні концентрацій важких металів у стічних та природних водах.
Аналіз стічних вод промислових підприємств має істотну перевагу – доступний об’єм аналізованої проби стічної води достатньо великий, тому можна його попередньо концентрувати різними методами, які ми розглянемо нижче.
2.1 Хімічні методи
Під час аналізу відносно концентрованих стічних вод (а іноді й розведених) використають титрометричні методи аналізу із застосуванням як кольорових індикаторів для фіксації кінця титрування, так і спеціальних приладів - електрохімічних (потенціометричне титрування, амперметричне, кондуктометричне) і оптичних (нефелометричне, колориметричне титрування). Титрометричні методи часто застосовують для визначення аніонів, особливо тоді, коли одночасно присутні різні аніони, що перешкоджають визначенню один одного. У хімічному аналізі стічних та природних вод до сьогодні використовують комплексонометричне титрування із допомогою ЕДТА, таким чином можна швидко та доволі точно визначити загальний вміст важких металів у воді, а при дотриманні певних умов можна проводити також і селективне титрування та визначення концентрації окремих іонів у розчині.
Гравіметричні методи в аналізі стічних вод застосовують рідко. Недоліки їх загальновідомі. Але основною їх перевагою є те, що не потрібна побудова каліброваних графіків. Гравіметричні методи застосовують у якості арбітражних при визначенні магнію, сульфатів-іонів.
Пряма потенціометрія знаходить застосування при визначенні багатьох іонів з використанням іоноселективних електродів. В аналізі природних вод і питної води іоноселективні електроди застосовують для визначення кадмію, міді, свинцю, срібла, лужних металів, бромід-, хлорид-, . ціанід-, фторид-, йодид- і сульфідів-іонів.
Полярографичні методи аналізу широко використають у хіміко-аналітичних лабораторіях підприємств кольоровий металургії для визначення міді, нікелю, кобальту, цинку, вісмуту, кадмію, сурми, олова й інших металів у рудах, сплавах та відходах виробництв. У тих же лабораторіях ці методи використають і для аналізу промислових стічних вод.
2.2 Фізико – хімічні методи
Основні методи визначення неорганічних компонентів стічних вод – фотометрія, атомно-абсорбційна спектрометрія, рентгено-спектральний аналіз й емісійна спектрометрія.
У фотометричних методах аналізу вимірюють поглинання світла аналізованим розчином після введення в нього реактиву, що реагує з певним компонентом стічних вод з утворенням інтенсивно поглинаючої світло сполуки.
Застосовувані у фотометрії прилади складаються із чотирьох частин, послідовно розташованих одна за іншою: джерело світла, світлофільтр або монохроматор, кювета з розчином, детектор (фотоелемент, що перетворює енергію випромінювання в електричну) .
Конструкції приладів залежать від того, у який області спектра (ультрафіолетовій, видимій або інфрачервоній) проводять виміри. Джерелом видимого випромінювання служить звичайна електрична лампа, для одержання УФ-випромінювання застосовують водневу лампу.
Звичайно для проведення аналізу вибирають випромінювання в тій області довжин хвиль, у якій отримана забарвлена сполука має максимальне світлопоглинання, а домішки – мінімальне.
У спектрофотометрах за допомогою монохроматора виділяють дуже вузький пучок світла із певною довжиною хвилі (1-2 нм.) і за допомогою самописців записується крива світло поглинання під час повільної зміни довжини хвилі випромінювання від малих довжин хвиль до більших. У фотоколориметрах для тієї ж мети (виділення випромінювання потрібної довжини) застосовують світлофільтри, що пропускають потік світла значно більшої ширини (20-50 нм). Спектрофотометри, звичайно, більше придатні для проведення точних досліджень, але вони значно дорожчі й менш доступні, чим фотоколориметри. Фото колориметричні методи також більш прості та не потребують довгої підготовки до своєї роботи. Під час аналізу стічних вод виміри проводять найчастіше у видимій області спектра.
Фотометричні методи аналізу обов'язково включають холостий дослід для усунення впливу сторонніх речовин. Існують два типи холостих дослідів:
1) Холостий дослід із дистильованою водою замість аналізованого розчину при додаванні всіх необхідних реактивів; так виключається вплив світлопоглинання реактивами;
2) Холостий дослід із аналізованим розчином без додавання реактивів; так виключається вплив сторонніх речовин, що є присутніми у самій аналізованій пробі.
Розглянемо особливості атомно-абсорбційного аналізу.
Метод заснований на
поглинанні ультрафіолетового або
видимого випромінювання атомами
газу. Щоб перевести пробу (хоча б
частково)
у газоподібний стан, її вводять у полум'я.
Як джерело випромінювання застосовують
лампу з полим катодом з аналізованого
металу. Інтервал довжин хвиль спектральної
лінії, що випромінюється джерелом
випромінювання, і лінії поглинання того
ж самого елемента в полум'ї дуже вузький,
тому поглинання інших елементів практично
не
позначається на результатах аналізу.
Суттєвою відмінністю атомної абсорбції від емісійної спектрометрії є те, що в останньому методі виміряється випромінювання, що випускається атомами в збудженому стані, а атомна абсорбція заснована на вимірі випромінювання, поглиненого нейтральними, не збудженими атомами, що перебувають у полум'ї, яких у полум'ї набагато більше, ніж збуджених. Цим пояснюється висока чутливість методу при визначенні елементів, що мають високу енергію збудження. Найбільшу чутливість атомно-абсорбційна спектроскопія проявляє при визначенні As, Be, Bi, Cd, Hg, Mg, Pb, Ті, Zn, Cs, In. Значно більшу чутливість емісійний метод проявляє при визначенні Li, К, Na, Ba, Sr, Tl. Чутливість визначення інших елементів приблизно однакова при визначенні їх обома методами,
В принципі атомно-абсорбційна спектрометрія подібна до звичайної спектрофотометрії, аналогічна й використовувана в обох методах апаратура. В обох методах випромінювання пропускають через аналізовану пробу, що частково його поглинає, а пропущене світло проходить через монохроматор і попадає на фотодетектор – пристрій, що реєструє кількість пропущеного або поглинутого випромінювання. Розходження цих методів - у джерелі світла й у кюветі для проби.
Джерелом світла в атомно-абсорбційній спектроскопії є лампа з полим катодом, яка випромінює вузький інтервал довжин хвиль, порядку 0,001 нм. Лінія поглинання аналізованого елемента дещо ширша випромінюваної полоси, що дозволяє вимірювати поглинання в її максимумі. Прилад містить необхідний набір ламп, кожна лампа призначається для визначення тільки одного елемента. Існують лампи, призначені для визначення декількох елементів (наприклад, Mg, Са, AI), але застосування їх не рекомендується із-за можливості помилок.
Кюветою в атомно-абсорбційній спектроскопії служить саме полум'я..
Застосовують полум'я, для одержання якого як пальне використають ацетилен, пропан або водень, а як окислювач – повітря, кисень або оксид азоту(I). Обрана газова суміш визначає температуру полум'я. Повітряно-ацетиленове й повітряно-пропанове полум'я мають низьку температуру (2200 – 2400°С). Таке полум'я, використають для визначення елементів, сполуки яких, легко розкладаються при цих температурах. Таких елементів більшість. При визначенні елементів, що утворять важкодисоціюючі сполуки, використають високотемпературне полум'я (3000 – 3200°С), створюване сумішшю оксид азоту (I) та ацетилену. Таке полум'я необхідне при визначенні алюмінію, берилію, кремнію, ванадію й молібдену.
Одним із методів фізико-хімічного аналізу речовин отриманих із стічних вод є рентгеноспектральній аналіз. Рентгеноспектральний аналіз використовують для кількісного визначення металів, які містяться у пробах. При цьому аналізовані зразки можуть мати складну хімічну та фазову будову. Як правило, зразки для аналізу повинні мати масу порядку одного грама, хоча на сьогодні створені прилади, які розраховані на мікро кількості речовин. Точність аналізу складає 2 -5 відносних %, а тривалість від 1 – 2 хвилин до 1 – 2 годин.
Для одержання спектра
рентгенівських променів у
рентгеноспектральному аналізі
використають
їхню дифракцію на кристалах (або на
штрихових дифракційних решітках) при
таких малих кутах
 (1 – 12°), що рентгенівські промені
відбиваються, ніби ковзаючи по поверхні
кристала.
(1 – 12°), що рентгенівські промені
відбиваються, ніби ковзаючи по поверхні
кристала.
Досліджуваний зразок при рентгеноспектральному аналізі опромінюється первинними рентгенівськими променями. Атоми елементів, що входять до складу зразка, під дією випромінювання збуджуються й самі стають джерелами вторинного рентгенівського випромінювання. Такий спосіб аналізу одержав назву флуоресцентного.
Специфічний для даної речовини спектр вторинного випромінювання описується як корінь квадратний із частот коливань променів, випущених атомами, що входять до складу зразка, і лінійно залежить від їхніх атомних номерів:
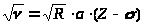 (1)
(1)
Де
 - частота коливань, пов'язана з довжиною
хвилі співвідношенням
- частота коливань, пов'язана з довжиною
хвилі співвідношенням
 R
– постійна Рідберга; а
- постійна для
кожної лінії спектра величина; Z –
атомний номер елемента;
R
– постійна Рідберга; а
- постійна для
кожної лінії спектра величина; Z –
атомний номер елемента;
 -
середня константа екранування.
-
середня константа екранування.

Рис. 2.1. Принципова схема рентгенівського спектрометра з вигнутим кристалом.
1 – додатковий електронний детектор; 2 – досліджуваний зразок; 3 – рентгенівська трубка; 4 – діафрагма; 5 – вигнутий кристал; 6 – електронний детектор флуоресцентного спектра.
З рівняння (1) видно, що кожному виду атомів властива певна частота коливань вторинних рентгенівських променів, збуджених первинним випромінюванням. Очевидно, що енергія кванта збудження повинна бути більше енергії, необхідної для вибивання глибинних електронів атомів досліджуваної речовини, тобто флуоресцентне випромінювання досліджуваного зразка виходить у тисячі разів слабкіше первинного випромінювання, що утрудняє реєстрацію спектрів.
На малюнку 1 наведена принципова схема рентгенівського спектрометра з вигнутим кристалом. Як видно з малюнка, первинні рентгенівські промені із джерела падають на досліджуваний зразок, викликаючи вторинне флуоресцентне випромінювання. Частина випромінювання через діафрагму подається під малим кутом на поверхню вигнутого кристала й під кутом ковзання відбивається від нього. Відбиті від вигнутого кристала промені, будучи сфокусованими на кільцевий екран, утворять на ньому спектр. Цей спектр фіксують фотографічними методами або ж за допомогою електронного детектора. Іноді можливе використання лічильників Гейзера для реєстрації енергії випромінювання.
Розділ 3. Практична частина. Отримання та аналіз важких металів із стічних вод підприємств методом сорбції
Розглянемо основні методи сорбції важких металів із стічних вод підприємств. Аналіз стічних вод має одну особливість, а саме – достатньо великі об’єми аналізованих розчинів, що дозволяє використовувати методи концентрування. Для концентрування стічних вод використовують методи екстракції, випарювання, сорбції. Кожен із приведених методів має як свої позитивні так і негативні сторони. Процеси екстракції потребують використання органічних розчинників: хлороформу, бензолу, толуолу, чотири хлористого вуглецю. Але використання органічних розчинників, випарювання їх досить вогненебезпечне. Методи випарювання не потребують ніяких розчинників, проводяться у водному середовищі, але по часу вони доволі тривалі і їх не можна використати для експрес-аналізу. Метод сорбції потребує використання спеціальних органічних чи неорганічних сорбентів. Метод сорбції в останній час активно розвивається, у його розвитку використовують методи та методики сорбції, які були розроблені раніше для виділення урану, плутонію. Наприклад, в Україні такі роботи велися на Придніпровському гірничо-збагачувальному комбінаті, де на основі методик первинного збагачення уранової руди розробили установки для промислової сорбції рідкоземельних та благородних металів. В останній час викликають інтерес природні сорбенти – цеоліти, які проявляють активну сорбційну дію.
3.1 Виділення важких металів із стічних вод методом сорбції
При аналізі стічних
вод широкими можливостями володіє метод
сорбції. При його використанні можна
досягти коефіцієнтів концентрування
до
 .
Сорбцію проводять як у статичних так і
у динамічних умовах, використовують
сорбційні фільтри. У якості сорбентів
використовують активне вугілля,
сульфовугілля, синтетичні іоніти,
комплексоутворюючі сорбенти.
.
Сорбцію проводять як у статичних так і
у динамічних умовах, використовують
сорбційні фільтри. У якості сорбентів
використовують активне вугілля,
сульфовугілля, синтетичні іоніти,
комплексоутворюючі сорбенти.
Розроблені методи
поглинання хелатів [8, 10], а саме Cd,
Co,
Cr,
Cu,
Dy,
Eu,
Hf,
Hg,
Mn,
Ni,
Pb,
Re,
Sm,
Tb,
Zn
переводили в 8-оксихінолінати при РН =
8 та поглинали утворені хелатні сполуки
активованим вугіллям. Мікроелементи
поглиналися кількісно, коефіцієнт
поглинання досягав значення
 .
Для подальшого аналізу використовували
методи атомно-абсорбційної спектрометрії.
.
Для подальшого аналізу використовували
методи атомно-абсорбційної спектрометрії.
Ще більш зручні для
проведення експрес-аналізів сорбційні
фільтри. Фільтр із привитими групами
 кількісно поглинає близько 12 мікроелементів
(в основному важкі метали та благородні),
які містяться у стічних водах та
промислових водах підприємств у звішеному
та іонному вигляді. Після висушування
фільтр аналізують методом ренггено-фазового
аналізу, границя виявлення мікроелементів
складає
кількісно поглинає близько 12 мікроелементів
(в основному важкі метали та благородні),
які містяться у стічних водах та
промислових водах підприємств у звішеному
та іонному вигляді. Після висушування
фільтр аналізують методом ренггено-фазового
аналізу, границя виявлення мікроелементів
складає
 .
.
Високі значення
коефіцієнтів концентрування досягаються
при використанні статичних умов сорбції.
Наприклад в [8] у якості сорбента
запропоновано використати метатитанову
кислоту. По методиці до проби об’ємом
2 літри додають 200 мг сорбента і
перемішують. Після відстоювання осаду
фільтрують для отримання осаду, потім
осад разом із беззольним фільтром
(баритові фільтри) прожарюють при
температурі 350 – 400ºС. отриманий концентрат
змішують із хімічно чистим графітовим
порошком та хлоридом натрію та аналізують.
Цим методом досягають кількісної сорбції
більшості металів, а саме Al,
Bi,
Co,
Cg,
Cr,
Cu,
Fe,
Ga,
Ge,
In,
Mn,
Mo,
Ni,
Pb,
Sn,
W,
V,
Zn.
Коефіцієнт концентрування складає
 ,
границя виявлення мікроелементів
,
границя виявлення мікроелементів
 .
.
Серед неорганічних сорбентів особливе місце по поширеності та по дешевизні займає активне вугілля різних марок та видів. Активне вугілля являється селективним полі функціональним катіонітом. Воно легко регенерується, досить стійке до хімічного, радіаційного та термічного впливу. Із допомогою активного вугілля проводять визначення хрому, молібдену та ванадію у водах різноманітної природи. Їх поглинають окисненим вугіллям та в подальшому спалюють отриманий концентрат в пальниках при атомно-емісійному аналізі.
В [12] розглянуто процеси сорбції на сорбентах різноманітної хімічної природи.
У книзі приведено класифікацію сорбентів на основі їх хімічної будови та властивостей. Згідно [12] виділяють сорбенти із комплексоутворюючими групами, сорбенти на неорганічній матриці, сорбенти модифіковані комплексоутворюючими реагентами, неорганічні сорбенти.
Промисловістю виготовляються промислові сорбенти із різноманітними комплексоутворюючими групами. Наприклад сорбент Келекс – 100 використовується для одночасного концентрування кадмію, кобальту, заліза, молібдену та нікелю при аналізі вод різної природи та біологічних об’єктів у токсикологічному аналізі. Для виявлення важких металів запропоновані умови: об’єм проби – 200 мл, РН = 7 – 8, тиски 200 – 300 кПа, час концентрування 20 хв. Фільтри після концентрування аналізують рентгенофлуоресцентним методом [12].
Останнім часом синтезовано сорбенти із різноманітними комплексоутворюючими групами. Наприклад сорбент Р-Д містить привитий дитизон (рис.3.1.), матрицею його слугує полістирол.

Рис. 3.1. Залишок комплексоутворюючой групи сорбента Р-Д.
Сорбент використовували для сорбції рідкоземельних та благородних металів із стічних вод гальванічних цехів, підприємств кольорової металургії.
Також синтезовані сорбенти ПВБ-МП, ПОЛІСОРГ VI, матрицями яких є сополімери стирола із дивініл бензолом, полівініленові волокна із комплексоутворюючими групами:

Отримані сорбенти використовують для аналізу та концентрування в основному благородних металів та деяких рідкоземельних металів при одночасному перебуванні у розчині таких поширених металів як мідь, алюміній, кобальт, нікель, залізо та інші.
У якості матриці
використовують не тільки синтетичні
полімери, а і природні, найчастіше
целюлозу. Так волокнистий сорбент Мтилон
Т, який містить групу
 ,
запропоновано для аналізу стічних вод
гальванічних цехів, для концентрування
таких металів як мідь, срібло, золото.
,
запропоновано для аналізу стічних вод
гальванічних цехів, для концентрування
таких металів як мідь, срібло, золото.
Такі метали як Al, Bi, Co, Cg, Cr, Cu, Fe, Ga, Ge, In, Mn, Mo, Ni, Pb, Sn, W, V, Zn запропоновано концентрувати за допомогою целюлозних обмінних фільтрів, попередньо в целюлозу вводиди групу хромотропової кислоти. Утворену сполуку можна зобразити формулою, що приведена на рисунку 3.2.

Рис. 3.2. структура целлюлозно-хромотропового сорбента.
Розроблений метод відрізняється простотою, оскільки целюлозні фільтри можна без попередньої обробки аналізувати за допомогою рентгено-флуоресцентного методу.
Також для концентрування важких металів запропоновано в [12] використовувати целюлозу оброблену 1-(2-оксофенілазо)-2-нафтолом:

Обмінна ємність отриманої смоли рвівна 0,5 мМоль/г.
Комплексоутворюючі групи можна привити не тільки на органічні речовини, створено велику кількість сорбентів на основі мінеральних матриць. У якості останніх найчастіше використовують силікагель та скляні кульки чи гранули. Отримані таким чином ненабухаючі сорбенти – це своєрідний гібрид синтетичних органічних та неорганічних сорбентів.
Комплексоутворюючі групи не обов’язково зв’язувати із матрицею хімічним шляхом, у всякому випадку міцними ковалентними зв’язками. Такі реагенти можна закріпити на поверхні іоніта у вигляді другого шару – шару притиіонів або ж використати пористі матриці у яких розчинятиметься комплексоутворювач.
Із допомогою вказаних вище модифікованих комплексоутворювачами сорбентів запропоновано концентрувати важкі метали, а зокрема ртуть та кадмій. Для цього використовували диетилтіокарбінат нартрію, який наносили на сорбент хромосорб W-DMCS. В залежності від природи іону та типу осаджувача отримані коефіцієнти концентрування 50 – 300.
До числа неорганічних сорбентів відносять оксиди та гідроксиди металів (силікагель, оксид алюмінію, гідратований оксид титану)солі металів (сульфіди, фосфат цирконію), солі гетерополікислот. Механізмом їх діє є комплексоутворення та іонний обмін. Перевагами неорганічних сорбентів є стійкість до нагрівання, радіації, органічних розчинників, висока вибірковість. До недоліків неорганічних сорбентів можна віднести невисоку ємність, не відтворюваність сорбційних властивостей у різних партіях сорбентів.
У якості перспективного сорбента можна використати гідратований оксид титану, який є напівпродуктом виробництва титанових пігментів из ільменіту. Йому притаманні дешевизна та поширеність, низька розчинність, стійкість до термообробки та старіння. При його допомозі в [23] розглянуто виділення тривалентного заліза, нікелю та міді із промислових вод.
У якості сорбента використовують також гідроксид та фосфат цирконію, які володіють по даних [15] високою вибірковістю, термічною та хімічною стійкістю, а також високою обмінною ємністю порівняно із іонітами та гідроксидами заліза, титану та алюмінію.
У якості неорганічних сорбентів використовуються гідратовані оксиди сурми (V), цирконію, для виявлення та сорбції сполук ртуті використовують сульфід свинцю. Але по цих речовинах точних данних та результатів досліджень недостатньо.
Із сказаного вище
можна зробити висновок, що процеси
сорбції дозволяють кількісно виділити
велику кількість важких металів із
розчинів. Високе значення коефіцієнту
концентрування, яке складає для більшості
адсорбентів величину порядку
 дозволяє проводити аналізи малої
кількості речовин та розчинів. Ала
відсутність селективних сорбентів не
дозволяє використовувати фотометричні
чи хімічні методи аналізу, більш
поширеними є рентгено-спектральні та
інші спектрометричні методи.
дозволяє проводити аналізи малої
кількості речовин та розчинів. Ала
відсутність селективних сорбентів не
дозволяє використовувати фотометричні
чи хімічні методи аналізу, більш
поширеними є рентгено-спектральні та
інші спектрометричні методи.
3.2 Методика виявлення іонів важких металів у розчинах
Визначення більшості іонів важких металів являється можливим за умови їх концентрації у розчині більшій за 100 мкг/л. Методи сорбції, екстракція чи випарювання дозволяють концентрувати розчини. Разом із тим потрібно підкреслити, що іноді аналізовані розчини потрібно не концентрувати, а розбавляти із метою отримання більш достовірних даних аналізів та зменшення похибок.
Для аналізування розчинів найчастіше використовують атомно-абсорбційний аналіз, рентгенівську спектрометрію. Хімічні методи використовують рідко із – за потреби маскування перешкоджаючих іонів.
Прилади для атомно-абсорбційного аналізу розрізняються і по конструкції і по методиці роботи із ними. Тому потрібно строго слідувати інструкціям. Наведемо лише загальні основи проведення аналізу.
При визначенні певного елемента вставляють пустотілу катодну лампу призначену для визначення певного хімічного елемента. Встановлюють необхідну довжину хвилі випромінювання. Визначають оптимальне співвідношення подачі горючого газу та газу-окисника. Визначають час досягнення рівноважного стану після приску аналізованої проби. Знаходять оптимальну ширину щілини, визначають оптимальну висоту оптичної осі над пальником, визнають максимум адсорбції стандартного розчину при переміщенні пальника в вертикальному напрямі.
Для побудови градуювального графіка вводять в полум’я робочі стандартні розчини, починаючи від мінімальної концентрації речовини. Для побудови графіка потрібно, згідно правил, використати не менш чотирьох точок, тобто чотирьох різних концентрацій. Кожен вимір проводять не менш трьох разів, для побудови графіка беруть середнє значення величини.
При визначенні заліза та марганцю в калібрувальні стандартні розчини (а згодом і в аналізований розчин) вводять по 25 мл розчину солі кальцію на 100 мл аналізованого розчину. При визначенні магнію та кальцію в розчини вводять по 25 мл солі лантану на 100 мл аналізованого розчину.
Абсорбцію аналізованих
розчинів проводять аналогічно аналізу
стандартних розчинів. Але попередньо
потрібно промити прилад дистильованою
водою в яку додають 15 мл концентрованої
азотної кислоти
 на 1 літр води.
на 1 літр води.
3.2.1 Визначення концентрації міді
Іони міді реагують із діетилкарбаматом натрію із утворенням коричневого нерозчинного у воді діетилкарбамата міді, який легко екстрагується хлороформом, забарвлюючи останній в жовто-коричневий колір. Інтенсивність забарвлення в широких межах пропорційна концентрації міді. Екстрагують утворену речовину із аміачних розчинів, що містять цитрат амонію та коплексон ІІІ, який маскує більшість металів, які також вступають у дану реакцію. Описаним методом можна виявити від 0,05 до 1 мг міді на 1 літр розчину.
При використанні атомно-абсорбційного аналізу вимірюють інтенсивність лінії 324,7 нм. Горючий газ – ацетилен, окисник – повітря.
3.2.2 Визначення концентрації свинцю
Для виявлення свинцю
отримують дитизонат свинцю, який має
червоний колір та розчинний у
 .
Дитизонат свинцю екстрагують при РН
рівному 8 – 9 в ціанідному середовищі,
в якому маскується наявність більшості
металів, які реагують із дитизоном. В
100 мл проби можна визначити свинець при
концентрації 0,1 – 1 мг/л.
.
Дитизонат свинцю екстрагують при РН
рівному 8 – 9 в ціанідному середовищі,
в якому маскується наявність більшості
металів, які реагують із дитизоном. В
100 мл проби можна визначити свинець при
концентрації 0,1 – 1 мг/л.
При використанні атомно-абсорбційного аналізу вимірюють інтенсивність лінії 283,3 нм. Горючий газ – ацетилен, окисник – повітря.
3.2.3 Визначення концентрації цинку
Для виявлення свинцю
отримують дитизонат цинку, який має
червоний колір та розчинний у
 .
Утворена комплексна сполука із дитизоном
має червоний колір і її концентрація
пропорційна кольору комплексу. Цинк
вступає у реакцію із дитизоном при РН
4 – 7. у цьому середовищі із дитизоном
реагують також і мідь, кадмій, свинець,
нікель, кобальт та інші метали. Щоб
зменшити перешкоджаючий вплив даних
металів екстракцію ведуть при РН = 5 із
тіосульфатом та ціанідом. Ціанід додають
для зв’язування кадмію, кобальту, нікелю
та паладію. В таких умовах із дитизоном
реагує тільки олово (ІІ). В обробленій
пробі можна визначити 0,005 – 0,03 мг цинку
на літр розчину.
.
Утворена комплексна сполука із дитизоном
має червоний колір і її концентрація
пропорційна кольору комплексу. Цинк
вступає у реакцію із дитизоном при РН
4 – 7. у цьому середовищі із дитизоном
реагують також і мідь, кадмій, свинець,
нікель, кобальт та інші метали. Щоб
зменшити перешкоджаючий вплив даних
металів екстракцію ведуть при РН = 5 із
тіосульфатом та ціанідом. Ціанід додають
для зв’язування кадмію, кобальту, нікелю
та паладію. В таких умовах із дитизоном
реагує тільки олово (ІІ). В обробленій
пробі можна визначити 0,005 – 0,03 мг цинку
на літр розчину.
При використанні атомно-абсорбційного аналізу вимірюють інтенсивність лінії 213,9 нм. Горючий газ – ацетилен, окисник – повітря.
3.2.4 Визначення концентрації нікелю
Іони нікелю в аміачному буферному розчині в присутності сильного окисника вступають у реакцію із диметилгліоксимом із утворенням комплексної сполуки червоного кольору. Інтенсивність забарвлення пропорційна концентрації нікелю. Прямим способом можна визначити 0,2 – 5 мг/л нікелю.
При використанні атомно-абсорбційного аналізу вимірюють інтенсивність лінії 232,0 нм. Горючий газ – ацетилен, окисник – повітря.
3.2.5 Визначення концентрації кадмію
Іони кадмію екстрагують
розчином дитизону в
 із сильно лужних розчинів, що містять
тар трат-іони. Інтенсивність забарвлення
екстракту, що містить дитизонат кадмію
червоного коьолору, в певних межах
пропорційна концентрації кадмію.
Наведеним способом можна виявити 0,01 –
0,5 мг кадмію в 1 літрі розчину.
із сильно лужних розчинів, що містять
тар трат-іони. Інтенсивність забарвлення
екстракту, що містить дитизонат кадмію
червоного коьолору, в певних межах
пропорційна концентрації кадмію.
Наведеним способом можна виявити 0,01 –
0,5 мг кадмію в 1 літрі розчину.
При використанні атомно-абсорбційного аналізу вимірюють інтенсивність лінії 228,8 нм. Горючий газ – ацетилен, окисник – повітря.
3.2.6 Визначення концентрації кобальту
При використанні атомно-абсорбційного аналізу вимірюють інтенсивність лінії 240,7 нм. Горючий газ – ацетилен, окисник – повітря.
3.2.7 Визначення концентрації ртуті
Під час екстрагування водного розчину солі ртуті дитизоном в хлороформі утворюється оранжевий дитизонат ртуті, який у хлороформі не розчиняеться. В середовищі ацетатного буфера та в присутності ЕДТА та роданіду калію реакція ртуті із дитизоном практично специфічна. Надлишок вільного дитизону із екстракту видаляють страхуванням із із розчином гідроксиду амонію та визначають оптичну густину розчину дитизоната ртуті у хлороформі.
При обробці 100 мл проби
можна визначити ртуть в концентрації
0,05 – 1 мг/л із точністю до
 .
Більш низькі концентрації ртуті можна
визначати екстрагуванням із більшого
об’єму проби (до 500 мл), випарюванням
або ж сорбцією.
.
Більш низькі концентрації ртуті можна
визначати екстрагуванням із більшого
об’єму проби (до 500 мл), випарюванням
або ж сорбцією.
При використанні атомно-абсорбційного аналізу вимірюють інтенсивність лінії 253,7 нм. Проводять безполуменевий аналіз на наявність іонів ртуті.
3.2.8 Визначення концентрації заліза
Залізо виявляють фото колориметричним методом в вигляді забарвленої сполуки із роданідом амонію в кислому середовищі тривалентне залізо утворює червону сполуку із роданідом. Склад сполуки неоднорідний, залежить від температури, РН розчину. Інтенсивність забарвлення пропорційна концентрації заліз у розчині. Прямим методом можна виявити 0,05 – 4 мг заліза на 1 літр води.
Крім реакції із роданідом використовують також реакцію із сульфосаліциловою кислотою та о-фенантроліном. Чутливість даних реакцій одного порядку як і у реакції із роданідом.
При використанні атомно-абсорбційного аналізу вимірюють інтенсивність лінії 248,3 нм. Горючий газ – ацетилен, окисник – повітря.
Висновки
Зростання кількості промислових стоків та викидів спричиняє посилений техногенний тиск на природне середовище. Окремі органічні та неорганічні речовини значною мірою змінюють органолептичні властивості води, або ж роблять її взагалі непридатною для споживання. Та промислових цілей. Тому технохімічний аналіз стічних та промислових вод є досить важливим завдання санітарно-епідеміологічних служб та заводських лабораторій. Розвиток техніки та технологій в останній час значною мірою покращив матеріальну базу лабораторій, більшість заводських лабораторій та лабораторій обласних СЕС обладнано сучасною технікою, що дозволяє проводити аналізи на сучасному технологічному рівні із використанням спектрометрії як у ІЧ-, УФ та рентгенівському діапазоні.
Проведення аналізу
та визначення важких металів у стічних
водах є досить важкою задачею, оскільки
потрібно забезпечити відбір проб у
польових умовах, забезпечити постійність
складу, тощо. Деякі вадкі метали можуть
міститися у стічних водах у досить малих
концентраціях, тому для концентрування
проб запропоновано досить багато
методів. Метод сорбції є одним із
найпростіших і може бути проведений у
польових умовах, із використанням
сорбційних фільтрів чи сорбційних
колонок. Це виключає проблему консервування
проб та їх транспортування в лабораторію.
В лабораторії аналізу можна буде піддати
тільки вже отримані сорбовані речовини.
Метод сорбції також дозволяє значною
мірою (до
 )
підвищити концентрацію важких металів
у аналізованому розчині. Використання
селективних сорбентів дозволяє виділяти
окремі метали із сумішей іонів чи
взвішених частинок.
)
підвищити концентрацію важких металів
у аналізованому розчині. Використання
селективних сорбентів дозволяє виділяти
окремі метали із сумішей іонів чи
взвішених частинок.
Метод сорбції є одним із перспективних методів концентрування важких металів, що дозволяє в подальшому покращити точність їх виявлення у стічних водах підприємств.
Список використаної літератури.
Васильев В. П. Аналитическая химия. В 2 кн. Кн. 2. Физико-химические методы анализа: Учеб. для студ. вузов, обучающихся по химико-технологическим специальностям – 2-е изд., перераб. и доп. - М.: Дрофа, 2002. - 384 с.
Глинка Н. Л. Общая химия. – Л.: Химия, 1988. – 702 с.
Гороновский И. Т., Назаренко Ю. П., Некряч Е. Ф. Краткий справочник по химии. – К.: Издательство АН СССР, 1962, 658 с.
Жарский И. М., Новиков И. Г. Физические методы исследования в неорганической химии. – М.: Высшая школа, 1988, - 271 с.
Зеликман А.Н., Коршунов Б.Г. Металлургия редких металлов. – М.:Металлургия, 1991.
Крешков А. П., Ярославцев А. А. Курс аналитической химии. – М.: Химия, 1964. – 430 с.
Кузьмин Н. М. Концентрирование следов элементов. – М.: Наука, 1988, - 267 с.
Лурье Ю. Ю. Аналитическая химия промышленных сточных вод. – М.: Химия, 1984.
Лурье Ю. Ю. Унифицированные методы анализа вод. – М.: Химия, 1973, - 376 с.
Меркин Э.Н. Экстракция металлов некоторыми органическими катионообменными реагентами - М.: Наука, 1968.
Моросанова С. А. Методы анализа природных и промышленных объектов. - М.: Издательство МГУ, 1988.
Москвин Л. Н., Царицина Л. Г. Методы разделения и концентрирования в аналитической химии. – Л.: Химия, 1991.
Муринов И. Ю. Экстракция металлов SN – органическими соединениями. - М.: Наука, 1993.
Некрасов Б. В. "Основы общей химии" т.1. - М.: Химия, 1973.
Определение малых концентраций элементов. Под ред. Ю. Ю. Лурье. - М.: Наука, 1986.
Ритчи Г. М., Эшбрук А. В. "Экстракция: принципы и применение в металлургии." Пер. с англ. - М.: Металлургия, 1983.
Скуг Д., Уэст Д. Основы аналитической химии. В 2 т. Пер. с англ. –М.: Мир, 1979, - 438 с.
Справочник химика. В 3-х т. - М.: Химия, 1966, - 1070 с.
Упор Андре Фотометрические методы определения следов неорганических соединений. – М.: Мир, 1985.
Физическая химия. Практическое и теоретическое руководство. Под ред. Б. П. Никольского, - Л.: Химия, 1987. – 875 с.
Химия и технология редких и рассеянных элементов. Ч. ІІІ. - М.: Высшая школа, 1976, - 320 с.
Химия: Справочное издание/ под ред. В. Шретер, К.-Х, Лаутеншлегер, Х. Бибрак и др.: Пер. с нем. – М.: Химия, 1989.– 648 с.
Химическая энциклопедия в 5 т. / под ред. И. Л. Кнунянца. – М.: Советская энциклопедия, 1990.
Ягодин Г.А., Синегрибова О.А., Чекмарев А.М. Технология редких металлов в атомной технике. - М.: Атомиздат, 1974.
2