Визначення теплоти розчинення і гідратації солі
Лабораторна робота № 1. „Визначення теплоти розчинення і гідратації солі”
Мета роботи:
Познайомитись з калориметричним методом вимірювання теплових ефектів.
Визначити теплоти розчинення безводного купрум (II) сульфату і мідного купоросу.
Визначити теплоту утворення кристалогідрату СuSО>4>•5Н>2>О з безводної солі.
На занятті необхідно:
Виконати роботу у відповідності до вимог даної методичної розробки.
Навчитись користуватись калориметром та визначати його теплоємність.
Розрахувати теплоту розчинення солі та теплоту гідратації.
Оформити звіт про виконану роботу і здати його викладачу.
Перелік обладнання та реактивів:
Калориметр;
термометр;
технохімічні ваги;
пробірки (3 шт.);
секундомір;
порцелянова ступка;
KNO>3>
СuSО>4>, СuSО>4>•5Н>2>О
Порядок виконання роботи:
Дослід 1. Визначення сталої калориметра
Суху пробірку попередньо зважити на технохімічних терезах.
Ретельно розтерти калій нітрат в порцеляновій ступці і засипати його у зважену пробірку приблизно на ¼ її висоти.
Зважити на технохімічних терезах пробірку з сіллю (з точністю до 0,01г). За різницею зважувань знайти масу солі, що повинна знаходитись в межах 4 -7 г. Отримані дані занести в таблицю 1.
У стакан калориметра налити 250 мл води, закрити калориметр кришкою і встановити в менший її отвір термометр, а в більший– пробірку з сіллю. (Для того щоб пробірка не провалювалась в калориметр на неї потрібно надіти гумове кільце!).
Вимірювання провести в три етапи (періоди): попередній, головний і заключний.
Ввімкнути калориметр в мережу змінного струму, потім ввімкнути тумблером мішалку, а через 1-2 хвилини– секундомір.
Попередній етап: вимірювання температури провести з точністю до 0,5°С через кожні 30 сек. протягом 5 хв.
Головний етап: не виключаючи секундоміра роз бити пробірку з сіллю так, щоб вся сіль висипалась у воду. Якщо температура змінюється дуже швидко, реєструвати її з меншою точністю.
Заключний етап: іще провести вимірювання температури через кожні 30 сек. протягом 5 хв. до встановлення рівномірного ходу температури (теж з точністю до 0,5°С).
Дані всіх вимірювань занести в таблицю 2.
Для розрахунку точної зміни температури на міліметровому папері побудувати графік, відкладаючи по вісі абсцис час, а по вісі ординат– зміну температури (масштаб на абсцисі- 1хв: 1см, а на ординаті– 1°К: 5см). З’єднані точки дадуть дві нахилені прямі для попереднього та заключного періодів. Їх продовжити вправо та вліво відповідно і через середину головного періоду провести пряму, паралельну до вісі ординат, до перетину її з продовженнями попередніх прямих. Відстань між точками перетину відповідає зміні температури при розчиненні солі.
Визначивши з графіка Δt>1>, розрахувати сталу калориметра (К):
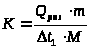
де Q>роз>- теплота розчинення солі ( -35,62 кДж/моль для KNO>3>);
m - маса нітрату калію;
М - молярна маса KNO>3> (101,1 г/моль );
Δt>1>- зміна температури при розчиненні солі.
Дослід 2. Визначення теплоти розчинення кристалогідрату (СuSО>4>•5Н>2>О)
Аналогічно до попереднього досліду зважують близько 5-7 г подрібненого мідного купоросу та вміщують його в пробірку, дані зважування заносять до таблиці 1.
Проводять вимірювання у відповідності до п.п. 6-10 попереднього досліду. Результати заносять в таблицю 2; будують графік, за яким визначають зміну температури при розчиненні солі (Δt>2>)
Визначають теплоту розчинення (Q>1>) солі за формулою:
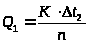 ,
,
де n - кількість речовини СuSО>4>•5Н>2>О.
Дослід 3. Визначення теплоти розчинення безводної солі (СuSО>4>)
Беруть наважку безводного сульфату міді масою 4-5г і проводять дослід аналогічно до попереднього. Дані заносять в таблицю 2. Будують відповідний графік і знаходять зміну температури при розчиненні безводної солі (Δt>3>).
Визначають теплоту розчинення (Q>2>) солі за формулою:
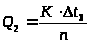 ,
,
де n - кількість речовини СuSО>4>.
Визначають теплоту утворення кристалогідрату (Q>3>) з безводної солі:
Q>3> = Q>2> – Q>1>
Розрахувати відносну похибку експерименту, якщо інтегральна теплота розчинення безводної солі +39,04кДж/моль, а кристалогідрату - рівна -11,72кДж/моль.
Результати всіх дослідів занести в таблиці 1 та 2.
Зробити відповідні висновки.
Результати роботи:
Дослід 1. Визначення сталої калориметра
Розрахунок маси наважки солі KNO>3>:
Таблиця 1.1
|
Пробірка з сіллю, г |
22,33 |
|
Пуста пробірка, г |
17,50 |
|
Сіль, г |
4,83 |
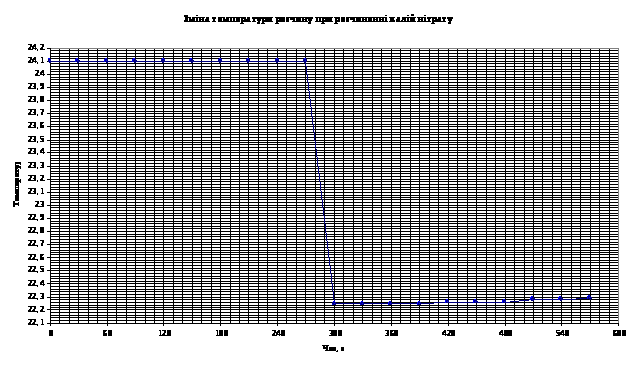
Температурні показники для розчину солі KNO>3>:
Таблиця 1.2
|
Температура |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
до розчинення |
24,10 |
24,10 |
24,10 |
24,10 |
24,10 |
24,10 |
24,10 |
24,10 |
24,10 |
24,10 |
|
після розчинення |
22,25 |
22,25 |
22,25 |
22,25 |
22,26 |
22,26 |
22,26 |
22,28 |
22,28 |
22,29 |
Розрахунок сталої калориметра:
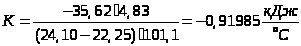
Дослід 2. Визначення теплоти розчинення кристалогідрату (СuSО>4>•5Н>2>О)
Розрахунок маси наважки солі СuSО>4>•5Н>2>О:
Таблиця 2.1
|
Пробірка з сіллю, г |
23,50 |
|
Пуста пробірка, г |
17,50 |
|
Сіль, г |
6,00 |
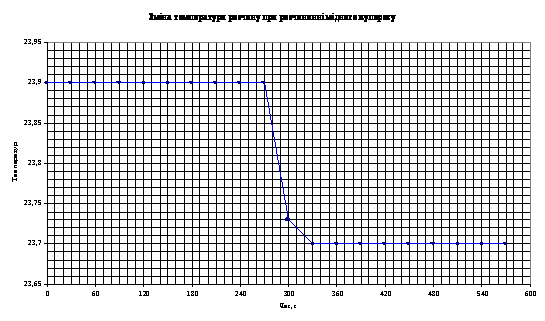
Температурні показники для розчину солі СuSО>4>•5Н>2>О:
Таблиця 2.2
|
Температура |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
до розчинення |
23,90 |
23,90 |
23,90 |
23,90 |
23,90 |
23,90 |
23,90 |
23,90 |
23,90 |
23,90 |
|
після розчинення |
23,73 |
23,70 |
23,70 |
23,70 |
23,70 |
23,70 |
23,70 |
23,70 |
23,70 |
23,70 |
Розрахунок теплоти гідратації солі СuSО>4>•5Н>2>О:
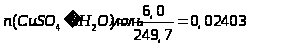 ;
;
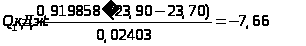
Дослід 3. Визначення теплоти розчинення безводної солі (СuSО>4>)
Розрахунок маси наважки солі СuSО>4>:
Таблиця 3.1
|
Пробірка з сіллю, г |
22,00 |
|
Пуста пробірка, г |
17,50 |
|
Сіль, г |
4,50 |
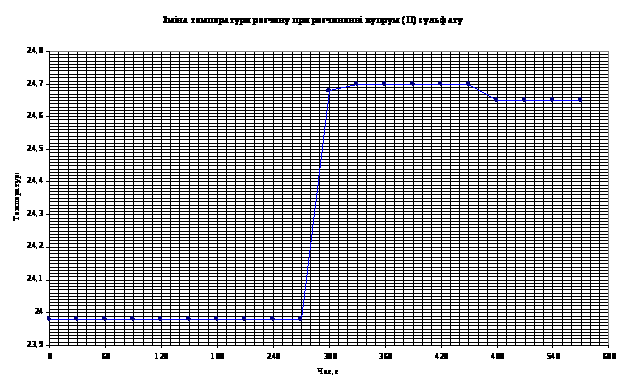
Температурні показники для розчину солі СuSО>4>:
Таблиця 3.2
|
Температура |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
до розчинення |
23,98 |
23,98 |
23,98 |
23,98 |
23,98 |
23,98 |
23,98 |
23,98 |
23,98 |
23,98 |
|
після розчинення |
24,68 |
24,70 |
24,70 |
24,70 |
24,70 |
24,70 |
24,65 |
24,65 |
24,65 |
24,65 |
Розрахунок теплоти гідратації солі СuSО>4>:
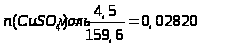 ;
;
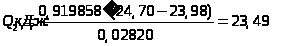
Визначення теплоти утворення кристалогідрату з безводної солі:
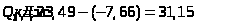
Розрахунок відносної похибки досліду:
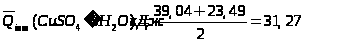
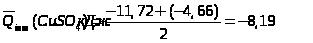
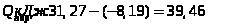
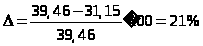
Висновок:
В процесі виконання роботи ми познайомились з калориметричним методом вимірювання теплових ефектів, визначили теплоти розчинення безводного купрум (II) сульфату і мідного купоросу, визначили теплоту утворення кристалогідрату СuSО>4>•5Н>2>О з безводної солі.