Кипение
Кипение – процесс парообразования в объеме перегретой жидкости (температура > температуры насыщения). Характеризуется образованием новых поверхностей раздела фаз.
Сведения о жидкостях.
Характерно сохранение объема, но принимает форму сосуда в котором она находится. Для жидкостей характерно сохранение ближнего порядка расположения молекул.
Френкель предложил такое строение жидкости: если рассмотреть объем жидкости, то молекула совершает колебательное движение около положения равновесия и перескакивает на другое место.
Продолжительность колебания для определенного вещества при определенной температуре – величины определенные с увеличением температуры длительность колебаний уменьшается и в пределе жидкость ведет себя как газ, снижается вязкость жидкости.
Поверхностное натяжение жидкости.
Рассмотрим некоторый объем жидкости имеющую свободную поверхность.
Т.о. поверхностный слой жидкости обладает дополнительной энергией, которая является основной составляющей внутренней энергии жидкости. Жидкость ведет себя как бы она была заключена в упругую оболочку. Система стремится занять положение соответствующее минимуму энергии.
Рассмотрим каплю жидкости в газе или паровой пузырь находящийся в жидкости.
Рассечем каплю жидкости и рассмотрим две полусферы


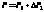
Средняя
длина поверхности :

Для
сферы
 т.к.
т.к.

Для
плоскости

Сфера

Плоскость

Формула
Лапласа
поправка Лапласа на избыточное давление.
Всё сказанное о силах поверхностного натяжения применительно жидкости справедливо и для твердых тел, поэтому при рассмотрении явлений на границе раздела фаз нельзя говорить о поверхностном натяжении какой-либо среды, надо рассматривать их во взаимодействии.
Граница раздела принимает форму соответствующего минимального суммарного раздела.
схема
сил действующих на линии раздела трех
фаз.


 -
краевой угол смачивания, определяется
как угол отсчитываемый внутри жидкости
и образованный касательными.
-
краевой угол смачивания, определяется
как угол отсчитываемый внутри жидкости
и образованный касательными.
 полное смачивание
полное смачивание

 жидкость абсолютно
не смачивает поверхность,
жидкость абсолютно
не смачивает поверхность,
 .
.
Внутренние характеристики кипения.
Для
роста пузырька пара давление внутри
этого пузырька должно быть больше сил
давления поверхностного натяжения и
внешнего давления



кривая упругости пара над плоской поверхностью (1), над вогнутой поверхностью (2).
 уравнение
Клапейрона-Клазиуса.
уравнение
Клапейрона-Клазиуса.
 удельные
объемы
удельные
объемы
 энтропии.
энтропии.
 ;
;

 ;
;
 ;
;




 число зародышей
пара.
число зародышей
пара.

Рост пузырька происходит от конечного размера, радиуса, который характеризуется свойствами поверхности.
Возьмем
воду при
 и определим критические радиусы пузырька
при различных перегревах.
и определим критические радиусы пузырька
при различных перегревах.




Минимальная работа образования пузырей критического размера.
 работа затрачиваемая
на образование пара.
работа затрачиваемая
на образование пара.
Первое слагаемое – работа расширения, второе – работа создание новой межфазной поверхности.
 избыточное давление.
избыточное давление.

 т.к.
т.к.

V
– объем пузырька,

F
– площадь поверхности пузырька,
 .
Подставим в нач. у-е и получим:
.
Подставим в нач. у-е и получим:


Отсюда следует:

С
увеличением перегрева
 работа
образования пузырька уменьшается. На
твердой поверхности силы сцепления
между молекулами жидкости и твердого
тела меньше нежели между молекулами
жидкости. Вероятность образования
пузырька на поверхности больше чем в
жидкости.
работа
образования пузырька уменьшается. На
твердой поверхности силы сцепления
между молекулами жидкости и твердого
тела меньше нежели между молекулами
жидкости. Вероятность образования
пузырька на поверхности больше чем в
жидкости.
Отрывной диаметр парового пузыря.
Отрывной
диаметр
 соответствует
среднестатистическому объему пузыря
в момент отрыва. Его значение определяется
по формуле:
соответствует
среднестатистическому объему пузыря
в момент отрыва. Его значение определяется
по формуле:


выражение под корнем представляет собой капиллярную постоянную Лапласа. Эта величина часто используется в качестве характерного размера в безразмерных уравнениях описывающих свойства безфазных потоков.
Форма пузыря зависит от соотношения между силами вязкости и инерции. В случае преобладания сил вязкости пузырь имеет сферическую форму. При больших скоростях роста паровых пузырей, а это может происходить при пониженных давлениях преобладают силы инерции.
Скорость роста парового пузырька.
r
– теплота парообразования. Рассмотрим
баланс теплоты. Через межфазную
поверхность через время
 передается количество теплоты. За этот
же период размер пузыря увеличивается
на dV.
передается количество теплоты. За этот
же период размер пузыря увеличивается
на dV.

 ;
;

 ;
;

 Рассмотрим плотность
теплового потока на границе межфазной
поверхности. Предложили Фриц и Энде.
Рассмотрим плотность
теплового потока на границе межфазной
поверхности. Предложили Фриц и Энде.

Принебрегая кривизной поверхности раздела фаз воспользуемся решением для плоской поверхности.

 выразим dR
выразим dR

Проинтегрировав данное выражение получим:
 далее
имеем:
далее
имеем:

Ja – число Якоба, характеризует соотношение между теплотой перегрева и теплотой парообразования.
Частота отрыва пузырей.
т. С – отрыв пузырька.
ДА – рост температуры стенки до образования нового пузырька.
 время от начала
образования пузырька до его отрыва.
время от начала
образования пузырька до его отрыва.
 время
ожидания.
время
ожидания.
Частота отрыва пузырьков:



 где
где

 ,
W’’-
средняя за цикл скорость роста пузыря.
Для воды W’’=0,48
м/с
,
W’’-
средняя за цикл скорость роста пузыря.
Для воды W’’=0,48
м/с
Число действующих центров парообразования.
 С ростом температуры
стенки все большее число неровностей,
шероховатостей становится центрами
парообразования.
С ростом температуры
стенки все большее число неровностей,
шероховатостей становится центрами
парообразования.
При


Интенсивность теплообмена при парообразовании.
Кипение – процесс парообразования в объеме перегретой жидкости (температура > температуры насыщения).
Кипение классифицируют по следующим признакам:
пузырьковое и пленочное;
по виду конвекции у поверхности теплообмена. При свободной и вынужденной конвекции;
по отношению к температуре насыщения. Без недогрева и кипение с недогревом;
По ориентации поверхности кипения в пространстве. На горизонтальных наклонных и вертикальных поверхностях;
По характеру кипения. Развитое и неразвитое, неустойчивое кипение.
Неразвитое – число центров парообразования невелико.
Неустойчивое – кипение случайным образом сменяется конвекцией.
Наиболее часто встречающийся – кипение в большом V на горизонтальной поверхности.
Характерный размер паровой фазы << характерного размера поверхности на которой происходит кипение.
Образуются паровые пузыри, которые увеличиваются, достигают отрывных диаметров и отрываются. В процессе всплытия рост пузырьков продолжается.
Кипение при недогреве – пузырьки растут у основания, отрываются и схлопываются.
В
первом случае пузырьки оторвались,
всплывают и растут в V.
Теплообмен при кипении характеризуется
коэффициентом теплоотдачи
 ,
а это позволяет отводить высокие
плотности тепловых потоков при низких
,
а это позволяет отводить высокие
плотности тепловых потоков при низких
 .
Кипение может быть в трубах, на трубах,
в порах, щелях.
.
Кипение может быть в трубах, на трубах,
в порах, щелях.
Способы подвода тепла теплообменной поверхности:
граничные условия первого рода;
граничные условия второго рода (q=const);
Г.у.
первого рода (t=const)
можно обеспечить либо за счет фазового
перехода, либо за счет

Кривая кипения.
Это
зависимость
 от
от
 .
.
Представляет наиболее реальный процесс кипения.
В области 1 – конвективный теплообмен.
В области В – плотность достигает такой величины, что начинают активизироваться первые центры парообразования. Значительная доля теплоты отводится конвекцией.
Область
1:

 ламинарный
режим;
ламинарный
режим;
 турбулентный
режим.
турбулентный
режим.
Зона 2а – количество центров парообразования невелико и значительная часть тепла отводится конвекцией.
Зона 2б – развитое пузырьковое кипение.
В т.С пузырьков пара настолько много и частота отрыва их настолько велика, что отдельные пузырьки пара начинают сливаться в отдельные паровые пленки.
т.С
– точка кризиса теплообмена, q
– достигает своего максимума
 .
.
Д – пленочное кипение.
Область
2б

Область 4 – режим пленочного кипения.
Коэффициент теплоотдачи при кипении в большом объеме.


 - объем пузыря,
- объем пузыря,
 - плотность пара, F
– частота отрыва,
- плотность пара, F
– частота отрыва,
 - количество центров
парообразования.
- количество центров
парообразования.


 - капиллярная
постоянная Лапласа.
- капиллярная
постоянная Лапласа.



формула Кутателадзе.


 формула
Лабунцова
формула
Лабунцова







для воды при P<5 МПа:






 - чем меньше отношение,
тем больше работа пузыря. Отложение на
поверхности увеличивают шероховатость.
Сами отложение имеют низкое
- чем меньше отношение,
тем больше работа пузыря. Отложение на
поверхности увеличивают шероховатость.
Сами отложение имеют низкое
 .
Сам слой создает дополнительное
термическое сопротивление.
.
Сам слой создает дополнительное
термическое сопротивление.

Кризисы теплоотдачи.
Называется процесс связанный с коренным изменением механизма и интенсивности теплообмена.
Будем медленно увеличивать плотность теплового потока.
С
ростом плотности теплового потока у
нас увеличивается
 ,
а следовательно растет коэффициент
парообразования.
,
а следовательно растет коэффициент
парообразования.
Увеличение частоты отрыва приводит к тому, что пузыри догоняют друг друга и сливаются в столбики пара.
Увеличение центров парообразования приводит к слиянию паровых пузырей отдельных ЦПО – движутся столбики пара.
Динамический
напор пара оценивается как
 .
Силы, которые стабилизируют систему
оцениваются величиной
.
Силы, которые стабилизируют систему
оцениваются величиной

 капиллярная
постоянная.
капиллярная
постоянная.
В момент кризиса отношение этих величин есть величина постоянная.



В
итоге так как у нас
 то
получаем
то
получаем

k – критерий устойчивости, характеризует меру отношения энергии динамического напора пара к энергии необходимой для ускорения частиц жидкости k=0,13…0,16 .




Второй кризис.
Разрушение паровой пленки при постоянном q приводит к переходному режиму. Величина зависит от рода жидкости, давления и физических и геометрических свойств поверхности.
С
возрастанием
 доля конвективного теплообмена
уменьшается, а доля лучистого теплообмена
возрастает.
доля конвективного теплообмена
уменьшается, а доля лучистого теплообмена
возрастает.
Влияние скорости движения жидкости на теплоотдачу при кипении.
На перегретый слой кроме возмущающего действия пузырей также воздействует турбулентные пульсации двухфазного потока. Движущиеся жидкость оказывает влияние на теплообмен.
1
– постоянная
 не зависимо от W,
она определяется кипением.
не зависимо от W,
она определяется кипением.
2
– совместное влияние скорости и плотности
теплового потока.

 при
при


3
-
 от скорости зависит в степени 0,8
от скорости зависит в степени 0,8
 .
Коэффициент теплоотдачи будет определяться
только конвекцией и кипение можно не
учитывать.
.
Коэффициент теплоотдачи будет определяться
только конвекцией и кипение можно не
учитывать.
Кризис при движении в двухфазном потоке.
Причиной
возникновения кризиса является нарушение
контакта жидкости с твердой поверхностью.
Повышение температуры в момент кризиса
может составлять от 1…100 градусов
цельсия. Кризис т/о объединяет ряд
процессов, которые приводят к ухудшению

и повышению температуры стенки.
А) кризис при течении недогретой жидкости, поверхностное кипение.
Резкое повышение температуры стенки, стенка может разрушиться.
Б) слабо догрета до температуры кипения.
Пузырьковое кипение. Кризис возникает в следствии нарушения устойчивости структуры двух фазного граничного слоя.
В) кризис в дисперсно кольцевом потоке. Жидкость движется в виде пленочки.
Г) кризис при дисперсном потоке. Капли несутся с паром и выпадают на поверхность орошая ее. Кризис наступает при недостаточном орошении поверхности каплями жидкости.
Теплообмен при кипении внутри труб.
Двухфазный поток называется адиабатным если отсутствует тепловой поток между стенкой и потоком. Если фазы жидкие и паровая имеют одинаковую температуру, то поток называется термодинамически равновесным.
Рассмотрим параметры двухфазного потока, расходные и истинные.
Рассмотрим сечение трубы.


Х – массовое расходное паросодержание.
 - объемное расходное
паросодержание.
- объемное расходное
паросодержание.



 - приведенная скорость
пара.
- приведенная скорость
пара.
 - истинная скорость
пара.
- истинная скорость
пара.


 -
истинное паросодержание.
-
истинное паросодержание.


 относительная
балансовая энтальпия.
относительная
балансовая энтальпия.
