Кислородосодержащие органические соединения
Реферат по химии
на тему:
«Кислородосодержащие органические соединения».
Выполнила: ученица 11б класса
школы № 34
Горбатовская О.
Проверила: Богданова Л.В.
Таганрог
2001
Содержание:
I. Общая характеристика:
спирты;
фенолы;
жиры – сложные эфиры;
альдегиды;
карбоновые кислоты.
II. Жиры:
структура молекул;
химические свойства;
распространение в природе;
применение.
III. Синтетические моющие свойства.
IV. Список литературы.
I.
Спирты – гидроксильные производные углеводородов различных типов.
Для гидроксильных производных бензола и его гомологов, содержащих ОН-группу непосредственно у бензольного ядра, употребляют название фенолы.
По химической природе жиры – это сложные эфиры трехатомного спирта глицерина и высших одноосновных кислот.
Для альдегидов характерно присутствие в молекуле кислорода, связанного двойной связью с атомом углерода.
Органические соединения, содержащие в качестве функциональной группы карбоксил, носят название карбоновых кислот. В зависимости от характера радикала, с которым связана карбоксильная группа, различают кислоты предельные, непредельные, ароматические и т.д. По числу имеющихся в молекуле карбоксильных групп их подразделяют на одноосновные, двухосновные и т.д.
II.
Жиры – вещества главным образом животного и растительного происхождения, состоящие в основном из сложных эфиров глицерина и одноосновных высших карбоновых кислот (триглицеридов):
СН>2> – ООС – R

CH – OOC – R

CH>2> – OOC – R
Чаще всего в состав жиров входят насыщенные кислоты - пальмитиновая С>15>Н>31>СООН, стеариновая С>17>Н>35>СООН и ненасыщенная кислота – олеиновая С>17>Н>33>СООН. В небольших количествах в природных жирах находятся также и другие предельные одноосновные кислоты от С>4 >до С>24> и непредельные кислоты с несколькими двойными связями. При этом в составе природных жиров встречаются исключительно кислоты с четным числом углеродных атомов. Это связано с характером обмена веществ в животных и растительных организмах.
Исследуя жиры, французский химик М.Э. Шеврель установил, что жиры состоят из глицерина и кислот, получивших название жирных. В дальнейшем это название было распространено вообще на соединения, содержащие нециклический углеводородный радикал. И сегодня еще употребительно для этих соединений название соединения жирного ряда. Синтез жиров из глицерина и жирных кислот был впервые осуществлен в 1854г. М. Бертло.
Вместе с белками и углеводами жиры входят в число важнейших с биохимической точки зрения веществ. Поступающие с пищей жиры в процессе пищеварения расщепляются на глицерин и жирные кислоты; эти вещества всасываются в кишечнике, затем из них вновь синтезируются жиры. Жиры источник энергии в организме; калорийность чистого жира 3770 кДж (900 ккал)/100 г.
Жиры разного происхождения внешне различаются прежде всего по своему физическому состоянию: они бывают твердыми (животные жиры) и жидкими (растительные масла: жирные, растительные жиры, получаемые из семян и плодов растений отжимом или экстрагированием. Различают р.м. твердые и (чаще) жидкие; высыхающие (льняное, конопляное), полувысыхающие (подсолнечное, хлопковое), невысыхающие (касторовое, кокосовое). Многие р.м. – важные пищевые продукты; их используют также для производства маргарина, мыла, олифы, лаков и др.). При химическом исследовании жиров было выяснено, что в твердых жирах преобладают триглицериды предельных кислот (пальмитиновой, стеариновой), в жидких – содержится значительный процент триглицерида непредельной (олеиновой) кислоты. В индивидуальном виде эти триглицериды имеют следующие точки плавления: трипальмитин +65оС, тристеарин +72оС, триолеин – 4оС.
В коровьем масле в отличие от других жиров содержится в некотором количестве также эфир глицерина с низкомолекулярной масляной кислотой – трибутирин. Отсюда масляная кислота и получила свое название. Осуществляя гидрогенизацию жиров (присоединение к ним водорода в присутствии никелевого катализатора), в промышленном масштабе превращают жидкие жиры в твердые, идущие на производство маргарина, а также для других целей.
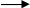
Старейшее техническое использование жиров – получение мыла. Если жир нагреть со щелочью, то происходит (как у всякого сложного эфира) его гидролиз с образованием глицерина и солей жирных кислот, которые и составляют мыло:
С Н>2>
– ООС – С>17>Н>35> СН>2>
– ОН
Н>2>
– ООС – С>17>Н>35> СН>2>
– ОН
С
 Н
– ООС – С>17>Н>35>
+ 3NаОН СН
– ОН + 3С>17>Н>35>СООNа
Н
– ООС – С>17>Н>35>
+ 3NаОН СН
– ОН + 3С>17>Н>35>СООNа
СН>2> – ООС – С>17>Н>35> СН>2> – ОН
Часто употребляемое для процессов гидролиза второе название – омыление обязано своим происхождением этому старинному процессу.
Технически более удобный способ расщепления жиров основан на использовании кислых катализаторов: серной кислоты, сульфокислот нафтеновых углеводородов (так называемый контакт Петрова), продуктов сульфирования касторового масла (реактив Твитчеля). В последнем случае жирные кислоты выделяются в свободном виде, легко отделяются от глицерина и уже потом перерабатываются действием щелочей (едкий натр, сода) на мыло или используются для других целей.
Моющее действие мыла основано на сложных физико-химических процессах. Являясь солью слабой кислоты и сильного основания, мыло в воде подвергается гидролизу:
С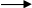
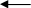 >17>Н>35>СООNа
+ Н>2>О
С>17>Н>35>СООН
+ NаОН
>17>Н>35>СООNа
+ Н>2>О
С>17>Н>35>СООН
+ NаОН
Выделяющаяся при гидролизе щелочь в некоторой степени обусловливает моющее действие мыла, однако главную роль играют процессы эмульгирования, связанные с изменением поверхностного натяжения воды под действием мыла.
Для получения мыла расходуются значительные количества жиров. Сокращение расходов пищевого сырья для технических целей достигается двумя путями. Во-первых, высокомолекулярные жирные кислоты, необходимые для производства мыла, получают не только из жиров, но и окислением парафина – смеси высокомолекулярных углеводородов, выделяемых из нефти. Окисление проводят, продувая воздух через расплавленный парафин при температуре около 100оС. катализаторами служат окислы марганца.
Второй путь уменьшения расхода жиров на технические нужды – замена мыла другими моющими средствами.
III.
Синтетические моющие средства.
Основу синтетических моющих средств составляют поверхностно-активные (обладающие способностью понижать поверхностное натяжение) органические вещества, характерной структурной особенностью которых является наличие длинной углеродной цепи и ионогенной группы. Последняя чаще всего представляет собой соль сульфокислоты. Такие вещества можно получить, например, одновременным действием хлора и сернистого газа (сульфохлорирование) на парафиновые углеводороды с 10-14 углеродными атомами и последующей обработкой полученных сульфохлоридов щелочами:
С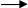 >10>Н>22>+SО>2>+Сl>2>
С>10>Н>21>SО>2>Cl+HCl
>10>Н>22>+SО>2>+Сl>2>
С>10>Н>21>SО>2>Cl+HCl
C >10>H>21>SO>2>Cl+2NaOH
C>10>H>21>SO>2>ONa+NaCl+H>2>O
>10>H>21>SO>2>Cl+2NaOH
C>10>H>21>SO>2>ONa+NaCl+H>2>O
В качестве сырья используют также ароматические углеводороды с длинной боковой цепью, подвергая их действию хлорсульфоновой кислоты:
HSO>3>Cl NaOH
C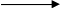
 >8>H>17>
– C>6>H>5
> C>8>H>17>
– C>6>H>4>
– SO>3>H
C>8>H>17>
– C>6>H>4>
– SO>3>Na
>8>H>17>
– C>6>H>5
> C>8>H>17>
– C>6>H>4>
– SO>3>H
C>8>H>17>
– C>6>H>4>
– SO>3>Na
Соли кислых сульфатов высокомолекулярных спиртов также являются поверхностно-активными веществами:
SO>3 > NaOH
C
 >12>H>25>OH
C>12>H>25>OSO>3>H
C>12>H>25>OSO>3>Na
>12>H>25>OH
C>12>H>25>OSO>3>H
C>12>H>25>OSO>3>Na
Перечисленные типы соединений образуют класс анионоактивных поверхностно-активных веществ, поскольку главную роль в них играет органический анион. В качестве катиона в состав таких поверхностно-активных веществ может входить не только натрий, но и калий, аммоний, органические основания – амины. Анионоактивные соединения – самый распространенный тип поверхностно-активных веществ.
Органический остаток может существовать также и в виде катиона, чаще всего в форме четвертичной аммониевой соли [R>4>N]+X-. Подобные вещества называют катионоактивными. Третий тип поверхностно-активных веществ содержит в органическом остатке как катионную, так и анионную группу. Такие вещества относятся к числу амфотерных. Наконец, известны и неионогенные поверхностно-активные вещества.
Моющие средства, используемые на практике, помимо того или иного вида поверхностно-активных веществ, содержат различные добавки, способствующие усилению моющего действия, это некоторые неорганические вещества щелочного характера (сода, различные фосфаты и др.). Кроме того, добавляют вещества, способствующие стабилизации пены, оптические отбеливатели (органические соединения, преобразующие поглощенный ими ультрафиолетовый свет в видимый голубой, повышая тем самым белизну ткани).
Современные синтетические моющие вещества не только являются полноценными заменителями мыла, но и превосходят его по некоторым свойствам. Так, обычное мыло теряет свое моющее действие в жесткой или морской воде. Происходит это из-за образования нерастворимых кальциевых солей жирных кислот:
2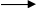 С>17>H>35>COONa+Ca(HCO>3>)>2>
(C>17>H>35>COO)>2>Ca+2NaHCO>3>
С>17>H>35>COONa+Ca(HCO>3>)>2>
(C>17>H>35>COO)>2>Ca+2NaHCO>3>
Синтетические моющие средства не обладают этим недостатком. Кроме того, из-за своей меньшей щелочности они меньше разрушают ткань. Все это привело к тому, что ныне производство синтетических моющих средств достигло больших размеров.
Отмечено вместе с тем и нежелательное побочное действие синтетических моющих средств: когда вода, содержащая их, в больших количествах попадает в реки, это вызывает сильное образование пены и ухудшает условия существования рыб и других обитателей рек. Поэтому сейчас стремятся выпускать моющие средства сравнительно нестойкие, легко подвергающиеся деструкции в природных условиях, биологическому разрушению. Такими свойствами прежде всего обладают алкилсульфонаты, в меньшей степени – алкилсульфаты. Хуже всего в этом отношении алкилбензолсульфонаты с разветвленной углеводородной цепью.
Список литературы:
В.М. Потапов «Органическая химия», М., «Просвещение»,1983г.
«Большая Российская энциклопедия», Научное издательство, М., 1998г.