Лабораторная работа по химии 1-3 (NPI)


 Кафедра
Кафедра
Инженерной
экологии
ГИДРОЛИЗ СОЛЕЙ

 №5
№5
 Цель
работы: изучить условия протекания
процессов гидролиза солей и влияние
факторов, обуславливающих смещение
ионного равновесия при гидролизе.
Цель
работы: изучить условия протекания
процессов гидролиза солей и влияние
факторов, обуславливающих смещение
ионного равновесия при гидролизе.
Оборудование и материалы: штатив с пробирками, растворы солей, кислот, щелочей, индикаторы, кристаллы солей, спиртовая горелка, пипетка.
Выполнение работы.
Опыт №1 Смещение ионного равновесия в растворах вследствие гидролиза В разные пробирки внесем небольшое количество следующих соединений: НС1, NaOH, NaCl, Ма>2>СОз, ZnCl>2>, Си(СНзСОО)2. Во все пробирки приливаем одинаковое количество воды и осторожным встряхиванием добиваемся полного растворения каждой соли. Полосками универсальной индикаторной бумаги измерим рН каждого раствора. Для сравнения такой же бумажкой измерим рН дистиллированной воды. Данные опыта сведены в таблицу
|
Формула соединения |
Сила кислоты и основания образующих данную соль |
Цвет индикаторной бумаги |
Реакция среды |
|
|
Na>2>CO>3> |
||||
|
NaGl, |
||||
|
ZnCl>2> |
||||
|
Cu(CH>3>COO)>2> |
Составим сокращенные ионные уравнения гидролиза солей и объясним изменение окраски индикаторной бумаги в растворах солей в сравнении с окраской ее в дистиллированной воде.
_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт №2 Усиление гидролиза одной соли раствором другой гидролизирующей соли
К 3 мл
концентрированного раствора РеС1з
(соль образована слабым основанием и
слабой
кислотой, ее гидролиз протекает
в основном только по 1-ой ступени) прильем
немного
концентрированного раствора
Ка>2>СОз (соль образована, напротив,
сильным основанием и
слабой кислотой,
ее гидролиз также протекает в основном
только по 1-ой ступени) до
образования
устойчивого осадка. При этом наблюдается
выделение пузырьков. В результате
сливания
двух вышеуказанных растворов происходит
образование соли, полученной из
слабых
оснований и кислоты. Эта соль
подвергается полному гидролизу. Напишем
молекулярные и
ионные уравнения
реакции:
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт №3 Растворение металлов в продуктах гидролиза солей
В первую пробирку нальем 3-4 мл концентрированного раствора ZnCl>2> и опустим в нее кусочек цинка. В другую пробирку нальем столько же концентрированного раствора Na>2>COs и
опускаем в этот раствор кусочек алюминия. Нагревая пробирки, наблюдаем растворение металлов и выделение газа в обоих случаях. Составим уравнения реакций и объясним наблюдаемые явления.
_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт №4 Влияние температуры на степень гидролиза солей В две пробирки нальем по 3-4 мл концентрированного раствора ZnCb и по 2 кацли индикатора - метилового оранжевого. Одну пробирку поставим в штатив, другую нагреваем почти до кипения. Сравним окраску индикатора в обеих пробирках. После остывания снова сравним окраску и объясним изменение окраски индикатора при нагревании раствора ZnCl>2>.
____________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт №5 Влияние концентрации раствора соли на степень ее гидролиза Вносим в пробирку немного кристаллов соли SnCb, 1 каплю 2,5 М НС1 и 10 капель дистиллированной воды. Встряхиванием пробирки добиваемся растворения кристаллов. Затем в пробирку прибавим еще 10 капель дистиллированной воды. Наблюдается выпадение осадка SnOHCl. Следовательно, разбавление (уменьшение концентрации соли) приводит к увеличению степени ее гидролиза. Составим молекулярное и ионное уравнения:
__________________________________________________________________________________________________________________________________________________________________
Опыт №6 Подавление гидролиза соли
В пробирку с осадком SnOHCl, взятую из предыдущего опыта, прибавим 3-4 капли 2,5 М раствора НС1. При этом происходит растворение осадка. Сделаем выводы относительно смещения равновесия реакции гидролизаОбщий вывод по работе:
____________________________________________________________________________________________________________________________________________________________________
Общий вывод по работе:
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
|
Работу выполнил Студент группы |
Работу принял Преподаватель |
Дата |
|
Ф.И.О. |
|
К

 афедра
Определение эквивалентной
Лабораторная работа №1
афедра
Определение эквивалентной
Лабораторная работа №1
инженерной массы металла по объему
экологии выделенного водорода
Цель работы: ознакомиться с методикой определения и расчета молярной массы эквивалента металлов.
Оборудование и материалы:
штатив, две бюретки на 50
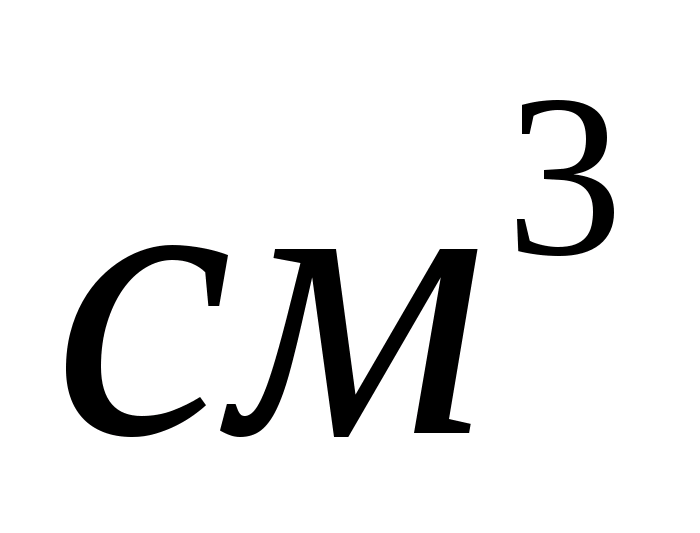 ,
пробирка с газоотводной трубкой,
термометр, барометр, аналитические весы
и разновес, навеска металла около 0,01 г,
2,5М раствор HCl.
,
пробирка с газоотводной трубкой,
термометр, барометр, аналитические весы
и разновес, навеска металла около 0,01 г,
2,5М раствор HCl.
Методика выполнения работы.
По объему вытесненного водорода можно определить молярные массы эквивалентов активных металлов (магния, алюминия, цинка и т.д.), способных вытеснять водород из разбавленных кислот.
Прибор для определения молярной
массы эквивалента металлов, изображенный
на рисунке, состоит из:
Двух бюреток на 50
 ,
соединенных
,
соединенных
резиновой трубкой;
Реакционной пробирки;
Газоотводной трубки;
Штатива.
Перед началом работы испытывают прибор на герметичность. Для этого соединяют верхний конец правой бюретки с пробиркой, опускают левую бюретку на 15-20 см, и наблюдают 3-5 мин. За положением уровня воды в ней. Если прибор герметичен, то уровень воды в бюретке за это время не изменится. При понижении уровня нужно исправить дефект в приборе.
После этого наливаем в пробирку
4,5
 2,5М раствора хлористо-водородной кислоты,
5 капель раствора
2,5М раствора хлористо-водородной кислоты,
5 капель раствора
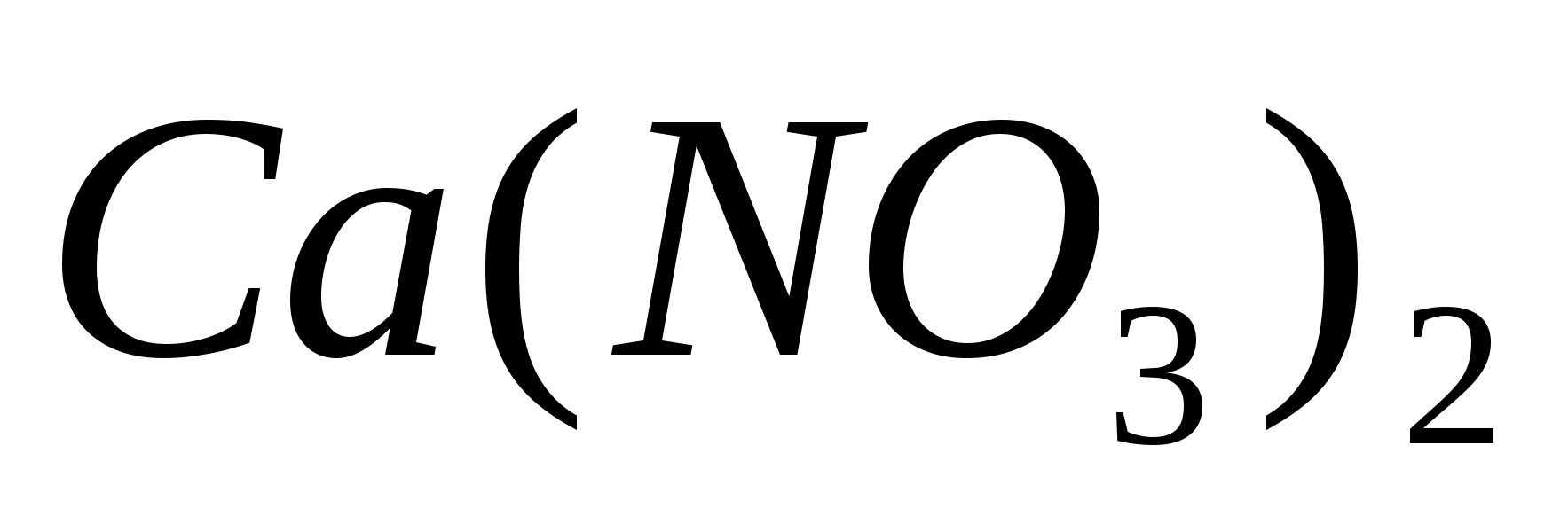 катализатора. Папиросную бумагу с
навеской металла смачивают каплей воды
и приклеивают к внутренней стенке
пробирки над кислотой. Пробирку с
кислотой и металлом плотно присоединяют
к прибору; бюретки устанавливаем так,
чтобы уровни воды в них были одинаковы.
катализатора. Папиросную бумагу с
навеской металла смачивают каплей воды
и приклеивают к внутренней стенке
пробирки над кислотой. Пробирку с
кислотой и металлом плотно присоединяют
к прибору; бюретки устанавливаем так,
чтобы уровни воды в них были одинаковы.
Записываем показания бюретки до опыта. Затем встряхиваем пробирку, и металл попадает в кислоту. Тотчас начинается выделение водорода и вода вытесняется из правой бюретки в левую. Левую бюретку при этом надо опускать и во время опыта держать воду на одном уровне, чтобы давление газа внутри прибора было все время близко к атмосферному.
Пока идет реакция, мы записываем показания барометра и термометра; по таблице определяем давление насыщенных паров воды.
Когда весь металл растворился, прекратится понижение уровня воды в бюретке. Окончательно точный отчет показаний бюретки производится после охлаждения прибора до комнатной температуры (через 10-15 мин.)
Результаты измерений записываем в форме:
Масса
металла,
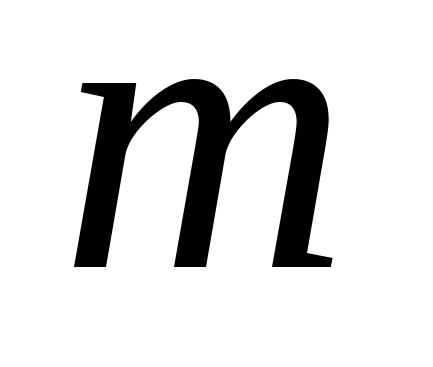 = ,
= ,
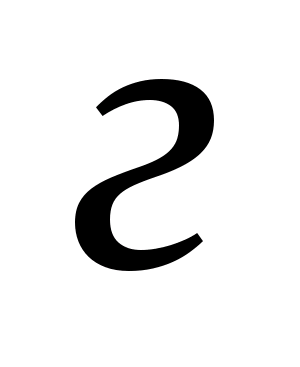 .
.
Показания
бюретки до проведения реакции,
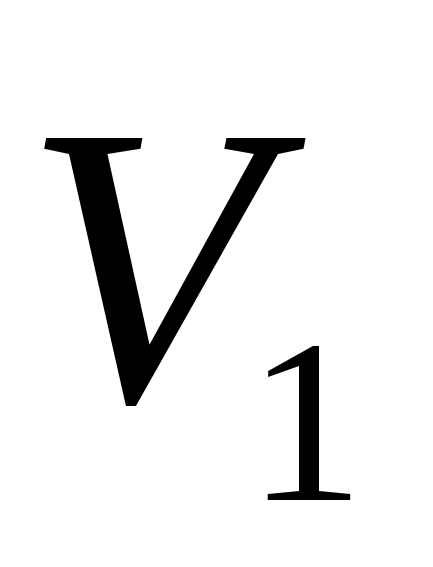 = ,
= ,
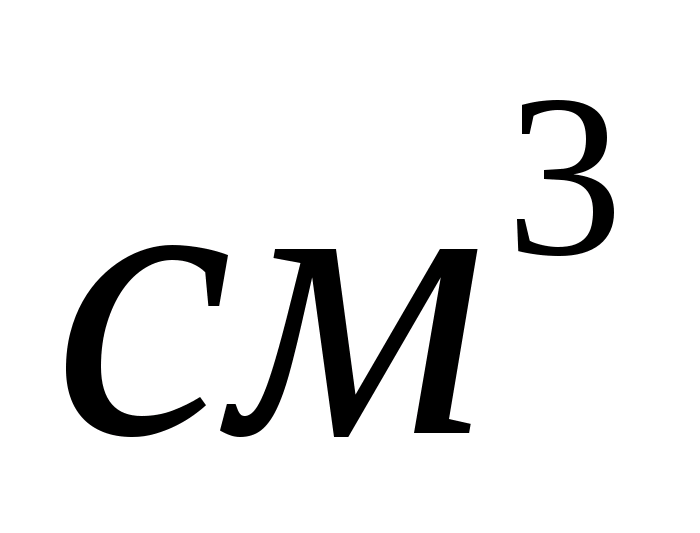
Показания
бюретки после реакции,
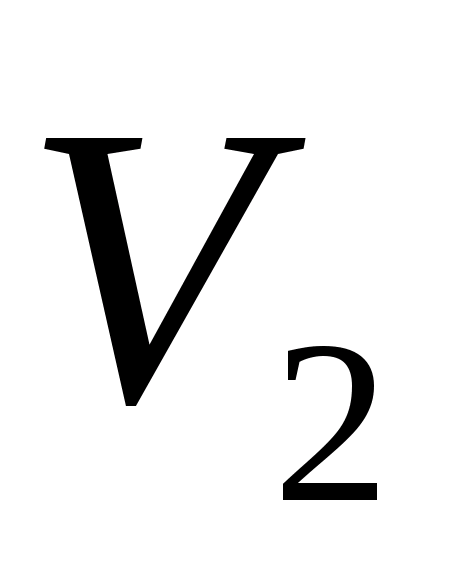 = ,
= ,

Объем
выделившегося водорода,
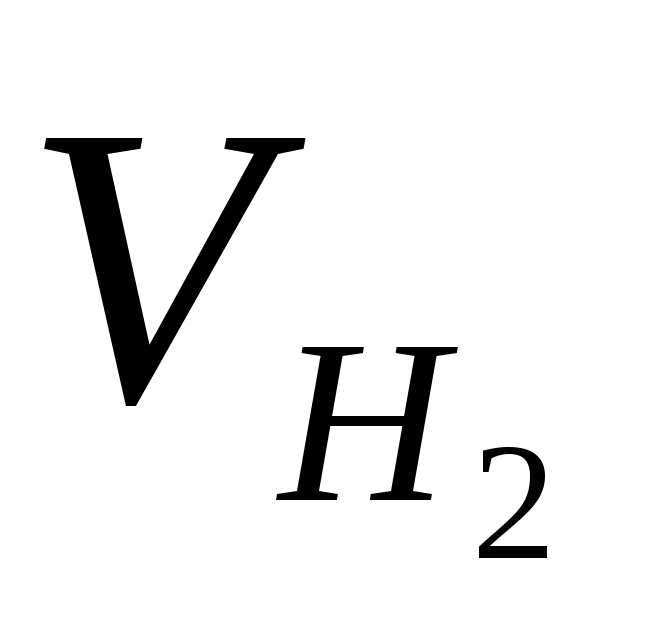 =
=
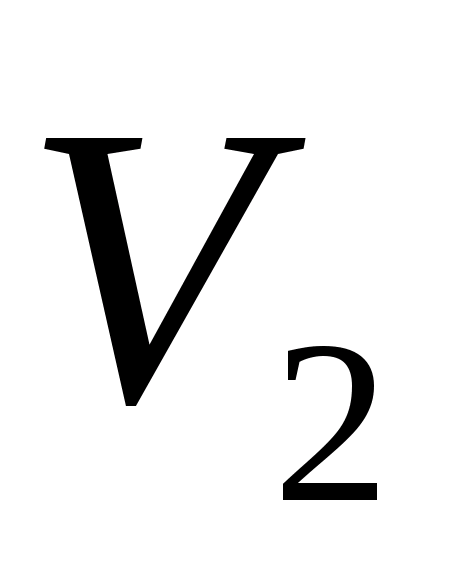 -
-
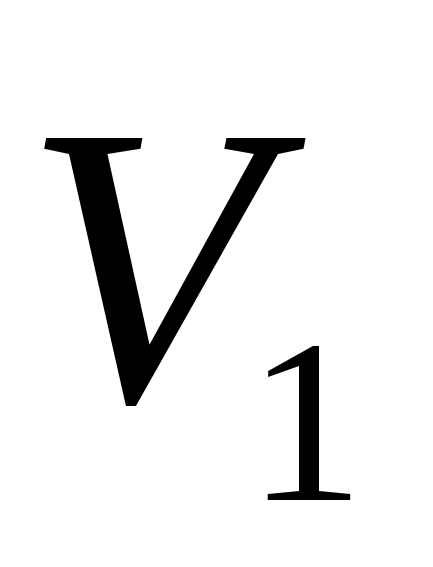 = = ,
= = ,

Температура
окружающей среды
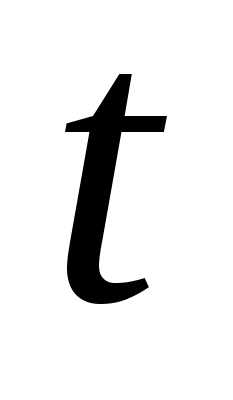 = ,
= ,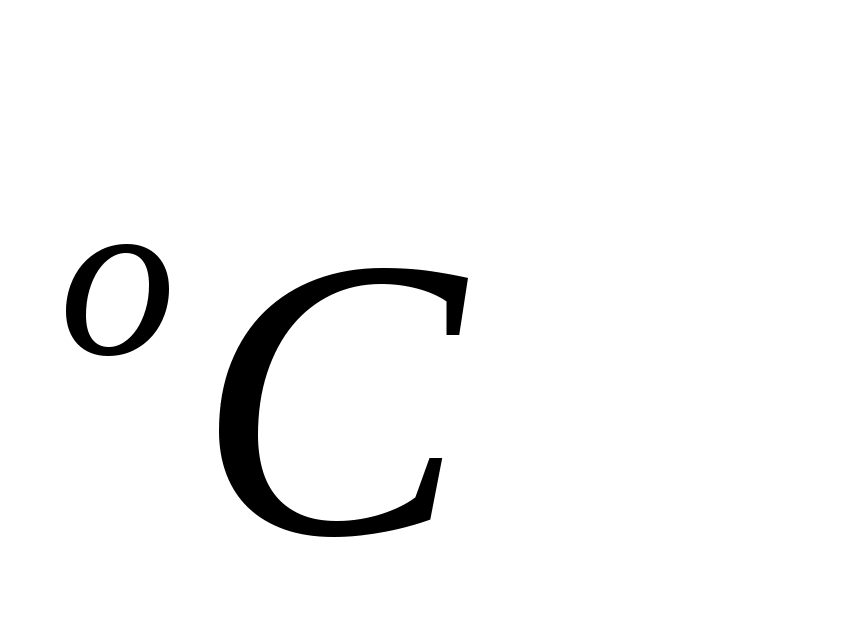
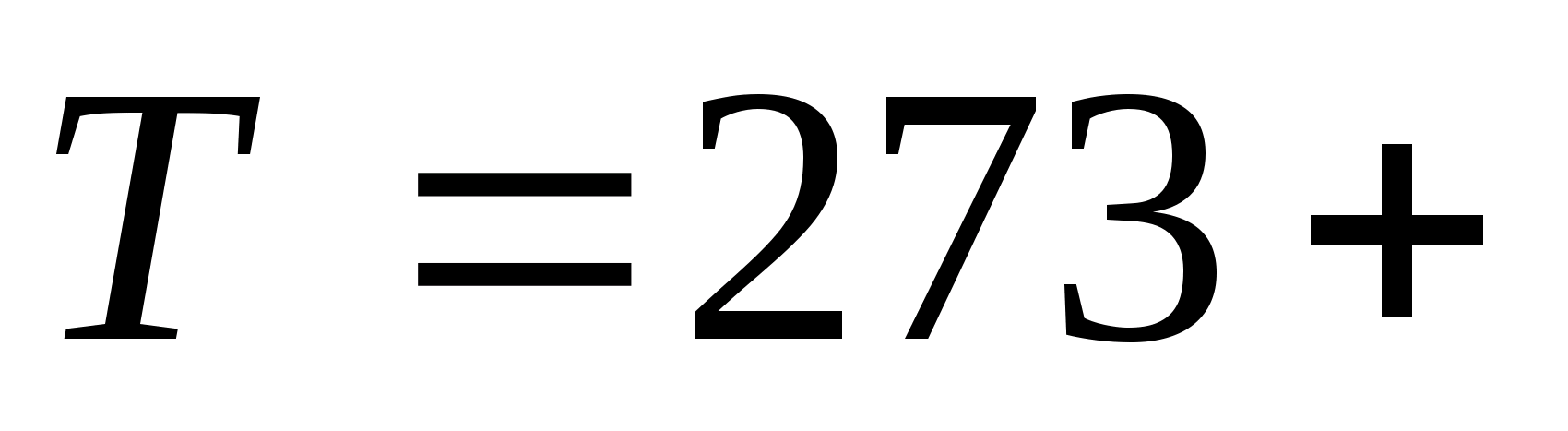 = ,
= ,
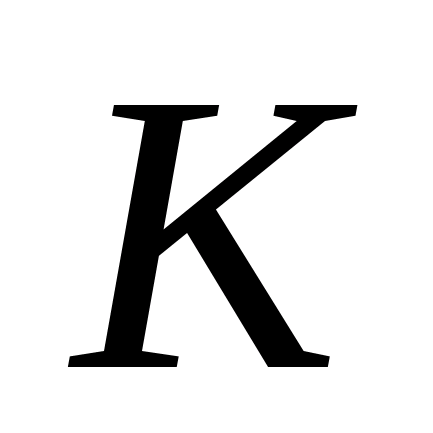
Атмосферное
давление
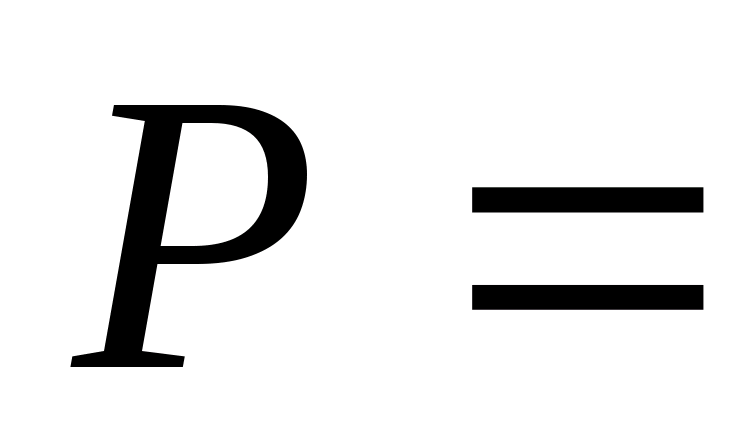 ,
,
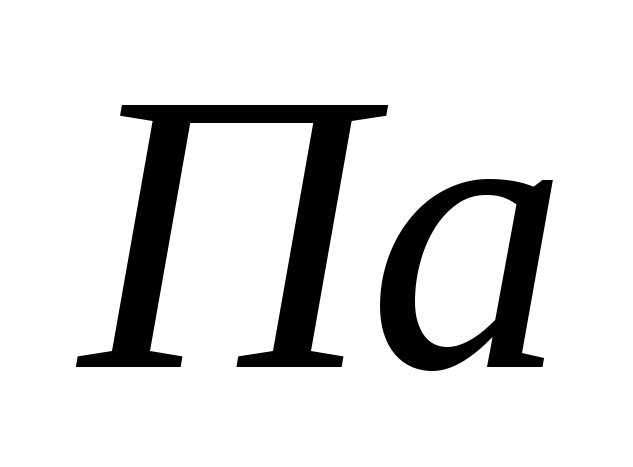
Давление
насыщенных паров воды
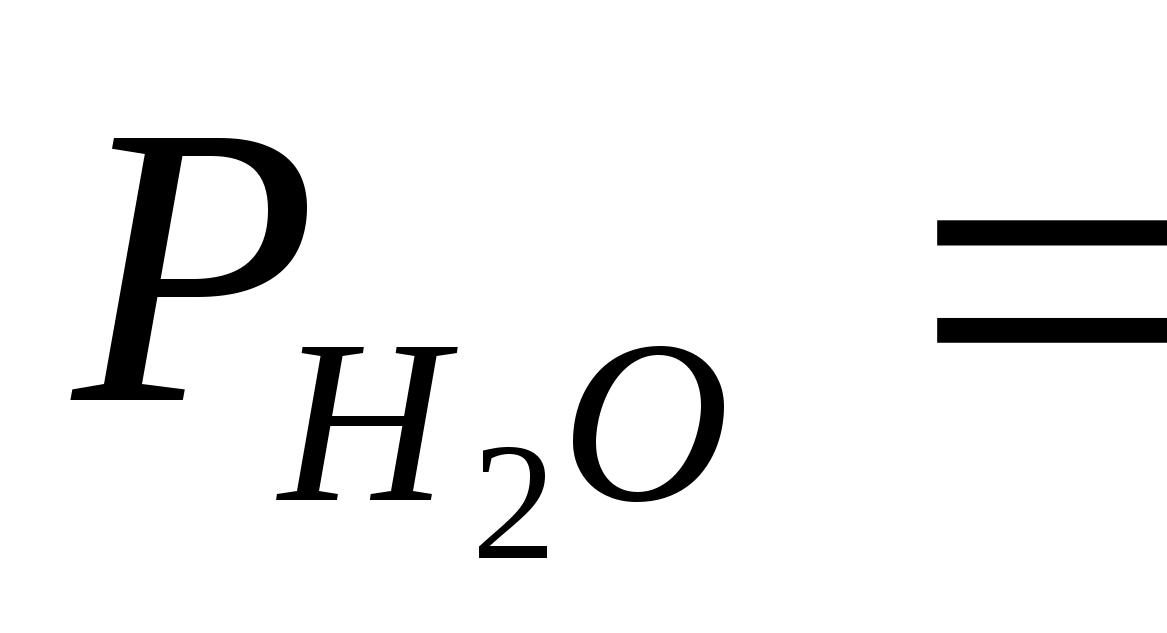 ,
,
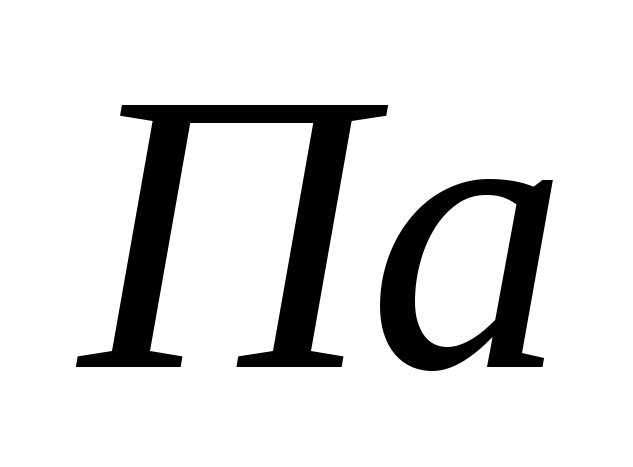
Парциальное
давление водорода
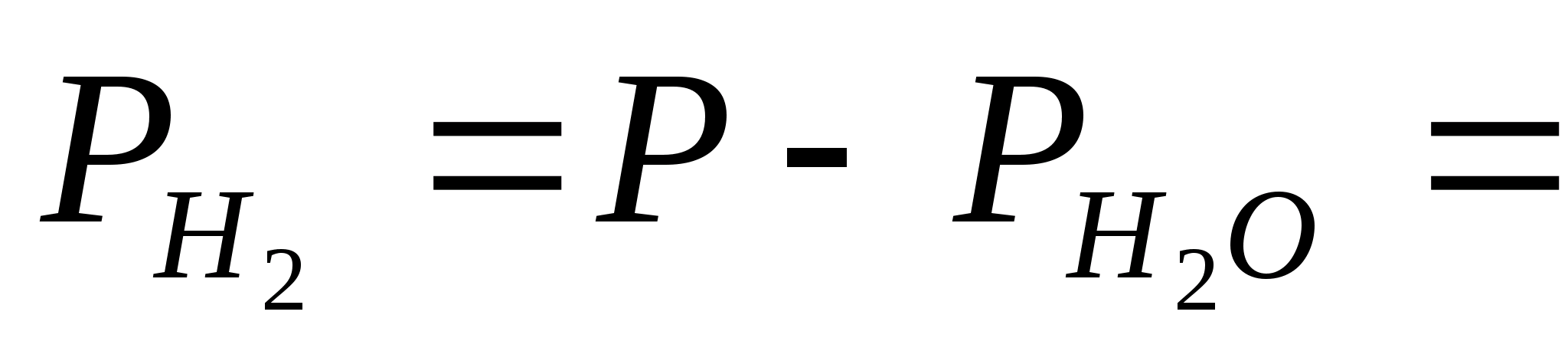 = ,
= ,
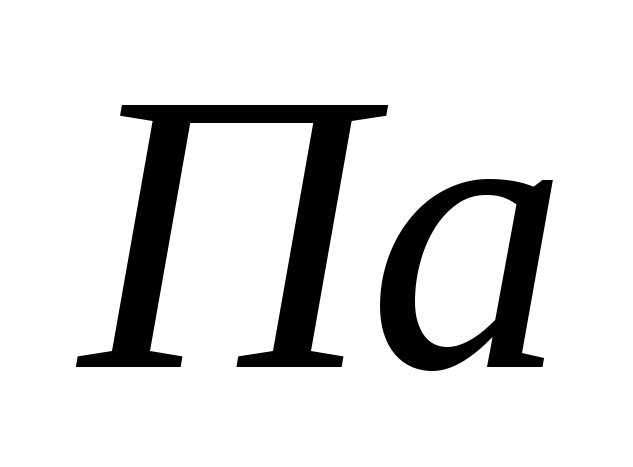
Объем выделившегося водорода приводим к нормальным условиям на основе уравнения состояния идеального газа, объединяющего законы Бойля-Мариотта и Гей-Люссака:
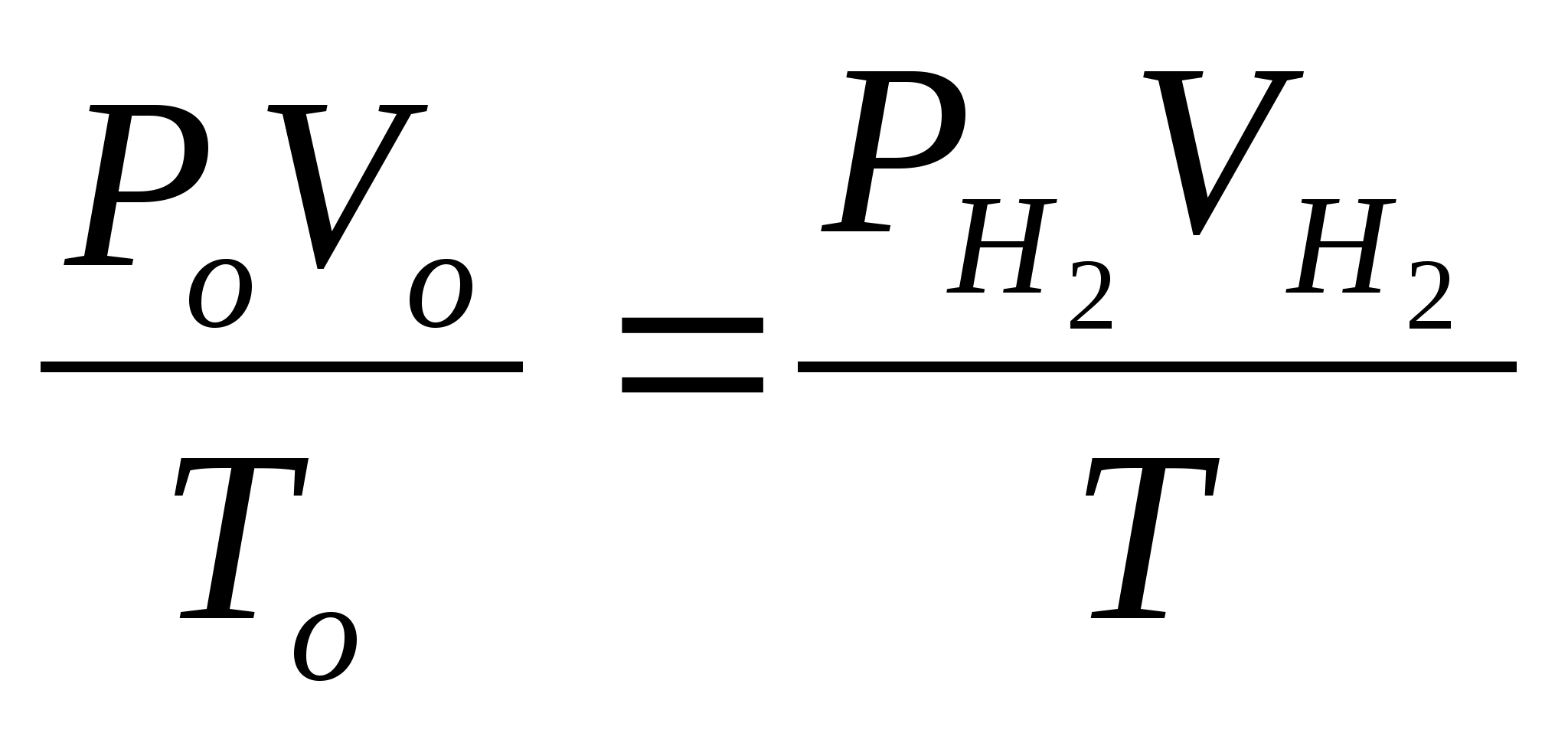 ,
,
где
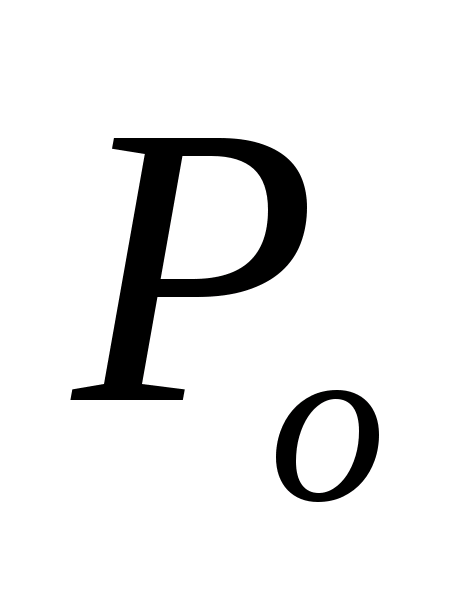 - нормальное давление, равное 101,325 кПа;
- нормальное давление, равное 101,325 кПа;
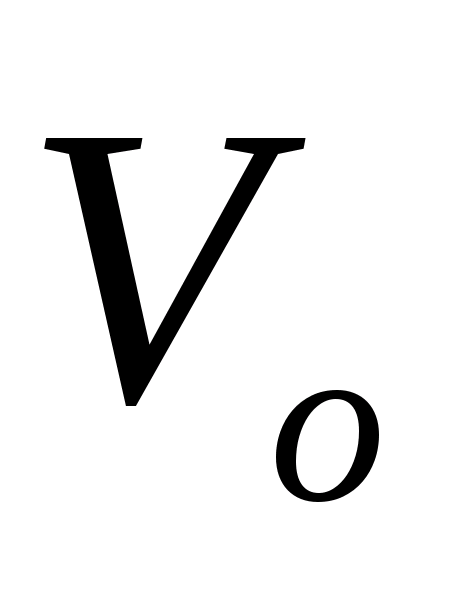 - объем газа при нормальных условиях,
- объем газа при нормальных условиях,
 ;
;
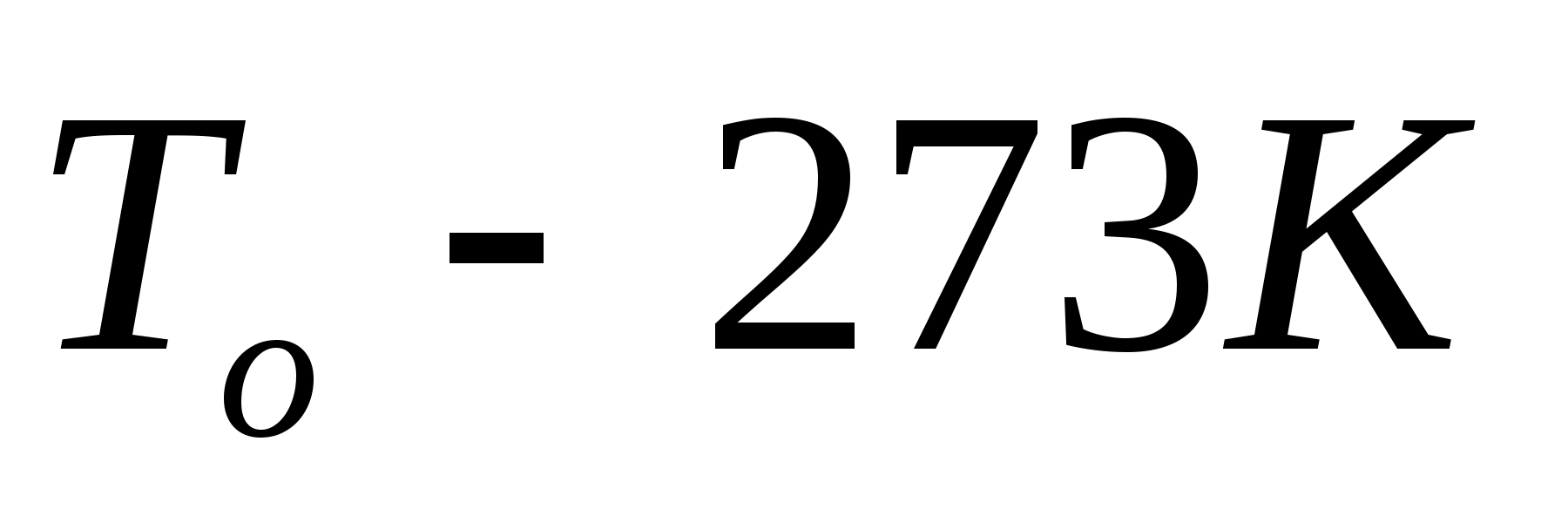 ;
;
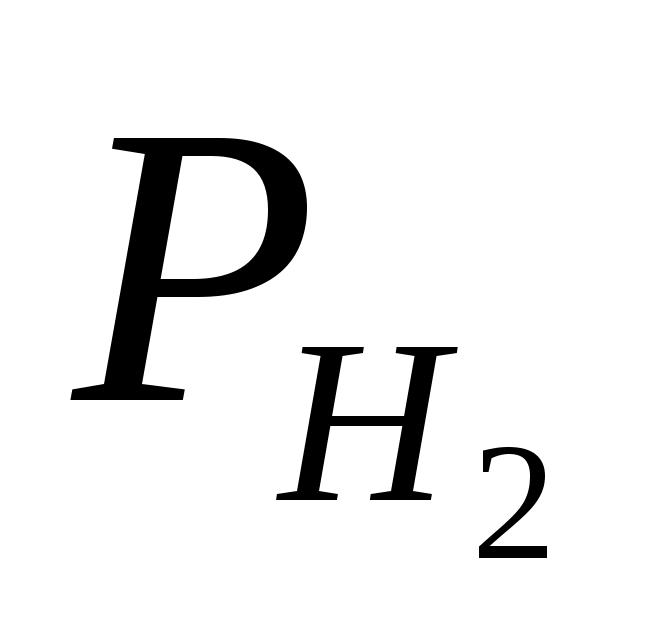 -
парциальное давление сухого водорода;
-
парциальное давление сухого водорода;
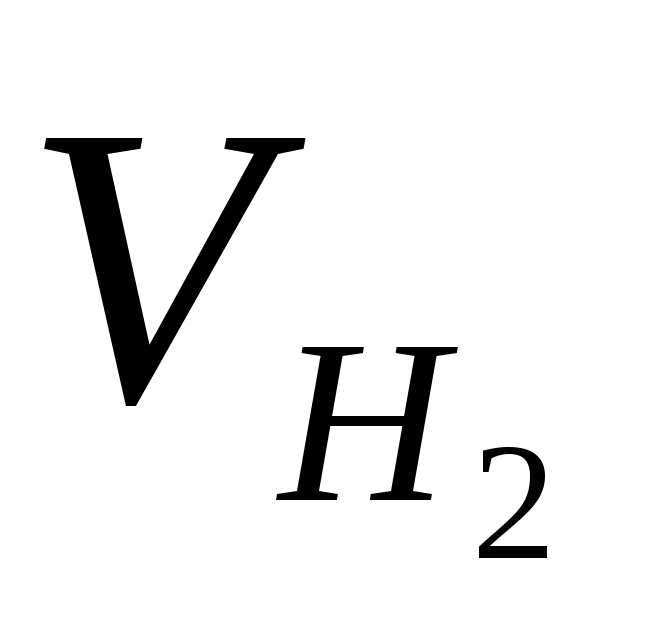 -
объем газа в условиях опыта;
-
объем газа в условиях опыта;
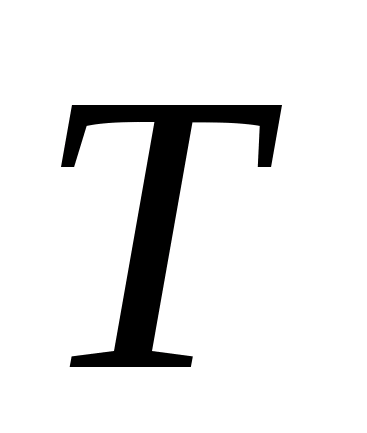 -
температура опыта по абсолютной шкале
температур.
-
температура опыта по абсолютной шкале
температур.
Таким образом, объем водорода,
приведенного к нормальным условиям
определяется по уравнению
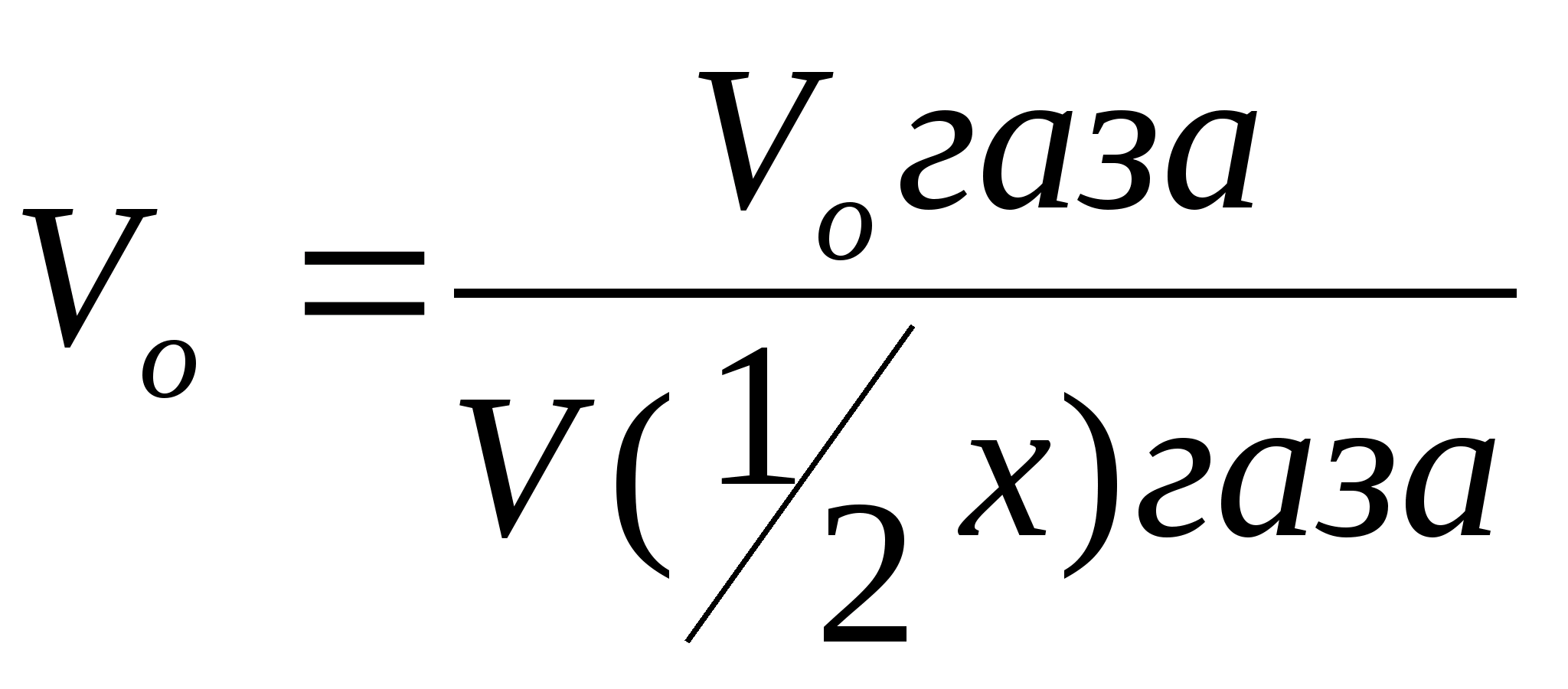 ,
,
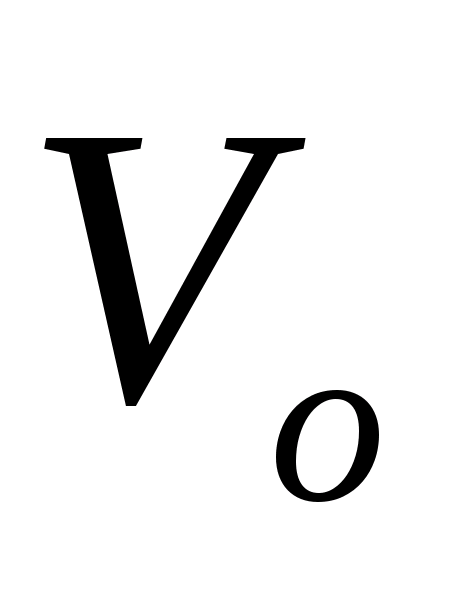 =
=
=
=

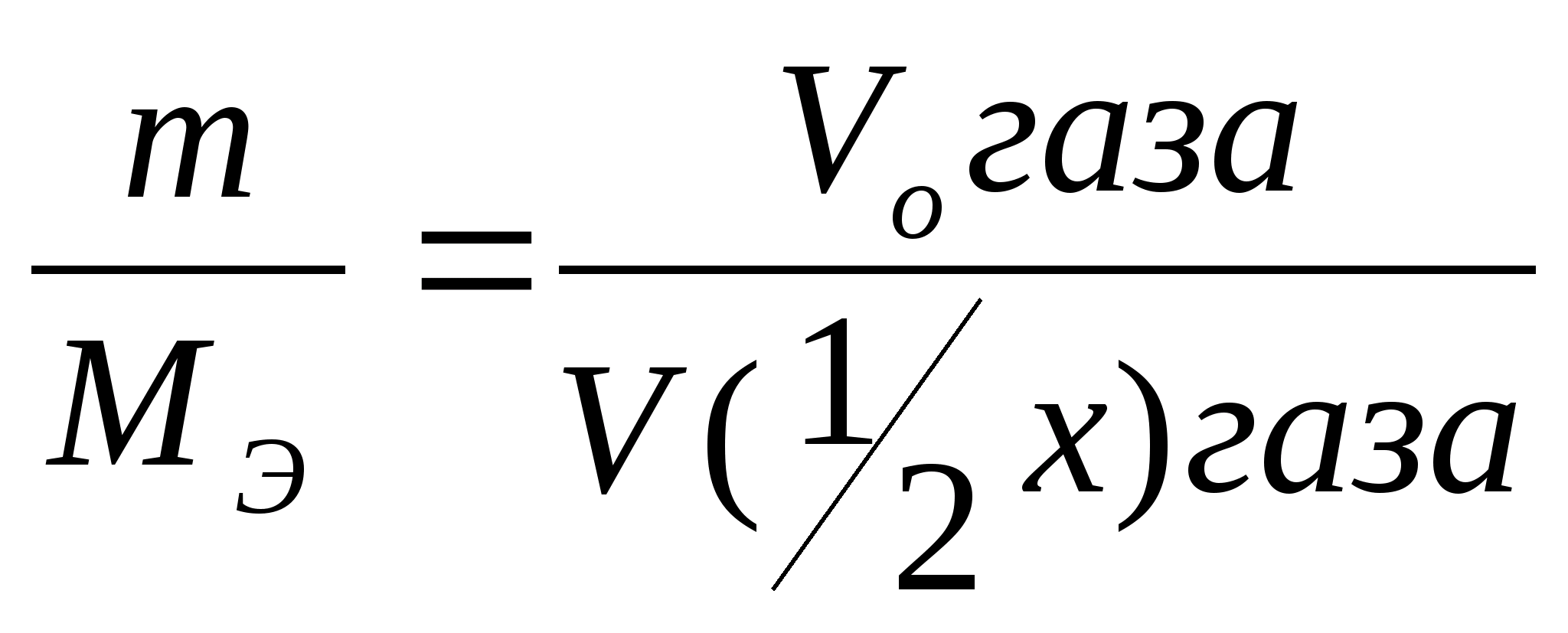 ,
,
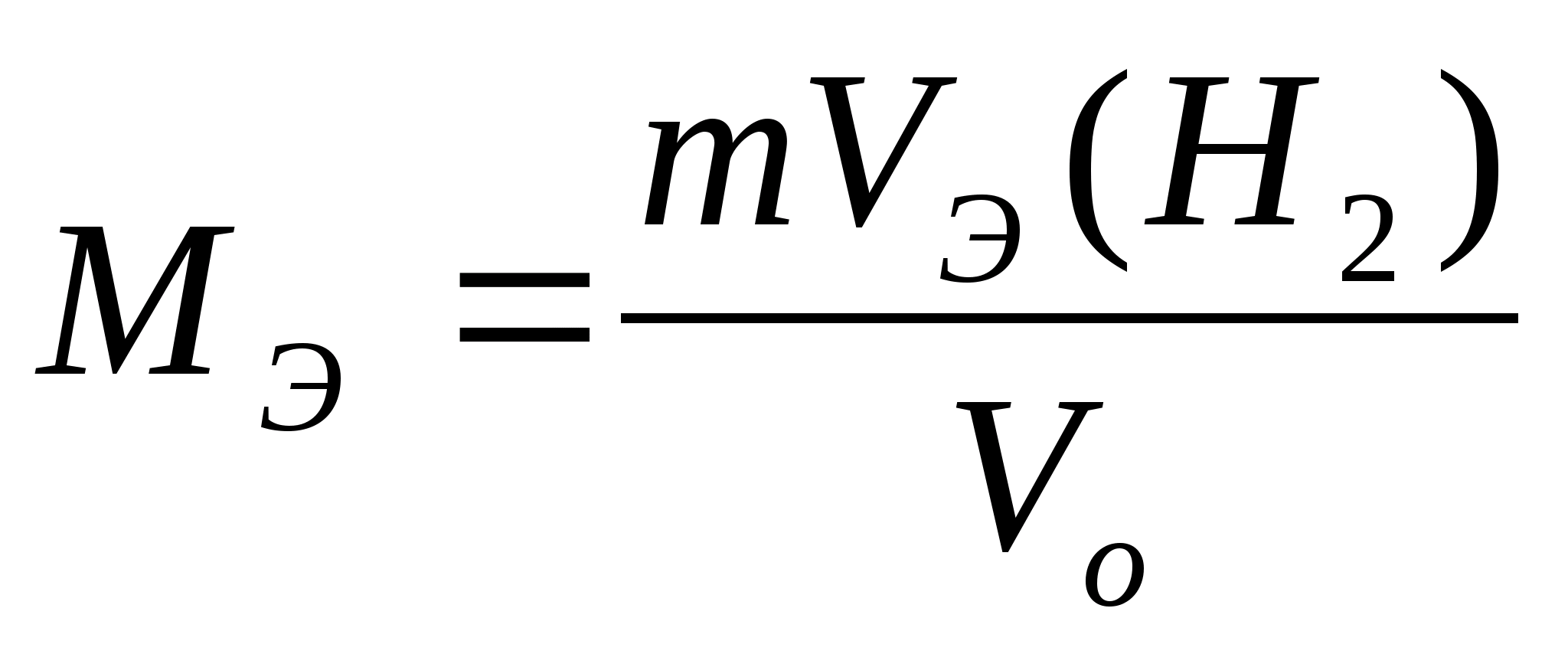 =
=
=
=
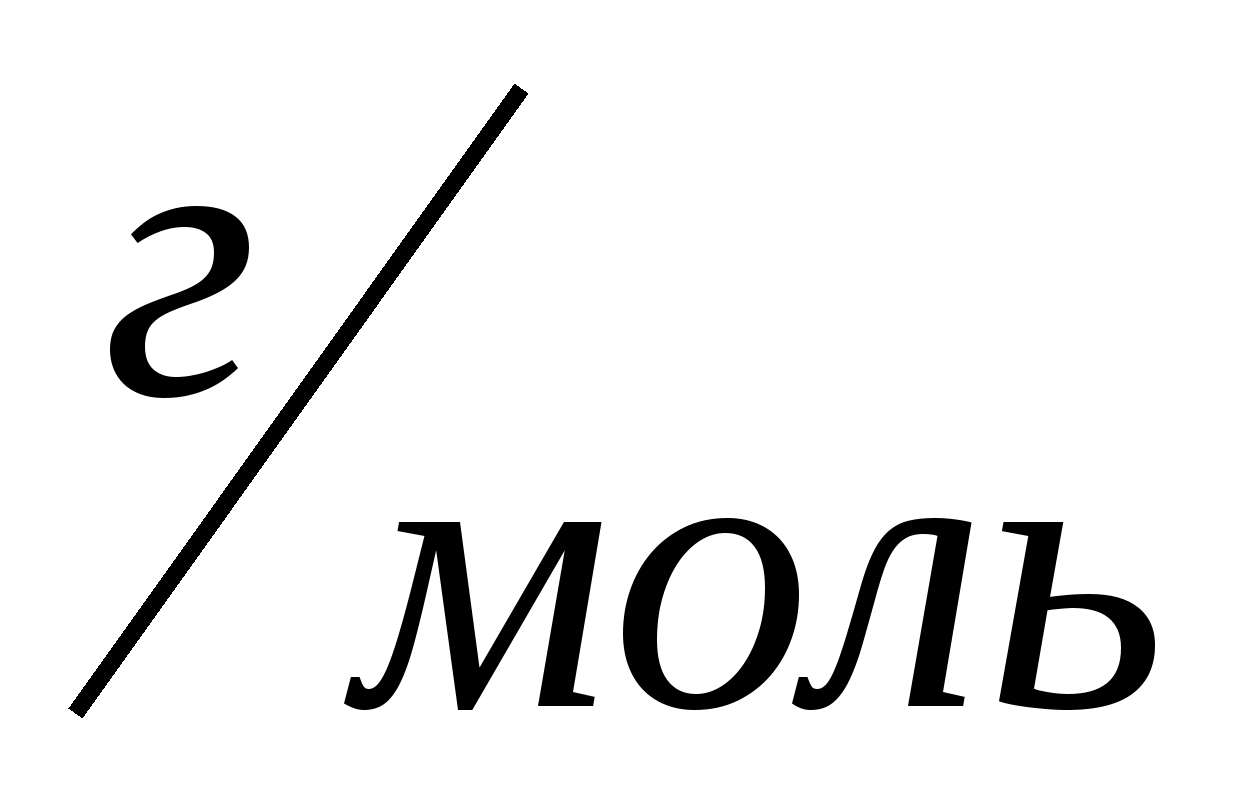 ,
где
,
где
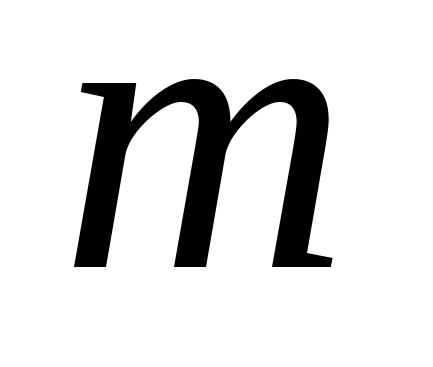 -
масса металла;
-
масса металла;
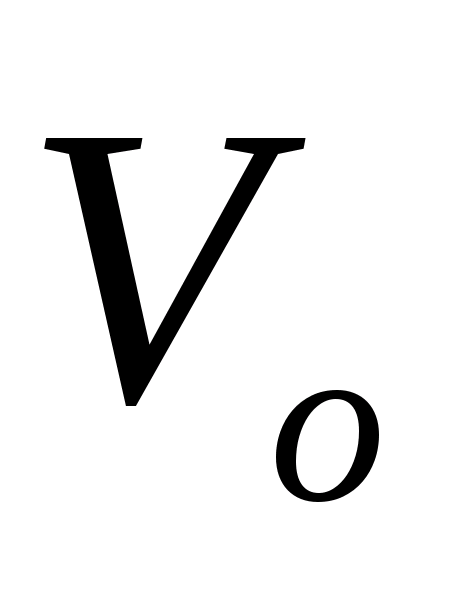 -
объем газа, приведенный к нормальным
условиям;
-
объем газа, приведенный к нормальным
условиям;
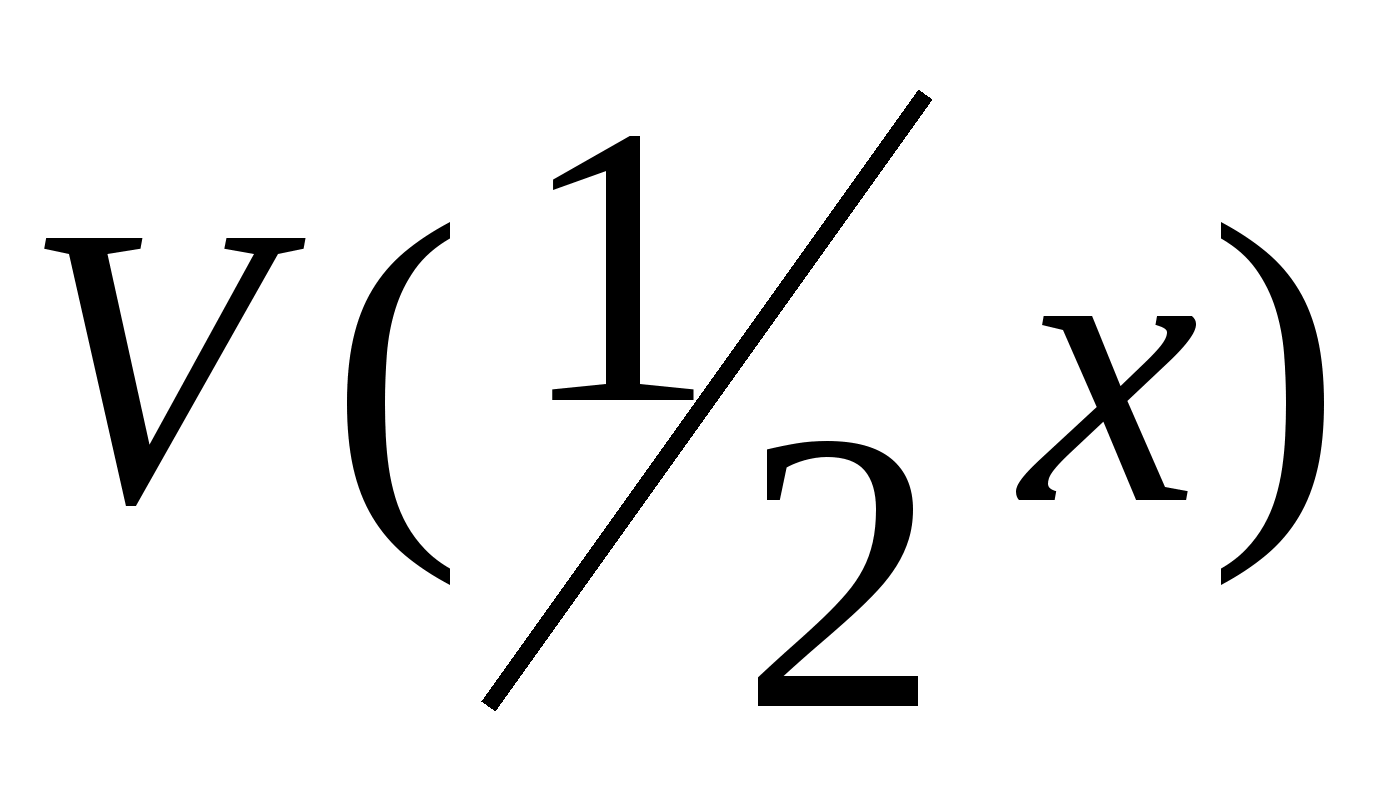 - молярный объем эквивалента газа.
Молярный объем эквивалента водорода,
составляющий
- молярный объем эквивалента газа.
Молярный объем эквивалента водорода,
составляющий
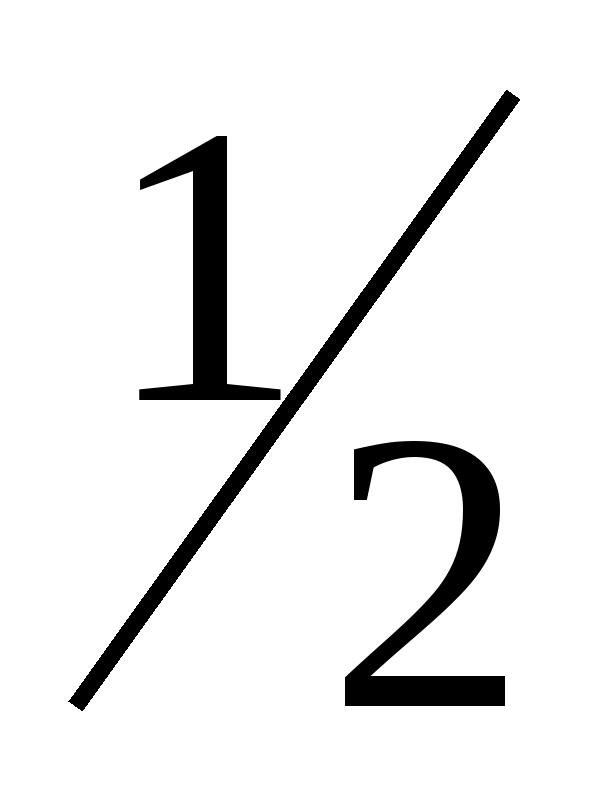 объема его моля, занимает при нормальных
условиях
объема его моля, занимает при нормальных
условиях
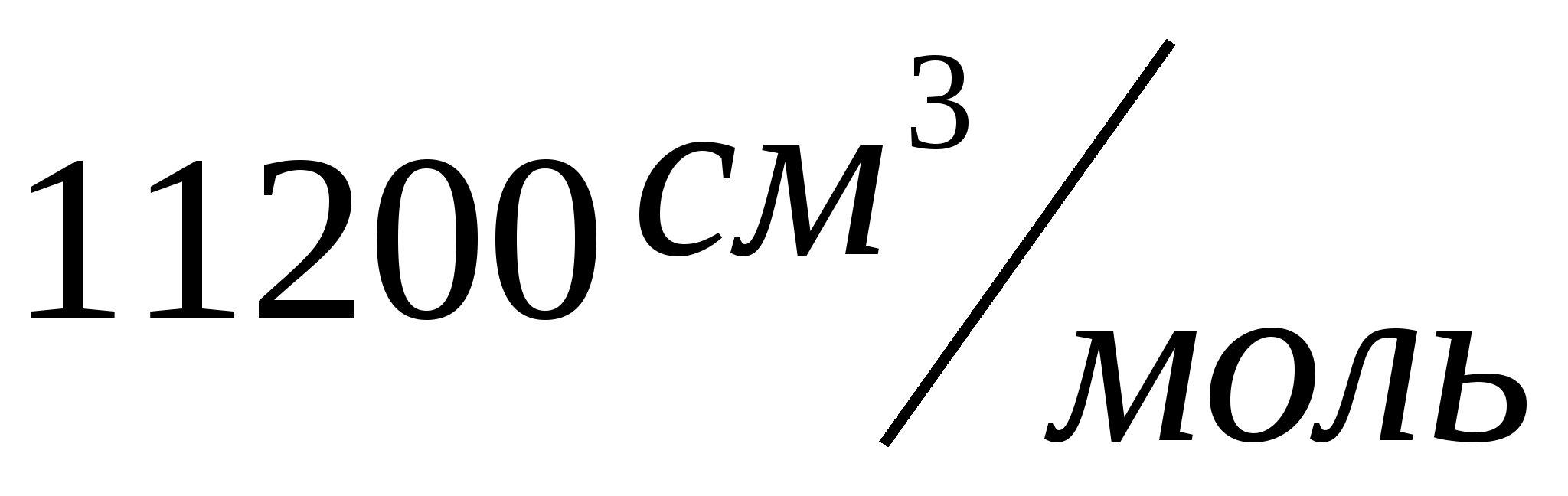 .
.
Давление насыщенного водяного пара в равновесии с водой.
|
|
|
|
|
|
15 |
1705 |
21 |
2486 |
|
16 |
1817 |
22 |
2643 |
|
17 |
1937 |
23 |
2810 |
|
18 |
2064 |
24 |
2983 |
|
19 |
2197 |
25 |
3167 |
|
20 |
2338 |
26 |
3361 |
Затем мы вычисляем теоретическую величину молярной массы эквивалента металла и находим относительную ошибку определения:
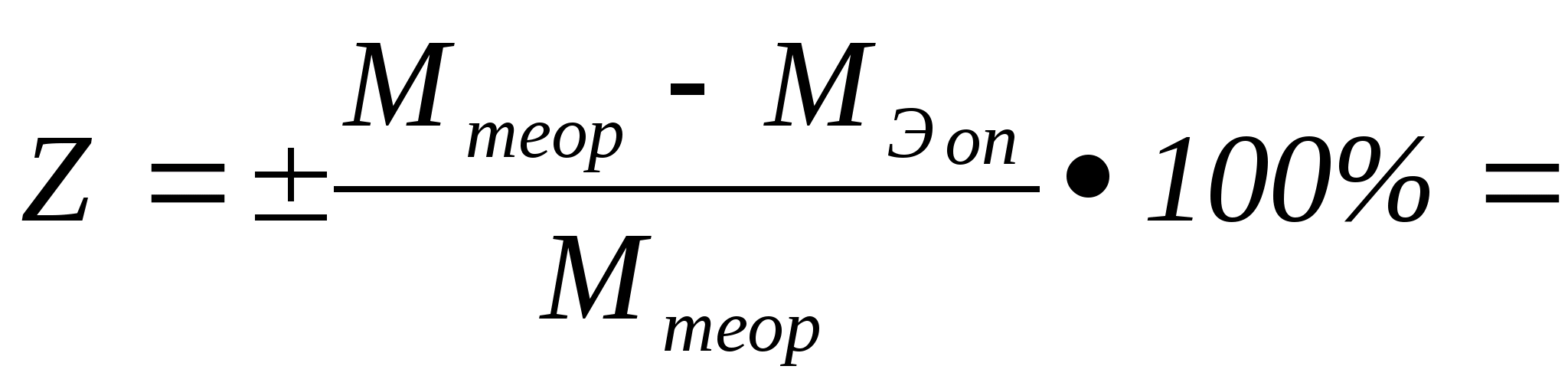



Вывод:
Работу выполнил учащийся Работу проверил:
группы ИС-02-Д1 преподаватель
Савельев Сергей
Владимирович
К

 афедра
Зависимость свойств
элементов Лабораторная работа №2
афедра
Зависимость свойств
элементов Лабораторная работа №2
инженерной от положения в периодической
экологии системы Д. И. Менделеева
Цель работы: изучить на практике, как изменяются свойства элементов и их соединений от заряда ядра атома на примере элементов III периода.
Оборудование и материалы:
аппарат киппа, спиртовая горелка,
коническая колба на 100 , фарфоровая чашка, часовое стекло, 8
пробирок, фенолфталеин, метилоранж,
сера цинковая пыль, натрий, магний,
алюминий. Растворы: соляной кислоты,
едкого натрия, хлорида олова (III),
гидроксида аммония.
, фарфоровая чашка, часовое стекло, 8
пробирок, фенолфталеин, метилоранж,
сера цинковая пыль, натрий, магний,
алюминий. Растворы: соляной кислоты,
едкого натрия, хлорида олова (III),
гидроксида аммония.
Методика выполнения работы.
Опыт №1. Взаимодействие щелочных металлов с водой.
Налить в фарфоровую чашку немного воды, опустить в нее кусочек натрия и быстро накрыть чашку воронкой. После окончания реакции прилить к полученному раствору 2-3 капли фенолфталеина. Составить уравнения протекающих реакций и сделать вывод относительно свойств щелочных металлов.
Опыт №2. Действие воды на металлический магний.
Поместить в пробирку стружку металлического магния. Добавить немного воды и 2-3 капли фенолфталеина. Обратить внимание на то, что цвет практически не изменится. Затем следует нагреть пробирку. Отметить изменение окраски раствора. Сделать вывод относительно щелочных свойств магния и написать уравнения протекающих реакций.
Опыт №3. Амфотерность металлического алюминия.
Поместить кусочек металлического алюминия в пробирку, прилить немного воды и 2-3 капли фенолфталеина. Убедиться в том, что ни в обычных условиях, ни при нагревании алюминий с водой не взаимодействует. Затем поместить в две другие пробирки по кусочку алюминия. В одну из них прилить разбавленную соляную кислоту, в другую – раствор крепкой щелочи NaOH. Пробирки нагреть. При этом наблюдается взаимодействие алюминия, как с кислотой, так и со щелочью. Написать уравнения протекающих реакций и сделать вывод о свойствах алюминия.
Опыт №4. Неметаллические свойства серы.
Кусочек серы поместить в пробирку и налить немного воды. Прибавить сначала 2-3 капли фенолфталеина, а затем столько же метилоранжа. Отметить, что сера не взаимодействует с водой в обычных условиях. Нагреть пробирку. Отметить что после нагревания взаимодействие серы с водой не происходит. Кусочек серы положить на железную ложечку, поджечь и опустить в коническую колбу, в которой было налито немного воды (не касаясь поверхности воды). После сгорания серы закрыть колбу пробкой и встряхнуть. Полученный раствор разделить на 3 пробирки и испытать различными индикаторами.
Опыт №5. Амфотерные свойства гидроксида олова (II).
Поместить в пробирку 8-10 капель
раствора
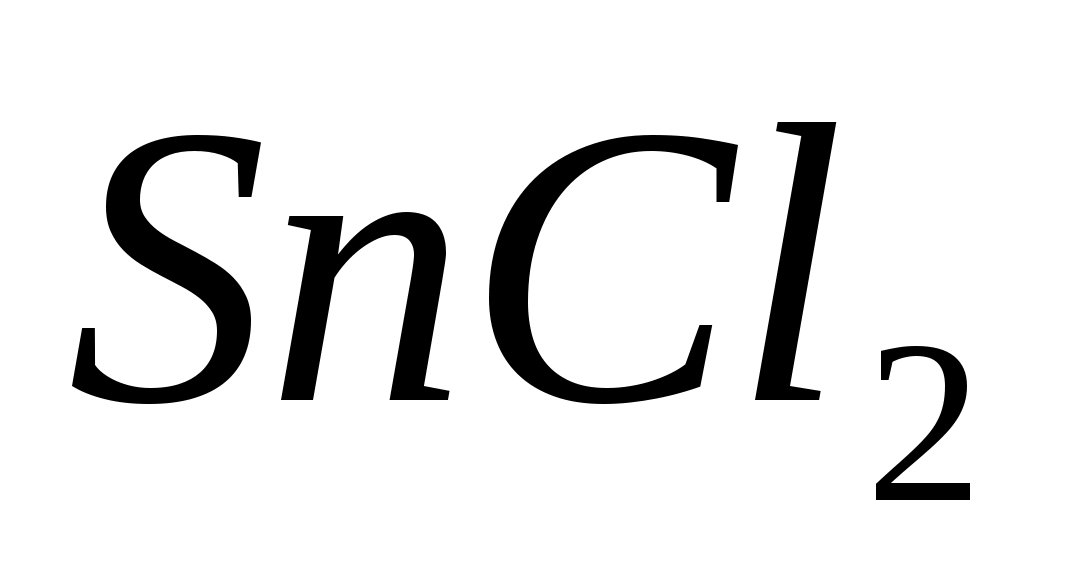 ,
добавить несколько капель
,
добавить несколько капель
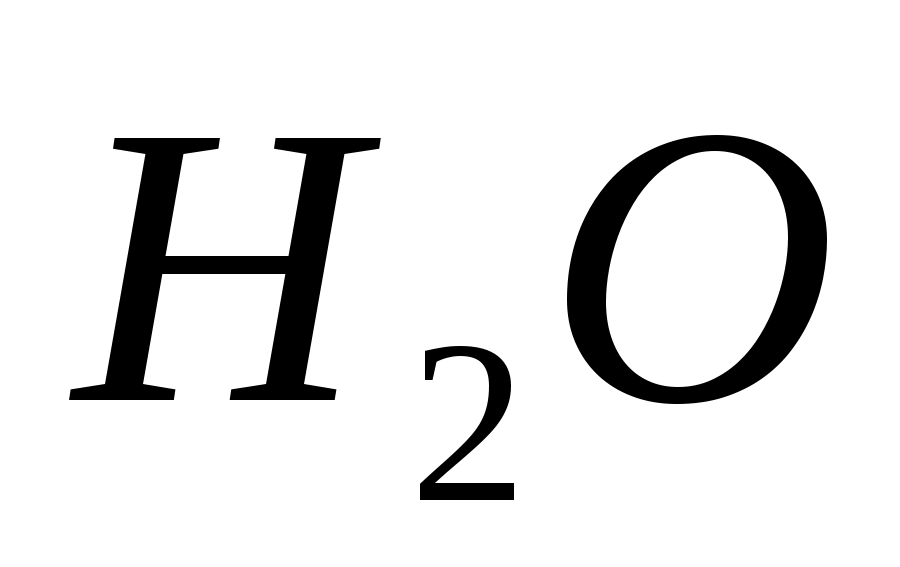 и раствор
и раствор
 в воде, до полного осаждения осадка.
Распределить содержимое на две пробирки
и добиться растворения осадка в каждой
из них с помощью: в одном случае 2М
раствора HCl,
в другом – 2М раствора NaOH.
Составить уравнения реакций, зная, что
при реакции гидроксида олова с NaOH
образуется тетрагидроксостаннат натрия
в воде, до полного осаждения осадка.
Распределить содержимое на две пробирки
и добиться растворения осадка в каждой
из них с помощью: в одном случае 2М
раствора HCl,
в другом – 2М раствора NaOH.
Составить уравнения реакций, зная, что
при реакции гидроксида олова с NaOH
образуется тетрагидроксостаннат натрия
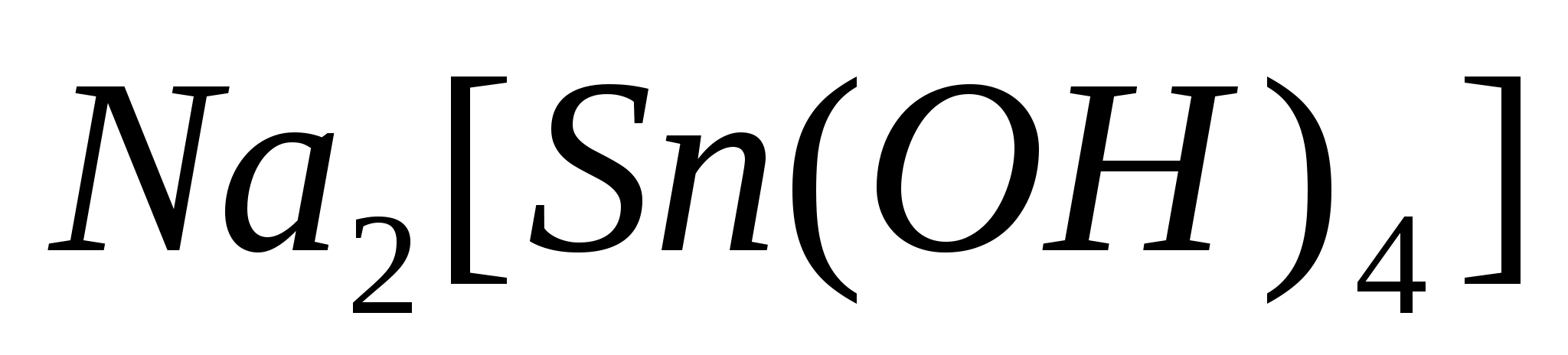
Работу выполнил учащийся Работу проверил:
группы ИС-02-Д1 преподаватель
Савельев Сергей
Владимирович
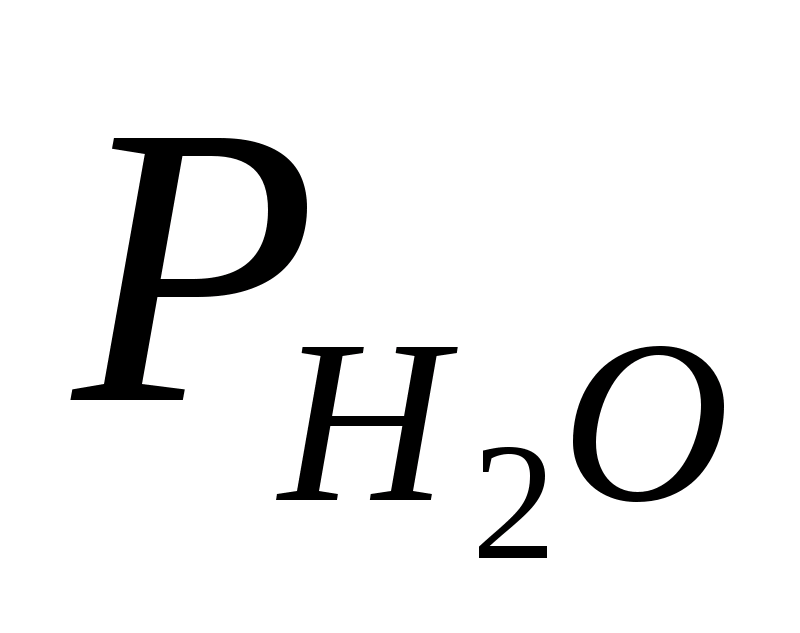 ,
,