Тепловые и массообменные процессы
Министерство образования и науки РФ
Федеральное агентство по образованию
Иркутский государственный технический университет
Тепловые и массообменные процессы
Методические указания к лабораторным работам по курсу
«Процессы и аппараты химической технологии»
Иркутск 2007
Тепловые и массообменные процессы. Методические указания к лабораторным работам по курсу «Процессы и аппараты химической технологии» для студентов очной, заочной и вечерней форм обучения специальностей:
240401.65 - Химическая технология органических веществ
240403.65 - Химическая технология природных энергоносителей и углеродных материалов
240406.65 -Технология химической переработки древесины.
Составители: Губанов Н.Д., Баяндин В.В. – Иркутск, 2007. – 33 с.
Иркутский государственный технический университет
664074, Иркутск, ул. Лермонтова, 83
ИСПЫТАНИЕ ДВУХКОРПУСНОЙ ВЫПАРНОЙ УСТАНОВКИ
Цель работы: изучение двухкорпусной выпарной установки непрерывного действия, определение количества выпариваемой воды, коэффициентов теплопередачи по корпусам и удельного расхода греющего пара.
Приборы и принадлежности: двухкорпусная выпарная установка, раствор глицерина, денсиметры.
Введение
Выпаривание – это процесс концентрирования растворов нелетучих веществ, заключающийся в удалении растворителя путем испарения его при кипении. Движущей силой выпаривания является разность температур между горячим теплоносителем и кипящим раствором, называемая полезной разностью температур.
Выпаривание является одним из наиболее энергоемких процессов химической и пищевой технологии, как по абсолютному количеству расходуемой энергии, так и по ее удельному расходу на 1кг перерабатываемого раствора. В промышленности в большинстве случаев выпаривают водные растворы нелетучих веществ.
Выпаривание ведут как под атмосферным давлением, так и под повышенным или пониженным давлениях. При выпаривании под атмосферным давлением образующийся вторичный пар удаляется в атмосферу. При выпаривании под пониженным давлением вакуум в аппарате создают за счет конденсации вторичного пара в барометрическом конденсаторе. Выпаривание под вакуумом позволяет снизить температуру кипения раствора, а значит увеличить разность температур между греющим паром и кипящим раствором, то есть повысить движущую силу процесса. Это дает возможность уменьшить поверхность теплообмена. Выпаривание под повышенным давлением позволяет образующийся вторичный пар использовать в качестве греющего или для других технологических нужд.
В промышленности применяют как однокорпусные, как и многокорпусные выпарные установки. Многокорпусные выпарные установки состоят из нескольких соединенных друг с другом выпарных аппаратов (корпусов). Различают прямоточные и противоточные многокорпусные выпарные установки.
В прямоточных выпарных установках греющий пар и выпариваемый раствор движутся прямотоком от корпуса к корпусу, а в противоточных – навстречу друг другу. Подробнее о многокорпусных выпарных установках в [1, 2]. В многокорпусных выпарных установках первичным паром обогревают только первый корпус, а вторичный пар, образующийся в каждом предыдущем корпусе, используют для обогрева последующего корпуса. Таким образом, в многокорпусных выпарных установках осуществляется многократное использование тепла, отдаваемого первичным греющим паром. Это позволяет значительно снизить расход первичного греющего пара. В качестве горячего теплоносителя в первом корпусе в основном используют насыщенный водяной пар.
1 Требования безопасности
Перед пуском установки по наружному осмотру проверить исправность аппаратов, трубопроводов, арматуры, приборов КИПиА, заземления, защитного отключения, тепловой изоляции. Пуск установки проводить в присутствии учебного мастера и при его непосредственном руководстве. Работая на площадках с высокой отметкой и вблизи вращающихся частей проявлять осторожность и аккуратность.
К выполнению лабораторной работы студенты допускаются только после прохождения инструктажа по безопасности труда и пожарной безопасности в лаборатории и на рабочем месте.
2 Описание установки и порядок выполнения работы
Выпарная установка (рисунок 1) состоит из двух аппаратов 1 и 1а с внутренней греющей камерой и центральной циркуляционной трубой. Выпарной аппарат состоит из двух основных частей: греющей камеры, в которой происходит кипение раствора, и сепаратора, в котором вторичный пар отделяется от раствора. Высота выпарного 1500мм, диаметр 408мм, поверхность теплообмена 1,5м2 .
Водный раствор глицерина из бака 2, снабженного указателем уровня, центробежным насосом 13 подается в выпарной аппарат 1. Расход раствора измеряется ротаметром 7. Обогрев корпуса 1 осуществляется насыщенным водяным паром, поступающим от электропарового котла. Давление пара в трубопроводе измеряется манометром и регулируется клапанами. Вторичный пар из корпуса 1 проходит брызгоуловитель 5 и поступает в греющую камеру корпуса 1а.
Раствор, упаренный до некоторой концентрации в корпусе 1, под действием разности давлений поступает в корпус 1а, где упаривается до заданной концентрации. Концентрированный раствор из корпуса 1а, пройдя через холодильник 9 и фонарь 16, поступает в сборники упаренного раствора 3 или 4, работающие попеременно. По мере их заполнения упаренный раствор переливается в бак 2.
|
|
|
I, Iа – выпарные аппараты; 2 – бак-хранилище; 3, 4 – сборники упаренного раствора; 5, 5а – брызгоуловители; 6 – барометрический конденсатор; 7, 8 – ротаметры; 9 – холодильник; 10 – барометрический ящик; 11, 12 – сборнки конденсата; 13 – центробежный насос; 14 – водокольцевой вакуум-насос; 15 – водоотделитель; 16 – смотровой фонарь, Рисунок 1 – Схема двухкорпусной выпарной установки |
Вторичный пар из корпуса 1а проходит через брызгоуловитель 5а и поступает в барометрический конденсатор 6, орошаемый водой. Расход воды измеряется ротаметром 8. Смесь воды и конденсата удаляется из конденсатора самотеком через барометрическую трубу в барометрический ящик 10, а затем в канализацию. Воздух из барометрического конденсатора отсасывается вакуум-насосом 14. Концентрацию разбавленного и упаренных растворов в корпусах 1 и 1а определяют ареометром. Давление в аппаратах измеряются манометрами, вынесенными на щит КИП. Измерение температур конденсата и поверхности аппаратов производится термометрами сопротивления, работающими в комплекте с лагометрами. Отбор проб исходного и упаренного растворов производится через пробоотборники.
Перед пуском установки необходимо: Закрыть все воздушные краны и вентили на линии вакуума, паровой линии и линии раствора. Проверить наличие исходного раствора в баке 2. Проверить наличие воды в водопроводе.
Пуск установки производить следующим образом: Открыть вентили на отборных устройствах манометров и вакуумметров. Подать воду в холодильник упаренного раствора. Затем заполнить аппарат 1 исходным раствором из бака 2 с помощью наноса 13 через ротаметр 7 до верхней красной черты и подать пар на установку. Продуть межтрубное пространство греющей камеры первого корпуса по обводной линии. После продувки направить конденсат через конденсационные горшки и нагреть раствор до кипения. После того, как раствор в корпусе 1 начнет кипеть, следует создать вакуум во втором аппарате. Под действием разности давлений раствор из корпуса 1 начнет самотеком переливаться в корпус 1а. Перелив раствора производить до тех пор, пока уровень в корпусе 1 не достигнет нижней красной черты. После этого первый аппарат заполнить до верхней красной черты и процесс повторить. Когда во втором аппарате уровень раствора достигнет красной черты, заполнение системы прекращают и начинают процесс выпаривания. Далее необходимо продуть греющую камеру второго аппарата, выпустив часть пара по обводной линии. Затем конденсат направить через конденсационный горшок. Установить по ротаметру указанный преподавателем расход исходного раствора в первый корпус. Начать подачу раствора из корпуса 1 в корпус 1а. для чего открыть регулирующий вентиль на линии раствора между корпусами с таким расчетом, чтобы уровень в первом аппарате не опускался ниже красной черты. Одновременно с началом подачи раствора подать воду в барометрический конденсатор. Расход воды установить по ротаметру 8. Подключить к корпусу 1а сборники упаренного раствора. Пустив, таким образом, всю установку, обязательно при непрерывной подаче раствора в аппараты, дать ей поработать 40-45 минут. После этого приступить к замерам. Измерения производятся через каждые 10-15 минут 3-4 раза. Результаты наблюдений сводятся в таблицу 1.
Таблица 1
Измеренные и рассчитанные параметры
|
Наименование величины |
Значение и момент измерения |
Среднее значение |
|
Расход исходной смеси, кг/с |
||
|
Расход воды на барометрический конденсатор, кг/с |
||
|
Давление греющего пара, Па |
||
|
Температура греющего пара, оС |
||
|
Температура исходного раствора, оС |
||
|
Давление в корпусе 1, Па |
||
|
Температура вторичного пара в первом корпусе, оС |
||
|
Температура кипения раствора в корпусе 1, оС |
||
|
Давление во втором корпусе, Па |
||
|
Температура вторичного пара в корпусе 1а, оС |
||
|
Температура кипения раствора во втором корпусе, оС |
||
|
Концентрация исходного раствора, % масс. |
||
|
Концентрация раствора после первого корпуса, % масс. |
||
|
Концентрация раствора после второго корпуса, % масс. |
||
|
Температура поверхности первого аппарата, оС |
||
|
Температура поверхности второго аппарата, оС |
||
|
Температура холодной воды, 0С |
||
|
Температура смеси в барометрической трубе, 0С |
||
|
Температура воздуха, 0С |
3 Обработка опытных данных
3.1 Материальный баланс установки
Количество воды, выпариваемой в первом корпусе
 ,
,
где
 -
количество исходного раствора, кг/с;
-
количество исходного раствора, кг/с;
 >1>
- концентрация исходного и упаренного
раствора после корпуса 1, % масс.
>1>
- концентрация исходного и упаренного
раствора после корпуса 1, % масс.
Количество воды, выпариваемое во втором корпусе
 ,
,
где
 -
количество раствора, поступающего из
первого во второй корпус, кг/с;
-
количество раствора, поступающего из
первого во второй корпус, кг/с;
 -
конечная концентрация раствора во
втором корпусе, % масс.
-
конечная концентрация раствора во
втором корпусе, % масс.
Общее количество выпариваемой воды

3.2 Тепловой баланс установки по корпусам
Расход тепла на выпаривание в первом корпусе

Количество тепла, затраченное на нагрев исходного раствора от начальной температуры t>H>> > до температуры кипения t>K>>1> определяется по уравнению
 ,
,
где C>H>> >– удельная теплоемкость исходного раствора, Дж/кг К.
Количество тепла, которое необходимо затратить на выпаривание воды в первом корпусе
 ,
,
где – удельная теплота парообразования
при давлении в корпусе 1, Дж/кг.
– удельная теплота парообразования
при давлении в корпусе 1, Дж/кг.
Расход тепла на выпаривание во втором корпусе

Количество теплоты, выделяющееся при охлаждении выпариваемого раствора от температуры кипения в первом корпусе t>K>>1> до температуры кипения t>K>>2 >во втором корпусе определяется по формуле
 ,
,
где С>К1 >- удельная теплоемкость раствора, поступающего из первого во второй корпус, Дж/кг К.
Количество тепла, затраченное на испарение воды во втором корпусе
 ,
,
где
 -
удельная теплота парообразования при
давлении во втором корпусе, Дж/кг.
-
удельная теплота парообразования при
давлении во втором корпусе, Дж/кг.
Потери тепла в окружающую среду первым и вторым корпусом установки можно определить по уравнениям

 ,
,
где >1>, >2> – суммарные коэффициенты теплоотдачи от стенки аппарата к воздуху, Вт/м2 К;
F>H>>1>, F>H>>2> – наружная поверхность выпарных аппаратов (F>H>>1 >= F>H>>2>=1.92 м2);
t>возд>., t>ст1, >t>ст2 > – температура воздуха и стенок аппаратов, оС.
Суммарные коэффициенты теплоотдачи конвекцией и излучением от стенки аппарата к воздуху вычисляются по формуле

Коэффициенты теплопередачи по корпусам
Коэффициенты теплопередачи определяют из основного уравнения теплопередачи для выпаривания
 ,
,
где Q – расход тепла на выпаривание в корпусе, Вт;
k – коэффициент теплопередачи, Вт/м2 К;
F – поверхность теплообмена, м2;
Δ t>пол> – полезная разность температур (движущая сила процесса).
Коэффициенты теплопередачи вычисляют по формулам
 ,
,
 .
.
Полезные разности температур по корпусам равны
 ,
,
 ,
,
где t>гр.п.>– температура греющего пара, оС;
t>вт.п.>– температура вторичного пара первого корпуса, оС.
Расход греющего пара
Расход первичного пара находят по уравнению
 ,
,
где r – удельная теплота конденсации греющего пара, Дж/кг;
x – паросодержание (степень сухости) греющего пара (x=0,95).
Расход греющего пара на 1 кг выпаренной воды определяют по формуле:
 .
.
ИЗУЧЕНИЕ ПРОЦЕССА РЕКТИФИКАЦИИ
Цель работы: изучение процесса ректификации в тарельчатой колонне непрерывного действия, определение числа теоретических тарелок и среднего КПД тарелок.
Приборы и принадлежности: установка ректификации, хроматограф ЛХМ-8 МД, бутылочки с пробками, смесь этиловый спирт – вода концентрацией 5 – 40 % массовых.
Введение
Ректификация – процесс разделения жидких гомогенных смесей путем взаимного обмена компонентами между жидкостью и паром, полученным испарением разделяемой смеси. Этот процесс основан на различной летучести компонентов, составляющих смесь, т.е. на различии в температурах кипения компонентов при одинаковом давлении.
Процесс ректификации осуществляют в колоннах, представляющих собой вертикальные цилиндрические аппараты, с контактными устройствами. Наибольшее распространение в промышленности получили ректификационные колонны, в которых в качестве контактных устройств используются колпачковые, ситчатые и провальные тарелки [1, 2]. В ректификационной колонне навстречу друг другу проходят неравновесные по составу потоки пара и жидкости. Пар в колонне идет снизу вверх, а жидкость стекает сверху вниз. На каждой тарелке колонны пар и жидкость вступают в контакт. Поскольку между жидкостью и паром отсутствует равновесие, то на тарелке между ними происходит обмен компонентами ( массообмен), в результате которого пар обогащается более летучим (низкокипящим) компонентом, а жидкость – менее летучим (высококипящим). В ректификационных колоннах массообмен между жидкостью и паром осуществляется через поверхность контакта паровой и жидкой фаз. Поверхность контакта фаз на тарелке образуется пузырьками и струями пара при прохождении (барботаже) его через слой жидкости. На рисунке 1 показана схема ректификационной колонны с провальными ситчатыми тарелками.
Пар, поступающий под нижнюю тарелку ректификационной колонны из кипятильника 1, имеет низкую концентрацию низкокипящего компонента. С верхней тарелки колонны пар с высокой концентрацией низкокипящего компонента уходит в дефлегматор 4, в котором он полностью конденсируется. Часть образовавшегося конденсата поступает на верхнюю тарелку для орошения колонны. Эта жидкость называется флегмой Ф. Остальную жидкость из дефлегматора отбирают в качестве верхнего продукта разделения – дистиллята Р. Деление конденсата на флегму и дистиллят осуществляется с помощью флегмоделителя 5. Часть жидкости, поступающей в кипятильник с нижней тарелки, отбирают в качестве кубового остатка W.
Исходную смесь F непрерывно подают на одну из тарелок в средней части, которая делит колонну на верхнюю укрепляющую 3 и нижнюю исчерпывающую 2 части. Таким образом, в ректификационной колонне осуществляется непрерывный процесс разделения исходной смеси F на дистиллят Р с высоким содержанием низкокипящего компонента и кубовой остаток W с низким его содержанием. Концентрации получаемых продуктов разделения зависят от числа тарелок в колонне и от режима ее работы.
1 Требования безопасности
Перед пуском установки убедиться в исправности ректификационной колонны, куба-испарителя, дефлегматора, трубопроводов, арматуры, приборов КИП, заземления, тепловой изоляции. Проверить наличие воды в магистральном трубопроводе.

1-кипятильник (куб-испаритель); 2-исчерпывающая часть колонны; 3-укрепляющая часть колонны; 4-дефлегматор; 5-флегмоделитель; 6-контактные тарелки.
Рисунок 1 - Схема работы ректификационной колонны
Пуск установки проводить в присутствии учебного мастера и под его непосредственным руководством.
Работая на площадках с высокой отметкой и вблизи вращающихся частей проявлять осторожность и аккуратность. Включение трубчатых электронагревателей производить стоя на диэлектрическом коврике. При отборе проб пара необходимо помнить, что на входе в пробоотборник он имеет температуру около 100оС. К выполнению лабораторной работы студенты допускаются только после прохождения инструктажа по безопасности труда и пожарной безопасности в лаборатории и на рабочем месте.
2 Описание установки и порядок выполнения работы
Исходная смесь хранится в баке-хранилище 3, из которого насосом 9 через фильтр 11 подается в напорный бак 4. Из напорного бака 4 исходная смесь самотеком через ротаметр поступает в подогреватель, расположенный в кубе 2, где она нагревается кубовым остатком. Температуру исходной смеси после подогрева определяют по показанию термометра. В ректификационную колонну 1 подогретая исходная смесь поступает на 7, 9 или 11 тарелку, считая сверху. Колонна имеет 12 ситчатых тарелок с сегментными сливными устройствами. Внутренний диаметр колонны 200мм. Для визуального наблюдения за процессом барботажа имеется смотровое окно.
С нижней тарелки жидкость стекает в куб-испаритель 2, имеющий внутри змеевик, обогреваемый паром. Конденсат греющего пара из змеевика отводится в канализацию через конденсационный горшок. Расход греющего пара регулируется вентилем, а давление определяется по манометру. В кубе-испарителя часть жидкости превращается в пар, а другая отводится в качестве кубового остатка. Кубовый остаток проходит холодильник 7, где охлаждается водой, и поступает в сборник 8. Из сборника 8 кубовый остаток возвращается в бак-хранилище 3. Сборники 6, 8 и межтрубное пространство дефлегматора 5 сообщены с атмосферой, что обеспечивает работу колонны под атмосферным давлением. С верхней тарелки колонны пар, обогащенный низкокипящим компонентом, поступает в дефлегматор 5, который охлаждается водой. Расход воды измеряется ротаметром, а температура ее на входе и выходе – термометрами. Жидкость, образовавшаяся в дефлегматоре после полной конденсации пара, делится на две части. Одна в виде флегмы подается на орошение колонны, а другая отбирается в виде дистиллята, который поступает в сборник 6 и далее направляется в бак-хранилище 3. Количество флегмы и дистиллята измеряется ротаметрами.
Колонна оборудована пробоотборниками жидкости с тарелок, флегмы, дистиллята, жидкости в кубе, а также пробоотборниками пара, поступающего на тарелку, и покидающего пенной слой. Пробоотборники пара снабжены теплообменниками типа «труба в трубе», в которых проба пара конденсируется, и конденсат собирается в бутылочки с пробками. На каждой тарелке колонны установлены датчики температуры, работающие в комплекте со вторичным прибором. Знание температуры жидкости на тарелках позволяет определить профиль температуры по высоте колонны. Перед пуском установки необходимо подать поду в дефлегматор, холодильник кубового остатка и в теплообменники на пробоотборниках пара. Открыть воздушники на дефлегматоре и сборниках.
|
|
|
1 – Ректификационная
колонна; 2 – куб; 3 – бак-хранилище; 4 –
напорный бак; Рисунок 2 – Принципиальная схема установки ректификации |
Проверяют, наполнен ли напорный бак 4 исходной смесью, и, если необходимо, насосом 9 подкачивают ее в этот бак из сборника – хранилища 3. Из напорного бака заполнить до указанной отметки куб-испаритель. Открывают вентиль на паропроводе, продувают конденсационный горшок и начинают прогрев куба-испарителя, следя за давлением греющего пара по манометру. Начало кипения смеси в кубе определяется визуально в смотровое окно (над тарелкой появляется пар и капли жидкости).
При этом необходимо полностью открыть вентиль на линии подачи флегмы в колонну и дать колонне поработать «самой на себя» (за высотой парожидкостного слоя на тарелках следить в смотровое стекло).
По заданию преподавателя установить по ротаметрам расходы исходной смеси, флегмы, дистиллята и кубового остатка. Чтобы расход питания не изменялся, уровень жидкости в напорном баке 4 должен быть постоянным. С этой целью включают насос 9 для непрерывной работы вплоть до окончания опыта. Все измерения и отбор проб производить после выхода установки на установившийся режим работы, который определяется по показаниям вторичного прибора (температура жидкости на тарелках не изменяется). Все полученные данные записывают в таблицу.
|
Наименование величин |
Значение |
Среднее значение |
||
|
1 |
2 |
3 |
||
|
Расход исходной смеси, кмоль/с |
||||
|
Расход дистиллята, кмоль/с |
||||
|
Расход кубового остатка, кмоль/с |
||||
|
Расход флегмы, кмоль/с |
||||
|
Расход воды в дефлегматоре, кг/с |
||||
|
Температура воды, поступающей в дефлегматор, 0С |
||||
|
Температура воды на выходе из дефлегматора, 0С |
||||
|
Температура пара, поступающего в дефлегматор из колонны, 0С |
||||
|
Температура флегмы, 0С |
||||
|
Концентрация, мольные доли: а) исходной смеси Х>F> б) флегмы (дистиллята) Х>р> в) кубового остатка Х>w> |
||||
|
Температура исходной смеси после подогрева, 0С |
Анализ проб пара и жидкости проводится методом газовой хроматографии на хроматографе ЛХМ-8 МД или рефрактометром.
После окончания работы закрывают вентили на линии греющего пара, прекращают подачу исходной смеси и отбор дистиллята, закрывают воду на холодильник кубового остатка и теплообменники на пробоотборниках пара. Воду на дефлегматоре закрывают только после того, как колонка остынет.
3 Обработка опытных данных
Переводят из массовых долей в мольные концентрации исходной смеси Х>F> и дистиллята Х>p>. Пересчитывают расходы исходной смеси F и дистиллята Р в мольные. Из уравнений материального баланса колонны находят расход и концентрацию кубового остатка по уравнениям
W=F – P, Х>w>=(FX>F> – PX>p>)/W,
гдеF, P, W-расходы исходной смеси, дистиллята, кубового остатка, кмоль/с;
X>f>. X>p>. X>w>-составы исходной смеси, дистиллята, кубового остатка, мол. доли.
Определяют флегмовое число R – отношение расхода флегмы к расходу дистиллята. Рассчитывают количество пара G, поднимающегося по колонне (рисунок 1).
Зная величину G и диаметр колонны, определяют скорость пара в свободном сечении колонны w. Скорость пара в колонне можно также рассчитать, определив количество пара из уравнения теплового баланса дефлегматора [1, 2] (этот расчет может быть использован как проверочный).
По справочным данным
строят на миллиметровой бумаге кривую
равновесия
 на диаграмме у-х (рисунок 3) и отмечают
на оси абсцисс значения концентраций
исходной смеси Х>F>
дистиллята Х>р>
и кубового остатка Х>w>.
на диаграмме у-х (рисунок 3) и отмечают
на оси абсцисс значения концентраций
исходной смеси Х>F>
дистиллята Х>р>
и кубового остатка Х>w>.
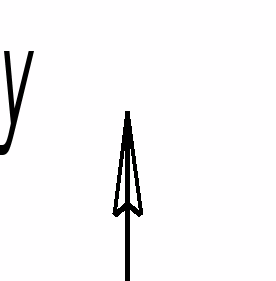
Рисунок 3 – Определение числа теоретических тарелок
Затем на диаграмму у-х наносят рабочие линии для укрепляющей и исчерпывающей частей колонны. Уравнения рабочих линий, получают из уравнений материального баланса. Они имеют следующий вид: для укрепляющей части колонны
 ,
,
для исчерпывающей части колонны
 ,
,
гдех, у–концентрация жидкости и пара в любом сечении колонны, мол. доли;
f – отношение расхода исходной смеси к расходу дистиллята.
Вычисляют отрезок
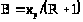 ,
который отсекает рабочая линия верхней
части колонны на оси ординат (рисунок
3). Через точку А (х>р>=
у>р>) и
полученный отрезок проводят рабочую
линию верхней части колонны. Через точку
Д (х>w>=
у>w>)
и точку С проводят рабочую линию нижней
части колонны. Между равновесной и
рабочими линиями строят ступени изменения
концентраций (рисунок 3). Каждая ступень
соответствует одной теоретической
тарелке. Определив число теоретических
ступеней n>Т>,
и, зная число реальных тарелок в колонне
n,
находят среднее значение КПД тарелки
по уравнению
,
который отсекает рабочая линия верхней
части колонны на оси ординат (рисунок
3). Через точку А (х>р>=
у>р>) и
полученный отрезок проводят рабочую
линию верхней части колонны. Через точку
Д (х>w>=
у>w>)
и точку С проводят рабочую линию нижней
части колонны. Между равновесной и
рабочими линиями строят ступени изменения
концентраций (рисунок 3). Каждая ступень
соответствует одной теоретической
тарелке. Определив число теоретических
ступеней n>Т>,
и, зная число реальных тарелок в колонне
n,
находят среднее значение КПД тарелки
по уравнению
 .
.
Величина КПД тарелки зависит от гидродинамических условий и физико-химических свойств пара и жидкости.
При работе колонны «на
себя» дистиллят не отбирается, т.е.
флегмовое число равно бесконечности
 .
В этом случае рабочая линия колонны
совпадает с диагональю.
.
В этом случае рабочая линия колонны
совпадает с диагональю.
Лабораторная работа
ЭКСТРАКЦИЯ
Цель работы: практическое ознакомление с работой противоточной экстракционной установки, экспериментальное определение движущей силы процесса экстракции и степени извлечения распределяемого вещества при различных соотношениях потоков.
Приборы и принадлежности: экстракционная установка, бюретка для титрования проб; 0,1 N раствор щелочи NaOH; индикатор – фенолфталеин; мерные цилиндры; конические колбы.
Введение
Экстракцией называют процесс извлечения одного или нескольких компонентов из растворов или твердых тел с помощью избирательных растворителей (экстрагентов). При взаимодействии раствора с экстрагентом в нем хорошо растворяются только извлекаемые компоненты и не растворяются остальные компоненты исходной смеси [1]. Экстракция в системах жидкость-жидкость представляет собой массообменный процесс, протекающий с участием двух взаимно нерастворимых или ограниченно растворимых жидких фаз, между которыми распределяется экстрагируемое вещество.
Процесс жидкостной экстракции состоит в том, что исходную смесь и экстрагент приводят в тесный контакт. В результате взаимодействия фаз получают экстракт – раствор извлеченных веществ в экстрагенте и рафинат – остаточный исходный раствор, из которого с той или иной степенью полноты удалены экстрагируемые компоненты. Полученные жидкие фазы (экстрагент и рафинат) разделяются отстаиванием, центрифуированием или другими гдромеханическими способами. После этого извлекают целевой продукт из экстракта и производят регенерацию экстрагента из рафината. Основное достоинство процесса экстакции по сравнению с другими процессами разделения жидких смесей (ректификация. выпаривание) состоит в том, что он осуществляется при низких рабочих температурах, чаще всего при комнатной температуре.
В зависимости от вида контакта между жидкими фазами экстракторы, как и другие массообменные аппараты, бывают: со ступенчатым контактом фаз (тарельчатые); с непрерывным контактом фаз (насадочные).
Методы осуществления жидкостной экстракции и аппаратура для нее весьма разнообразны. При противоточной экстракции исходная смесь и экстрагент поступают в экстракционную колонну навстречу друг другу и движутся в ней противотоком из-за разности в плотностях. Снизу в колонну подают более легкий продукт, сверху – более тяжелый. Рассмотрим случай, когда плотность экстрагента больше плотности исходной смеси. Экстрагент подается сверху и движется вниз, извлекая растворенный в исходной смеси целевой компонент. Образующийся при этом экстракт выводится из колонны снизу. Первичный растворитель исходной смеси по мере движения вверх освобождается от целевого компонента. Очищенный первичный растворитель – рафинат выводится из колонны сверху. При таком движении жидкостей в верхней части колонны разбавленный раствор экстрагируемого вещества в первичном растворителе обрабатывается свежим экстрагентом. Благодаря этому обеспечивается наиболее полное извлечение экстрагируемого компонента из рафината.
Любой процесс, связанный с переходом вещества из одной фазы в другую обратим, т.е. молекулы вещества могут переходить, как в одном, так и в другом направлении. Предел этого перехода – состояние равновесия между фазами. При полной взаимной нерастворимости первичного и вторичного растворителей каждый из них присутствует только в одной фазе. Степень отклонения рассматриваемой двухфазной системы от состояния равновесия является движущей силой процесса массообмена. Графически движущая сила выражается отрезком, заключенным между равновесной и рабочей линиями. Равновесия при экстрагировании можно достигнуть лишь через длительный промежуток времени взаимодействия сред. Практически в экстракционных аппаратах равновесие не достигается и концентрация У (действительная, рабочая) отличается от У* (равновесной).
На рисунке 1 представлена
схема процесса противоточной экстракции.
Обозначим массовый расход исходной
смеси (в данном случае керосин с бензойной
кислотой) через G,
содержание извлекаемого компонента в
ней через
 ;
массовый расход экстракта (вода с
бензойной кислотой) через L;
содержание извлеченного компонента
через
;
массовый расход экстракта (вода с
бензойной кислотой) через L;
содержание извлеченного компонента
через
 .
Концентрации
.
Концентрации
 выражены в относительных массовых
концентрациях.
выражены в относительных массовых
концентрациях.
Для противоточного экстрактора уравнение материального баланса имеет вид
 ,
,
где М – масса вещества, перешедшего в единицу времени из первичного растворителя в экстракт, кг/с.
Рассмотрим сечение I – I экстрактора (рисунок 1) и составим материальный баланс для верхней части аппарата

Из этого уравнения определим концентрацию в любом сечении верхней части аппарата
 .
.
Мы получили уравнение
рабочей линии процесса экстракции,
которое графически выражается прямой
линией. В случае действующего экстрактора
значения
 определяются
экспериментально и по двум точкам
определяются
экспериментально и по двум точкам
 и
и
 , строится рабочая линия, наклон которой
зависит от соотношения потоков
, строится рабочая линия, наклон которой
зависит от соотношения потоков
 (рисунок
1).
(рисунок
1).


ОС – линия равновесия;
АВ – рабочая линия, прямая, проходящая
через точки А и
В
и
В ,
при соотношениях потоков
,
при соотношениях потоков
 ;
А>1>В>1>
– рабочая линия, полученная при
соотношения потоков
;
А>1>В>1>
– рабочая линия, полученная при
соотношения потоков
 .
.
Рисунок 1- Схема процесса противоточной экстракции
Положение равновесной линии определяется физическими свойствами системы и условиями (температура, давление), в которых находится данная система. Данные по равновесию приведены в таблице 1.
Таблица 1
Равновесные концентрации
бензойной кислоты
в воде
и в керосине
|
|
0,185 |
0,661 |
1,073 |
1,705 |
|
|
0,440 |
0,851 |
1,076 |
1,387 |
Чем больше система отклонена от равновесия, тем интенсивнее она стремится к нему и наоборот, при малых отклонениях от равновесия движущая сила мала.
Движущая сила процесса
переменна по высоте аппарата; внизу
аппарата она равна отрезку
 :
:
 ;
вверху аппарата она равна
;
вверху аппарата она равна
 :
:
 .
.
Средняя движущая сила
процесса экстракции равна среднему
арифметическому (если
 )
или среднему логарифмическому значению.
)
или среднему логарифмическому значению.

Чем больше движущая сила
процесса, тем больше вещества передается
за одно и то же время на одном и том же
участке аппарата из одной фазы в другую
 .
.
Изменяя соотношения потоков, мы изменяем и движущую силу процесса.
1 Требования безопасности
К работе на установке допускаются студенты, прошедшие в начале семестра инструктаж по технике безопасности в лаборатории Б-011 и расписавшиеся в книге инструктажей. Студенты обязаны перед началом работы надеть спецодежду и убрать волосы под косынку. Следует убедиться в наличии средств пожаротушения и медицинской аптечки. Начинать работу можно только в присутствии учебного мастера и преподавателя, и только с их разрешения. Перед началом работы студенты должны отчитаться перед преподавателем о своей подготовке к работе. Каждый студент должен знать место нахождения средств пожаротушения и уметь ими пользоваться. При появлении течи через вентили или фланцевые соединения, прекратить подачу растворителя и экстрагируемой смеси, закрыв все вентили на линии подачи. В случае поломки ротаметров закрыть вентили на линии подачи и выключить насосы, если они включены. В случае разлива рабочей смеси на пол, необходимо немедленно ее убрать в канализацию с помощью тряпки или щетки. По окончании работы каждый студент обязан проверить и привести в порядок рабочее место, вымыть пробирки. Запрещается: находиться в верхней одежде или хранить ее в помещении лаборатории; принимать пищу в лаборатории; уходить с рабочего места и оставлять включенную установку без присмотра.
2 Описание установки и порядок выполнения работы
Экстракционная установка состоит из колонного экстрактора 1 (рисунок 2), баков для жидкостей 2, 3, 4, 5, емкостью 0,1668м3, 2-х напорных баков 6, 7, центробежных насосов с электродвигателями 8, 9, приборов КИП и системы трубопроводов. Колонный экстрактор состоит из 4-х секций, разделенных между собой ситчатыми тарелками. Размеры больших секций: высота – 0,282м, диаметр – 0,170м; промежуточных секций: высота – 0,290м, диаметр – 0,065м. В верхней и нижней секциях имеются по два патрубка для входа и выхода рабочих жидкостей. В баках 2, 3 находится экстрагент (вода), в баках 4, 5 исходная смесь (керосин с бензойной кислотой).
Экстрагент из бака 2 или 3, снабженных указателями уровня, посредством насоса 9 подается в напорный бак 6 и из него самотеком поступает в верхнюю часть экстрактора 1. Напорный бак 6 служит для поддержания постоянного напора экстрагента, расход которого замеряется с помощью ротаметров, расположенных на линии подачи экстрагента в колонну. Исходная смесь из бака 4 или 5, снабженных указателями уровня посредством насоса 8 подается в напорный бак 7, а оттуда в нижнюю часть экстрактора 1. Расход исходной смеси определяется с помощью ротаметров, расположенных на линии подачи исходной смеси в экстрактор.
Поступая в экстрактор, экстрагируемая смесь и растворитель смешиваются. Благодаря ситчатым тарелкам достигается более полное смешение рабочих жидкостей. Осуществляется противоточное экстрагирование, так как экстрагируемая смесь с меньшей плотностью идет снизу вверх колонн; вода отнимает бензойную кислоту из керосина, выходит из нижней секции колонны и поступает в бак 2 или 3 через гребенку 10, которая служит для регулирования положения границы раздела фаз в колонне. Рафинат (керосин) при выходе из колонного экстрактора по трубопроводу сливается в бак 4 или 5. Для контроля за процессом экстракции в каждой секции колонны имеются пробники. Для определения состава фаз до и после процесса предусмотрены пробники на линиях подачи и выхода продуктов. Все бачки и верхние части трубопроводов имеют воздушники, сообщающиеся с атмосферой.
Открыть вентиль на линии подачи экстрагента из бака 2 или 3 к насосу 8, открыть вентили на трубопроводе нагнетания экстрагента в напорный бак 6 и включить насос 8. Когда бак 6 наполнится и вода по сливной трубе будет сливаться обратно в бак 2 или 3, необходимо насос выключить Открыть вентиль на линии подачи исходной смеси из бака 3 или 4 к насосу 9, открыть вентили на нагнетательном трубопроводе исходной смеси в напорный бак 7 и включить насос 9. После наполнения бака 7 по сливной трубе жидкость будет стекать обратно в бак для исходной смеси. Необходимо насос 9 сразу отключить, иначе может произойти переполнение бака 7 и разбрызгивание керосина через воздушный патрубок, расположенный в верхней крышке бака 7.
Регулировочными вентилями по ротаметрам Р установить заданные преподавателем расходы экстрагента и исходной смеси в экстрактор и поддерживать их постоянными в течение всего опыта.
После заполнения полностью колонны и установления четкой линии раздела фаз (в середине второй или третьей секции) приступить к отбору проб через пробники П. После отбора проб изменить расход экстрагента и через 5-10 минут отобрать еще раз пробы через пробники П.
После окончания отбора проб прекратить подачу исходной смеси, закрыть вентиль на линии слива экстракта из колонны и продолжать подачу воды в колонну. Поверхность раздела фаз при этом будет подниматься, и когда она достигнет верха колонны, т.е. весь керосин сольется из экстрактора, необходимо быстро открыть вентиль на линии слива экстракта и прекратить подачу экстрагента.
|
|
|
1 – экстрактор; 2, 3 – баки для воды; 4, 5 – баки для керосина; 6, 7 – напорные баки; 8, 9 – насосы; 10 – гребенка; П – пробники; Р – ротаметры. Рисунок 2 – Схема экстракционной установки |
3 Обработка опытных данных
Содержание бензойной
кислоты  определяем
титрованием отобранных проб 0.1 N
раствором NаОН
в присутствии индикатора - фенолфталеина.
определяем
титрованием отобранных проб 0.1 N
раствором NаОН
в присутствии индикатора - фенолфталеина.
Нормальность раствора
бензойной кислоты определяется по
зависимости
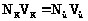
Для титрования берется
20-25 мл исследуемой жидкости. Содержание
бензойной кислоты в исследуемой жидкости
определяется (кг/м3), где
Эк – эквивалент кислоты равный 122.
(кг/м3), где
Эк – эквивалент кислоты равный 122.
Затем необходимо пересчитать объемную массовую концентрацию в относительные массовые доли по формулам

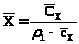 ,
,
Можно принять при рабочих концентрациях ρ>1 >- плотность керосина, ρ>2> - плотность воды, кг/м3.
Построить на диаграмме
Х – У равновесную и рабочие линии,
соответствующие разным соотношениям
 .
Определить массовый расход первичного
растворителя (керосина)
.
Определить массовый расход первичного
растворителя (керосина)
 .
Определить массовый расход экстрагента
(вода)
.
Определить массовый расход экстрагента
(вода)
 ,
где V>B>,
V>K>,
ρ>2, >ρ>1
– > объемный расход и
плотность воды и керосина. Полученные
данные занести в таблицу 2.
,
где V>B>,
V>K>,
ρ>2, >ρ>1
– > объемный расход и
плотность воды и керосина. Полученные
данные занести в таблицу 2.
Убедится, что при увеличении движущей силы процесса, увеличивается количество переданного из фазы в фазу вещества М, которое определяется из уравнения материального баланса. Сравнить конечные концентрации продуктов и сделать вывод о ходе процесса экстракции, определить степень извлечения бензойной кислоты в обоих
случаях по формуле:

Таблица 2
Опытные и рассчитанные данные
|
Параметр |
Значения |
Среднее значение |
||
|
Расход исходной смеси, кг/с |
||||
|
Расход экстрагента, кг/с |
||||
|
Относительная массовая концентрация бензойной кислоты в керосине
|
||||
|
Относительная массовая концентрация бензойной кислоты в воде
|
||||
|
Средняя движущая сила процесса
|
||||
|
Количество переданного из фазы в фазу вещества М |
||||
|
Степень
извлечения бензойной кислоты
|
Лабораторная работа
АБСОРБЦИЯ
Цель работы: практическое ознакомление с работой тарельчатого абсорбера, экспериментальное определение коэффициента массопередачи и сравнение его с рассчитанным теоретически.
Приборы и принадлежности: абсорбционная установка, бюретка для титрования; 0.1 N раствор соляной кислоты; индикатор-фенолфталеин; конические колбы.
Введение
Абсорбцией называют процесс избирательного поглощения газа из смеси газов (или пара из парогазовой смеси) жидким поглотителем. В абсорбционных процессах участвуют две фазы – газовая и жидкая. При абсорбции происходит переход вещества из газовой фазы в жидкую, обратный процесс называется десорбцией, при этом происходит переход вещества из жидкой фазы в газовую. Все процессы массопередачи обратимы, т.е. в зависимости от условий, направление перехода распределяемого вещества может быть различным. Равновесие в процессах абсорбции определяет состояние, которое устанавливается при продолжительном соприкосновении фаз и зависит от состава одной из фаз, температуры, давления и термодинамических свойств компонента и поглотителя [1,2].
Для каждой конкретной
системы газ-жидкость при определенной
температуре и давлении существует
строго определенная зависимость между
равновесными концентрациями, т.е. каждому
значению Х соответствует строго
определенное равновесное значение У*
и эту связь можно представить
в виде функции

В общем случае эта
зависимость находится опытным путем.
Для большего числа систем имеются данные
в справочной литературе. Для разбавленных
растворов хорошо растворимых газов
равновесная зависимость
 хорошо описывается законом Генри,
который имеет вид
хорошо описывается законом Генри,
который имеет вид
 ,
где
,
где
 -
константа фазового равновесия, величина
которой зависит от природы газа и
жидкости и единиц, в которых выражены
концентрации.
-
константа фазового равновесия, величина
которой зависит от природы газа и
жидкости и единиц, в которых выражены
концентрации.

ОС – линия равновесия  ;
АВ – рабочая линия - прямая,проходящая
через точки (Y>H>>,
>X>K>)
и (Y>K>,
X>H>)
;
АВ – рабочая линия - прямая,проходящая
через точки (Y>H>>,
>X>K>)
и (Y>K>,
X>H>)
Рисунок 1 - Схема процесса абсорбции
Примем расходы фаз по высоте аппарата постоянными и выразим содержание поглощаемого газа в относительных мольных концентрациях. Обозначим: G – расход инертного газа, кмоль/с; Y>H> ,Y>K>> >-начальная и конечная концентрации компонента в газовой смеси, кмоль/кмоль инертного газа; L – расход абсорбента, кмоль/сек; его концентрации X>H> и X>K>, кмоль/кмоль абсорбента.
Уравнение материального баланса абсорбера имеет вид
 .
.
Выделим любое сечение в аппарате (рисунок 1), например, 1-1, в котором имеются рабочие концентрации X и Y. Напишем материальный баланс для верхней части аппарата по распределяемому компоненту

Если исходный абсорбент не содержит распределяемый компонент (X>H>> >= 0), то
 .
.
Полученная зависимость называется уравнением рабочей линии.
Это уравнение позволяет нам определить значение рабочей концентрации в любой точке аппарата. Так как G, L – величины постоянные для каждого конкретного случая, то это уравнение прямой линии и для ее построения необходимо всего две точки. Можно взять вверху колонны B (X>H>, Y>K>) и внизу колонны A (X>K>, Y>H>).
Разность между рабочей
и равновесной концентрациями вещества
в данной фазе называется движущей силой
массопередачи ΔY=Y
– Y*.
Она непрерывно меняется по высоте
аппарата. В частном случае, когда
линия равновесия является прямой,
 определяется
как средняя логарифмическая величина
из движущих сил массопередачи у концов
аппарата
определяется
как средняя логарифмическая величина
из движущих сил массопередачи у концов
аппарата
 ,
,
где ΔУ>б >, ΔУ>м> – большая и меньшая разность рабочих и равновесных концентраций на концах аппарата> >.
Основное уравнение массопередачи для процесса абсорбции

где М – количество компонента, передаваемое через поверхность контакта фаз, кмоль/с;
 -
поверхность контакта фаз, м2.
-
поверхность контакта фаз, м2.
Так как поверхность контакта газа и жидкости зависит от скорости потока, физических свойств фаз и типа аппарата, то обычно расчеты тарельчатых абсорберов проводят по модифицированному уравнению массопередачи, в котором коэффициенты массопередачи относят к единице рабочей площади тарелки
 ,
,
где
 -
коэффициент массопередачи, отнесенный
к единице площади тарелки,
моль/м2(кмоль/кмоль)с;
-
коэффициент массопередачи, отнесенный
к единице площади тарелки,
моль/м2(кмоль/кмоль)с;
F- суммарная рабочая площадь тарелок в абсорбере, м2;
 ,
,
где
 -
рабочая площадь тарелке, м2;
-
рабочая площадь тарелке, м2;
n - число тарелок в абсорбере.
Рабочая площадь провальной
тарелки может быть принята равной
сечению абсорбера. Зная М – количество
поглащенного аммиака (в кмоль/с), и
рассчитав F
и
 можно определить коэффициент массопередачи
можно определить коэффициент массопередачи
 .
.
Коэффициенты массопередачи определяют по уравнениям аддитивности фазовых диффузионных сопротивлений

где β>yf>. β>xf>> >– коэффициенты массоотдачи, отнесённые к единице рабочей площади тарелки, соответственно в газовой и жидкой фазах, кмоль/м2 (кмоль/кмлоь)с.
При абсорбции хорошо
растворимых газов
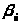 <<
<< ,
и в этом случае величиной m/β>y>
,
и в этом случае величиной m/β>y> можно
пренебречь, т.е.
можно
пренебречь, т.е.
 .
Поэтому при абсорбции аммиака водой
можно приравнять общий коэффициент
массопередачи частному коэффициенту
массоотдачи в газовой фазе.
.
Поэтому при абсорбции аммиака водой
можно приравнять общий коэффициент
массопередачи частному коэффициенту
массоотдачи в газовой фазе.
Требования безопасности
К работе на установке
допускаются студенты, прошедшие в начале
семестра инструктаж по технике
безопасности в лаборатории
Б-011 и
расписавшиеся в журнале инструктажей.
Студенты обязаны перед началом работы
надеть спецодежду и убрать волосы под
косынку. Начинать работу можно только
в присутствии учебного мастера и
преподавателя, и только с их разрешения.
Перед началом работы студенты должны
отчитаться перед преподавателем о своей
подготовке к работе.
При появлении запаха аммиака во время работы немедленно прекратить его подачу, перекрыв вентиль расхода, а расход воды в абсорбер увеличить до полного удаления запаха. В случае попадания раствора аммиака на кожу или в глаза немедленно обильное промывание широко раскрытого глаза водой или 0.5-1% раствором квасцов, наложить вазелиновое или оливковое масло. Необходимо помнить, что высокая концентрация аммиака в воздухе вызывает обильное слезотечение, боль в глазах, удушье, сильные приступы кашля, ПДК аммиака в воздухе – 20 мг/м3 . При отравлении аммиаком через дыхательные пути необходимо вынести человека на воздух, вдыхание теплых водяных паров, пить теплое молоко с содой. По окончании занятия каждый студент обязан проверить и привести в порядок рабочее место.
Описание установки и порядок выполнения работы
Абсорбер представляет собой колонну 1 с внутренним диаметром 0,2м, высотой 1,68м, выполненную из органического стекла (рисунок 2). В колонне установлены 4 тарелки провального типа с отверстиями 3,5мм, долей свободного сечения 20%. В верхней части колонны имеется брызгоотделитель, внутри которого размещены распределитель жидкости и каплеотборник, уменьшающий унос жидкости уходящими газами. Колонна установлена на сборнике 2 диаметром 0.44 и высотой 0.7м. Установка снабжена баллоном с аммиаком 5, системой трубопроводов, арматурой и КИП.
Абсорбент (вода) подается в верхнюю часть колонны 1. Расход воды регулируется вентилями по показаниям ротаметра 10. Воздух к установке подается от компрессора, расположенного в лаборатории Б-03, через коллектор 7. Скорость воздуха замеряется с помощью диафрагмы 8 и соединенного с ней дифманометра 9. Аммиак из баллона 5 дросселируется редукционным вентилем, расход NH>3> определяется ротаметром 11. Аммиак поступает в коллектор 7, а затем в смеситель 6; куда подается и воздух, а затем аммиачно-воздушная смесь подается вниз абсорбера 1. Смесь движется снизу вверх, а сверху вниз по тарелкам стекает вода. На тарелках образуется газо-жидкостный слой. Вода поглощает абсорбтив (аммиак) и поступает в сборник 2. Воздух, содержащий газ, выбрасывается в атмосферу. В нижней части абсорбера находится пробоотборник для отбора пробы жидкости, поглотившей аммиак. Концентрация аммиакта в воде определяется титрованием пробы 0.1 HCℓ. Для определения гидравлического сопротивления на 2-х тарелках служит дифманометр 12.
При выполнении работы строго соблюдать очередность подачи. Сначала необходимо подать воду в абсорбер, установить заданный расход и поддерживать его постоянным. Затем подать воздух в колонну, установить и поддерживать постоянную его скорость в колонне и замерить перепад давления на 2-х тарелках. И только потом открыть редукционный вентиль и подать аммиак в абсорбер. Установить расход аммиака не более 10-20 делений по ротаметру, через 3-5 минут отобрать пробу жидкости внизу колонны и прекратить подачу аммиака, затем воздуха и не ранее 10-15 минут закрыть вентили на линии подачи воды в абсорбер.
Все измеренные величины занести в таблицу.

1 – абсорбер; 2 – сборник; 3 – фильтр; 4 – гидрозатвор; 5 – баллон с аммиаком; 6 – смеситель; 7 – коллектор; 8 – диафрагма; 9 – дифманометр; 10,11 – ротаметры; 12 – дифманометр; В – вентили
Рисунок 2 - Схема абсорбционной установки
Обработка опытных данных
Таблица 1
Опытные и рассчитанные данные
|
Наименование величин |
Значение |
Среднее значение |
||
|
1 |
2 |
3 |
||
|
Расход воды; кмоль/с |
||||
|
Скорость воздуха в колонне; м/с |
||||
|
Расход воздуха в колонне; кмоль/с |
||||
|
Расход аммиака, кмоль/с |
||||
|
Перепад давления на 2-х тарелках; Па |
||||
|
Концентрация
аммиака в исходной смеси |
||||
|
Концентрация
аммиака в воздухе на выходе из колонны
|
||||
|
Концентрация
аммиака в воде на выходе из колонны
|
||||
|
Движущая
сила массопередачи
|
||||
|
Коэффициент
массопередачи |
||||
|
Коэффициент
массоотдачи |
Расходы воды, воздуха и аммиака необходимо выразить в мольных единицах. Концентрацию аммиака в воздухе Y>H> определяем исходя из расходов аммиака и воздуха в кмоль NH>3>/кмоль воздуха.
Конечная концентрация аммиака в воздухе Y>K>> >рассчитывается из уравнения материального баланса
 .
.
Начальная концентрация аммиака в воде X>H>=0, так как вода, поступающая в абсорбер, аммиака не содержит аммиак.
Конечная концентрация аммиака в воде X>K> определяется титрованием отобранной пробы 0.1 н раствором HCℓ. Определив в результате титрования нормальность раствора, выразить концентрацию поглощаемого газа в C>х> [кмоль/м3] и пересчитать в относительные мольные единицы по формуле

где М>ж>,> >М>К >– молекулярные массы воды и аммиака, кг/кмоль;
ρ>ж> – плотность воды, кг/м3.
Расход воздуха в колонне определяется по уравнению расхода.
Рассчитав концентрации Y>H>, Y>K>, X>H>, X>K>, строим рабочую линию по 2 точкам (X>H> , Y>K>), (X>K>, Y>H> ).
Линия равновесия
определяется по уравнению
 ,
где m=1.825
– найдена экспериментально для водных
растворов NH>3>.
Наносим рабочую и равновесную линии на
график, определяем
,
где m=1.825
– найдена экспериментально для водных
растворов NH>3>.
Наносим рабочую и равновесную линии на
график, определяем
 .
Зная количество поглощенного аммиака,
определяем коэффициент массопередачи
K>yf>.
Коэффициент массоотдачи β>yf>>
>определяем из критерия
Нуссельта диффузионного
.
Зная количество поглощенного аммиака,
определяем коэффициент массопередачи
K>yf>.
Коэффициент массоотдачи β>yf>>
>определяем из критерия
Нуссельта диффузионного
 ,
,
где Д – коэффициент молекулярной диффузии компонента в газе, м2/с;
ℓ – характерный линейный
размер, в данном случае ℓ =κ - капиллярная
константа, м.
– характерный линейный
размер, в данном случае ℓ =κ - капиллярная
константа, м.
где
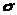 - поверхностное натяжение на границе
газ - жидкость, н/м .
- поверхностное натяжение на границе
газ - жидкость, н/м .
Критерий Нуссельта
диффузионный для провальных тарелок
рассчитывается по уравнению  ,
,
где критерий Рейнольдса
 ;
;
критерий Прандтля
 ;
;
критерий Вебера
 .
.
Высота столба жидкости на тарелке h>ст>, рассчитывается из гидравлического сопротивления орошаемой тарелки ΔР>т>, измеренного U-образным дифференциальным манометром, м.
 ,
,
где ΔР> сух >– сопротивление сухой тарелки, Па;
ΔРσ-сопротивление тарелки, вызываемое силами поверхностного натяжения, Па;
ΔР>г-ж >- сопротивление газожидкостного слоя на тарелке, Па.
Сопротивление сухой тарелки рассчитывается по уравнению

где ζ – коэффициент сопротивления тарелки (ζ=2.1);
ω>о >– скорость газа в отверстиях тарелки (ω>о >=ω/ƒ>св>),м/с;
ƒ>св >- свободное сечение тарелки (ƒ>св>=0.2).
Сопротивление тарелки, вызванное действием сил поверхностного натяжения, определяют по уравнению

где d>о> – диаметр отверстий тарелки, м.
Сопротивление газожидкостного слоя принимают равным статическому давлению слоя
ΔР>г-ж>=gρ>ж>h>ст>
Определив критерий Нуссельта диффузионный, рассчитывают β>yf> и сравниваем K>yf> и β>yf>.
Сделать вывод о сопоставимости полученных значений коэффициентов.
Список литературы
Дытнерский Ю.И. Процессы и аппараты химической технологии: Учебник для вузов. Изд. 3-е. В 2-х кн. / Ю.И. Дытнерский. – М.: Химия, 2002. –кн.1. - 400 с.: ил. -кн. 2. -368 с.: ил.
Павлов К.Ф. Примеры и задачи по курсу процессов и аппаратов химической технологии. 9-е изд., пер. и доп. / К.Ф. Павлов, Н.Г. Романков, А.А. Носков. – Л.: Химия, 1981. - 560 с.
Руководство к практическим занятиям в лаборатории процессов и аппаратов химической технологии: Учеб. пособие для вузов. / Под. ред. чл.-корр. АН СССР П.Г. Романкова - 6-е изд., перераб. и доп. – Л: Химия, 1990. - 272 с.: ил.


 ,
кг/м3
,
кг/м3 ,
кг/м3
,
кг/м3








