Липиды центральной нервной системы и структура клеточных мембран
Липиды центральной нервной системы и структура клеточных мембран
Введение
Липиды являются не только структурными компонентами ЦНС, но и важнейшими участниками функциональной активности. Головной мозг характеризуется высоким содержанием липидов. Мозг содержит уникальные мембранные структуры – миелиновые оболочки, которые имеют самое высокое содержание липидов по сравнению с другими тканями или субклеточными структурами, за исключением адипозной ткани. Для ЦНС характерно и наибольшее структурное разнообразие липидов по сравнению с мембранами других органов.
Липидный состав нервной ткани практически постоянен и остается неизменным даже под влиянием внешних факторов, которые меняют липвдный состав висцеральных органов и плазмы. Это – следствие защищенности ЦНС от различных внешних воздействий. Изменение липидного состава нервной ткани рассматривается обычно как патология, хотя при этом следует помнить, что существенные изменения в липидном составе нервной системы происходят в период развития.
Вся сложнейшая деятельность нервной ткани опосредуется через мембраны, в формировании и функционировании которых липиды принимают непосредственное участие.
В клетках нервной системы представлено несколько типов высокоспециализированных мембран: соматические мембраны мульти- и униполярных нейронов, мембраны дендритов, миелинизированных и немиелинизированных аксонов, аксонного холмика, где генерируется потенциал действия, мембраны рыхлого и компактного миелина, мембраны синаптических пузырьков, пре- и постсинаптические мембраны, мембраны макро- и микроглии. Возбудимость этих мембран колеблется в широких пределах от высоковозбудимых до относительно устойчивых мультимембранных структур миелина. В составе, строении и функционировании мембран нервной ткани еще очень много неясного. Для того чтобы раскрыть надмолекулярную организацию этих мембран, надо иметь достаточно полное представление об их липидном и белковом составе. Однако исследователи пока не владеют этими сведениями в полной мере, хотя ряд важных закономерностей уже намечен.
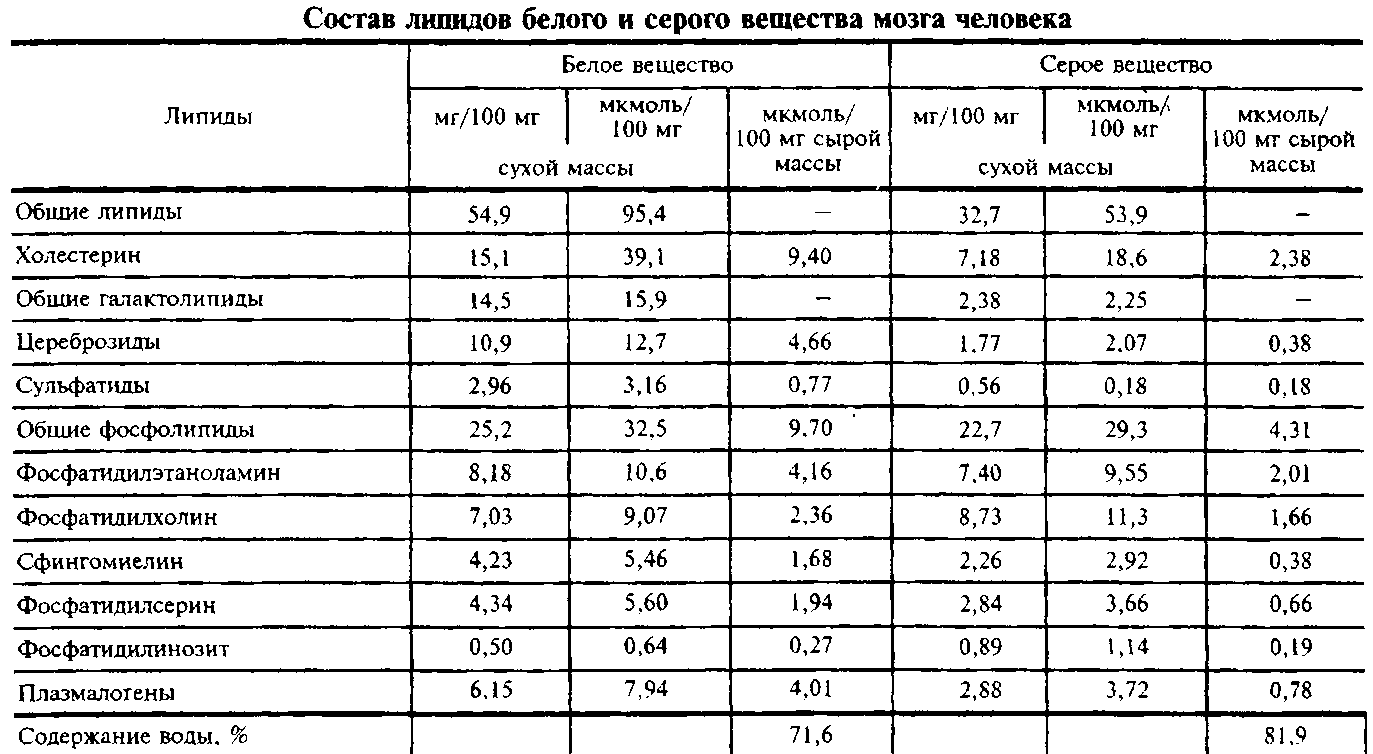
Липидный состав серого и белого вещества мозга человека представлен в табл. 1, а различных клеток мозга – в табл. 2. Видно, что липидный состав белого вещества ближе к миелину, а серое вещество содержит меньше типичных миелиновых ли-пидов, но относительно больше ганглиозидов.
Сравнивая молярное содержание основных классов липидов в специализированных клетках мозга, можно видеть, что оли-годендроглия и миелин наиболее обогащены цереброзидами, а нейроны и астроглия имеют более высокое содержание фосфолипидов. Это лишний раз подтверждает, что плазматические мембраны совершенно отличны от миелина.
Состав фосфолипидов обогащенных фракций нейронов и нейроглии коры мозга крысы представлен в табл. 3.
Чем более анатомически дифференцированно подходить к нервной ткани, тем больше различий обнаруживается в липидном составе, поскольку функционально различные нейрональ-ные и глиальные клетки имеют своеобразный липидный состав.
В состав большинства липидов входят жирные кислоты. В мозге они гораздо разнообразнее, чем в других тканях. Это намного увеличивает число индивидуальных липидов мозга. Содержание жирных кислот в головном мозге гораздо выше, чем в других органах, и составляет примерно 20–25% в расчете на сухую массу ткани. Разнообразие жирных кислот в этом органе поразительно. Применение газожидкостной хроматографии позволило продемонстрировать наличие в головном мозге более 50 жирных кислот с длиной цепи от 12 до 26 углеродных атомов, среди которых найдены насыщенные, ненасыщенные, нормальные, гидроксизамещенные, нечетные и др. Ненасыщенные кислоты мозга могут содержать от 1 до 6 двойных связей. Особенностью, липидов мозга является относительно большое содержание длинноцепочечных полиеновых кислот 20:4, 22: 5, 22:6.
Отдельные классы и фракции липидов мозга характеризуются своим набором жирных кислот. Имеет место также определенная специфичность жирнокислотного состава в лип идах разных отделов мозга, разных типов его клеток, субклеточных структур. Иллюстрацией этого могут служить данные табл. 4, где приведен жирнокислотный состав фосфолипидов синаптосом и миелина – двух разных типов мембранных структур ЦНС,
Состав липидов основных типов нервных клеток мозга крысы
|
Липиды |
Нейроны |
Астроглия |
Олигоден-дроглия |
Миелин |
|
Холестерин |
6,610 |
14,100 |
10,800 |
54,900 |
|
Цереброзиды |
0,513 |
0,689 |
2,610 |
22,000 |
|
Сульфатиды |
0,090 |
0,142 |
0,472 |
2,890 |
|
Общие фосфолипиды |
22,400 |
35,600 |
23,400 |
41,800 |
|
Ганглиозиды |
0,223 |
0,582 |
0,239 |
0,0453 |
|
Молярное отношение: холестерин – цереброзиды-фосфолипиды |
1:0,075:3,5 |
1:0,05:2,5 |
1:0,25:2,2 |
1:0,40:0,76 |
|
Фосфолипиды |
Нейроны |
Нейроглия |
|
Лизофосфатидилхолин |
3,9 |
1,9 |
|
Фосфатидилхолин |
46,1 |
46,9 |
|
Сфингомиелин |
6,7 |
9,5 |
|
Фосфатидилсерин |
9,1 |
7,1 |
|
Фосфатидилинозит |
7,7 |
5,9 |
|
Фосфатидил этанол а мин |
25,1 |
24,9 |
|
Фосфатидная кислота |
1,8 |
3,6 |
Содержание индивидуальных фосфолипидов в коре мозга крысы резко различающихся по своему происхождению и функциям.
В синаптосомах велико содержание жирных кислот – С 22:6, а в миелине высок процент моноеновых кислот – 18:1. Возможно, что высокое содержание докозагексаеновой кислоты в синаптосомах необходимо для активного транспорта ионов, так как активность Na+, К+-АТФазы в них зависит от присутствия полиеновых кислот в фосфолипидах. В мозге имеются регуля-торные механизмы, поддерживающие степень ненасыщенности и специфичность жирнокислотного состава в липидах.
Состав жирных кислот фосфолипидов сннаптосомальных и миеляновых мембран коры мозга обезьяны
|
Шифр жирной кислоты |
Фосфатид ил- |
|||||
|
холи н |
этанол амин |
серин+монофосфо-инозитид |
||||
|
синапто-сомы |
миелин |
синапто-сомы |
миелин |
синапто-сомы |
миелин |
|
|
16:0 |
50 |
33,1 |
7,4 |
4,9 |
3,5 |
2,6 |
|
18:0 |
12,4 |
17 |
25,5 |
15,9 |
44,3 |
43 |
|
18:1 |
27,2 |
42,3 |
12,1 |
33,2 |
П, 4 |
38,5 |
|
20:1 |
0,7 |
0,9 |
1,6 ■ |
9,3 |
- |
2,5 |
|
20:4 |
3,8 |
3,2 |
10,1 |
11,6 |
8,3 |
6,3 |
|
22:4 |
0,8 |
0,6 |
6,4 |
13,1 |
3,5 |
3,7 |
|
22:6 |
3 |
2,3 |
24,9 |
10,6 |
26,9 |
2,9 |
Изменение жирнокислотного состава приводит к нарушению функциональной деятельности мозга.
1. РОЛЬ АЦИЛОБМЕННОГО МЕХАНИЗМА
В мембранах головного мозга имеет место цикл деацилирование – реацилирование, при котором происходит замена жирных кислот в молекуле фосфолипидов, в то время как другие компоненты молекулы остаются неизменными. Этот ацилобменный механизм является особенно важным для включения тех или иных жирных кислот во второе положение остатка глицерина, и его рассматривают как средство локального регулирования физических и функциональных свойств мембран. Существенную роль играет и переход диацильных форм фосфолипидов в моноацильные и обратно. Все это оказывает влияние на такие мембранные процессы, как проницаемость для различных веществ, транспорт ионов и т.д.
Ацилобменные реакции имеют прямое отношение ко многим процессам, влияя на активность ряда ферментов, на синтез простагландинов и чувствительность фоторецепторов. Некоторые исследователи связывают ферментативное деацилирование – реацилирование с эффектом синаптической передачи. Так, под влиянием норадреналина в синаптосомах происходит активирование фосфолипазы А>2>, отщепляющей жирную кислоту во втором положении глицерофосфолипида. Таким образом, нейромедиатор модифицирует обмен фосфолигавдов в синаптических мембранах путем вовлечения в этот процесс реакций деацилирования. Предложена следующая схема регуляции активности ацилобменного цикла нейромедиаторами.

2. ОРГАНИЗАЦИЯ ЛИПИДОВ В МЕМБРАНЕ
Образование липидных молекул в ходе эволюции и выбор именно этих молекул в качестве строительных блоков мембран сыграли решающую роль в возникновении жизни. Липидам принадлежит жизненно важная роль в клетке. Следующие особые физико-химические свойства липидов определяют их роль в построении мембран:
1. Сочетание гидрофильных и липофильных свойств в структуре одной молекулы, их амфифильность.
2. Способность липидов четко ориентироваться на границе раздела фаз, так что полярные группы направлены в водные среды, а неполярные экранированы от них.
3. Способность липидов самопроизвольно упаковываться в прочные, плотные мономолекулярные слои или пленки, устойчивые к сжатию. Плотность такой упаковки зависит от рН, температуры и молекулярной организации липидов. Такие плотные слои создают определенный барьер для диффузии молекул.
4. Способность липидов агрегировать в хорошо упорядоченные сферические, цилиндрические, ламеллярные мицеллы. В мицеллах липиды ориентированы таким образом, чтобы максимальное число полярных групп находилось в контакте с водой, а гидрофобная часть была максимально удалена от контакта с ней.
Способность липидов образовывать прочные мономолекулярные слои лежит в основе молекулярной организации мембран. Более 60 лет назад было высказано предположение, что в основе мембран лежит бимолекулярный слой липидов.
В бимолекулярном липидном слое гидрофобные цепочки молекул липидов направлены друг к другу и внутренность бислоя совершенно гидрофобна, а гидрофильные части образуют поверхности внутреннего и внешнего монослоев, открытые для разнообразного рода взаимодействий.
Липидный состав мембран нервной ткани и распределение липидов по слоям генетически детерминированы. Наружный и внутренний монослои липидов характеризуются планарной и поперечной микрогетерогенностью>у> что создает асимметричность мембран. Существует несколько механизмов, поддерживающих асимметричное распределение липидов в мембране. Один из них связан с термодинамической вероятностью размещения липид-ных молекул с учетом их стереоконфигурации, заряда и гидратации полярных групп. Так, основная часть фосфатидилхолина, сфингомиелина, полифосфоинозитидов, холестерина, церебро-зидов и сульфатидов локализована в наружном слое, а амино-фосфолипиды находятся во внутреннем, цитоплазматическом слое. Неодинакова степень ненасыщенности монослоев: во внутреннем обнаруживается 2/3 двойных связей в жирных кислотах липидов, а в наружном – только 1/3.
Асимметрия бислоя является фактором, обеспечивающим создание градиента кривизны, складок, сморщиваний, отшнуровки части мембраны в виде везикул что существенно для обеспечения межклеточных взаимодействий.
Другой механизм поддержания асимметрии бислоя реализуется за счет различий ионного состава вне- и внутриклеточной среды, что вносит вклад в создание и поддержание изгибов мембраны.
Асимметрия бислоя обеспечивается также ферментами ли-пидного обмена, к ним прежде всего относятся липазы, ферменты обмена холестерина и метилазы фосфатидилэтанолами-на. Метилирование фосфатидилэтаноламина с превращением его в фосфатидилхолин осуществляется в два этапа и происходит в разных слоях липидкого матрикса. Образование мономе-тилфосфатидилэтаноламина под влиянием метилтрансферазы I осуществляется во внутреннем слое, где и локализован фермент. Монометил фосфатидилэтаноламин переходит из цитоплаз-матического слоя на внешний, где под действием метилтрансферазы II завершается его превращение в фосфатидилхолин. Фактически осуществляется так называемый ферментативный флип-флоп.
Этот транслокационный процесс меняет жидкостность мембраны и рассматривается как фактор, стимулирующий функционально важные процессы в мембране: связывание рецепторов с лигандами, Са* – вызванное освобождение медиаторов из си-наптических окончаний, активирование ЛТФаз.
Асимметричность билипидного слоя может поддерживаться транспортом липидов: спонтанным, везикулярным или с участием липидпереносящих белков. Липидпереносящие белки различной степени специфичности «стоят на страже» асимметрии мембран, перенося липиды только в наружный или только во внутренний слой. Перенос липидных молекул осуществляется в виде комплексов с белками-переносчиками.
3. ДИНАМИЧНОСТЬ БИЛИПИДНОГО СЛОЯ МЕМБРАНЫ
Строгая организованность липидного слоя мембраны не лишает его большой динамичности, которая возникает из-за передвижения липидных молекул в пределах мембраны, т.е. за счет интрамолекулярных движений липидов в пределах бислоя. Известно по крайней мере четыре типа интрамолекулярных движений липидов в пределах мембраны: латеральная диффузия, вращательная диффузия, вертикальные колебания и упоминавшийся выше так называемый флип-флоп.
Для большинства липидов скорость латеральной диффузии ощутима. Коэффициент латеральной диффузии для липидов Ю – см/с, а для белков намного ниже – 10~ ш/с. Вращательная диффузия молекул осуществляется также легко. Скорость же флип-флопа очень низка. Особенно медленно флип-флоп происходит в чисто липидных везикулах. Даже в присутствии липидпереносящих белков перемещение из наружного слоя во внутренний занимает более 4 часов, а перемещение в обратную сторону – более 10 часов. Не ускоряет флип-флоп повышение температуры до 80°С Это движение фосфолипидов усиливается под влиянием окисленных липидов, лизолецити-на. Как правило, холестерин подвергается более быстрому флип-флопу, чем фосфолипиды. Следует отметить, что не только флип-флоп запускает функционально важные события в мембране. Латеральная и вращательная диффузия липидов оказывает регулирующее влияние на активность мембранных белков.
4. ФАЗОВЫЕ ПЕРЕХОДЫ ЛИПИДОВ В МЕМБРАНЕ
На все типы молекулярных движений липидных молекул сильное влияние оказывает структура, в которой в данный момент находится липвды бислоя – гелеобразная или жидко-кристаллическая.
Липиды обладают замечательным свойством – способностью к фазовым переходам в физиологических условиях. При определенных температурах, строго характерных для каждого вида липидов, липидные мицеллы могут быть в «твердом» кристаллическом, организованном, гелеобразном состоянии или в «жидком», мезофазном, так называемом жидко-кристаллическом состоянии. Жидкие кристаллы – это анизотропные жидкости, так как оптически они сходны с кристаллами, проявляя разные свойства в разных направлениях, а механически сходны с жидкостью, они текут в зависимости от вязкости.
От состояния липидов в мембране зависит уровень молекулярной организации. Липиды в кристаллическом состоянии могут быть упакованы в кубический или гексагональный кристалл. Жидко-кристаллическая организация липидов в мембране очень разнообразна – это так называемые нематики, смек-тики, холестерики.
Нематики – наименее упорядоченная организация жидко-кристаллического состояния липидов. Молекулы нематика при умеренной температуре стремятся ориентироваться вдоль одного направления. В нематике очень многие молекулы одинаково ориентированы, их продольные оси параллельны друг другу, но такие области существуют недолго и границы их размыты. Области с одинаковой ориентацией молекул непрерывно рождаются и исчезают, что зависит от многих условий – внешних границ, включений и различных воздействий. Магнитное и электрическое поля ориентируют молекулы нематика, причем выстраивают молекулярные оси параллельно своему направлению.
Смектики – похожи на мыльные пленки, они более организованы, чем нематики, их молекулы образуют слои. В каждом индивидуальном слое молекулы передвигаются вдоль плоскости, все плоскости слоев находятся на одном и том же расстоянии. Смектики очень пластичны. Так, смектик в нативной мембране при охлаждении превращается в нематик.
Спиральная упаковка молекул вносит новое в ориентацию оптической оси жидкого кристалла. У холестериков – слоистое строение с различным шагом спирали. Холестерическую спираль обозначают нередко как твист-ориентацию. Разбавление холестерика и увеличение шага спирали приводит к нема-тику. Оптическая активность холестериков очень велика, они избирательно отражают свет в зависимости от температуры, механической нагрузки, примесей, электромагнитных полей.
Жидкие кристаллы, сочетая в себе упорядоченность твердого тела и подвижность жидкости, отличаются высокой чувствительностью к внешним воздействиям, температуре, примесям, свету, внешним полям, они очень пластичны и очень долго хранят информацию. Эти свойства приобретают первостепенное значение в мембранах нервной ткани, где изменения электрических свойств лежат в основе проведения возбуждения.
Фазовый переход липидов является эндотермическим процессом, сопровождающимся изменением энтропии и энтальпии. Липидным структурам присущ лиотропный мезоморфизм и термотропный мезоморфизм. Оба свойства связаны между собой. Фазовый переход липидов «гель – жидкий кристалл» осуществляется при температуре, значение которой зависит от содержания воды в системе. Оно минимально, если общее содержание воды превышает то количество, которое могут связать липидные структуры. В то же время при температуре выше критической липиды могут находиться в упорядоченном состоянии при недостатке воды. Перекисное окисление липидов, увеличивающее содержание воды в бислое, существенно влияет на фазовое состояние мембраны.
Термотропные фазовые переходы липидов в мембране происходят в сравнительно широком температурном интервале. Это обусловлено тем, что в бислое одна фаза обязательно возникает в матриксе другой. Сосуществование в липидном бислое двух фаз устанавливает между ними сложное равновесие, приводя к снижению степени кооперативное™ перехода. Обычно кооперативные фазовые переходы липидов в мембране затрагивают несколько сотен молекул. В нативной мембране постоянно находится большое число кооперативных единиц той или иной фазы. Этот полиморфизм является мощным регулятором транспортных систем мембраны.
Следует отметить, что на температуру фазового перехода большое влияние оказывают структура липидной молекулы, длина углеводородного скелета, наличие цис- и транс-двойных связей, структура полярных групп.
При переходе в жидко-кристаллическое состояние имеет место несколько одновременных событий: возрастает подвижность полярных групп липидов, увеличивается вращательная подвижность жирнокислотных радикалов относительно С–С-связей, увеличивается скорость латеральной диффузии. Это приводит к изменению геометрических размеров бислоя из-за латерального расширения площади, занимаемой каждой молекулой липида. Например, площадь, занимаемая 2С>]6>-фосфати-дилхолином, меняется от 0,49 до 0,58 нм, среднее расстояние между цепями увеличивается от 0,49 до 0,52 нм, а толщина углеводородного скелета уменьшается почти на 0,5 нм, т.е. латеральное расширение компенсируется утончением слоя. Гидрофобный объем мембраны увеличивается примерно на 1,5%.
В результате этих и ряда других изменений состояния липидов в мембране создаются особые условия для проникновения гидрофобных вешеств, изменения работы ионных каналов, внедрения в мембрану различных белков.
Микрогетерогенность бислоя и образование в нем кластеров молекул липидов способствует проявлению такого явления, как разделение фаз в мембране. Латеральное разделение липидных молекул в плоскости бислоя – важная особенность мембраны. Особая сегрегирующая роль в мембране принадлежит холестерину. При низких концентрациях его в мембране происходит латеральное разделение фосфолипид-холе-стсриновых комплексов и свободных молекул фосфолипидов. При этом холестерин взаимодействует в первую очередь с теми молекулами фосфолипидов, которые имеют низкую температуру фазового перехода. Благодаря этому в бислое будут существовать области только жидкие и только твердые, а также области, где обе фазы сосуществуют. Наличие таких жидких и твердых областей в пределах мембраны изменяет ее сжимаемость, что сказывается на глубине погружения мембранных белков и на эффективности работы мембранных насосов.
Необходимо отметить, что кроме сегрегирующего холестерин проявляет и другое важное влияние на структуру и физические свойства липидного бислоя. Встраивание холестерина в фосфолипидный бислой вызывает как нарушение квазикристаллической упаковки цепей, так и уменьшение подвижности цепей – Эти эффекты холестерина называют, соответственно, «разжижающим» и «конденсирующим». При температуре, превышающей точку фазового перехода фосфолипида, холестерин уменьшает подвижность углеводородных цепей. При добавлении холестерина площадь молекулы лецитина уменьшается с 0,96 до 0,56 нм. Вот почему высокое содержание холестерина характерно для миелина и плазматических мембран, тогда как внутриклеточные мембраны содержат его в небольших количествах. В плотных миелиновых мембранах фосфолипиды и холестерин содержатся в отношении 1:1, а в менее плотных мито-хондриальных мембранах это отношение равно 3:1 или 8:1. Этот уплотняющий эффект холестерина максимален в районе центрального участка жирнокислотных радикалов и ослабевает в направлении концевых метальных групп. При температуре ниже точки фазового перехода фосфолипидов холестерин разжижает углеводородную область бислоя.
Фазовые переходы липидов при постоянной температуре могут быть вызваны изменениями заряда полярных групп липидов, возникающими при изменениях рН, ионной силы, концентрации ионов. Доказано, что температура фазового перехода есть функция величина заряда и плотности заряда на липидной молекуле. Любое увеличение заряда полярных групп благоприятствует жидкому состоянию из-за латерального электростатического отталкивания, тогда как уменьшение заряда обусловливает переход в твердокристаллическое состояние.
Важным путем изменения поверхностного заряда липидов в физиологических условиях является адсорбция катионов. Связывание катионов заряженными липидами сильно зависит от поверхностного потенциала, значительно различающегося в твердом и жидком состояниях из-за различий в молекулярной упаковке.
Освобождение или адсорбция катионов на мембранной поверхности может запускать фазовые переходы липидов. При определенных физиологических условиях структурные изменения липидов могут вызывать освобождение двухвалентных катионов с поверхности мембраны. Так, при переходе гель – жидкий кристалл с липидной поверхности освобождаются ионы кальция. Са+ 'и Mg+ стабилизируют организованную структуру, увеличивая температуру фазового перехода, а одновалентные катионы оказывают противоположный эффект. Двухвалентные катионы благоприятствуют гелеобразному, а одновалентные – жидкому состоянию мембраны. Поверхность липидов может рассматриваться как резервуар катионов, который способен регулироваться структурными изменениями.
■ Подводя итог вышеизложенному, можно заключить, что в организации липидов, в их асимметричном размещении, подвижности, модификации внутримолекулярных взаимодействий сокрыты многообразные регулирующие возможности.
5. РОЛЬ БЕЛКОВ В ДИНАМИЧНОСТИ ЛИПИДНОГО БИСЛОЯ
Рассматривать динамичность бислоя мембраны без связи с белками нельзя. При липидных структурных перестройках в процесс вовлекаются интегральные, периферические и поверхностные белки мембраны. Более того, белки могут выступать в роли триггеров температурных структурных перестроек мембран, и белку часто принадлежит ведущая роль не только в инициации, но и в реализации структурной перестройки.
Одна из функций липидов в мембране – придание белкам через межмолекулярные взаимодействия оптимальной конформации для функциональной активности. Липиды могут непосредственно участвовать в катализе. Липидный бислой определяет размещение белков, создает условия для их латерального перемещения и через фазовые переходы выполняет регуляторные функции. Жидкостность липидов влияет как на вращательную, так и диффузную свободу интегральных белков и их способность подвергаться конформационным изменениям. Вращательная и латеральная диффузия белков является отчасти следствием латерального движения мембранных липидов. Широкий спектр липидных молекул делает возможным широкое разнообразие специфических взаимодействий с мембранными белками.
Внедрение белка в фосфолипидный бислой упорядочивает его – в результате структура бислоя становится более жесткой.
Считается, что это происходит за счет прилипания и ориентации фосфолипидных молекул, примыкающих к поверхности белка, ограничивающего подвижность этого слоя. У многих мембранных белков те их части, которые погружены в липид-ный бислой, особенно богаты гидрофобными аминокислотами, что повышает устойчивость их связей с липидами и фиксирует их ориентацию в мембране.
В бимолекулярном слое имеется два пула липидов, подвергающихся существенно различным скоростям диффузии. Один пул липидов находится в короткорадиусном взаимодействии с белками и потому подвергается ограниченной латеральной диффузии. Короткорадиусные взаимодействия могут быть очень специфичными и их может осуществлять только определенный тип липидов с особыми белками. Такие специфические липиды необходимы, в частности, для активации мембранных ферментов; они выступают здесь в качестве аллосте-рических эффекторов. Так, белковую молекулу Na+, К+-АТФа-зы окружает кольцевой слой липидов из 30–32 молекул. Применение разнообразных физических методов показало, что кольцевые липиды могут многократно обмениваться с общим липидным пулом мембраны. Время обмена таких прочно связанных липидов с соседними молекулами составляет 10~ – 10~ с. Это несоизмеримо меньше продолжительности одного ферментного цикла. Кроме того, оказалось, что сама фракция кольцевых липидов очень гетерогенна по своей обме-ниваемости, по фазовому состоянию и по способности к реактивации белка. Как минимум, роль кольцевых липидов заключается в поддержании строго определенного гидрофобного окружения данного белка.
В области температурных фазовых переходов таких липидов отмечается изменение каталитических и транспортных свойств белков. Общая доля кольцевых липидов довольно велика – около 20%. Доказано, что можно изменять активность мембранных белков изменением связанных с ними липидов.
Другой пул липидов, удаленных от белков и подвергающихся быстрой латеральной диффузии, характерной для билипидного слоя, не пронизанного белком, составляет около 80%. Действие этих липидов на мембранные белки аналогично растворяющему эффекту воды на свойства растворимого белка.
Приведем примеры функциональной роли индивидуальных липидов в мембранах ЦНС. В табл. 5 представлены данные о влиянии различных фосфолипидов на активность мембранных ферментов.
Активирование отдельными фосфолипидами мембранных ферментов

6. УЧАСТИЕ ЛИПИДОВ В РЕЦЕПЦИИ И ПЕРЕДАЧЕ ВНУТРЬ КЛЕТКИ СИГНАЛА
Межклеточные контакты, без которых немыслима деятельность ЦНС, обеспечивают постоянную передачу информации через плазматическую мембрану. Эта передача не может не касаться билипидного слоя. Процесс передачи информации через мембрану включает рецепцию внешнего химического сигнала и трансформацию его во внутриклеточный эффект.
Возникает вопрос, принимают ли участие липиды бислоя в рецепции внешних сигналов. В последнее десятилетие установлено, что сульфоиереброзиды играют довольно специфическую роль в рецепции опиоидов. Частично очищенный препарат рецептора опиоидов содержит высокую концентрацию сульфатидов. Предполагают, что сульфатная группа це-реброзидсульфата входит в состав или соседствует с активным центром опиатных рецепторов, который имеет белковую природу. Возможно, что взаимодействие опиатов с цереброзидсульфатами выполняет вспомогательную функцию, способствуя сосредоточению лигандов в области центра белковой природы.
При исследовании ряда кислых липидов только сульфатиды проявляли наивысшее сродство к опиатам в различных физиологических условиях. Доказательством важной роли сульфати-дов в рецепции опиоидов может служить и тот факт, что антитела к цереброзидсульфату, введенные в мозг крысы, снимали наркотическое действие морфина.
Если липиды бислоя могут быть участниками процесса рецепции, то естественно ожидать их участия в каскаде реакций, возникающих после активации рецепторов. М.Н. Хокин и Л. Э. Хокин впервые связали холинергическую стимуляцию с усилением обмена фосфатидилинозита и фосфатидной кислоты. Явление получило название «фосфолипидного эффекта»; этот термин сейчас заменен на термин «фосфоинозитид-ный эффект», поскольку появилось большое число работ, показывающих именно их регуляторную роль в транспорте вторичного мессенджера – ионов кальция – через мембраны.
Содержание фосфоинозитидов в мембранах ЦНС не превышает 0,5–2% от общих липидов, локализованы они преимущественно в плазматических мембранах, в миелине, в эндоплазматическом ретикулуме, наружной митохондриальной и ядерной мембранах. В состав фосфоинозитидов входит арахидоновая кислота, являющаяся важным источником простагландинов. Деполяризация мембраны приводит к быстрому высвобождению арахидо-новой кислоты именно из фосфоинозитидов. Р. Митчелл высказал гипотезу о прямой связи расщепления фосфоинозитидов с рецепторным аппаратом клетки и увеличением внутриклеточной активности. В синаптосомах стимуляция части мускариновых и а>х>-адренерги-ческих рецепторов обусловливает фосфоинозитидный эффект, сопровождающийся изменением проницаемости плазматической мембраны для ионов кальция.
Участие фосфоинозитидов и продуктов их обмена в регуляции транспорта кальция осуществляется несколькими путями:
1) при распаде фосфатидилинозитидов образуется 1,2 – диа-цилглицерин, стимулирующий активность протеинкиназы С, которая, в свою очередь, фосфорилирует белок Са-каналов и некоторые другие белки;
2) трифосфоинозитол, освобождающийся при расщеплении фосфатидилинозитидов, обладает высокой способностью связывать двухвалентные катионы; по этой причине он индуцирует мобилизацию мембранно-связанного кальция;
3) инозитол-трифосфат способен также повышать уровень внутриклеточного кальция за счет открытия кальциевых каналов эндоплазматического ретикулума. Таким образом, происходит сопряжение выброса кальция из внутриклеточных мест хранения с входом кальция через мембраны.
До включения описанного механизма концентрация свободного кальция в цитоплазме нейрона составляет примерно 1 – .10~М. Концентрация кальция снаружи нейрона в десятки тысяч раз выше. Мобилизация Са+ из внутриклеточных и внеклеточных источников в сотни-тысячи раз повышает его уровень в цитоплазме. Повышенный уровень Са+ служит активатором ряда процессов, в том числе некоторых протеинкиназ.
На молекулярном уровне передача этого сигнала через мембрану осуществляется цепочкой мембранных белков, последовательно взаимодействующих друг с другом для передачи сигнала малым молекулам, находящимся в цитоплазме. Информация от рецептора на поверхности клетки передается так называемому G-белку, который активирует фермент фосфодиэстеразу, расщепляющую трифосфоинозитид до инозитол – 1,4, 5-трифосфата и 1,2 – диацилглицерина. Инозитолтрифосфат растворим в воде, диффундирует в цитоплазму, где и вызывает описанное выше освобождение кальция. Освободившийся кальций участвует в активации протеинкиназ.
Липофильный диацилглицерин, отличный по своему жирно-кислотному составу от стабильного пула диацилглицеринов, остается в мембране, изменяет ее текучесть и, как уже упоминалось, активирует мембранно-связанную протеинкиназу С,
Эти две различные ветви фосфоинозитидного цикла ведут в конечном счете к фосфорилированию двух различных наборов белков. Оказалось, что с помощью активирующих веществ каждую из ветвей цикла можно привести в действие независимо друг от друга. С другой стороны, применение сочетанного действия фор-боловых эфиров и кальциевых ионофоров помогло установить синергизм двух сигнальных ветвей инозитидного цикла. В таком раздвоенном сигнальном пути совместным действием веществ можно запустить большое число внутриклеточных процессов.
В дальнейшем образовавшиеся 1,2 – диапилглицерин и инозитолтрифосфат подвергаются химическим превращениям, требующим АТФ и ЦТФ и приводящим к восстановлению три-фосфоинозитида. Таким образом, цикл замыкается и уровень полифосфоинозитидов в мембране восстанавливается.
7. МИЕЛИН В ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЕ
Мозг человека содержит 120 г миелина, что составляет одну треть его сухой массы. Миелин – уникальное образование, организация которого позволяет проводить импульс в аксоне с минимальной затратой энергии. Миелиновая оболочка – высокоорганизованная многослойная структура, состоящая из сильно растянутой и модифицированной плазматической мембраны олигодендроглиальной клетки.

Плазматическая мембрана олигодендроцита образует вокруг аксона сложную мембранную структуру – мезаксон, который является элементарной единицей миелина, имеет пятислойную структуру: белок-липид-белок-липид-белок. Эта пя-тислойная структура, многократно закручиваясь вокруг аксона,
конденсируется в компактную миелиновую оболочку. На электронных микрофотографиях миелин представляет собой серию чередующихся липидных и белковых слоев, число таких слоев у крупных аксонов может достигать 250. Сплав цитоплазматиче-ских поверхностей мембраны олигодендроцита образует главный период, а сплав экстраклеточных поверхностей – половинный или промежуточный период, который часто виден в виде двойной линии. Это указывает на то, что взаимопроникновение белков экстраклеточных поверхностей мембран не было полным.

Повторяющийся период миелина определяется толщиной составляющего его липидного бислоя, «зажатого» двумя белковыми слоями, и равен 15–16 нм. Белки, частично пронизывающие бислой, занимают 5–10% площади; распределение его по поверхности бислоя неравномерно – есть области, не занятые белком. Полярные группы липидов образуют слой толщиной в 1 нм, а гидрофобная область занимает 3,3–3,8 нм.
Из всех существующих мембран миелин имеет самое низкое содержание воды и самое высокое отношение липидов к белку. В миелине белка – 15–30, липидов – 70–85 на сухую массу, из них холестерин составляет 25–28, общие галактолипи-ды – 27–30, а фосфолипиды – 41–45.

Состав миелина центральной нервной системы человека
|
Компоненты |
Миелин |
Белое вещество |
Серое вещество |
|
Белок |
30 |
39 |
55,3 |
|
Липиды |
70 |
54,9 |
32,7 |
|
Холестерин |
27,7 |
27,5 |
22 |
|
Цереброзиды |
22,7 |
19,8 |
5,4 |
|
Сульфат иды |
3,8 |
5,4 |
1,7 |
|
Общие галактолипиды |
27,5 |
26,4 |
7,3 |
|
Общие фосфолипиды |
43,1 |
45,9 |
69,5 |
|
Фосфатидилэтаноламин |
15,6 |
14,9 |
22,7 |
|
Фосфатидилхолкн |
11,2 |
12,8 |
26,7 |
|
Сфингомиелин |
7,9 |
7,7 |
6,9 |
|
Фосфатидил серии |
4,8 |
7,9 |
8,7 |
|
Фосфатидилинозитол |
0,6 |
0,9 |
2,7 |
|
Плазмалогены |
12,3 |
П, 2 |
8,8 |
Доказано, что полифосфоинозитиды локализованы преимущественно в миелине, предположительно в зоне главного периода, поэтому их можно считать маркерами миелина. На долю три- и дифосфоинозитидов приходится, соответственно, 3–6 и 1–1,5% общего липидного фосфора миелина. Они характеризуются высокой скоростью обмена фосфатных групп, что отражает их функции в миелине. В составе миелина содержатся алка-ны с 21–35 углеродными атомами и равным количеством четных и нечетных гомологов. Считают, что эти абсолютно гидрофобные вещества оказывают значительное влияние на свойства миелина как электроизолятора. Кроме обычных галактолипи-дов, цереброзидов и сульфатидов в миелине обнаружены моно-и диталактозилдиглицериды. Роль их и топографическое распределение в мембране миелина не ясны, но их синтез тесно связан с процессом миелинизации.
Для миелина характерен очень низкий уровень ганглиозидов – 0,15% от общих лигшдов миелина. Моносиалоганглиозид G>M>>1 >преобладает и, кроме того, в миелине человека обнаружен необычный сиалилгалактозилцерамид G>7>, содержащий в основном длинноцепочечные жирные кислоты. Метаболические характеристики миелиновых ганглиозвдов сходны с липидами миелина, а не с ганглиозидами коры. Ганглиозиды локализованы в зоне промежуточного периода и роль их в структуре и функции миелина пока не ясна.
Углеводородные цепочки жирных кислот миелина упакованы плотнее, чем в других мембранах, но ближе к середине бислоя они обладают большей свободой движения. Поскольку более чем у 25% жирных кислот миелина углеродный скелет на 4–5 атомов длиннее, чем в других мембранах, то в центре бислоя может происходить переплетение ацильных радикалов. Это особенно характерно для сфинголипидов. Церебрознды, сульфамиды и полифосфоинозитнды локализованы преимущественно в наружном монослое, в котором в два раза больше холестерина. Холестерин имеет предпочтительное сродство к длинноцепо-чечным радикалам сфинголипидов и к моноеновым оксикис-лотам галактолипидов. Он интеркалирован между гидрофобными цепочками и модулирует латеральную подвижность липидов и движение ацилов внутри бислоя. В зависимости от концентрации холестерин проявляет уплотняющий, сегрегирующий эффект или увеличивает жидкостность.
Фазовые переходы и внутримолекулярные движения компонентов миелина пока мало изучены.
Белковый состав миелина ЦНС относительно прост, два главных белка – сильноосновный, гистоноподобный белок и гидрофобный протеолипидный белок – составляют 60–80% от общих белков миелина. Оставшаяся часть падает на гетерогенную группу, включающую некоторые ферменты, гликопротеины, белок Вольфграма и неопределенное число минорных компонентов.
Гликопротеины миелина ЦНС являются минорными поверхностными компонентами промежуточного периода и играют определенную роль в нейронально-глиальном узнавании в процессе миелинизации.
Для миелина характерен ограниченный набор ферментов. Маркерным ферментом миелина является 2,3 – циклическая нуклео-твд-З-фосфогвдролаза, 60% от активности этого фермента в мозге приходится на миелин. Относительно специфическим ферментом миелина является также гидролаза эфиров холестерина, 70–80% его активности обнаружено в миелине. В поддержании низкого содержания воды в миелине принимает участие карбо-ангидраза Кроме того, в миелине присутствуют в относительно небольшом количестве зависимые и независимые от цАМФ протеинкиназы и фосфатаза.
Белок Вольфграма олигодендроглиального происхождения составляет менее 20% белков миелина и состоит из двух фракций с молекулярной массой 62000 и 54000. Это – кислый про-теолипид, обогащенный дикарбоновыми аминокислотами и содержащий 53% полярных и 47% неполярных аминокислот.
Протеолшшдная фракция Фолча-Ли гетерогенна и включает несколько белков. Наибольшей является доля липо-филина – белка с молекулярной массой 28000, составляющего 50% от общего протеолипидного белка. Его гидрофобность очень значительна. Он содержит 66% гидрофобных и только 18% заряженных аминокислот. В состав липофилина входит 2–3% ко-валентносвязанных жирных кислот, что еще более увеличивает его гидрофобность. Интересной особенностью этого белка является его конформационная гибкость. В водной среде степень его а-спирализации составляет 16–40%, в хлороформе-метаноле она выше, в совершенно гидрофобной среде липофилин имеет 100%-ную а-спиральную конфигурацию. Степень спирализа-ции липофилина в мембране составляет 75%. Кроме того, липофилин склонен к агрегации. Из-за своей гидрофобное™ он может быть погружен в углеводородную область бислоя и образовывать внутримембранные частицы. Белок прочно связывается с кислыми и нейтральными липидами и вызывает фазовое разделение кислых и нейтральных липидов. Около 15 молекул липидов окружают каждую молекулу липофилина. Благодаря некоторой избирательности гидрофобных взаимодействий липофилин вытесняет из своего окружения холестерин. В общем, липофилин, как и другие протеолипидные белки, поддерживает стабильность миелиновых мембран, создавая межла-меллярные взаимодействия между белковыми молекулами соседних слоев, в результате которых эти слои удерживаются вместе.
Катионный основной белок миелина с М>г> ~1б~18кД является исключительно белком миелина и локализован в зоне главного периода. Он содержит 170 а.о., из них 30% заряженных и 52% гидрофобных. КБМ характеризуется несколькими необычными особенностями.
КБМ – антиген, индуцирующий при введении со стимуляторами иммунитета экспериментальный аллергический энцефаломиелит, заболевание, сходное с рассеянным склерозом и сопровождающееся демиелинизацией. Установлено, что трип-тофансодержащий декапептид КБМ–Phe-Ala-Ser-Trp-Gly-Ala-Glu-Gly-Glu-Arg близок по энцефалитогенной активности целому КБМ человека. Описаны и некоторые другие олигопептидные участки КБМ, обладающие несколько меньшим, но четким энцефалитогенным действием. По-видимому, внемозговые системы иммуногенеза воспринимают КБМ или его фрагменты как чужеродный белок. В норме КБМ с ними не взаимодействует в силу иммуноавтономности ЦНС. Какие-то, пока неясные повреждения, нарушая эту автономию, открывают путь этим взаимодействиям и обусловливают «агрессию» иммунной системы организма в отношении собственного миелина.
КБМ может гликолизироваться по треонину-981Ч-ацетил-галактозаминилтрансферазой и в отличие от других белков миелина может фосфорилироваться по некоторым остаткам серина, треонина, аргинина и гистидина. Фосфорилирование основного белка рассматривается как инициация миелиниза-ции.
Основной белок, связывая кластеры кислых липидов через полярные группы, изменяет упаковку ацилов в области полярных группировок и не оказывает существенного эффекта на центр бислоя. Этот белок изменяет энтальпию Т-фазового перехода кислых липидов и проницаемость бислоя, Липидный состав мембраны определяет, какие участки основного белка будут экранированы липидной фазой, а какие – экспонированы в водную фазу. Таким образом, от липидного состава мембраны зависит, будет ли антигенная или энцефалитегенная сторона подвержена атаке антителами и макрофагами. Этим, видимо, объясняется варьирование энцефалитогенных участков основного белка от вида к виду.
Электростатическое и гидрофобное взаимодействие основного белка с липидами близлежащих слоев, так же как и в случае липофилина, создает межламеллярные взаимодействия и поддерживает адгезию миелиновых слоев, стабилизируя многослойную структуру миелина.
Для понимания молекулярной организации мембраны миелина критическим является изучение коротко- и длинноради-усных взаимодействий между белками и липидами. Несомненно, что изменение структуры белков или липидов ведет к изменению такого рода взаимодействий и приводит к нестабильности миелина, в том числе к демиелинизации.
Пока мало известно о факторах, начинающих и заканчивающих образование миелиновых мембран. Возможно, что миели-низация запускается критическим диаметром аксона или каким-то нейротропным фактором. В этом строго контролируемом и синхронизированном процессе большую роль играют контакты между мембранами аксона и олигодендроглии.
Ранний, рыхлый, некомпактный миелин морфологически отличается от зрелого миелина наличием остатков цитоплазмы между слоями. Пластинчатые структуры рыхлого миелина химически сходны с плазматической мембраной олигодендроцита и не имеют физических свойств компактного миелина. Для превращения рыхлого миелина в компактный мозг 20-дневной крысы ежедневно синтезирует 3,5 мг миелина, т.е. каждый олигодендроцит производит миелина в 3 раза больше своей массы.
Компактность миелина увеличивается по мере включения основного и протеолипидного белков, холестерина, длинноцепочечных галактолипидов, плазмалогенов и, соответственно, по мере уменьшения доли высокомолекулярных белков, десмостерола, исчезновения полисиалоганглиозидов.
Мало известно о месте синтеза белков миелина, их транспорте и модификации перед сборкой, их деградации. Скорее всего, протеолипидный белок синтезируется на мембранносвязанных, а основной – на свободных рибосомах. Белки вступают в зреющую мембрану раньше липидов. В период активной мие-линизации катионный и протеолипидный белки активнее вступают в миелин, чем высокомолекулярные белки.
Зрелый миелин – не инертная структура, он биохимически активен, включает экзогенный материал, обменивает свои компоненты с другими мембранами. Миелин не обменивается как единое целое, поскольку различные белки и липиды покидают миелин и появляются в нем с различной скоростью. Наблюдаемая метаболическая стабильность компонентов миелина частично объясняется топографическими особенностями миелиновой оболочки. Одна глиальная клетка одновременно «одевает» миелином 30–50 сегментов аксонов и создает мембрану, которая в 620 раз больше ее собственной. Метаболизм этой обширнейшей мембраны поддерживается цитоплазмой всего одной клетки.
Для нормального функционирования необходимы определенные соотношения и взаимодействия аксона, миелиновой оболочки и глии. Любое повреждение одного из этих элементов нарушает всю систему. Так, например, метахроматическая лейкодистро-фия характеризуется почти полным отсутствием фермента суль-фатазы, что приводит к резкому накоплению сульфатидов и сопровождается недостатком миелина.
Глобоидно-клеточная лейкодистрофия сопровождается дефектом фермента fi-галактозидазы. Избыток цереброзидов накапливается в многоядерных глобоидных клетках, обычное отношение цереброзидов к сульфатидам 4:1 трансформируется в 10:1. Наблюдается резкое изменение белого вещества, недостаточность миелина и олигодендроглии.
Болезнь Рефсума характеризуется недостаточностью а-гидро-ксилазы фитановой кислоты. Накапливающаяся фитановая кислота эстерифицирует лецитин миелина и составляет 5–8% от всех жирных кислот миелина.
Общей чертой вышеприведенных заболеваний является искажение структуры миелина, уменьшение отношения липидов к белку, снижение количества холестерина, плазмалогенов, га-лактолипидов, увеличение количества воды и постепенная замена миелина астроцитами, макрофагами и межклеточной жидкостью.
Важным путем в изучении процесса демиелинизации является исследование мутантов с нарушенным или ограниченным образованием миелина.
Jumpy-мутанты – это аугосомальное рецессивное заболевание мышей, характеризующееся почти полным отсутствием миелина.
Quaking-мугаюы – рецессивное заболевание мышей, сцепленное с полом, характеризующееся некомпактностью миелина и нарушением дифференциация олигодендроглии. У этого вида мышей резко уменьшен уровень основных липидов миелина, особенно трифосфоинозитидов, изменен жирнокислотный состав.
8. ЛИПИДЫ ВНЕШНЕЙ ЗОНЫ МЕМБРАН МОЗГА
В последние десятилетия для выяснения природы возбудимости мембран нейрона обратили внимание на экстраклеточную зону. Эта зона, так называемый гликокаликс или экстраклеточный матрикс, занимающий слой толщиной от 10 до 50 нм, влияет на многие макромолекулярные процессы: ионный обмен, проницаемость, эндо- и экзоцитоз, межклеточные контакты, морфогенетическую и тканеспецифическую агрегацию клеток.
Поверхностный матрикс содержит внешние компоненты рецепторов гормонов, медиаторов, ростовых факторов, нейро-пептидов, антигенов и других факторов. Экстраклеточный матрикс – комплексная, динамичная интегративная система, в которой изменение взаимодействия отдельных компонентов приводит к глубоким изменениям матрикса в целом.
Специфичность экстраклеточного матрикса определяется:
1) первичной структурой олигосахаридной части гликопро-теинов, гликолипидов, гликозаминогликанов;
2) их конформацией и положением на плоскости мембраны;
3) «удельной» площадью, занимаемой гликопротеинами и гликолипидами.
Состав, структура и динамизм поверхностных гликозилиро-ванных молекул влияют на функции деления, роста, дифференциацию и гибель клетки. Особая роль принадлежит при этом гликолипидам и в особенности кислым гликолипидам – ганг-лиозидам.-
Ганглиозиды – специфические липиды экстраклеточного матрикса мембран мозга
Кислые гликолипиды – ганглиозиды находятся в нервной ткани в высоких концентрациях и обогащают поверхность наиболее возбудимых мембран.
Термин ганглиозиды – общее название гликосфинголипи-дов, содержащих сиаловую кислоту, был впервые предложен Е. Кленком в 1941 г. Они содержат гидрофобную церамидную часть и гидрофильную, богатую заряженными группами олигосахаридную часть. Ниже приводится структура моносиалоганглиозида головного мозга:

Гидрофобная часть ганглиозидов включает две длинные углеводородные цепочки – сфингозин и жирную кислоту, которая связана с аминогруппой сфингозина пептидной связью. Обращает на себя внимание почти полное отсутствие в ганглиозидах мозга гидроксикислот, кетокислот и разветвленных жирных кислот. Состав сфингозиновых оснований ганглиозидов головного мозга не отличается большим разнообразием. Структура и недавно принятая номенклатура сфингозиновых оснований ганглиозидов представлены в табл. 8.
Содержание ганглиозидов в тканях человека
|
Ткани |
Концентрация* |
|
Серое вещество мозга |
2850–3530 |
|
Белое вещество мозга |
900–1570 |
|
Серое вещество спинного мозга |
751 |
|
Белое вещество спинного мозга |
450 |
|
Сетчатка |
366 |
|
Седалищный нерв |
259 |
|
Надпочечники |
407–757 |
|
Печень |
2J4 |
|
Мышцы |
52 |
|
Плазма |
п, з |
|
Спинномозговая жидкость |
0,841 |
* Концентрация выражена в н-молях липидосвязанной сиаловой кислоты – характерного компонента ганглиозидов – на 1 г свежей ткани
Структура и номенклатура сфингозиновых оснований ганглиозидов
|
Тривиальное название |
Структура |
Новое название |
|
Сфингозин |
СНэ-12-СН=СН-СН-СН-СНгОН ОН NH2 |
4-Сфингенин |
|
Дигидросфингозин |
СН3-12-СН2-СНа-СН-СН-СН2ОН ОН NH2 |
Сфинганин |
|
См-Сфингозин |
СНэ-14-СН=СН-СН-СН-СН2ОН ОН NH2 |
4-Эйкозасфинге-нин |
|
С^-Дигидросфин – гозин |
СН,-14-СНг-СН2-СН-СН-СН2ОН ОН NH2 |
Эйкозасфинганин |
Таким образом, гидрофобная часть ганглиозидов мозга млекопитающих достаточно консервативна по длине, числу и месту двойных связей, присутствию метальных групп. Й хотя ганглиозиды из различных источников отличаются по составу церамидной части, но эти различия никогда не рассматриваются как характерная особенность для классификации ганглиозидов.
Разветвленная олигосахаридная часть присоединена $-связью к ОН-группе первого атома углерода сфингозина. Большинство ганглиозидов мозга имеют общую нейтральную углеводную часть, содержащую глюкозу, две молекулы галактозы, ацетилированный галактозамин и различное число молекул сиаловой кислоты, прикрепленных либо к интернальной, либо к терминальной галактозе.
Олигосахаридная часть является доминирующей в проявлении физических, химических и иммунологических свойств молекул ганглиозидов. Различие в строении олигосахаридной части порождает исключительную гетерогенность этих соединений, которых к настоящему времени в нервной ткани млекопитающих охарактеризовано свыше 50, причем число это быстро возрастает.
Особенности строения олигосахаридной части индивидуальных ганглиозидов – важнейшая характеристика, которая дает основу для существующей номенклатуры ганглиозидов. Единства в системе обозначений индивидуальных ганглиозидов среди исследователей нет, но все же чаще всего используется и наиболее удобна номенклатура, предложенная Свеннерхольмом. Согласно ей, все индивидуальные ганглиозиды делятся на моно-, ди-, три-, тетра- и пентасиалоганглиозиды по числу молекул N-ацетилнейраминовой кислоты, приходящихся на цера-мидный остаток.
Свеннерхольм предложил буквой G обозначать ганглиозиды; подстрочными буквами М, D, Т, Q и Р – число молекул NAHK; цифрой 1 – основную нейтральную тетрасахаридную цепочку; цифрой 2 – олигосахаридную последовательность без терминальной галактозы; цифрой 3 – цепочку, не имеющую терминальной галактозы и N-ацетилгалактозамина; цифрой 4 – цепочку с единственным углеводов; а буквами «а», «в» и «с» – разное число молекул NAHK, связанных с интернальной галактозой.
Предложенная Свеннерхольмом номенклатура не охватывает, однако, всех открытых в последнее десятилетие индивидуальных ганглиозидов с очень разнообразной структурой олигосахаридной цепочки. Недавно описаны гекса- и декасиалоганглиозиды, имеющие, соответственно, от 6 до 10 сиаловых кислот на церамидный остаток.
В настоящее время Международной комиссией по номенклатуре предложена новая система обозначения индивидуальных ганглиозидов, в которой учитывается структура олигосахарид-ной части, число молекул N-ацетил- или гликолилнейрамино-вых кислот, место и способ их присоединения к олигосахариду. В этой номенклатуре N-ацетилнейраминовая кислота получает обозначение NeuAc, гликолилнейраминовая – NeuGc, римские цифры I, II, III и IV – указывают номер сахарного остатка от церамида, к которому присоединена нейраминовая кислота, арабская цифра вверху обозначает атом углерода сахарного остатка, к которому присоединена нейраминовая кислота кетозидной связью. Структура трисахарида обозначается как GgOse>3>, структура тетрасахарида – GgOse>4>. Тогда, например, структура моно-сиалоганглиозида будет записана как IINeuAc-GgOse>4>Cer,
В силу большей, чем у фосфолипидов, гидрофобное™ углеводородных цепочек ганглиозиды увеличивают жесткость би-липидного слоя и гидрофобно взаимодействуют с фосфолипидами и интегральными белками мембраны.
■ Увеличение числа углеводородных атомов и ненасыщенности сфингозина, изменение природы жирной кислоты ганглиозидов вызывают конформационные изменения в близлежащих белках. Церамидная часть участвует в обеспечении определенного состава фосфолипидно-холестерин-белкового окружения индивидуальных ганглиозидов.
8.1 Локализация ганглиозидов в головном мозге
Ганглиозиды обнаружены фактически в каждом типе клеток и большинстве субклеточных образований ЦНС,
На долю собственно митохондрий приходится менее 5% ганглиозидов, на долю миелина – 28,5, а на нервные окончания – более 67%. Основным местом локализации ганглиозидов являются синаптические мембраны, которые составляют примерно 6% сухой массы мозга, причем обнаружена корреляция между накоплением ганглиозидов и синаптогенезом во время формирования мембран. Использование специальных методов показало, что ганглиозиды расположены на наружной стороне пре- и постси-наптических терминалей, принимающих непосредственное участие в передаче нервного импульса.
■ Ганглиозиды имеют отношение не только к синаптиче-ским контактам, но локализованы и в других типах нейрональ-ных и глиальных мембран, о чем свидетельствуют различия в содержании и составе ганглиозидов в различных областях мозга.
8.2 Организация ганглиозидов в мембране
Молекулярная организация ганглиозидов в мембране очень динамична, что создает, с одной стороны, некоторую локальную неустойчивость мембраны, а с другой – поддерживает ее целостность. Молекулы ганглиозидов не подвержены флип-флопу, но способны к латеральной диффузии с широко варьирующей скоростью.
Несмотря на большую подвижность ганглиозидов, они не вносят хаотичность в распределение компонентов мембраны. Это достигается, во-первых, образованием горизонтальных связей между олигосахаридными цепочкам гликопротеинов и гли-колипидов, приводящих к устойчивому полимерному комплексу. Во-вторых, гликолипиды и гликопротеины могут сцепляться периферическими гликозаминогликанами, которые, как правило, не закреплены в интегральной зоне мембраны, свободно диффундируют и взаимодействуют с гликолипидами и глико-протеинами ионными и водородными связями, образуя своеобразный латекс. В-третьих, ограничение латерального движения гликолипидов достигается сосредоточением их в определенных областях с повышенной вязкостью. В-четвертых, топографию поверхности стабилизируют цитоскелетные системы клетки.

Различные поливалентные лиганды гликопротеиновой природы с помощью цитоскелетной системы вызывают в мембранах перераспределение гликолипидов в группы, участки, полюса. Степень агрегации зависит от степени взаимодействия олигосахаридных структур с лектинами, причем один и тот же агент может вызывать агрегацию одних молекул в группы, а других – в полюса.
Как правило, большие плотные массы олигосахаридных цепочек гликопротеинов служат фокусной точкой, вокруг которой увеличивается степень упаковки ганглиозидов. Нековалент-ное кооперативное взаимодействие ганглиозидов приводит к тому, что в участках скопления ганглиозидов резко возрастает отношение ганглиозидов к фосфолипидам. В результате возникают весьма сложные эффекты. Жидкостность в этих локусах становится ниже, ганглиозидные кластеры приобретают максимальную нестабильность из-за взаимного отталкивания отрицательно заряженных сиаловых кислот, мембранный потенциал в этом локусе становится максимальным.
Участки, занятые заряженными ганглиозидными молекулами, имеют повышенное сродство к водорастворимым, экзогенным лигандам, а области, свободные от ганглиозидов, осуществляют гидрофобное взаимодействие с лигандами другой природы. Оба рода взаимодействия вызывают кооперативные и некооперативные структурные перестройки в мембране, оказывают разнообразные влияния на состояние клетки.
Агрегация ганглиозидов и гликопротеинов на поверхности важна для поддержания контактов между клетками, поскольку конгломераты молекул обеспечивают более устойчивые контакты, чем молекулы, случайно или дисперсно разбросанные на поверхности. Подобные агрегаты могут содержать различные рецепторы или несколько копий одного рецептора, или составлять единый рецепторный комплекс, состоящий из гликолипидов и гликопротеинов,
■ Таким образом, зона, где происходит кодирование и декодирование информации, передача ее внутрь клетки и где реализуется прямая и обратная связь с ядром, представляет собой обширную систему перекрестносвязанных гетерогенных гликозилированных молекул. Эта область является своеобразным распределительным щитом регуляторных сигналов, в котором молекулы ганглиозидов могут выполнять роль триггеров, регуляторов или трансдукторов, функции сигнальных молекул на стадии дифференциации и участвовать в определении видовой и тканевой специфичности.

8.3 Ганглиозиды и передача информации через мембраны
Ганглиозиды участвуют в модулировании рецепторных функций.
Диапазон рецепторных свойств ганглиозидов широк: они связывают токсины, вирусы, медиаторы и гормоны. Есть данные о том, что ганглиозиды потенциируют действие нейроро-стового фактора и участвуют в рецепции интерферона.
Из всего множества индивидуальных ганглиозидов только для девяти строго доказана специфичность связывания. Это прежде всего моносиалоганглиозид G>MI>, который высокоспецифично взаимодействует с холерным токсином, дофамином, тиротропином; а также пента-, тетра-, три- и дисиалоганглиозиды – компоненты рецепторного комплекса для токсинов, вирусов, гормонов, и дисиалоганглиозид G>D>>3>, который в эквимолекулярных соотношениях соединяется с серотонином.
Сродство ганглиозидов головного мозга к различным лигаидам
|
Лиганлы |
Ганглиозид, обладаюший преимущественным сродством к лиганлу |
|
Холерный токсин |
GMi' GDlb |
|
Столбнячный токсин |
GQIb> GDlb* GTlb |
|
Ботулинический токсин |
GTIb |
|
Токсин Е. coli |
GM1 |
|
Вирус Сендай |
GPi> GQlb> GTla |
|
Вирус гриппа |
GTlb> GDlb |
|
Дофамин |
GM1 |
|
Серотонин |
GD3 |
|
Интерферон |
GM2> GT1 |
|
Тиротропин |
GTlb> GDlb> GM1 |
|
Лютеотропин |
GTlb> GDib |
|
Гонадотропин |
GTlb |
|
Фибронектин |
GTh GDlo |
Взаимодействие ганглиозидов с холерным токсином привлекает особое внимание, что обусловлено широким использованием его для изучения механизмов действия нейрорецепторов. В настоящее время наиболее изучен механизм взаимодействия холерного токсина с моносиалоганглиозидом G>M>>1>. Некоторое функциональное значение в опосредовании действия холерного токсина, кроме G^, имеет дисиалоганглиозид G>DIfcr> Установлено, что взаимодействие между ними модифицирует структуру холерного токсина и нарушает бислой мембраны. Олигосахаридная часть моносиалоганглиозида G>M>>1> связывается с узнающей молекулой холерного токсина – протомером В, что вызывает увеличение локальной плотности ганглиозидов, их ми-целлообразование. Мицеллы ганглиозидов взаимодействуют с регуляторной единицей холерного токсина – протомером А. Этот протомер А обладает АДФ-рибозилирующей активностью. В результате АДФ-рибозилирования компонентов некоторых из так называемых медленных рецепторов происходит активация аде-нилатциклазы.
Мицеллы ганглиозидов способствуют погружению нротоме-ра А в липидную фазу и транслокации протомера А внутрь клетки. Чем выше концентрация ганглиозидов и мицеллообразова-ние, тем выше рибозилтрансферазная активность протомера А. Ганглиозиды в немицеллярной форме не способны «погрузить» протомер А в мембрану.
■ Мицеллообразование ганглиозидов способствует, таким образом, реорганизации липидного слоя, причем это свойство зависит от структуры комплекса токсин-ганглиозид.
8.4 Участие ганглиозидов в дифференциации клеток
Была предложена модель клеточного цикла, в которой кроме стадии покоя G>0>, неустойчивой и регулируемой циклическими нуклеотидами, постулируется стадия D-дифференциации, контролируемая ганглиозидами. По мере формирования ней-рон-нейрональных взаимодействий меняется структура и количество ганглиозидов и увеличивается число высокоаффинных контактов.
Участвуя в дифференциации клеток, ганглиозиды увеличивают время выживания клеток и вызывают морфологические изменения клеток, проявляя нейритогенный эффект. Нейритогенный эффект экзогенных ганглиозидов обнаружен в культурах клеточных линий нейронального и хромаффинного происхождения, в симпатических и парасимпатических ганглиях и в нервно-мышечных препаратах.
На рис. 6 представлен нейритогенный эффект моносиалоганглиозида G>MI> в концентрации 10~М на рост отростков спи-нального ганглия эмбриона цыпленка. Экзогенные ганглиозиды оказывают влияние на протяженность отростков, их число на клетку и на разветвленность отростков. Интересно, что моносиалоганглиозид G>M>>1> вызывает только увеличение длины аксонов, а три- и тетрасиалоганглиозиды в тех же концентрациях усиливают спрутинг и арборизацию.

8.5 Терапевтические эффекты ганглиозидов
Ганглиозиды in vivo обладают уникальными свойствами: при введении в организм подкожно, внутримышечно или интраперитонеально они относительно длительное время сохраняются в кровяном русле, лишены токсичности, в небольших количествах проникают через гемато-энцефалический барьер и активно встраиваются в нейрональные мембраны. Они способствуют репарации поврежденных аксонов, обладают выраженными терапевтическими эффектами при травмах головного и спинного мозга.
В настоящее время наиболее изучена молекулярная и биологическая роль в этих процессах моносиалоганглиозида G>M>>1>, который при введении in vivo:
а) восстанавливает нейрохимические параметры дофаминер-гических нейронов после нарушения нигростриатной системы, усиливает захват дофамина и активность ирозингидроксилазы;
б) восстанавливает нейрохимические характеристики при частичной холинергической и глутаматергической деафферен-тации гиппокампа, увеличивает активность холинацетилтрансферазы и ацетилхолинэстеразы;
в) восстанавливает высокоаффинный захват холина в коре больших полушарий после нарушений ядер переднего мозга;
г) нормализует дисбаланс между активностью дофамин- и серотонинергических нейронов, вызванный введением апомор-фина;
д) оказывает рост-стимулирующий эффект и защитное действие против вторичной дегенерации серотонин- и норадре-нергических нейронов, вызванной нейротоксинами;
е) уменьшает церебральный отек и восстанавливает ионный баланс после травмы;
ж) способствует регенерации зрительного нерва после перерезки.
С другой стороны, введение антител к G>M>>]> вызывает у развивающихся животных нарушение дендритной арборизации и поведения, ухудшение обучаемости, появление эпилептиформ-ной активности.
Моносиалоганглиозид G>M>>1> хорошо внедряется в мембраны, причем особенно хорошо встраивается молекула G>MI>, имеющая в своем составе С >2>о-эритросфингозин. Возможно, это объясняется его более высокой способностью к мицеллообразованию. Он образует дископодобные мицеллы с М^ЗОО кД, имеющие гидродинамический диаметр около 60 нм.
Интересно, что мицеллы из моносиалоганглиозида G>MI> по-тенциируют действие ионофора грамицидина D. Ганглиозид-ные мицеллы с заключенными в них молекулами грамицидина включаются в модельную мембрану из фосфатидилсерина и изменяют ее проводимость для ионов калия. После добавления мицелл с ионофором увеличивается время открытия ионных каналов и изменяется их амплитуда.
■ Таким образом, ганглиозидные мицеллы могут участвовать в ионтранспортном процессе в мембране, «маркируя» входы в селективные ионные каналы,
О механизмах и функциональной последовательности действия ганглиозидов известно мало. Встраивание экзогенных ганглиозидов, приводящее к перестройке мембранных ансамблей, изменяет ряд внутриклеточных процессов. Вызванная ганглиозидами дифференциация сопровождается изменением активности Na>5>K-ATOa3bi, увеличением внутриклеточного уровня цАМФ, уменьшением включения меченого тимидина в ДНК и значительным удлинением фазы G>(> клеточного цикла. Внедрение ганглиозидов вызывает немедленную перестройку мик-рофиламентной и микротубулиновой системы клеток.
Включение в мембрану экзогенных ганглиозидов усиливает аксональный ток гликозилированных белков и липидов, увеличивает количество гликопротеинов с терминальной манно-зой. Внедрение моносиалоганглиозида G>M>>1> увеличивает в мембране количество эндогенных моносиалоганглиозидов и изменяет активность гликозилтрансфераз: усиливается активность эктофукозилтрансферазы при неизменности активностей сиалил-и галактозилтрансфераз. Внедрение в мембрану трисиалоганг-лиозида G>Tlb> вызывает противоположный эффект.
Недавно выявлено влияние индивидуальных ганглиозидов на фосфорилирование гистона Hj и тубулина, причем в отношении фосфорилирования гистона были особенно эффективны GOJb > GDl* > GTia > GD3> а тубулина – G>xlb> > G>Tla> > G>Qlb>> >> G>Dla>. Показано, что тетрасиалоганглиозид Gg>lb> проявляет зависимое от концентрации влияние на активность Са+ – фос-фолипид-, Са +-кальмодулин-, цАМФ- и цГМФ-активируемых протеиякиназ
8.6 Межклеточное гликозирование ганглиозидов
Своеобразный процесс межклеточного гликозилирования поверхностных гликолипидов и гликопротеинов осуществляется ферментами мембран. Полагают, что гликозилтрансферазы одной клеточной поверхности удлиняют, надстраивают олигосахаридные цепочки гликолипидов и гликопротеинов соседней, противоположной поверхности. Важная регу-ляторная роль в этом процессе принадлежит ионам кальция. Са*+ препятствует образованию субстрат-ферментного комплекса между ганглиозидами и гликозилгрансферазами, а вытеснение его другими ионами способствует межклеточному гликозилированию.
Контактное гликозилирование, как предполагаемый механизм модификации клеточной поверхности в нейрональных мембранах, может быть особенно значимым в образовании синапсов. Вероятно, при этом происходит некая «подгонка» контактирующих мембран.
Роль гликозилирования в синаптической области согласуется с концепцией об участии сиалогликомакромолекул в синаптической передаче и формировании памяти. Полагают, что вхождение сиалогликомакромолекул в контактные зоны является важным звеном молекулярных механизмов в проторении определенных нейрональных путей. Возможно, именно ганглиозиды способствуют образованию ансамблей нейронов, устойчиво связанных друг с другом. Возникновение таких ансамблей исключительно важно для хранения и передачи информации.
8.7 Электрогенность ганглиозидов и ее модификация
Необычайная молекулярная вариабельность ганглиозидов сочетается с лабильной электрогенностью. Для каждой молекулы ганглиозидов характерен свой отрицательный заряд, обусловленный карбоксильной группой сиаловой кислоты. На 1 г ткани мозга приходится не менее 1,3 – Ю анионных групп ганглиозидов. Число анионных групп и, следовательно, уровень отрицательного заряда могут быть объектом регуляции. В этом процессе особая роль принадлежит ферментам – нейрамнни-дазам и сиалилтрансферазам. Они определяют число молекул N-ацетнлнейраминовой кислоты, присутствующих в ганглиозидах, и через цикл сиалирования – десиалирования – отрицательный заряд поверхности.
Сиалилтрансферазы и нейраминидазы находятся на поверхности синаптических мембран там же, где и субстраты, и являются внутренними компонентами синаптической области. В синаптосомалъных мембранах содержится около половиньг ганглиозидов, нейраминидаз и сиалилтрансфераз. Иначе говоря, эти мембраны содержат в 5–6 раз больше ганглиозидов и в 6,5 раз больше нейраминидаз, чем другие плазматические мембраны мозга.
Существенное влияние на поверхностный заряд ганглиозидов в мембране оказывает конформация нейраминовой кислоты и ближайших радикалов. Отщеплению нейраминовой кислоты препятствует соседний N-ацетилгалактозамин. В силу этого гли-козидный кислород нейраминовой кислоты вместе с другими атомами, включающими и карбоксильный кислород N-аиетил-галактозамина, лежит как бы в «кислородной клетке»:

Такая конфигурация атомов вокруг гликозидной связи защищает ее от действия фермента и способствует сохранению отрицательного заряда молекулы. Иная картина наблюдается с ганглиозидами, лишенными N-ацетилгалактозамина: G>T>>3>, G>D>>3>,
GM3> GM4
Нейраминовая кислота недоступна ферментам, когда карбоксильные группы близлежащих ганглиозидов соединены с Са+:

В этом случае исключено не только устранение N-ацетил-нейраминовой кислоты, но и присоединение дополнительного числа ее молекул сиалилтрансферазами.
8.8 Лактонные формы ганглиозидов
Между карбоксильной группой N-апетилнейраминовой кислоты и ее гидроксильными группами могут возникать внутримолекулярные взаимодействия, приводящие к образованию лак-тонов – внутренних сложных эфиров.
В создании лактонов могут участвовать гидроксилы, расположенные'у 4, 7, 8 и 9-го атомов углерода нейраминовой кислоты. Лактоны могут возникать и с участием гидроксильных групп соседней галактозы, приводя к образованию 6-членного кольца:

Молекулы нейраминовой кислоты, находящиеся в димерной связи, также образуют лактоны, по структуре аналогичные лактонам коломиновой кислоты, в которой карбоксильная группа одной молекулы связана с гидроксилом 7-го или 9-го атома углерода соседней нейраминовой кислоты.
Лактоны были обнаружены в ганглиозидах мозга. В нейтральной или слабокислой среде терминальная молекула нейраминовой кислоты полисиалоганглиозидов спонтанно образует лак-тон, а в более кислой среде этот процесс затрагивает и другие молекулы нейраминовой кислоты. Установлено, что ионы кальция предотвращают образование лактонов в терминальных молекулах нейраминовой кислоты,
ш Ганглиозиды, имеющие нейраминовую кислоту в лактон-ной форме, обладают иными физико-химическими свойствами, они не заряжены, нейтральны. Поэтому образование лактонов является процессом, изменяющим заряд молекулы, и в более общем виде является примером модификации структуры отдельного компонента ганглиозидов, приводящей к изменению информационной емкости всей сложной молекулы.
8.9 О-ацетилирование ганглиозидов – один из возможных механизмов изменения их структуры
В структуре нейраминовой кислоты очень важна боковая по-лиеидроксильиая группировка, уникальная среди олигосахарид-ных компонентов поверхности:

Эта полигидроксильная группировка может быть дополнительно ацетилирована и, возможно, метилирована. В природе известно несколько производных О-ацетилнейраминовых кислот, в которых ацетилированы гидроксилы у 4, 7, 8 и 9-го атомов углерода:


Пока неизвестно, осуществляется ли модификация ганглиозидов ацетилированием ферментативно и что является источником ацетила.
Появление дополнительных ацетильных групп изменяет структуру и конформацию нейраминовой кислоты и ее внутри-и межмолекулярные взаимодействия. Оно делает ее менее доступной сиалилтрансферазам и резко меняет способность ганглиозидов связывать металлы. Увеличивается структурное разнообразие индивидуальных ганглиозидов. Участки поверхности, занятые ацетилированными ганглиозидами, будут иметь иные архитектурные и опознавательно-информационные свойства.
В настоящее время считают, что N-ацетилнейраминовая кислота выполняет антиадгезывную роль в гликоконъюгатах поверхности, маскируя специальные рецепторные стороны. Баланс между сиало- и асиалоганглиозидами определяет адгезию и узнавание клеток. Специфическое присоединение нейраминовой кислоты к рецепторам является одним из механизмов, с помощью которого клетка модулирует свой потенциал узнавания и изменяет свое поведение.
■ Таким образом, ганглиозиды вносят существенный вклад в функции нейрональных мембран. Ганглиозиды несут многочисленные отрицательные заряды, образуя поверхностный анионный слой с выраженным сродством к катионам. Все структурные изменения ганглиозидов за счет гликозилирования, ре-и десиалирования, ацетилирования, образования лактонов и взаимодействия с ионами, гликопротеинами, фосфолипидами и белками влияют, прежде всего, на их заряд и затрагивают электрогенную природу мембран. Сочетание необычайной структурной пластичности с лабильной электрогенностью и способностью к узнаванию других молекул делает эти уникальные соединения участниками проведения нервного импульса в нейронах и регуляции этого процесса.
8.10 Иммунологические свойства ганглиозидов
Антитела специфически реагируют с олигосахаридной частью ганглиозидов независимо от того, прикреплена ли она к липидам, белку, нуклеиновой кислоте. В последнее время начинает вырисовываться и роль церамидной части в антигенных свойствах ганглиозидов.
Введенные интрацеребрально антиганглиозидные антитела нарушают функции ЦНС, причем эти изменения были следствием нарушения синаптических контактов. Особенно полезными в такого рода исследованиях оказались анти-С>М>1 антитела, поскольку четко доказаны рецепторные функции G>M>>1> и его большая экспонированность и доступность антителам на поверхности клетки в экстраклеточном пространстве. Введение анти-G^ji антител ингибирует обучение путем блокирования стадии консолидации, задерживает развитие молодых животных, блокирует обезболивание морфином и седативное действие резерпина, нарушает некоторые холинергические функции в гипоталамусе.
Как уже упоминалось выше, ганглиозиды могут обеспечивать некоторые сигнальные механизмы, регулирующие последовательность процессов развития ЦНС. Это подтвердилось при исследовании поведенческих, морфологических и химических изменений при введении aHTH-G>M>>1> антител новорожденным животным. У молодых животных наблюдался дефицит в обучаемости, потеря пирамидных клеток, тонких корешков дендри-тов и миелина, а в соматосенсорном кортексе на 30% снижалось содержание ганглиозидов, галактозилцерамида и РНК. Точное выяснение дифференциального участия индивидуальных ганглиозидов в этих процессах может оказаться важнейшим ключом к синаптическим механизмам.
В последние годы накапливаются факты о роли ганглиозидов как физиологических модуляторов иммунного ответа лимфоцитов. Следует отметить, что уникальной иммунологической роли тимуса соответствует тот факт, что в составе его ганглиозидов преобладает N-гликолилнейраминовая кислота, присутствие которой в олигосахаридной цепочке придает ганглиозидам более выраженные антигенные свойства. При злокачественной трансформации В- и Т-лимфоцитов опухолевые клетки «сбрасывают» со своей мембраны большое количество ганглиозидов, которые способны ингибировать действие макрофагов и естественных киллеров. С другой стороны, встраивание ганглиозидов в мембрану активирует естественные киллеры и помогает уничтожать опухолевые клетки.
8.11 Ганглиозидозы
Ганглиозидозы – наследственные заболевания, характеризующиеся распадом психических функций вплоть до идиотии, дегенерацией нейронов, демиелинизацией, прогрессирующим депонированием ганглиозидов в цитоплазме нейронов.
В 1881 г. британский офтальмолог У. Тей впервые описал врожденное заболевание, связанное с метаболизмом ганглиозидов. Оно теперь известно как болезнь Тей-Сакса, или С>М2>-ганглио-зидоз. Второе нарушение обмена ганглиозидов – G^-ганглио-зидоз – было открыто на 84 года позже, в 1965 г. Описанные заболевания имеют пять общих признаков: 1) прогрессирующие умственные и двигательные расстройства с началом в детстве и летальным исходом; 2) аутосомальное рецессивное наследование; 3) нейрональный липидоз с накоплением G>M>>1> или G>M>>2>; 4) накопление структурно-родственных гликолипидов, гликопротеинов, полисахаридов; 5) отсутствие или серьезный дефицит специфических лизосомальных гликогидролаз.
В последние годы к известным формам ганглиозидозов прибавились врожденные нарушения, связанные с дефицитом ферментов сиалндаз и фукозвдаз.
9. ИЗМЕНЕНИЕ СОСТАВА ЛИПИДОВ В ОНТОГЕНЕЗЕ
Наиболее быстрое увеличение содержания липидов мозга наблюдается после периода интенсивного синтеза ДНК и белка, т.е. в период, когда происходит рост нейронов, глиальный митоз, аксодендритная пролиферация, формирование синаптических связей и, наконец, миелинизация.
До миелинизации липидный состав мозга сходен с другими органами, но миелинизация драматически изменяет состав липидов мозга. Правда, даже после завершения миелинизации содержание общих липидов в мозге человека продолжает увеличиваться до 30 лет и только после этого начинается их медленное снижение. Причем это снижение касается прежде всего фосфолипидов и жирных кислот и едва ощутимо затрагивает содержание холестерина и цереброзидов.
Липиды развивающегося мозга подразделяют на 4 группы на основе преимущественных: изменений в период миелинизации. Рассмотрим это на примере мозга крысы как объекта наиболее изученного, у которого лостнатальная миелинизация наиболее выражена в период с 21-го по 40-й день.
Содержание основных ганглиозидов мозга человека
|
Ганглиозиды |
Серое вещество |
Белое вещество |
||
|
новорожденные |
взрослые |
новорожденные |
взрослые |
|
|
GM3 |
1 |
- |
1 |
|
|
GM2 |
3,6 |
1,7 |
6,9 |
1>9 |
|
GM1 |
14,6 |
12,8 |
19,1 |
12,6 |
|
GDU |
71,6 |
22,8 |
57,8 |
18,4 |
|
GDlb |
1,8 |
23,5 |
2,1 |
30,4 |
|
GTI |
7,3 |
31,2 |
3,4 |
27,9 |
Первая группа липидов – эфиры холестерина и ганглиозиды. Концентрация их резко меняется в первые 6 дней постнатального развития крыс. Содержание эфиров холестерина уменьшается от 2 мкмолей на 1 г сырой массы до концентрации, составляющей менее 5% от начальной. У крыс это снижение происходит задолго до начала миелинизации, что отражает пролиферацию клеток или очень раннюю дифференциацию гли-альных клеток.
Ганглиозиды на 3-й день постнатального развития составляют 27% от содержания во взрослом организме. Концентрация ганглиозидов за 24 последующих дня быстро увеличивается, достигая 90% от уровня взрослого животного. Спектр индивидуальных ганглиозидов также меняется: при рождении преобладает моносиалоганглиозид G^m, а затем увеличивается содержание дисиалоганглиозидов. Увеличение количества ганглиозидов и изменение их состава связано с ростом аксонов и ден-дритов.
Вторая группа включает цереброзиды, сульфатиды, сфинго-миелин, трифосфоинозитиды, фосфатидные кислоты, галакто-зилдиглицериды. На 3-й день постнатального развития их концентрация невелика, а затем резко увеличивается в период от 12-го до 18-го дня. Пять первых перечисленных липидов являются основными комлонентами миелиновых мембран, их низкая концентрация при рождении подтверждает, что они локализованы в специальных мембранных структурах, которые появляются в мозге во время миелинизации. Полифосфоинозитиды и фосфатидные кислоты отличаются от других липидов этой группы, так как они продолжают заметно увеличиваться и после 24 дней, когда уровень других липидов этой группы стабилизируется.
Третья группа липидов включает фосфатидальэтаноламин, фосфатидальхолин, холестерин, фосфатидилсерин, фосфати-дилглицерин, концентрация которых составляет 12–34% от уровня взрослого организма и увеличивается во время миелинизации, но не столь значительно, как у липидов второй группы. Первые три представителя этой группы локализованы в мембранах миелина и нарастание их связано с миелинизацией.
Четвертая группа липидов охватывает три лииида мозга – фосфатидилэтаноламин, фосфатидилхолин и моно-фосфоинозитид, концентрация которых составляет 50–59% от содержания взрослого мозга и очень медленно увеличивается в период развития. Известно, что эти липиды являются повсеместными компонентами большинства мембранных структур и спектр их изменений не связан с преимущественными изменениями каких-либо специфических мембранных образований. Но в ходе онтогенеза в мембранах мозга увеличивается отношение ФЭ:ФХ и количество сфингомиелина. Диацильные формы фосфолипидов заменяются на плазмалогенные и значительно увеличивается микровязкость мембран.
Таким образом, различные классы липидов характеризуются индивидуальным характером накопления в период созревания мозга.
Выводы
1. Для нервной ткани характерно особенно высокое содержание липидов – до 50% от сухой массы ткани. Наряду с этим установлено огромное разнообразие и наличие специфических только для мозга индивидуальных липидов.
2. Фосфолипиды нервной ткани составляют до 70% от суммарного содержания липидов в сером веществе и до 45–50% – в белом веществе мозга. Обнаружена необычайно высокая гетерогенность фосфолипидов мозга по сравнению с висцеральными органами.
3. Основной представитель стеролов в нервной ткани – холестерин, на долю которого приходится около 25% от суммарного содержания липидов. В то же время в мозге взрослых животных мало эфиров холестерина.
4. Значительная часть сфинголипидов мозга представлена га-лактоцереброзидами и галактосульфатидами, количество которых в белом веществе значительно выше, чем в сером. Для мозга характерна высокая концентрация и большое разнообразие индивидуальных ганглиозидов.
5. Уровень свободных жирных кислот в мозге весьма невелик; напротив, установлено высокое содержание и огромное разнообразие жирных кислот в липидах нервной ткани. Основную массу жирных кислот липидов мозга составляют пальмитиновая 16:0, стеариновая 18:0, олеиновая 18:1 и арахидоновая 20:4 кислоты. В мозге идентифицировано около 40 индивидуальных жирных кислот, в том числе полиненасыщенных, длин-ноцепочечных и гидрокислот, которыми особенно богаты це-реброзиды и сульфатиды. Гетерогенность жирных кислот липидов мозга лежит в основе структурной лабильности мембран и определяет их важнейшие физико-химические свойства.
6. Содержание и соотношение отдельных классов липидов значительно изменяются в ходе развития и дифференцировки мозга. Наиболее интенсивно эти процессы протекают в раннем постнатальном онтогенезе.
7. Установлены существенные различия в липидном составе важнейших мембранных образований нервной ткани. Обращает на себя внимание высокое содержание и чрезвычайное разнообразие ганглиозидов, особенно в мембранах нервных окончаний и в дендритах. Именно здесь наиболее полно проявляется функциональная роль этих специфических липидов, участвующих в связывании различных катионов, в процессах адгезии, в обеспечении иммунохимической специфичности и др.
8. Специфическими липидными компонентами миелина являются цереброзиды и сульфоцереброзиды; установлено высокое содержание в миелине холестерина и фосфолипидов, в том числе плазмалогенов, доля которых в миелине составляет более 90% от его количества в целом мозге.
9. Липиды мембран мозга организованы в бислой с планар-ной и поперечной асимметричностью размещения липидов по слоям. Она поддерживается механизмами, учитывающими структуру липидов, их ненасыщенность, стереоконфигурацию полярных групп, специфичность липид-переносящих белков, ферментативные превращения липидов.
10. Динамичность липидного бислоя определяется интрамолекулярными движениями и фазовыми переходами липидов, что создает основу для структурных перестроек в мембранах.
11. Липиды бислоя принимают участие в передаче информации через мембрану и в осуществлении внутриклеточного ответа.
12. Организованная многослойная структура миелина, имеющая самое высокое содержание липидов, поддерживается длинно- и короткорадиусными взаимодействиями между липидами и основным и протеолипидным белками. Формирование миелина является сложным синхронизированным процессом взаимодействия аксонаиглии, любое его нарушение вызывает демиелинизацию.
13. Экстраклеточный матрикс мембран мозга представляет собой комплексную, динамичную систему, где происходит распределение регуляторных сигналов, передача информации внутрь клетки, реализуется прямая и обратная связь с ядром.
14. Специфичность экстраклеточного матрикса определяется первичной структурой, организацией и площадью, занимаемой гликолипидами и гликопротеинами. Экстраклеточный матрикс нейрональных мембран обогащен разнообразными ганглиозидами.