27. Механика – квантовая физика (качественная задача)
Демонстрационный вариант Единый государственный экзамен ЕГЭ 2017 г. – задание №27
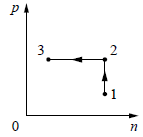
Постоянное количество одноатомного идеального газа участвует в процессе, график которого изображён на рисунке в координатах p – n, где p – давление газа, n – его концентрация. Определите, получает газ теплоту или отдаёт в процессах 1–2 и 2–3. Ответ поясните, опираясь на законы молекулярной физики и термодинамики.
Решение:
По первому закону термодинамики количество теплоты, которое получает газ, равно сумме изменения его внутренней энергии ΔU и работы газа А: Q = ΔU + A. Концентрация молекул газа n=N/V, где N – число молекул газа, V – его объём. Для идеального одноатомного газа внутренняя энергия U=3/2vRT (где ν – количество моль газа). По условию задачи N = const.
Так как на участке 1–2 концентрация газа не изменяется, то его объём постоянен (изохорный процесс), значит, работа газа А = 0. В этом процессе давление газа растёт, согласно закону Шарля температура газа также растёт, т.е. его внутренняя энергия увеличивается: ΔU > 0. Значит, Q > 0, и газ получает тепло.
На участке 2–3 концентрация газа уменьшается, значит, его объём увеличивается, и работа газа положительна: А > 0. Давление газа постоянно (изобарный процесс), по закону Гей-Люссака температура газа также увеличивается. Поэтому ΔU > 0 . По первому закону термодинамики Q > 0. В этом процессе газ получает тепло.
Ответ: газ получает положительное количество теплоты в процессах 1–2 и 2–3
Демонстрационный вариант Единый государственный экзамен ЕГЭ 2016 г. – задание №28
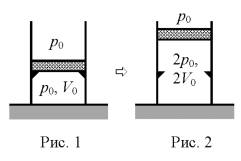
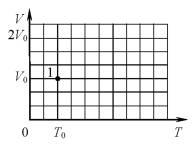
В вертикальном цилиндре с гладкими стенками под массивным металлическим поршнем находится идеальный газ. В первоначальном состоянии 1 поршень опирается на жёсткие выступы на внутренней стороне стенок цилиндра (рис. 1), а газ занимает объём V0 и находится под давлением р0, равным внешнему атмосферному. Его температура в этом состоянии равна Т0. Газ медленно нагревают, и он переходит из состояния 1 в состояние 2, в котором давление газа равно 2р0, а его объём равен 2V0 (рис. 2). Количество вещества газа при этом не меняется. Постройте график зависимости объёма газа от его температуры при переходе из состояния 1 в состояние 2. Ответ поясните, указав, какие явления и закономерности Вы использовали для объяснения.
Решение:
1. Уравнение Клайперона-Менделеева для состояний газа в 1 и 2 будут иметь вид:
 , откуда получаем
, откуда получаем 
2. Рассмотрим силы, приложенные к поршню, когда он уже не опирается на выступы на стенках цилиндра (см. рисунок ниже).
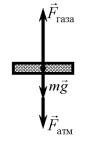
Очевидно, что сила тяжести, равная  и сила, действующая со стороны атмосферы
и сила, действующая со стороны атмосферы  , постоянны и направлены вниз. Учитывая, что поршень перемещается медленно, силу давления на поршень будем считать постоянной и равной
, постоянны и направлены вниз. Учитывая, что поршень перемещается медленно, силу давления на поршень будем считать постоянной и равной  , где
, где  – площадь горизонтального сечения поршня. Так как площадь
– площадь горизонтального сечения поршня. Так как площадь  постоянна, то и
постоянна, то и  также постоянно. При
также постоянно. При  получаем изобарный процесс при
получаем изобарный процесс при  . Температура начала этого процесса
. Температура начала этого процесса  найдем из системы уравнений
найдем из системы уравнений  ,откуда получаем
,откуда получаем 
3. На отрезке температур  процесс нагревания газа изохорный (
процесс нагревания газа изохорный ( ), давление газа с ростом его температуры при нагревании увеличивается от
), давление газа с ростом его температуры при нагревании увеличивается от  до
до  .
.
Ответ: а) при 

б) при  объем газа меняется от
объем газа меняется от  до
до  по закону
по закону  .
.
График, изображающий зависимости из п. а) и б), представляет собой ломаную линию:
