Острый гломерулонефрит (работа 2)
РЕФЕРАТ
НА ТЕМУ: ОСТРЫЙ ГЛОМЕРУЛОНЕФРИТ
ОСТРЫЙ ГЛОМЕРУЛОНЕФРИТ
(Glomerulonephritis acuta)
Острый гломерулонефрит (нефрит) — двустороннее иммуновоспалительное заболевание, являющееся одним из наиболее распространенных заболеваний почек. Среди взрослых острый гломерулонефрит наблюдается преимущественно в возрасте 20— 40 лет. Чаще болеют мужчины,
В связи с тем что при остром гломерулонефрите наблюдаются изменения и в канальцевом отделе нефрона (см. ниже), вместо термина «острый гломерулонефрит» часто применяют термин «острый нефрит».
Этиология. Развитию острого гломерулонефрита в 90 % случаев предшествует инфекционный процесс. Чаще всего это ангина, обострение хронического тонзиллита, острое респираторное заболевание, грипп, отит и синусит (острый или обострение хронического), скарлатина, пневмония, гнойничковые поражения кожи и др. Этиологическое значение последних особенно важно в странах с жарким климатом. Между вспышкой инфекции и появлением первых симптомов острого гломерулонефрита чаще всего проходит — 10 дней. Однако может наблюдаться как более короткий, так и более продолжительный промежуток (до 30 дней).
Раньше считали, что охлаждение, особенно «влажный холод», является непосредственной причиной острого гломерулонефрита. В настоящее время многие клиницисты рассматривают его скорее как фактор, способствующий обострению дремлющей очаговой инфекции.
Связь между тяжестью перенесенной инфекции и возможностью развития и тяжестью течения острого гломерулонефрита не установлена. Поражение почек возможно после нетяжелого обострения хронического тонзиллита, и, наоборот, оно может отсутствовать после тяжелой ангины.
Среди инфекционных агентов, обусловливающих развитие острого гломерулонефрита, ведущая роль принадлежит стрептококку. Последний часто обнаруживается в миндалинах и зеве при ангине, обострении хронического тонзиллита, остром респираторном заболевании. Развитие гломерулонефрита связано с наличием особых «нефритогенных» штаммов стрептококка (гемолитического стрептококка группы А типов 12, 25,4). Первый чаще ведет к развитию небольших «эпидемий» гломерулонефрита, остальные два обычно являются причиной спорадических случаев. Следует, однако, подчеркнуть, что иногда острый гломерулонефрит развивается после инфекции, вызванной другими типами стрептококков и, наоборот, не развивается при наличии в очагах инфекции стрептококков указанных выше типов. Определение при остром гломерулонефрите высоких титров стрептококковых антител (чаще — антистрептолизина-О, реже — антистрептокиназы и антигиалуронидазы) является еще одним доказательством этиологической роли стрептококка. Реже развитию острого гломерулонефрита предшествуют заболевания, вызванные стафилококком, стрептококком пневмонии (пневмококком), а в некоторых случаях и вирусные (пневмония, эпидемический паротит, краснуха, ветряная оспа, инфекционный мононуклеоз и т. д.).
В последние годы появился ряд исследований, подтверждающих возможность микоплазменной и вирусной этиологии гломерулонефрита. В частности, доказана «нефритогенность» вируса гепатита В.
Острый гломерулонефрит может быть также проявлением (правда, лишь в редких случаях основным) лекарственной и пищевой аллергии.
Приблизительно в 10 % случаев острый гломерулонефрит развивается постепенно, не давая вначале ярких проявлений, в связи с чем причину его установить не удается.
Патогенез. Наиболее доказательной является иммуноаллергическая теория патогенеза гломерулонефрита. Эта теория основывается на экспериментальных исследованиях. В. К. Линдеману еще в 1900 г. с помощью гетерологической антисыворотки, содержащей противопочечные антитела, удалось вызвать у кроликов гломерулонефрит, морфологически весьма сходный с таковым у человека.
Намного позже (1933, 1934) японский исследователь Масуги, пользуясь методикой В. К. Линдемана, описал развитие типичной клинической и морфологической картины гломерулонефрита у кроликов, которым вводилась сыворотка уток, предварительно сенсибилизированных повторными инъекциями кашицы из почки кроликов. Поражение почек происходит в результате взаимодействия противопочечных антител, содержащихся в нефротоксической сыворотке, с тканью почек животного, которому эта сыворотка вводится. Антитела фиксируются, в основном, в корковом веществе почек, особенно в базальных мембранах капилляров клубочка.
Механизм экспериментального гломерулонефрита существенно отличается от механизма развития заболевания у человека, прежде всего тем, что используется гетерогенная сыворотка. В 1945 г. Кавелти с соавторами создал экспериментальную модель, почти аналогичную гломерулонефриту у человека. По его данным, у кроликов и особенно у крыс одновременное парентеральное введение кашицы из ткани гомологичных почек и убитых стрептококков группы А часто вызывает острый гломерулонефрит, который может переходить в хронический. Позднее удалось вызвать у крыс нефропатию, по характеру близкую к гломерулонефриту, путем введения гомологичной почечной ткани или даже ткани собственной почки с микобактериальным стимулятором Фрейнда.
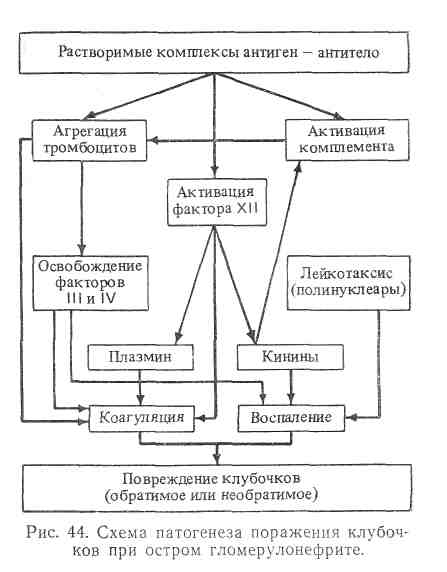
В настоящее время считают, что поражение клубочков при этом заболевании в 70 % случаев вызывается растворимым, циркулирующим в крови иммунным комплексом, состоящим из антигенов «нефритогенных» стрептококков и их антител, причем количество первых значительно больше, чем вторых. Эти комплексы, откладывающиеся вдоль наружной поверхности базальной мембраны капилляров клубочка, сами по себе мало повреждают ее, но вызывают цепную реакцию, в которой принимают участие три биологические системы: комплемента, коагуляции и кининовая, а также два типа клеток — полинуклеары и тромбоциты. Иммунные комплексы фиксируют комплемент и активируют третий компонент его, что, с одной стороны, способствует оседанию их в капиллярах клубочка, на которые воздействуют сосудодвигательные субстанции комплемента, а с другой — приводит к образованию факторов хемотаксиса, привлекающих полинуклеары и способствующих их фиксации подэндотелиально у базальной мембраны капилляров клубочка. Лизосомные энзимы полинуклеароз повреждают мембрану, вызывая «энзиматическую перфорацию» ее. Кроме того, полинуклеары выделяют гистамин и серотонин, повышающие проницаемость стенки сосудов, и катепсины, усиливающие синтез вазоактивных полипептидов — кининов.
Важную роль в повреждении клубочков играют также феномены коагуляции. Они обусловлены рядом причин: уже упомянутая выше активация комплемента иммунными комплексами ведет к необратимой агрегации тромбоцитов; с другой стороны, эти иммунные комплексы активируют XII фактор свертывания (фактор Хагемана), который также может образовывать кинины, благодаря активированию сывороточного калликреиногена. Кроме того, эти комплексы способствуют освобождению тромбоцитами фактора III (активирует превращение протромбина в тромбин) и IV (антигепаринового), а также факторов, повышающих проницаемость стенки сосудов. Все это приводит к образованию в просвете капилляров клубочка тромбина, который переводит фибриноген в фибрин, откладывающийся в их стенке. Эти депо весьма агрессивны. Они вызывают быструю пролиферацию эндотелиальных и мезангиальных клеток, которые их фагоцитируют, затем внутриклеточное отложение гиалиновой субстанции. Если учесть, что феномены коагуляции в свою очередь способны активировать комплемент и реакция носит цепной характер, то процесс может заканчиваться прогрессирующей облитерацией капилляров клубочка. Фибриновые депо являются фактором, вызывающим воспаление клубочка и обусловливающим его автоматизацию, т. е. переход процесса в хроническую форму.
Депо небольших размеров фагоцитируются и лизируются в результате местной активации системы фибринолиза, и наступает выздоровление. При значительных отложениях и ослаблении системы фибринолиза воспалительный процесс приобретает хронический характер. Все изложенное иллюстрируется схемой, представленной на рис. 44.
В последнее время появились данные, свидетельствующие о том, что в патогенезе гломерулонефрита известную роль играют и реакции клеточного иммунитета. В. В. Сура, И. Е. Тареева, Т. Г. Троянова обнаружили при гломерулонефрите уменьшение количества Т-лимфоцитоз (по тесту спонтанного розетко-образования), а также замедление миграции лейкоцитов и усиление бластной трансформации лимфоцитов под влиянием почечного антигена. Последнее является доказательством наличия аутосенсибилизированных лимфоцитов, что наряду с наличием противопочечных антител свидетельствует о роли аутоиммунного компонента в патогенезе гломерулонефрита.
В развитии «иммунокомплексного» гломерулонефрита у человека наряду с экзогенными, в первую очередь инфекционными, имеют значение и эндогенные факторы, определяющие иммунологическую реактивность организма. Видимо, имеют значение и конституционные факторы.
Наиболее частые симптомы острого гломерулонефрита — протеинурия, отеки, артериальная гипертензия.
Протеинурия возникает главным образом в результате повышения проницаемости базальной мембраны капилляров клубочка для белковых молекул в результате ее «энзиматической перфорации», т. е. является клубочковой.
Отеки обусловлены в основном снижением клубочковой фильтрации, уменьшением фильтрационного заряда натрия и повышенной реабсорбцией его в канальцах, ведущими к задержке воды и натрия в организме. Нельзя отрицать роли гиперальдостеронизма, повышения проницаемости стенки сосудов, а также присоединяющейся недостаточности кровообращения.
Патогенез артериальной гипертензии при остром гломерулонефрите до конца не выяснен. Количество ренина и ангиотензина при этом не увеличено ни в периферической крови, ни в крови, взятой из почечной вены. Возможно, стенка сосудов в связи
с накоплением в ней натрия может повышенно реагировать и на нормальное количество прессорных субстанций. Но основное значение имеет увеличение объема циркулирующей крови, ведущее к повышению сердечного выброса. Нельзя исключить образования в почке еще не известных нам прессорных веществ или инактивации депрессорных факторов.
Пато морфологи я. В начальном периоде острого гломерулонефрита макроскопически почки мало изменены. Более выраженные изменения обнаруживаются на 8—10-й день заболевания. К этому времени на поверхности почек и на разрезе можно видеть картину «пестрой почки», а также красные полоски или мелкие полупрозрачные сероватые зерна по ходу пирамид. Иногда почки увеличены. Консистенция их мягкая, волокнистая капсула снимается легко.
Метод пункционной биопсии почек позволил установить, что микроскопическая картина зависит от формы и стадии заболевания. Гиперемия, имеющаяся в первые дни, с развитием пролиферативных и экссудатив
ных процессов в клубочках сменяется их ишемией, вслед за которой вновь развивается гиперемия.
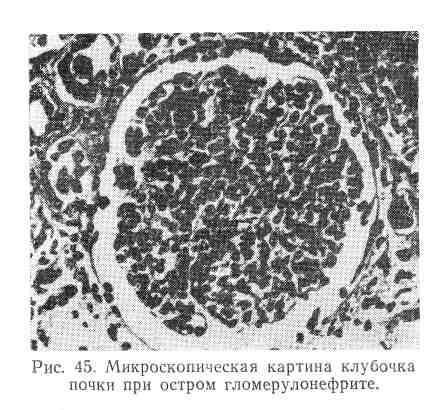
Основным проявлением острого гломерулонефрита является диффузный гломерулит с развитием интракапиллярной пролиферации. Клубочки увеличены, заполняют просвет капсулы (рис. 45). Среди клеток клубочка встречается много полиморф-ноядерных лейкоцитов. Поражение базальной мембраны капилляров клубочка, как правило, незначительно и ограничивается очаговым утолщением ее в местах пролиферации эндотелия. В зависимости от того, преобладает ли белковый экссудат, слущенный эпителий или лейкоциты и эритроциты в просвете капсулы клубочка, выделяют экссудативную, деструктивную и геморрагическую формы гломерулонефрита.
Если процесс затягивается, могут появиться изменения, характерные для мембранозного, мебранозно-пролиферативного гломерулонефрита, а иногда даже начальные элементы фибропластической трансформации.
Поражение канальцев неоднородно: наблюдается гиалиново-капельная, вакуольная или зернистая дистрофия. В просвете почечных канальцев видны цилиндры (эритроцитвые, гиалиновые, смешанные). Строма почки поражена незначительно. Повторная биопсия свидетельствует о том, что при излечении все изменения подвергаются обратному развитию в течение 4—6, иногда 12 месяцев.
Клиника. Различают два варианта течения острого гломерулонефрита: полисиндромный с бурным началом, рядом резко выраженных симптомов, как внепочечных, так и почечных (протеинурия, эритроцитурия и др.), и моносиндромный (мочевой синдром) с постепенным неярким началом, без выраженных субъективных и с ограниченными нерезко выраженными объективными проявлениями. На существование моносиндромного варианта указывал еще Ф. Г. Яновский (1927). В последнее время он встречается не менее чем в 20 % случаев.
При расспросе больного нужно выяснить, не перенес ли он за несколько дней или недель до появления первых симптомов заболевания ангины, острого респираторного заболевания, гриппа, скарлатины, другого инфекционного заболевания или переохлаждения.
Наиболее часто больные жалуются на слабость, боль в пояснице, головокружение, одышку, головную боль, потерю аппетита, тошноту, рвоту, боль или тяжесть в животе, в области сердца, сердцебиение. Боль в пояснице тупая, обычно двусторонняя, наблюдается приблизительно у половины больных. (Редкие случаи острого гломерулонефрита, протекающие с сильной болью в пояснице и сопровождающиеся иногда дизурическими явлениями, обозначались старыми авторами как «болевой нефрит» — nephritis dolorosa.) Сравнительно редко (в 10—15 % случаев) отмечается субфебрильная температура.
Часто первым симптомом заболевания, на который обращает внимание сам больной или его окружающие, являются отеки, обычно наиболее выраженные по утрам на лице, особенно на веках и под глазами. Бывают отеки на мошонке, а также на голенях и стопах. К вечеру они менее заметны, особенно у больных, не придерживающихся строгого постельного режима. Общие отеки, а также гидроторакс, асцит, гидроперикард наблюдаются относительно редко (примерно в 25 % случаев). Характерно быстрое (в течение нескольких часов) нарастание отеков и относительно быстрое их исчезновение (в большинстве случаев через четыре, а в 25 % случаев через две недели от начала болезни). Возможны скрытые отеки, которые обнаруживаются лишь при систематическом взвешивании и поэтому часто не регистрируются.
Одним из кардинальных признаков острого гломерулонефрита в случае его бурного начала является повышение артериального давления. Обычно повышение относительно небольшое (24/12,7--13,3 кПа, т. е. 180/95—100 мм рт. ст.), причем наиболее высокий уровень наблюдается в первые дни заболевания. Гипертензия обычно исчезает раньше других внепочечных симптомов (в 65 % случаев в течение одного месяца от начала заболевания). Изменения глазного дна относительно редки (в 25 % случаев) и обычно мало выражены, изменяется главным образом калибр сосудов.
Во многих случаях наблюдаются признаки недостаточности кровообращения, хотя в последние годы отмечается тенденция к уменьшению частоты и тяжести их. Так, гораздо реже наблюдается острая левожелудочковая недостаточность, в частности приступы сердечной астмы. Однако иногда они могут .явиться первым проявлением заболевания. Еще реже наблюдается правожелудочковая или тотальная недостаточность сердца. Считавшаяся раньше характерной для острого гломерулонефрита брадикардия теперь встречается относительно редко, чаще наблюдается нормальная частота пульса или тахикардия, что может считаться проявлением начальной стадии недостаточности кровообращения. Сердце несколько расширено (особенно влево). Сердечный толчок, в отличие от такового при обострении хронического гломерулонефрита, обычно нерезистентный. Тоны сердца приглушены, особенно при наличии жидкости в перикарде. Характерны акцент II тона над аортой и систолический шум над верхушкой сердца, обычно исчезающий через несколько недель (относительная недостаточность митрального клапана). При более выраженном поражении мышцы сердца может кратковременно выслушиваться ритм галопа.
При ЭКГ исследовании наиболее характерно замедление предсердно-желудочковой проводимости, низкий вольтаж зубцов Ρ и R, снижение зубца Τ (он может быть двухфазным или отрицательным) и конкордатное смещение интервала S—Τ ниже изо< электрической линии в I—II стандартных и левых грудных отведениях. Перечисленные выше нарушения сердечно-сосудистой деятельности наиболее ярко выражены на высоте болезни (1—3 недели). При нормализации артериального давления и ликвидации отеков они обычно исчезают. Изменение миокарда при остром гломерулонефрите следует трактовать как миокардиострофию, миокардит наблюдается редко.
В период отеков и повышения артериального давления может развиться ангиоспастическая энцефалопатия (почечная эклампсия). В настоящее время это осложнение наблюдается редко (в 1—2 % случаев). Предвестниками ангиоспастической энцефалопатии являются мучительная головная боль, тошнота, рвота, возбуждение, кратковременный амавроз, повышение сухожильных рефлексов, положительный симптом Бабин-ского. Затем больной внезапно теряет сознание, появляются эпилептоидные судороги, расширяются зрачки. Приступ продолжается 3—5 мин и может повторяться несколько раз в сутки. Почечная эклампсия обусловлена ангиоспазмом, отеком мозга и повышением внутричерепного давления. При исследовании глазного дна обнаруживается отек сетчатки и диска зрительного нерва.
При исследовании крови в начале заболевания нередко определяется незначительный лейкоцитоз с лимфопенией, увеличение СОЭ, эозинофилия, реже — анемия. Реакция на С-реактивный протеин, дифениламиновая и сиаловая пробы положительные обычно только в первые дни заболевания. Если же они положительны в более поздние сроки, это свидетельствует о наличии активных очагов инфекции.
Следует подчеркнуть, что далеко не всегда наблюдается соответствие между степенью внепочечных и почечных проявлений заболевания. Суточное количество мочи при остром гломерулонефрите в разгар заболевания снижается до 500—400 мл. При этом относительная плотность мочи сравнительно высокая с обычно нормальным содержанием мочевины и сниженным — хлорида натрия. Резко выраженная олигурия (100—150 мл в сутки) или анурия наблюдается редко и обычно через 1—3 дня сменяется полиурией. При этом относительная плотность мочи, в отличие от таковой при острой недостаточности почек, сравнительно быстро нормализуется. На прогнозе заболевания анурия не отражается.
Одним из кардинальных признаков острого гломерулонефрита является эритроцитурия, наблюдающаяся во всех случаях заболевания. Количество эритроцитов (преимущественно выщелоченных) чаще всего колеблется от 4—5 до 50—60 в поле зрения. При наличии единичных эритроцитов в поле зрения нужно исследовать осадок мочи по методу Каковского— Аддиса. Макрогематурия, по данным большинства клиницистов, наблюдается в 10—20 % случаев острого гломерулонефрита. Она может наблюдаться в первые дни заболевания и продолжаться несколько дней, а иногда несколько часов (в последнем случае может быть незамеченной) , на более длительный срок (неделя и больше) затягивается редко. Иногда в период выраженного улучшения, когда снижается артериальное давление, исчезают отеки, улучшается кровообращение в клубочках, появляется на короткий срок гематурия или усиливается эритроцитурия, что не следует считать неблагоприятным признаком,
Протеинурия встречается так же часто, как и гематурия. Она особенно значительна в начале заболевания. достигая изредка в утренней порции мочи 35 г/л. Однако суточное выделение белка с мочой редко превышает 3 г. При благоприятном течении заболевания протеинурия быстро снижается (в течение 2—3 недель). Электрофоретическое исследование белков мочи показывает, что при остром гломерулонефрите с нефротическим компонентом (отеки, высокая протеинурия, диспротеинемия) альбумины значительно превалируют над глобулинами (высокая селективность протеинурии), при других вариантах заболевания в мочу поступают и высокомолекулярные белки (α2-, γ-глобулины), что соответствует средней и низкой степени селективности протеинурии.
В осадке мочи часто обнаруживают повышение количества лейкоцитов (число Каковского—Аддиса свыше 2—4 млн.). Кроме того, в нем имеются клетки почечного эпителия, гиалиновые, зернистые, эритроцитные цилиндры.
Бактериурии, как правило, нет (число бактерий в 1 мл мочи не превышает 1 00 000), пробы с трифенил-тетразолийхлоридом (ТТХ) и нитритная отрицательны. Положительные пробы свидетельствуют о присоединении инфекции мочевых путей.
Клубочковая фильтрация снижается, канальцевая реабсорбция воды нормальная, почечный плазмоток уменьшается относительно мало, а нередко и вовсе не меняется или даже повышается в результате воспалительной гиперемии почек, благодаря чему фильтрационная фракция (отношение клубочковой фильтрации к плазмотоку) падает ниже нормы (0,13—0,2). Количество остаточного азота и мочевины в крови обычно в пределах нормы или слегка повышено (до 8 ммоль/л). Более значительное повышение наблюдается лишь при анурии или резкой и длительной олигурии. В ранние сроки болезни отмечается незначительная гиперхлоремия. Гипопротеинемия и диспротеинемия обычно незначительны. Возможно появление гиперхолес-теринемии и гиперлипемии, что в сочетании с отеками, выраженной протеинурией, диспротеинемией указывает на развитие нефротического синдрома (компонента).
Снижение кальций и магниуреза, а также нарушение ритма клубочковой фильтрации (с более выраженным уменьшением ее днем по сравнению с ночью) при остром гломерулонефрите наблюдаются чаше и выражены больше, чем другие нарушения функции почек.
Продолжительность острого гломерулонефрита в среднем равна 1 — 4 месяцам. Выздоровление наступает в 70—80 % случаев и чаще при бурном начале заболевания, нежели при постепенном. Острый гломерулонефрит в пожилом возрасте протекает тяжелее, чем в молодом.
Смертельный исход в настоящее время встречается редко (1 % случаев) и главным образом в пожилом возрасте (особенно при позднем распознавании болезни). Причиной смерти может быть недостаточность кровообращения, почечная эклампсия, кровоизлияние в мозг. В пожилом возрасте одышка, отеки, гипертензия, боль в области сердца более значительны и часто являются начальными проявлениями болезни.
Прогностически наиболее неблагоприятными факторами при остром гломерулонефрите являются «беспричинное» и постепенное начало его, затянувшееся течение (свыше 4— 6 месяцев), особенно если нефротический синдром в сочетании с гипертензией сохраняется свыше 2—3 месяцев; в 75—90% таких случаев наблюдается переход в хронический нефрит.
Переход острого гломерулонефрита в хронический может происходить двумя путями: без наличия светлого промежутка и с наличием более или менее длительного латентного периода. В первом случае ряд клинических проявлений острого гломерулонефрита сохраняется в течение многих месяцев, хотя интенсивность их обычно уменьшается. Во втором — наступает как бы полное выздоровление. Явных симптомов гломерулонефрита в течение длительного времени не наблюдается. Затем, иногда через много месяцев или даже лет (чаще после охлаждения или инфекции), снова появляются отеки, гипертензия, изменения в моче.
Критериями выздоровления являются исчезновение внепочечных симптомов, нормальные результаты исследования мочи в течение года даже при интеркуррентной инфекции. Эти критерии могут быть правильно оценены лишь при диспансерном наблюдении, которое должно продолжаться один год с момента нормализации показателей исследований мочи. Если в течение этого времени снова появляются изменения в моче, подъемы артериального давления, отеки, то срок диспансерного наблюдения продлевается до двух лет.
Сохранение (или появление) в течение двух лет изменений в моче, а также внепочечных симптомов свидетельствует о переходе острого гломерулонефрита в хронический.
Диагноз острого гломерулонефрита при наличии характерной триады симптомов — отеков, мочевого синдрома и артериальной гипертензии, возникающих после инфекционных заболеваний или охлаждения, обычно не представляет трудностей. В таких случаях приходится, главным образом, исключить подострый злокачественный гломерулонефрит и обострение хронического гломерулонефрита. Затруднения возникают в тех случаях, когда заболевание началось исподволь и протекает с изолированным мочевым синдромом, внепочечных проявлений или нет, или они успели исчезнуть к моменту исследования больного. Поэтому всегда после заболеваний, чаще всего предшествующих возникновению острого гломерулонефрита, следует исследовать мочу.
Дифференциальный диагноз. При выраженной гематурии проводят дифференциальный диагноз с опухолями почек и мочевых путей, туберкулезом почек, почечнокаменной болезнью. Диагноз острого гломерулонефрита может быть поставлен лишь после исключения этих заболеваний, что возможно после тщательноголабораторно-инструментального исследования.
О туберкулезе почек свидетельствуют наличие внепочечного туберкулеза у больного, а также данные рентгенологического, радиоиндикационного и бактериологического (посев мочи на специальные среды и введение ее морской свинке) исследований.
Почечно-каменная болезнь характеризуется приступообразной интенсивной болью в пояснице, дизурией, нередко повышением температуры тела, диспепсическими явлениями, в частности задержкой стула. Эритроцитурия обычно не сопровождается протеинурией или последняя незначительна (белково-эритропитарная диссоциация). Диагноз подтверждается при рентгенологическом и урологическом исследованиях.
Острый гломерулонефрит с изолированным мочевым синдромом дифференцируют с латентно протекающим острым пиелонефритом и сердечной почкой. Для первого характерна лейкоцитурия и особенно высокая степень бактериурии (свыше 100 000 бактерий в 1 мл мочи), сравнительно низкая относительная плотность мочи. В сомнительных случаях помогают урологические исследования и пункиионная биопсия почки.
О сердечной почке можно предполагать при наличии выраженной недостаточности кровообращения. Иногда вопрос решает исчезновение изменений в моче после лечения сердечными гликозидами и диуретическими средствами.
Дифференциальная диагностика амилоидоза дана в соответствующем разделе.
Лечение. Строгий постельный режим до исчезновения отеков, гипертензии, признаков недостаточности кровообращения и выраженной гематурии и протеинурии. Средняя продолжительность постельного режима—4—6 недель. Горизонтальное положение в постели с равномерным согреванием тела улучшает почечный плазмоток и клубочковую фильтрацию, способствует устранению спазма сосудов, что снижает протеинурию. Незначительная протеинурия, которая может длиться месяцами, не является противопоказанием для расширения режима.
При выраженных внепочечных проявлениях острого гломерулонефрита диетическое лечение следует начинать с назначения режима голода и жажды (в течение 1—2 дней), после чего рекомендуется ограничение жидкости (в зависимости от водного баланса), соли (вплоть до полного исключения) и одновременное назначение пищевых продуктов, богатых калием, магнием и кальцием (овощные, фруктовые дни). Белка рекомендуют от 0,6 г в первые недели до 1 г на 1 кг массы тела. Более резкое ограничение и даже исключение белка необходимо только при олиго- и анурии. Достаточная энергетическая ценность должна обеспечиваться жирами (преимущественно растительными) и углеводами. Такой пищевой режим обычно дает быстрый терапевтический эффект. После исчезновения отеков, снижения артериального давления, ликвидации недостаточности сердца диету можно расширить (обычно через 1 —1,5 месяца после начала болезни).
Введение антибиотиков показано с первых же дней заболевания, особенно при наличии в организме очага инфекции. В связи с преимущественным значением стрептококковой инфекции наиболее рационально назначать бензплпенициллин, эритромицин, олеандомицин (1 000 000—-1500 000 ЕД в сутки) в течение 10— 20 дней. Целесообразность применения этих антибиотиков определяется также относительно небольшим их нефротоксическим действием. При выраженном нефротическом компоненте доза должна быть увеличена в 1,5—2 раза.
Целесообразно назначать антибиотики после предварительного определения антибиограммы очагов инфекции (миндалин, зубов и т. п.). Чем раньше начата антибактериальная терапия, тем выше ее эффект. Поэтому рекомендуется параллельно с бактериологическим исследованием и определением антибиограммы проводить антибактериальную терапию по указанной выше методике. В случае отрицательных данных антибиограммы рекомендуется назначить другой антибиотик с учетом клинических симптомов. Антибактериальное лечение показано также при присоединении вторичной инфекции мочевых путей.
Учитывая аллергизирующее действие антибиотиков, с одной стороны, и повышенную сенсибилизацию организма при остром гломерулонефрите, с другой стороны, необходимо в сочетании с антибиотиками назначать десенсибилизирующие средства (димедрол — 0,03—0,05 г 3 раза в день; дипразин — пипольфен — 0,025 г 2— 3 раза в день; супрастин — 0,025— 0,05 г 3 раза в день; диазолин — 0,05 г 3 раза в день: кальция глюконат—1 г 3 раза в день), а также комплекс витаминов, особенно аскорбиновую кислоту и витамин Р. Применение кальция хлорида (по 1 столовой ложке 10 % раствора через каждые 2 ч) или кальция глюконата, а также витаминов уменьшает проницаемость стенки сосудов.
Стероидная терапия должна применяться только в случае резистентного, не поддающегося симптоматическому лечению нефротического синдрома, а также при опасности перехода острого гломерулонефрита з хронический (стабилизация мочевого синдрома свыше двух месяцев от начала заболевания). Стероиды лучше назначать после предварительной санации очагов хронической инфекции. При наличии нефротического синдрома лечение кортикостероидами следует начинать не позднее 5— 6 недель от начала заболевания. Назначают преднизолон (0,75— 1 мг/кг, в сутки — 40—70 мг) либо эквивалентные дозы других препаратов (триамцинолона, дексаметазона, урбазона) в течение 3—4 недель (предпочтителен прием в утренние часы) с последующим постепенным уменьшением дозы до полной отмены препарата или переходом (при недостаточном эффекте) на поддерживающие дозы (20 мг в сутки) по альтернирующей (двойная доза через день) или интермиттирующей (4 дня в неделю) схеме. При наличии противопоказаний к применению стероидов можно назначать цитостатики, индометанин или гепарин (см. «Хронический гломерулонефрит»).
При выраженном повышении артериального давления показаны препараты раувольфии, метилдофа в сочетании с дихлотиазидом (гипотиазидом) и внутримышечным введением дибазола, папаверина, эуфиллина.
Препараты наперстянки, горицвета, кофеин показаны лишь при недостаточности кровообращения. При отеках применяют производные пурина (теобромин, эуфиллин), фуросемид (лазикс), этакриновую кислоту (урегит), дихлотиазид, спиронолак-тон (альдактон, верошпирон). Применение ртутных диуретических средств противопоказано ввиду их выраженной нефротоксичности.
Очаги инфекции (хронический тонзиллит, гранулирующий периодонтит, синусит и т. д.) необходимо санировать. Соответствующее консервативное лечение должно проводиться с первых же дней болезни. Хирургическое вмешательство (тонзиллэктомия, экстракция зубов и т. д.) в остром периоде противопоказано. Его можно рекомендовать при неэффективности консервативного лечения в случаях затяжного течения острого гломерулонефрита с наличием протеинурии и небольшой гематурии, но лишь после снижения артериального давления, нормализации функции почек и исчезновения недостаточности кровообращения. Однако и в этих случаях иногда наступает обострение заболевания после операции.
При затяжном течении острого гломерулонефрита с изолированным мочевым синдромом может быть рекомендовано лечение на курортах Байрам-Али, Бухары, Элисты. В случаях затянувшегося нефротического синдрома показано лечение на курортах Средней Азии не ранее чем через 6—7 месяцев от начала заболевания.
Санаторно-курортное лечение в специализированных нефрологических санаториях Южного берега Крыма можно рекомендовать не ранее чем через 3 месяца после нормализации показателей анализа мочи, а при стабилизации мочевого синдрома— лишь после использования всех других методов лечения.
Больной может приступить к работе лишь после полного выздоровления. Но и в этом случае ему не рекомендуется работа, связанная с охлаждением, перенапряжением (физическим и психическим), опасностью инфицирования.
При наличии остаточных явлений (протеинурия, небольшая гематурия) может быть разрешена легкая работа в закрытом помещении.
Лечение при осложнениях острого гломерулонефрита. При почечной эклампсии необходимо быстро снизить артериальное давление, а также уменьшить отек мозга. С этой целью вводят однократно или повторно внутривенно 1—2 мл 1 % раствора дибазола, 10 мл 2,4% раствора эуфиллина, 40 мл 40 % раствора глюкозы; резерпин в больших дозах (0,001—0,002 г), аминазин (1 мл 2,5 % раствора внутримышечно). В предэклампсической стадии эффективны пиявки (по 3 пиявки на каждый сосцевидный отросток). При выраженной эклампсии необходимо массивное кровопускание (300—400 мл) с последующим внутривенным введением 100 мл 40 % раствора глюкозы или 20 % раствора маннита (маннитола) из расчета 1 г на 1 кг массы тела. Рекомендуется также фуросемид (лазикс) до 160 мг внутривенно. При неэффективности перечисленных мероприятий и выраженном повышении внутримозгового давления показана поясничная пункция (выпускать спинномозговую жидкость медленно).
При острой анурии необходимо придерживаться тактики, изложенной в разделе «Острая недостаточность почек». Следует подчеркнуть, что в связи с кратковременностью анурии при остром гломерулонефрите к методам внепочечного очищения (гемодиализ, перитонеальный диализ и др.) редко прибегают, так как обычно эффективна консервативная терапия.
Лечение при острой левожелудочковой недостаточности — см. «Острая левожелудочковая недостаточность сердца».
Профилактика. Среди профилактических мероприятий основное место занимает санация очагов инфекции, включая оперативную (тонзиллэктомия, радикальная операция по поводу хронического гнойного отита, удаление кариозного зуба и т. п.). При вспышках инфекционного процесса должны применяться сульфаниламидные препараты, антибиотики в сочетании с антигистаминными препаратами. После заболеваний, при которых возможно развитие острого гломерулонефрита, рекомендуется в течение 3—4 недель 1—2 раза в неделю исследовать мочу.
В первый месяц после выписки из стационара больной обследуется каждые 10 дней, затем один раз в месяц и наконец 1 раз в 2—3 месяца. Показаниями для проведения обследования являются также обострения хронических инфекций, интеркуррентные заболевания, перенесенные ангина, грипп, острые респираторные заболевания, переохлаждение, оперативное вмешательство.
Вторичная профилактика заключается в осуществлении диспансерного наблюдения (1—2 года) за лицами, перенесшими острый гломерулонефрит, с целью предупреждения перехода его в хроническую форму.
Диспансерное обследование должно включать опрос, осмотр, измерение артериального давления, общин анализ мочи, определение суточной протеинурии, а при скудном мочевом осадке и его количественное исследование.
При снятии с диспансерного учета желательно также провести исследование белков крови, пробу Зимницкого, а в случае отклонения ее от нормы определить клубочковую фильтрацию или произвести нуклидную ренографию.
В рамках диспансерного наблюдения осуществляют лечебно-профилактические мероприятия, включающие организацию труда и быта (избегать переутомления, переохлаждения), трудоустройство, диетическое питание (ограничение соли до 6 г в сутки), ликвидацию очагов хронической инфекции, лечение интеркуррентных заболеваний (но без приема нефротоксических средств). Женщинам в течение 1—2 лет противопоказаны беременность и роды.
Использованная литература
1. Внутренние болезни / Под. ред. проф. Г. И. Бурчинского. ― 4-е изд., перераб. и доп. ― К.: Вища шк. Головное изд-во, 2000. ― 656 с.