Обзор биологических наномоторов
Обзор биологических наномоторов
Свидиненко Юрий (Svidinenko)
Многие молекулярные наномашины, давно работающие в живых организмах, могут послужить первыми строительными кирпичиками будущих нанороботов. Причем таких "моторов" в природе достаточно много. В этой статье мы расскажем об основных биомоторах и их возможном применении в наносистемах будущего.
Одним из препятствий, ограничивающих размеры МЭМС-устройств, является то, что до сих пор нет работоспособного миниатюрного мотора размерами около 500-100 нанометров. Недавно Алексом Зеттлом был продемонстрирован рабочий наномотор с размером ротора около 500 нанометров, но конструктивное исполнение мотора затрудняет его использование в МЭМС. Мотор был изготовлен на основе кремниевой подложки и золотых электродов. В качестве оси для ротора исследователи использовали нанотрубку.
До использования подобных "неорганических" моторов в микро- и наносистемах еще далеко - их трудно изготовить, а интегрировать в готовое МЭМС-устройство еще труднее. Сегодня многие исследователи настаивают на том, что биологические моторы сыграют не последнюю роль в качестве актюаторов в МЭМС-устройствах. Тем более, что можно наладить их массовое производство методами генной инженерии и биотехнологий уже сейчас. Да и технические характеристики (соотношение размера, массы, генерируемого механического момента и потребляемой энергии) биологических моторов достаточно неплохие. Некоторые исследователи заинтересованы в использовании бактериальных жгутиковых моторов в качестве актюаторов для наноробототехники.
Интересно также то, что различные типы биологических моторов соответствуют некоторым макроскопическим машинам по принципу действия. Майкл Маер, профессор химико-биологического отделения из Мичиганского университета, после изучения молекулы кинезина сказал: "Эти штуки - настоящие машины! Было бы замечательно искусственно построить одну из них".
Энзим АТФаза и некоторые жгутиковые моторы, например, работают аналогично обычному электродвигателю: ротор вращается внутри неподвижного статора. Молекула кинезина, перемещаясь вдоль микротрубок цитоскелета, напоминает линейный двигатель. А актюатор бактериофага phi29, выбрасывающий виральную ДНК из капсида внутрь клетки-хозяина, работает по принципу двигателя внутреннего сгорания с несколькими рабочими цилиндрами.
Необычный энзим
Энзим АТФ-синтаза предназначен для синтеза или гидролиза молекул АТФ, а также для переноса протонов (Н+) через мембрану клетки, чем обеспечивает стабильный внутриклеточный рН цитоплазмы. Ученые установили, что при гидролизе АТФ одна из частей энзима совершает вращательное движение. Тогда у исследователей-нанотехнологов и возник интерес к этому необычному энзиму.
АТФаза состоит из двух отдельных частей: (1) F>0>, гидрофобной части, связанной с мембраной, ответственной за транспорт протонов, и (2) F>1>, гидрофильной части, ответственной за синтез и гидролиз АТФ (см. рис.1).
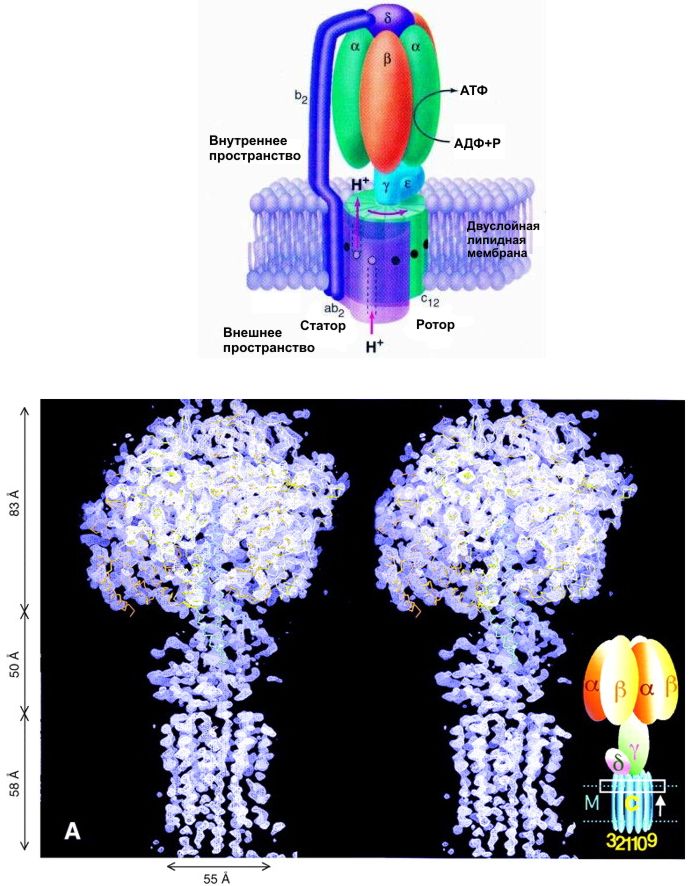
Рисунок 1. Строение и модель энзима АТФаза
По мере того как протоны протекают через F>0> часть энзима, γ-субъединица части F>1>-ATФазы вращается по часовой стрелке и идет синтез АТФ. Гидролиз АТФ происходит при вращении γ-субъединицы против часовой стрелки; при этом направление протекания протонов меняется на обратное. Субъединицы a, b, и c части F>0>-АТФазы формируют канал переноса протонов через клеточную мембрану. Места катализа и присоединения нуклеотидов были обнаружены исследователями (Kinosita и др., 1998) на трех а и трех b субъединицах части F>1>-ATФазы. γ-субъединица расположена в центре гексамера α>3>β>3> и вращается при синтезе или гидролизе АТФ.
Самое удивительное заключается в том, что АТФаза представляет собой полную аналогию макроскопических моторов, сделанных человеком, которые тоже состоят из ротора и статора.
Группа исследователей из Корнелльского университета во главе с Карло Монтеманьо попыталась интегрировать этот природный наномотор [1] в НЭМС. Исследователям удалось измерить радиальное отклонение микросферы при вращении субъединицы, когда они присоединили флуоресцентную микросферу диаметром 1 мкм к γ-субъединице АТФазы (см. рис.2).
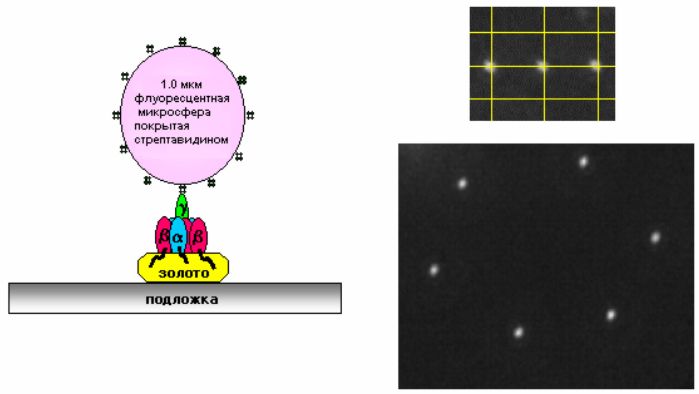
Рисунок 2. Строение наномотора и микрофотографии радиального отклонения микросферы
При добавлении к набору получившихся наномоторов 2 мM Na2ATФ и при присутствии в растворе 4 мM MgCl>2> дифференциальным интерферометром наблюдалось вращение микросферы, составляющее 9.5-10.5 Гц, или 3-4 об/сек. Причем вращение представляло собой дискретные изменения угла, образованного γ-субъединицей и α>3>β>3> - комплексом, каждый раз на 120°.
Дальнейшие исследования будут направлены на изучение инженерных свойств мотора и его производительности. Это необходимо для дальнейшей разработки функционирующих наномеханических устройств, приводимых в движение F1-АТФазой. Нужно, например, определить зависимость производительности мотора как обобщенную функцию от теплоотдачи, выхода протонов, рН, загрузки энзима молекулами АТФ. Более того, необходимо изучить взаимодействие между субъединицами α>3>β>3>γ, чтобы в будущем методами протеиновой инженерии улучшить производительность мотора, если это будет возможно.
АТФсинтаза является своего рода рекордсменом среди молекулярных моторов своей "весовой категории". По эффективности работы и развиваемой ею силе она существенно превосходит все известные в природе молекулярные моторы. Так, например, молекула АТФсинтазы приблизительно в 10 раз сильнее актомиозинового комплекса - молекулярной машины, специализирующейся в клетках мышц и различных органах на "профессиональном" выполнении механической работы. Таким образом, за сотни миллионов лет до того, как появился человек, который изобрел колесо, преимущества вращательного характера движения были успешно реализованы Природой на молекулярном уровне.
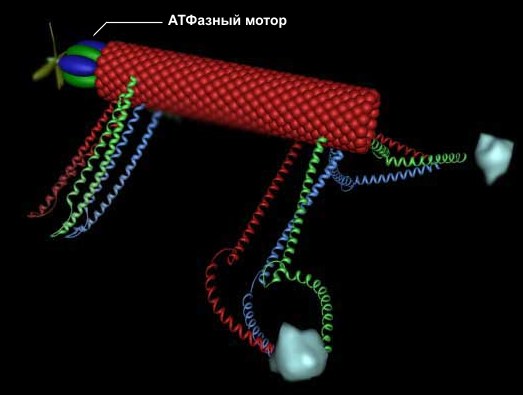
Рис. 3. Наноробот с пропеллером на АТФазе
Уже существуют первые проекты интеграции моторов на основе АТФазы в будущую наноробототехнику. Доктор Константин Мавродис из Рутгерского университета предложил "блочную схему" одного из простейших нанороботов, который использует именно такой мотор (см. рис. 3). Тело наноробота состоит из нанотрубки, манипуляторы выполнены в виде сложных пептидных цепей. Пропеллер (правда, по последним данным математического моделирования, пропеллерные системы актюации в нано- и микроразмерных вязких средах неэффективны), обеспечивающий передвижение в вязких средах, расположен на АТФазе. Как утверждает автор, подобные гибридные устройства могут появиться уже через 10 лет. Правда, Константин не акцентирует внимание на системах управления такими устройствами, что само по себе представляет более сложную задачу, чем приведение его в движение.
Самый маленький в мире грузчик
Другой не менее известный биологический мотор, который тоже будет полезен нанотехнологам, - молекула белка кинезина. Это представитель другого класса линейных моторов. Среди механохимических преобразователей энергии, распространенных в живой природе, они играют важную роль. Эти белковые машины движутся вдоль полимерных нитей, используя в качестве "топлива" молекулы АТФ. К таким моторам относятся белки актомиозинового комплекса, входящего в состав сократительного аппарата мышц. Движение микроворсинок (жгутиков и ресничек бактерий и простейших) определяется взаимодействием другой пары моторных белков - динеина и тубулина. Смещение головок динеина относительно тубулиновых микротрубочек белков обеспечивает волнообразные движения микроворсинок. Среди большого числа моторных белков миозин скелетных мышц и кинезин из клеток мозга являются наиболее изученными молекулярными моторами. Несмотря на то, что функции миозина и кинезина в клетке различаются, они удивительно похожи по своему строению и механизмам действия.
Расскажем, как работает молекула кинезина. Совместно с микротрубками цитоскелета она выполняет транспорт веществ внутри клетки и перемещение везикул. Если провести аналогию с макромиром, то микротрубки играют роль рельсов, по которым перемещаются молекулы белков кинезина (вагоны), неся на себе полезный груз. Один конец этой молекулы прикрепляется к везикуле, которую необходимо транспортировать, а другой - к микротрубке, которая направляет движение. Молекулы кинезина выполняют работу практически во всех растениях и животных (см. рис. 4).
Молекула кинезина представляет собой димер, образованный двумя одинаковыми полипептидными цепями. Подобно молекуле миозина, с одной стороны каждой полипептидной цепи кинезина формируется глобулярная головка, соединенная со сравнительно длинным хвостом. Линейные размеры головки сравнительно невелики, они составляют 7,5 х 4,5 х 4,5 нм. Длина молекулы - 50 нанометров. Хвосты двух мономерных цепей сплетены вместе, а наклоненные в разные стороны головки образуют своеобразную рогатину, которая непосредственно взаимодействует с глобулярными мономерами микротрубочки, вдоль которой перемещается кинезин.
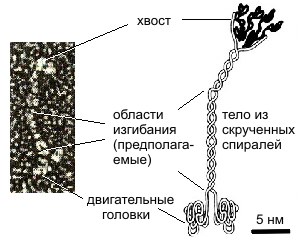
Рис. 4. Строение молекулы кинезина
Интересно то, что молекула "шагает" вдоль микротрубки (см. рис.5), делая 8-нанометровые шаги. На рисунке кинезиновый комплекс перемещает органеллу меланосому (ответственную за синтез меланина) вдоль микротрубки. Для того, чтобы так шагнуть, молекула использует в качестве топлива 1 молекулу АТФ. При этом сила, развиваемая одной молекулой кинезина, составляет величину 6 пН. Если бы такой мощностью в расчете на единицу массы обладали автомобильные моторы, то они могли бы легко разгонять машины до скоростей, существенно превышающих скорость звука. Коэффициент полезного действия кинезинового мотора также велик - примерно 50%.
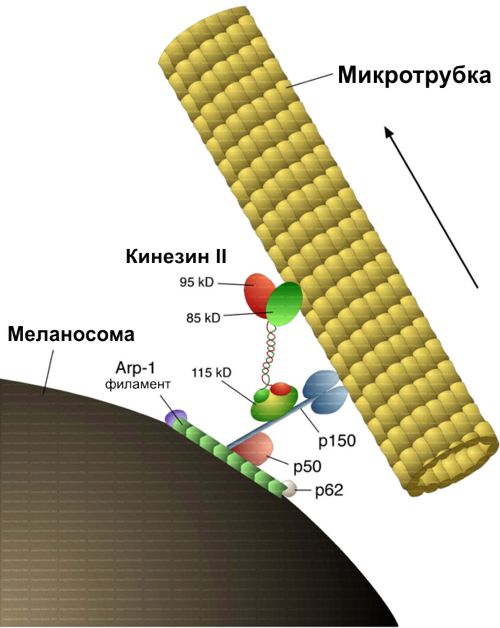
Рис. 5. Перемещение кинезином меланосомы (клеточной органеллы) вдоль микротрубки
В процессе "ходьбы" молекула кинезина может расщепить за одну секунду до 100 молекул АТФ, переместившись на 800 нанометров. Работая в качестве индивидуального молекулярного извозчика, кинезин может совершать перемещения на очень большие расстояния (до 1 мм).
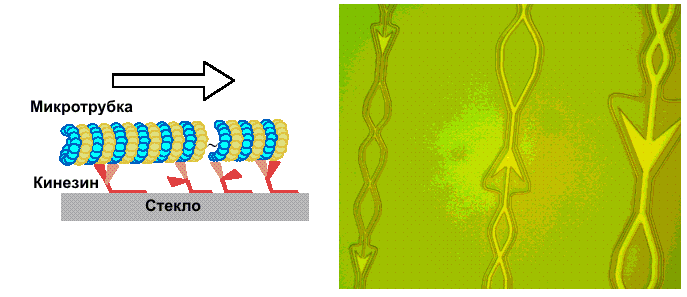
Рис. 6. Кинезиновый наноконвейер
Ученые из института им. Макса Планка попытались "приручить" кинезин вне клетки. Для этого они покрыли молекулами кинезина гладкую стеклянную поверхность, создав что-то вроде ковра, ворсинки которого представляли собой молекулы кинезина. Потом исследователи разместили на этой поверхности ряд микротрубок и микросфер. Исследователи добавили к среде раствор АТФ - и получился огромный "трубочный" конвейер. Если в клетке кинезин шагает вдоль микротрубки сам, то в искусственной системе молекула была жестко закреплена, и свободные концы молекул "шагали" по микротрубкам, передвигая их. Движения микротрубок можно увидеть на этом видео. Запись велась с помощью оптического микроскопа.
В дальнейшем команда планирует создать микрочипы со встроенными конвейерами, работающими в разных направлениях. Это, конечно, будет большим плюсом для будущих систем наносборки, так как НЭМС-конвейеры пока сделать достаточно трудно. Наверняка такие транспортные системы будут полезны и в лабораториях-на-чипе.
Камера сгорания внутри вируса
Как мы уже видели, биологические системы раньше человека использовали вращательное движение в молекулярных машинах. Ранее мы уже рассказывали о том, как молекулы РНК могут быть использованы в качестве строительных блоков для будущих наномашин. Однако до проведения этой работы профессор Пейхуан Гу описал работу вирального мотора на основе РНК-гексамера. РНК-гексамер - это комплекс, состоящий из шести отдельных РНК-мономеров.
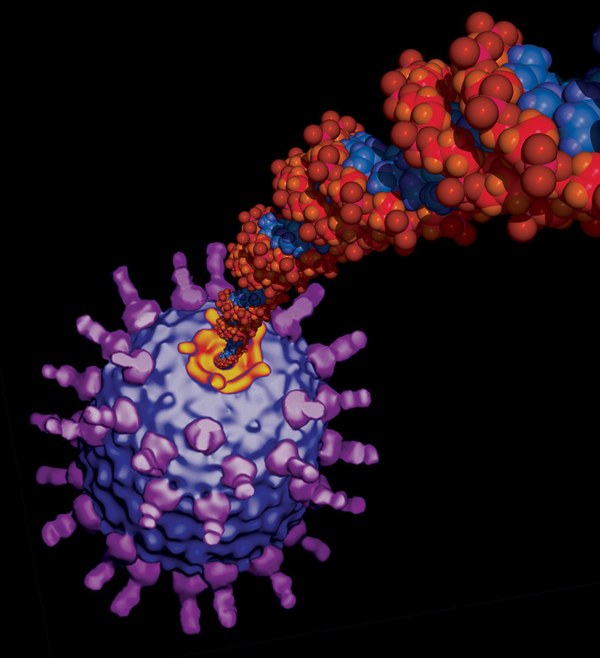
Рис. 7. Вирус phi29 выбрасывает ДНК из капсида
Оказалось, что вирус-бактериофаг phi29 использует гексамер молекул РНК для выброса молекулы ДНК из капсида вируса (см. рис. 7). При этом сам процесс работы мотора похож на работу двигателя внутреннего сгорания автомобиля. Роль камеры сгорания играет портал - образование внутри капсида вируса, занятое молекулами РНК и ротором. Мономеры молекулы РНК, подобно поршням, поочередно толкают центральный пятисторонний ротор, заставляя его вращаться. Каждый РНК-мономер толкает ротор всего на 12°, потребляя одну молекулу АТФ. Таким образом, за один цикл портал поворачивается на 72°, затратив 6 молекул (см. рис. 8).
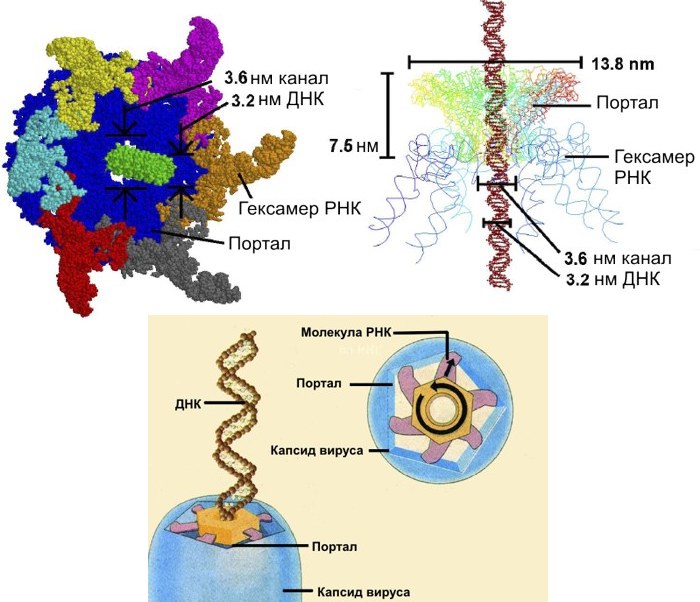
Рис. 8. Структура и модель вирального мотора
В центре ротора находится молекула ДНК. По мере того, как ротор вращается, молекула перемещается из капсида вируса во внешнее пространство.
Исследователи еще не смогли искусственно воссоздать из молекул РНК основу мотора. Пока они собрали "кольца", "треугольники" и "стержни". Они считают, что эти структуры можно интегрировать с нанотранзисторами, нанопроводниками, нанотрубками, биосенсорами и другими уже существующими наноструктурами, чтобы получить сложные НЭМС-системы.
Дайтер Молл, исследователь из группы Гу, говорит, что "самосборка молекул РНК позволит значительно уменьшить стоимость будущих РНК-НЭМС."
Жгутиковый мотор
Бактерия Esherichia Coli (E. Coli) - мечта нанотехнологов. Это почти готовая "база" для будущих нанобиороботов. Чтобы плавать, она с помощью специальных биологических электромоторов вращает свои жгутики. Когда жгутики начинают синхронно вращаться против часовой стрелки, они сплетаются в единый пучок, который образует своеобразный пропеллер. Вращение пропеллера создает силу, заставляющую бактерию двигаться почти по прямой линии. После того как направление вращения жгутиков изменяется на противоположное, пучок расплетается и бактерия останавливается, вместо поступательного движения она начинает хаотически вращаться, ее ориентация изменяется.
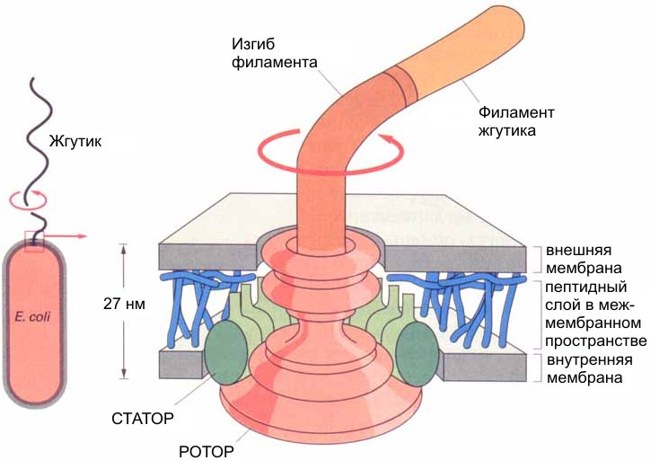
Рис. 9. Строение жгутикового мотора
Как и протонные АТФсинтазы, электромоторы бактерий являются устройствами, которые в качестве источника энергии используют разность протонных потенциалов на цитоплазматической мембране. Принципы работы АТФсинтазы и бактериального мотора одинаковы, хотя сами эти конструкции различаются по своим размерам и устройству (см. рис. 9, 10). Можно с уверенностью сказать, что бактериальный мотор - аналог машины постоянного тока, созданной человеком.
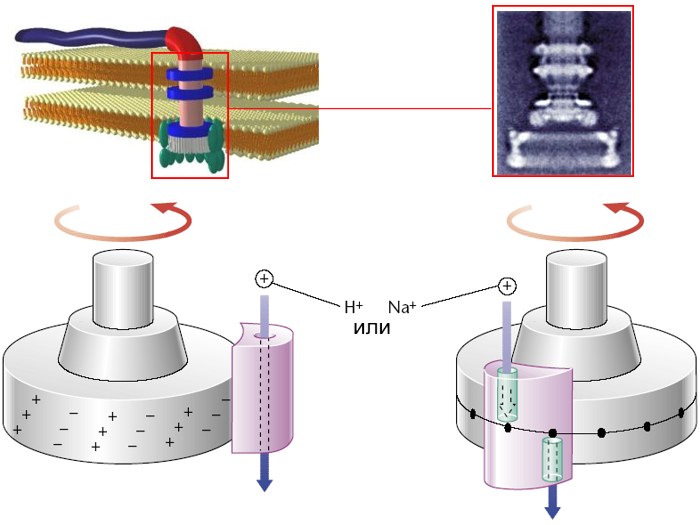
Рис. 10. Структурная модель, принцип работы и микрофотография жгутикового мотора
Электромоторы бактерий работают очень эффективно. Бактерии плавают со средней скоростью около 25 мкм/с, но некоторые виды могут двигаться поступательно со скоростью больше 100 мкм/с. Это означает, что за одну секунду бактерия перемещается на расстояние, которое в десять или больше раз превышает ее собственную длину. Любопытно провести аналогию с движением систем макроскопических размеров. Например, если бы пловцы преодолевали за одну секунду расстояние, на порядок превышающее их собственный рост, то стометровую дорожку плавательного бассейна они бы проплывали приблизительно за 5 с. Обычно электромотор бактерий вращается со скоростью, достигающей 50-100 оборотов в секунду, однако у некоторых видов бактерий скорость вращения превышает 1000 оборотов в секунду. Электромоторы, которые могут так быстро вращать жгутики бактерий, очень экономичны - они потребляют не более 1% энергетических ресурсов бактериальной клетки.
Роберт Фрайтас и Адриано Кавальканти, одни из ведущих мировых ученых в области наномедицины, неоднократно заявляли, что именно подобные жгутиковые моторы будут наиболее эффективны в наноробототехнике.
Заключение
Итак, как мы видим, на первых порах нет необходимости разрабатывать какие-либо "продвинутые" актюаторы, как это делал Эрик Дрекслер в "Наносистемах". Для построения первых примитивных наносистем достаточно и этих готовых "кирпичиков", которые миллионы лет эффективно работают в природе. Но, как только можно будет конструировать произвольные структуры из алмазоида с атомарной точностью, для многих наноустройств такие моторы будут непригодны.
У всех рассмотренных выше биологических моторов есть ряд недостатков. Важнейший недостаток - малая степень управляемости. То есть, если вы захотите использовать тот же АТФазный мотор для управления наноманипулятором, задать перемещение ротора в 10-20° будет практически невозможно, так как дискретность работы мотора - 120°. Конечно, можно воспользоваться редукторами и прочими преобразователями движения, но это усложнит конструкцию и увеличит размер устройства. Также один из недостатков биомоторов - условие работы в жидкой среде, что существенно ограничивает их круг применения.
Но все-таки, повторюсь, все вышеперечисленные моторы как нельзя лучше подходят по характеристикам для современных исследований в области нанотехнологий и нанопроизводства. Так что в течение следующих 10-15 лет им не предвидится альтернативы.
Список литературы
1. Carlo Montemagno и др., Nanotechnology 10 (1999) 225-231. Constructing Biological Motor Powered Nanomechanical Devices.
2. ISA: Engineering team working to create nanomotor
3. Constantinos Mavroidis, Ph.D., Associate Professor Department of Mechanical and Aerospace Engineering Rutgers University: PROTEIN BASED NANO-MACHINES FOR SPACE APPLICATIONS;
4. А. Н. Тихонов. Молекулярные моторы, ИР file:///C:/Documents%20and%20Settings/Test/Desktop/Моторы/www.nature.ru, 2001
5. Peixuan Guo, Purdue University: Construction of a Viral Nanomotor Driven by a Synthetic RNA
6. Свидиненко Юрий: РНК может формировать строительные блоки для наномашин
7. Richard M Berry, The Randall Institute, King’s College London, London, UK: Bacterial Flagella: Flagellar Motor